在2019年,施一公,颜宁,柴继杰及周强在Cell,Nature 及Science共发表12篇研究成果,在结构领域取得重大进展。iNature就系统盘点一下这些研究成果:
【1】在哺乳动物的电压门控钙(Cav)通道(VGCC)的10个亚型中,Cav3.1–3.3构成T型或低电压激活的亚家族,其异常活动与癫痫,精神病和 疼痛相关。2019年11月25日,颜宁团队在Nature在线发表题为“Cryo-EM structures of apo and antagonist-bound human Cav3.1”的研究论文,该研究报告了单独的人类Cav3.1的冷冻电镜结构以及与高度Cav3选择性阻滞剂Z944结合的冷冻EM结构,其分辨率分别为3.3Å和3.1Å。弓形的Z944分子在孔结构域的中心腔中倾斜,宽端插入重复序列II和III之间的界面的窗孔中,窄端像塞子一样悬在细胞内门上方。这些结构为比较研究不同Cav亚家族之间不同的通道特性提供了框架。
【2】2019年7月5日,原清华大学颜宁(清华大学第一单位)等人Nature 在线发表题为“Modulation of cardiac ryanodine receptor 2 by calmodulin”的研究论文,该研究报道了RyR2的8个冷冻电子显微镜(cryo-EM)结构,它们共同揭示了不同形式CaM的分子识别特征,并提供了对CaM对RyR2通道门控的调节的见解。Apo-CaM和Ca2 + -CaM结合由手柄,螺旋和中心区域形成的细长裂缝中的不同但重叠的位点。RyR2上CaM结合位点的转变受Ca2 +与CaM结合而不是RyR2的控制。Ca2 + -CaM诱导各个中心结构域的旋转和域内移位,导致PCB95和Ca2 +激活的通道的孔闭合。相比之下,ATP,咖啡因和Ca2 +激活通道的孔在Ca2 + -CaM存在下保持开放,这表明Ca2 + -CaM是RyR2门控的许多竞争调节剂之一;
【3】2019年5月30日,颜宁(清华大学为第一通讯单位)及吴建平共同通讯在Cell 在线发表题为“Molecular Basis for Ligand Modulation of a Mammalian Voltage-Gated Ca2+ Channel”的研究论文,该研究报告了Cav1.1与拮抗药物硝苯地平,地尔硫卓和维拉帕米的复合物的冷冻电子显微镜(cryo-EM)结构,分辨率分别为2.9Å,3.0Å和2.7Å;Cav1.1与DHP激动剂Bay K 8644复合物的冷冻电子显微镜(cryo-EM)结构,分辨率为2.8Å。地尔硫卓和维拉帕米穿过孔域的中心腔,直接阻断离子渗透。尽管硝苯地平和Bay K 8644在重复III和IV的界面处占据相同的位点,但协调细节支持以前的功能观察。这些结构阐明了不同Cav配体的作用模式,并为结构引导的药物发现建立了框架。总之,结构研究阐明了三种临床应用的拮抗剂和原型激动剂在原子水平上识别和调节L型Cav通道的分子基础,并为大量实验和临床数据提供结构解释。这些结构为未来针对Cav通道病的药物发现奠定了基础;
【4/5】2019年2月15日,原清华大学颜宁团队Science背靠背同期发表2篇论文,发表发表题为“Structures of human Nav1.7 channel in complex with auxiliary subunits and animal toxins”及“Molecular basis for pore blockade of human Na+ channel Nav1.2 by the μ-conotoxin KIIIA”,共同阐述离子通道结构;
【6】2019年1月1日,施一公研究组在Nature 在线发表题为“Structural basis of Notch recognition by human γ-secretase”的研究论文,该论文报告人类γ-分泌酶与Notch片段的复合物的冷冻电子显微镜结构,分辨率为2.7Å。Notch的跨膜螺旋被PS1的三个跨膜结构域包围,并且Notch片段的羧基末端β-链形成β-折叠,其在细胞内侧具有两个底物诱导的PS1的β-链。杂合β-折叠的形成对于底物裂解是必需的,其发生在Notch跨膜螺旋的羧基末端。PS1在底物结合后经历明显的构象重排。这些特征揭示了Notch识别的结构基础,并且对γ-分泌酶对淀粉样蛋白前体蛋白的募集具有意义;
【7】2019年1月11日,清华大学施一公团队在Science在线发表题为“Recognition of the amyloid precursor protein by human γ-secretase”的研究论文,该论文报告了人类γ-分泌酶与跨膜APP片段的复合物的冷冻电子显微镜(cryo-EM)结构,分辨率达到2.6Å。 该结构用作发现γ-分泌酶的底物特异性*制剂抑**和理解γ-分泌酶的生物学功能以及AD的疾病机制的重要框架;
【8】2019年3月14日,施一公研究组在Cell 在线发表题为“Structures of the Catalytically Activated Yeast Spliceosome Reveal the Mechanism of Branching”的研究论文,该研究得到了酿酒酵母的两种不同前mRNA上组装了B *复合物,并确定了四种不同B *复合物的冷冻EM结构,总分辨率为2.9-3.8Å。 U2核小RNA(snRNA)和分支点序列(BPS)之间的双链离散地远离5个B *复合物中的5'-剪接位点(5'SS),其缺乏步骤I剪接因子Yju2和Cwc25。将Yju2募集到活性位点使U2 / BPS双链体进入5'SS附近,BPS亲核试剂位于距催化金属M24Å处。该分析揭示了Yju2和Cwc25在分支中的功能机制。 不同前mRNA上的这些结构揭示了在主要功能状态下剪接体的底物特异性构象。 这些构象状态的比较揭示了对支化反应的机理见解;
【9/10】2019年4月4日,清华大学柴继杰课题组、中科院遗传发育所周俭民课题组和清华大学王宏伟课题联合同期背靠背发表两篇重量级Science文章,完成了植物NLR蛋白复合物的组装、结构和功能分析,揭示了NLR作用的关键分子机制,是植物免疫研究的里程碑事件。两篇文章分别是: "Ligand-triggered allosteric ADP release primes a plant NLR complex”的研究论文。该研究通过重建了拟南芥中NLB蛋白ZAR1-RKS1和ZAR1-RKS1-PBL2UMP复合物,并分别以3.7和4.3Å的分辨率确定了它们冷冻电子显微镜(cryo-EM)结构,揭示了ZAR1-RKS1识别PBL2UMP和PBL2UMP激活ZAR1的机制,为理解NLR蛋白提供了结构模板!"Reconstitution and structure of a plant NLR resistosome conferring immunity”的研究论文。该研究重建了ZAR1-RKS1-PBL2UMP-dATP活性复合体,证明了其复合体在免疫激活过程中进行寡聚化,并揭示了其激活免疫反应的机制!这两项研究在植物免疫研究领域取得历史性的重大突破,填补了人们25年来对植物抗病蛋白认知的巨大空白,将为研究其它抗病蛋白提供范本。Science杂志同期发表评论文章,认为“首个抗病小体的发现,为植物如何控制细胞死亡和免疫提供了线索”“显著推进了人们对植物免疫机制的认识”“打开了多个开拓性研究方向”;
【11】2019年7月10日,清华大学柴继杰与东安格利亚大学Cyril Zipfel共同通讯在Nature在线发表题为“Mechanisms of RALF peptide perception by a heterotypic receptor complex”的研究论文,该研究报道RALF23诱导CrRLK1L FERONIA(FER)和LORELEI(LRE)-LIKE GLYCOSYLPHOSPHATIDYLINOSITOL(GPI)-ACHORED PROTEIN 1(LLG1)之间的复合物以调节免疫信号。该研究工作揭示了GPI锚定蛋白与植物遗传学上不相关的RK一致的植物肽感知的意外机制,这提供了一个分子框架,通过CrRLK1L RK和GPI锚定 的LRE / LLG家族蛋白质之间的不同异源复合物的感知,提供了一种分子框架来理解RALF多肽如何调节多个过程;
【12】2019年3月13日,西湖大学周强团队(第一单位清华大学)在Nature在线发表题为“Structure of the human LAT1–4F2hc heteromeric amino acid transporter complex”的研究论文,该研究阐明了LAT1-4F2hc复合体的结构,并提供了对其功能及其可能与疾病相关的机制的见解;
1

Cav通道介导Ca2 +流入细胞质,响应膜电位的变化,这是将膜上的电信号转换为细胞内化学信号的重要过程。由于涉及Ca2 +的信号事件的频谱范围很广,因此Cav通道参与了各种生理过程,例如收缩,分泌,基因表达和细胞死亡。已经确定了编码哺乳动物Cav通道孔形成亚基的10个基因,并将产物分为三类,Cav1(Cav1.1-Cav1.4),Cav2(Cav2.1-Cav2.3)和Cav3(Cav3 .1-Cav3.3)。
Cav3通道仅与其他两个亚家族共享〜20%的序列同一性和〜45%的相似性。克隆Cav3通道(人类Cav3.1)比兔Cav1.1(第一个克隆的Cav通道)晚了十二年。序列变化遍及整个序列,包括选择性过滤结构域(SF)。尽管Cav1和Cav2成员均具有四个Glu(EEEE),每个重复序列的相应位点定义了Ca2 +选择性,但最后两个重复序列中的相应基因座被Cav3通道(EEDD)中的Asp取代。此外,重组表达通道的表征支持Cav3核心亚基的自主功能,而其他家族则需要辅助亚基来适当地进行膜定位和活性调节。
Cav3通道可以在低膜电位下被激活,甚至比静息电位低,去灭活常常需要超极化。因此,Cav3成员被指定为低电压激活(LVA)通道,而Cav1和Cav2被指定为高电压激活(HVA)。与由L型Cav1通道介导的较大,持久的电导相反,Cav3也被称为T型瞬态单通道。T型VGCC的低电压激活支持了它们在细胞兴奋性调节,低阈值激发和起搏活动中的生理作用。
已经确定T型VGCC突变与癫痫发作,共济失调和精神疾病有关,Cav3.2基因敲除小鼠的疼痛反应减弱。T型VGCC选择性拮抗药的开发代表了减轻这些疾病的诱人策略。Z944是一种高度Cav3选择性阻滞剂,是II期临床试验中治疗癫痫和神经性疼痛的候选药物。它可阻断T型通道,IC50介于50-160 nM之间,与HVA Ca2 +通道,Nav1.5和hERG相比,具有260-2000倍的选择性。然而,其特异性结合位点和亚型选择性的分子基础仍然不清楚。
研究人员已经解决了包含核心亚基α1和辅助亚基β1a,α2δ-1和γ的组织提取兔Cav1.1复合物的冷冻电镜结构。然而,用于样品制备的内源性来源阻止了具有病理生理学意义和机制意义的Cav突变体的结构研究。重组表达的Cav通道的结构阐明对于建立结构-功能关系将是无价的。
尽管先前在重组Nav通道方面取得了成功,但Cav通道却困难重重,直到现在,才确定了合适的结构。在该研究中,显示了在I-II接头内缺失的小鼠Cav3.1剪接变体,称为Cav3.1-Δ8b,可增加其表达。研究人员设计了一个相应的人Cav3.1-Δ8b变体,其中从全长蛋白(Uniprot ID:O43497-9)中删除了509-642位残基。
在该研究中,分别针对人类Cav3.1-Δ8b及Cav3.1-Δ8b与Z944的冷冻电镜结构,分辨率分别为3.3Å和3.1Å。弓形的Z944分子在孔结构域的中心腔中倾斜,宽端插入重复序列II和III之间的界面的窗孔中,窄端像塞子一样悬在细胞内门上方。这些结构为比较研究不同Cav亚家族之间不同的通道特性提供了框架。
参考消息:
https://www.nature.com/articles/s41586-019-1801-3
2

心肌收缩是由Ca2 +进入细胞质引起的,最初来自细胞外环境,由Cav1.2介导,随后由肌浆网Ca2 +储存,由RyR2介导。 Ryanodine受体是已知最大的离子通道,由分子量大于2兆道尔顿的同源四聚体组成。超过80%的蛋白质折叠成多结构域,感知与各种调节剂的相互作用,从离子到蛋白质。 RyR2活性的精确调节对于每次心跳都是至关重要的, RyR2的异常活动与危及生命的心律失常相关。
17kDa的CaM蛋白是一种重要的钙传感器,在大多数钙信号传导事件中起着重要作用。 CaM由大致对称的N-和C-末端叶组成,通过柔性铰链连接。每个叶可以通过两个EF-手(螺旋E和F-手)基序与两个Ca2 +离子配合,具有微摩尔范围的结合亲和力。在Ca2 +结合后,两个叶中的几个疏水残基的暴露促进CaM与靶序列的结合。 CaM与ryanodine受体直接相互作用,CaM-RyR的化学计量比为1:1,在纳摩尔范围的结合亲和力。
然而,CaM对ryanodine受体的调节是同种型特异性的。 CaM显示RyR1的双相调节,作为纳摩尔水平的Ca2 +(apo-CaM)的弱激活剂和微摩尔水平的Ca2 +(Ca2 + -CaM)的*制剂抑**。相反,apo-CaM对RyR2没有作用或抑制作用,而Ca2 + -CaM抑制RyR2。 CaM还被证明有助于终止存储过载诱导的Ca2 +释放(SOICR)。 CaM和RyR2之间的异常相互作用与心力衰竭相关,CaM-RyR2相互作用受损的纠正可以作为压力超负荷引起的心力衰竭致死性心律失常的治疗。
RyR-CaM复合物的结构表征局限于低分辨率电子显微镜图,其表明在RyR1中对于apo-和Ca2 + -CaM存在两个重叠但不同的结合位点。对应于RyR1的残基3614-3643(RyR2的中心结构域中的残基3581-3612)的肽结合apo-CaM和Ca2 + -CaM。与肽结合的Ca2 + -CaM的晶体结构揭示了肽的N和C末端的疏水锚,其分别容纳Ca2 + -CaM的C-和N-叶。
为了阐明CaM对RyR2的调节,该研究报道了RyR2的8个冷冻电子显微镜(cryo-EM)结构,它们共同揭示了不同形式CaM的分子识别特征,并提供了对CaM对RyR2通道门控的调节的见解。Apo-CaM和Ca2 + -CaM结合由手柄,螺旋和中心区域形成的细长裂缝中的不同但重叠的位点。RyR2上CaM结合位点的转变受Ca2 +与CaM结合而不是RyR2的控制。Ca2 + -CaM诱导各个中心结构域的旋转和域内移位,导致PCB95和Ca2 +激活的通道的孔闭合。 相比之下,ATP,咖啡因和Ca2 +激活通道的孔在Ca2 + -CaM存在下保持开放,这表明Ca2 + -CaM是RyR2门控的许多竞争调节剂之一。
参考信息:
https://www.nature.com/articles/s41586-019-1377-y
3

心肌收缩是由Ca2 +进入细胞质引起的,最初来自细胞外环境,由Cav1.2介导,随后由肌浆网Ca2 +储存,由RyR2介导。 Ryanodine受体是已知最大的离子通道,由分子量大于2兆道尔顿的同源四聚体组成。超过80%的蛋白质折叠成多结构域,感知与各种调节剂的相互作用,从离子到蛋白质。 RyR2活性的精确调节对于每次心跳都是至关重要的, RyR2的异常活动与危及生命的心律失常相关。
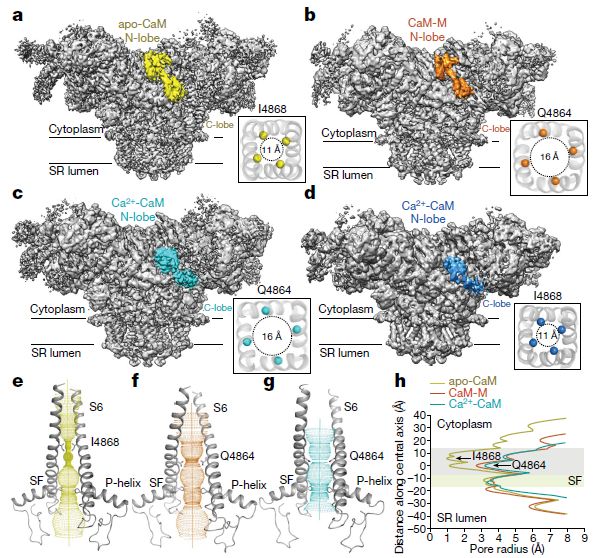
RyR2-CaM复合物的Cryo-EM结构
17kDa的CaM蛋白是一种重要的钙传感器,在大多数钙信号传导事件中起着重要作用。 CaM由大致对称的N-和C-末端叶组成,通过柔性铰链连接。每个叶可以通过两个EF-手(螺旋E和F-手)基序与两个Ca2 +离子配合,具有微摩尔范围的结合亲和力。在Ca2 +结合后,两个叶中的几个疏水残基的暴露促进CaM与靶序列的结合。 CaM与ryanodine受体直接相互作用,CaM-RyR的化学计量比为1:1,在纳摩尔范围的结合亲和力。
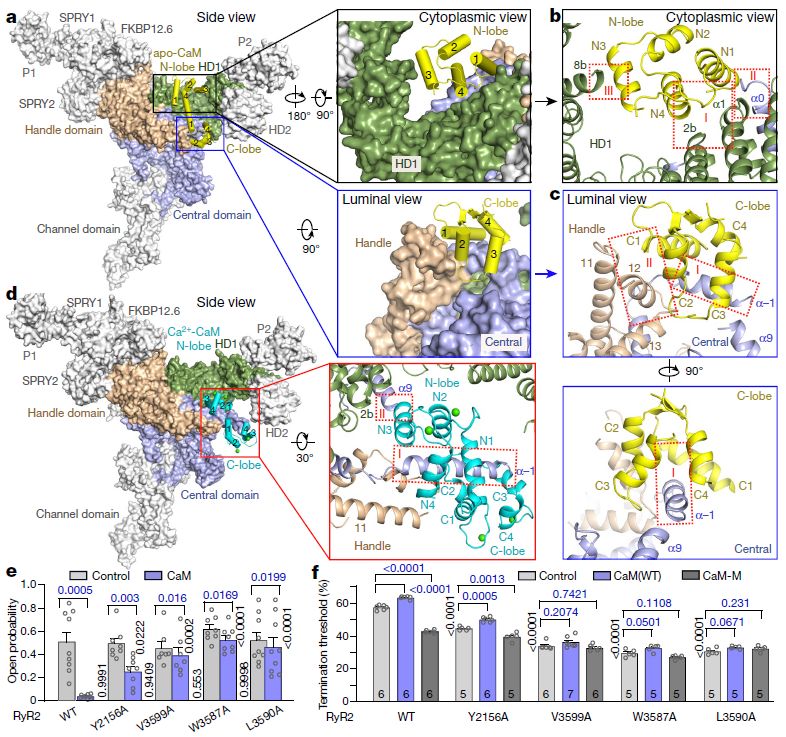
CaM和RyR2之间的接口
然而,CaM对ryanodine受体的调节是同种型特异性的。 CaM显示RyR1的双相调节,作为纳摩尔水平的Ca2 +(apo-CaM)的弱激活剂和微摩尔水平的Ca2 +(Ca2 + -CaM)的*制剂抑**。相反,apo-CaM对RyR2没有作用或抑制作用,而Ca2 + -CaM抑制RyR2。 CaM还被证明有助于终止存储过载诱导的Ca2 +释放(SOICR)。 CaM和RyR2之间的异常相互作用与心力衰竭相关,CaM-RyR2相互作用受损的纠正可以作为压力超负荷引起的心力衰竭致死性心律失常的治疗。
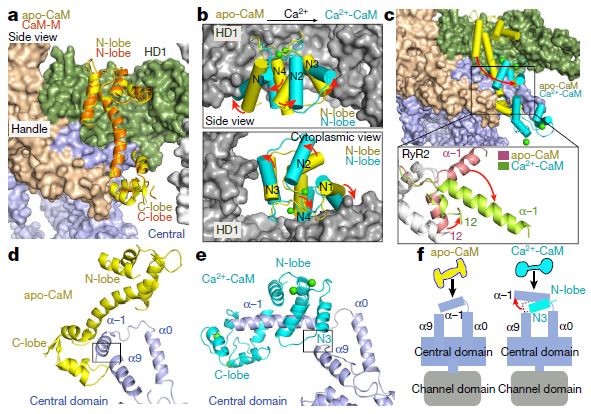
Ca2 +负载后CaM结合位点移位的分子基础
RyR-CaM复合物的结构表征局限于低分辨率电子显微镜图,其表明在RyR1中对于apo-和Ca2 + -CaM存在两个重叠但不同的结合位点。对应于RyR1的残基3614-3643(RyR2的中心结构域中的残基3581-3612)的肽结合apo-CaM和Ca2 + -CaM。与肽结合的Ca2 + -CaM的晶体结构揭示了肽的N和C末端的疏水锚,其分别容纳Ca2 + -CaM的C-和N-叶。
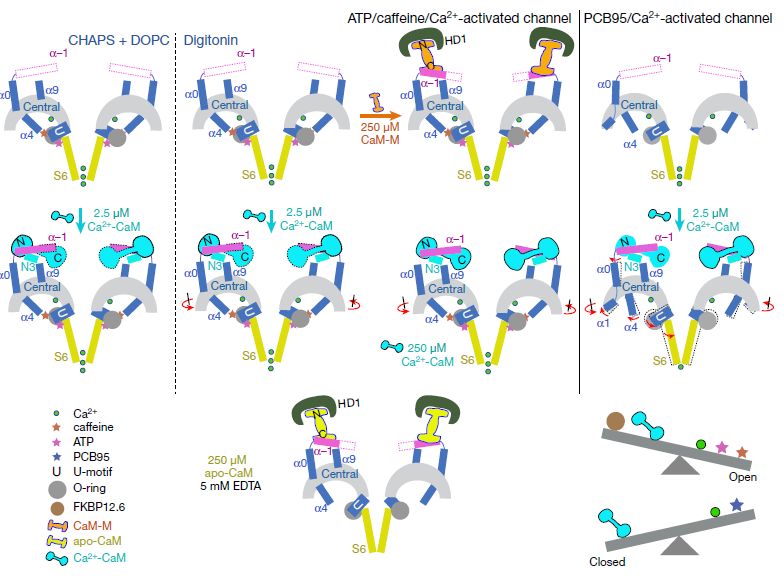
通过CaM调制RyR2的示意图
为了阐明CaM对RyR2的调节,该研究报道了RyR2的8个冷冻电子显微镜(cryo-EM)结构,它们共同揭示了不同形式CaM的分子识别特征,并提供了对CaM对RyR2通道门控的调节的见解。Apo-CaM和Ca2 + -CaM结合由手柄,螺旋和中心区域形成的细长裂缝中的不同但重叠的位点。RyR2上CaM结合位点的转变受Ca2 +与CaM结合而不是RyR2的控制。Ca2 + -CaM诱导各个中心结构域的旋转和域内移位,导致PCB95和Ca2 +激活的通道的孔闭合。 相比之下,ATP,咖啡因和Ca2 +激活通道的孔在Ca2 + -CaM存在下保持开放,这表明Ca2 + -CaM是RyR2门控的许多竞争调节剂之一。
参考信息:
https://www.nature.com/articles/s41586-019-1377-y
4

在人电压门控钠(Nav)通道的九种亚型中,由SCN9A编码并在外周感觉神经元中高表达的Nav1.7与疼痛综合征有直接关系。Nav1.7的突变出现在许多疼痛综合征中,包括极度疼痛障碍等。Nav1.7的精确结构模型将有助于这一有前途的目标的药物发现。
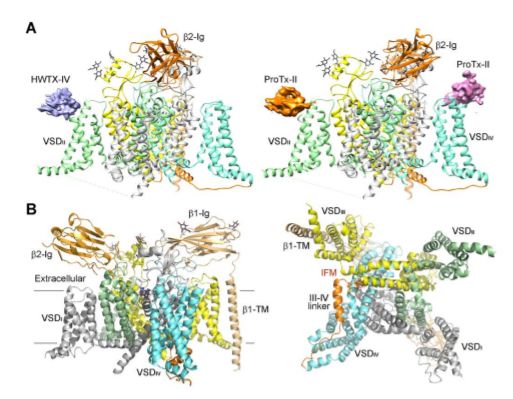
Nav1.7-PT和Nav1.7-HS的总体结构
真核细胞人Nav通道具有较高的序列相似性。昆虫、电鳗和人类具有代表性的NaV通道的冷电镜结构揭示了核心α亚基的相同结构。一个单一的多肽链,即α亚基,折叠成4个同源重复序列,每个重复包含6个跨膜螺旋,命名为S1-S6。每个重复序列中的S1-S4片段构成电压传感域(VSD),它附着在由S5和S6螺旋所包围的中心离子导电孔域(PD)上。VSD和PD段符合在电压门控离子通道(VGIC)超家族中流行的规范域交换组装。S5和S6之间的序列包括选择性过滤器(SF),它被两个半膜穿透的再入孔螺旋P1和P2夹在一起。四个重复序列(Asp/Glu/Lys/Ala(DEKA)中相应的SF位点上的四个不同的残基是Na选择(21)的特征基序。
虽然α亚基本身就足以用于离子渗透的电压依赖性门控,但它受一个或多个β辅助亚基的调节。所有四个β亚基,即β1-β4,都会影响Nav1.7的通道特性,尽管β1和β2通常与Nav1.7α亚基共同表达以进行生物物理表征。电鳗和人类的Nav1.4-β1复合物的结构揭示了α与β1(17,18)之间的相互作用细节,但其他β亚基的结合模式仍有待于结构上的阐明。
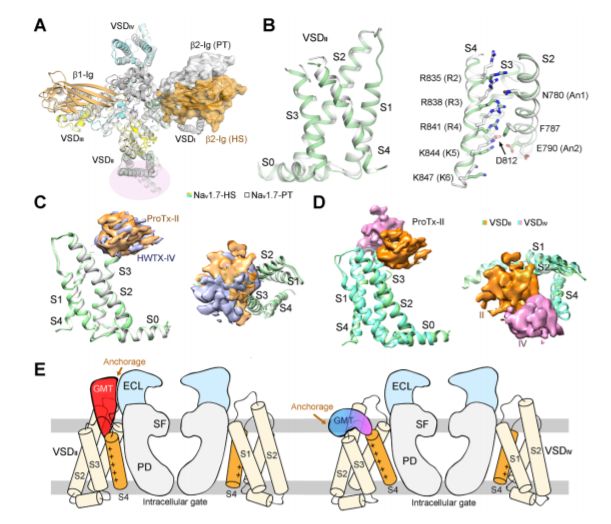
HWTX-IV和ProTx-Ⅱ的结合位点和潜在工作机制
在这里,研究人员报道了人源Nav1.7-β1-β2复合物与孔阻滞剂和门控改性剂毒素(GMT)结合的冷冻电镜结构,其中河豚毒素与原毒素-Ⅱ结合,Saxitoxin与Huwentoxin-IV结合,整体分辨率达到3.2 Å。除了VSDII的小位移外,这两种结构几乎相同,VSDII的S3-S4连接器以类似的方式容纳这两个GMT。另外一种原毒素-II位于VSDIV中S3-S4链接器的顶部。这些结构可能代表一种灭活状态,所有四个VSD“向上”和细胞内的门关闭。这些结构说明了机械理解Nav1.7的功能和疾病的途径,并为结构辅助止痛药的发展奠定了基础。
原文链接:
http://science.sciencemag.org/content/early/2019/02/13/science.aaw2493
5

电压门控钠(Nav)通道负责动作电位的快速上升,因此在细胞膜兴奋性和电信号传递中起着至关重要的作用。NAV通道复合体通常由一个由SCNxA编码的核心α亚基(x=1-5对应于Nav1.1-NaV1.5,x=8-11,对应于Nav1.6-Nav1.9)和一个或两个辅助β亚单位组成。当α亚基足够用于电压传感和离子选择性电导时,β亚基调节α亚基的膜定位,调节Na电流的峰值,改变电压依赖性通道激活和失活的动力学。β亚基包括一个氨基(N)末端免疫球蛋白(Ig)结构域、一个单跨膜螺旋(TM)和一个胞内结构域,β1和β3通过非共价相互作用与α结合,而β2和β4分别与α(6-10)形成二硫键。
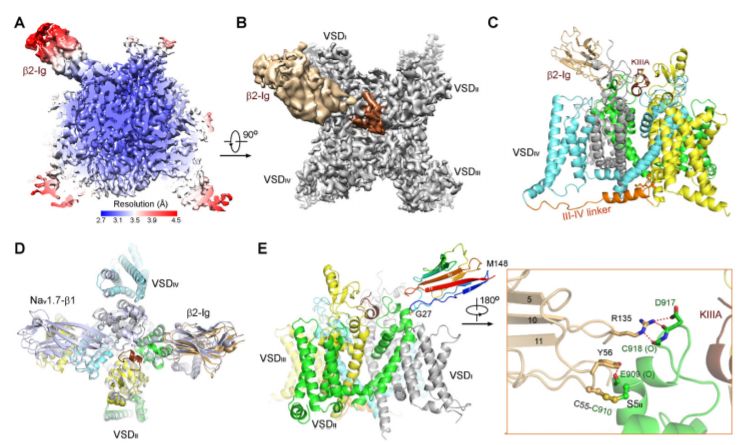
人Nav1.2-β2复合物与μ-圆锥毒素KIIIA结合的冷冻电镜分析
来自电鳗和人类Nav1.4与β1的复合物的结构显示界面在这两个物种之间是保守的。 洞察其他β亚基的识别主要来自诱变分析和个体β亚基的结构信息。
除了β亚基外,NAV通道还受到各种动物毒液中大量天然毒素的调节。通常有两类毒素,孔阻滞剂和门控改性剂毒素(GMT)。前者以胍类神经毒素河豚毒素(TTX)和Saxitoxin(STX)为例,直接阻断离子电导。后者通常是长度从几个残基到几十个残基的肽,与电压敏感域(VSD)结合,改变通道的电压依赖的门控特性。一些肽类毒素,例如从锥形蜗牛中鉴定出的μ-圆锥毒素,也起着孔隙阻滞剂的作用。与小分子孔道阻滞剂相比,肽类阻滞剂具有更严格的NaV亚型特异性,因此由于NAV通道的病理生理意义,代表了药理学意义的线索。
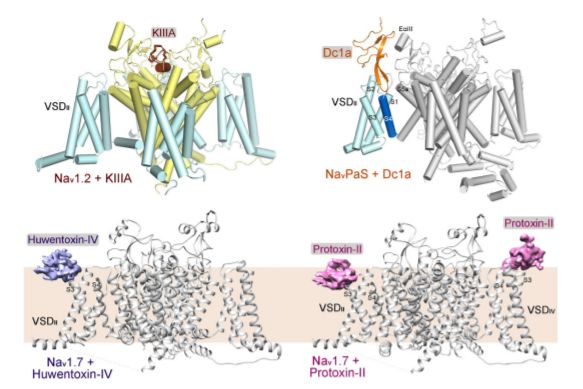
肽类毒素与NaV通道的结合方式不同
昆虫Nav通道NavPaS的结构与TTX、STX和GMT,Dc1a相互配合,揭示了这些具有代表性的毒素的识别和作用方式的分子基础。在该研究中,研究人员介绍了β1和β2亚基的配合物Nav1.7的结构,以及(1)GMTs Pro毒素II(ProTxII)和TTX(Nav1.7-PT)和(II)Huwentoxin-IV(HWTX-IV)和STX(Nav1.7-HS)的结构。然而,关于NAV通道与肽类孔阻滞剂之间的分子识别,还没有任何结构信息。
在这里,研究人员报告了在辅助亚基β2存在下,人源Nav1.2与肽类孔阻滞剂μ-cono毒素KIIIA结合的冷冻电镜结构,分辨率达到3.0 Å。β2的免疫球蛋白(Ig)结构域通过二硫键与孔隙结构域的肩部相互作用。16-残基KIIIA在重复I至Ⅲ中与胞外段相互作用,将Lys 7置于选择性过滤器的入口。许多相互作用的残基是Nav1.2特有的,揭示了KIIIA特异性的分子基础。该结构为NaV通道特定亚型阻滞剂的合理设计建立了一个框架.
原文链接:
http://science.sciencemag.org/content/early/2019/02/13/science.aaw2999
6

γ-分泌酶对Notch的异常切割,会导致几种类型的癌症,但γ-分泌酶如何识别其底物仍然未知。 在这里,施一公研究组报告人类γ-分泌酶与Notch片段的复合物的冷冻电子显微镜结构,分辨率为2.7Å。
Notch的跨膜螺旋被PS1的三个跨膜结构域包围,并且Notch片段的羧基末端β-链形成β-折叠,其在细胞内侧具有两个底物诱导的PS1的β-链。 杂合β-折叠的形成对于底物裂解是必需的,其发生在Notch跨膜螺旋的羧基末端。 PS1在底物结合后经历明显的构象重排。 这些特征揭示了Notch识别的结构基础,并且对γ-分泌酶对淀粉样蛋白前体蛋白的募集具有意义。
原文链接:
https://ezproxy.eastern.edu:2648/articles/s41586-018-0813-8
7

阿尔茨海默病(AD)的标志是AD患者脑中存在淀粉样蛋白斑。淀粉样斑块的主要成分是源自淀粉样蛋白前体蛋白(APP)的β-淀粉样肽(Aβ)。 I型跨膜蛋白APP首先被α-或β-分泌酶切割,分别产生83或99个残基的跨膜片段(APP-C83或APP-C99)。然后APP-C99通过其内肽酶活性被γ-分泌酶切割,产生48-残基肽Aβ48或49-残基肽Aβ49。随后通过γ-分泌酶的羧基末端肽酶活性切割Aβ49导致产生Aβ46,Aβ43和Aβ40的产生。类似地,Aβ48的切割产生Aβ45,Aβ42和Aβ38。其中,Aβ42和Aβ43特别容易聚集并形成淀粉样蛋白斑。除APP外,Notch受体也是α-和γ-分泌酶的底物。在α-分泌酶切割后,所得的跨膜Notch片段被γ-分泌酶切割以产生细胞内信号传导结构域。
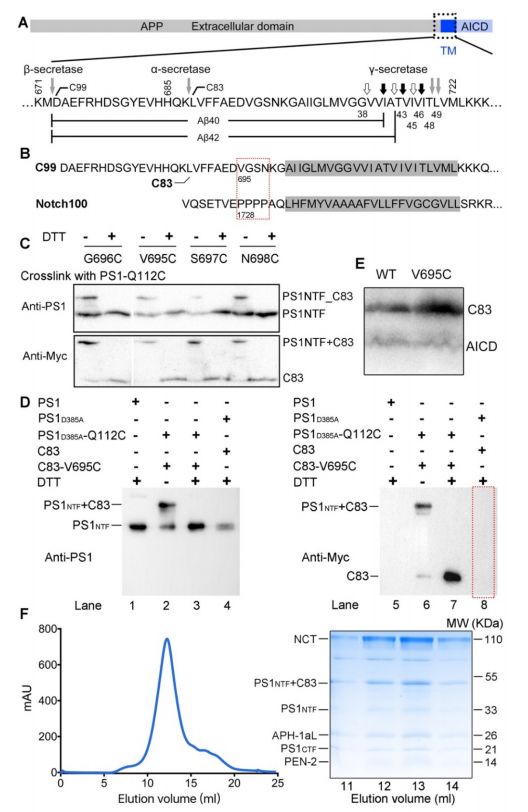
通过在PS1和APP-C83之间形成特定的二硫键产生稳定的γ-分泌酶-APP复合物
人γ-分泌酶包含四个亚基:早老蛋白(PS),PEN-2,APH-1和nicastrin。作为γ-分泌酶的催化亚基,早老素是具有两个催化Asp残基的天冬氨酰蛋白酶,并且具有两种同种型PS1和PS2。在γ-分泌酶组装期间,PS1经历自身蛋白水解以产生氨基末端片段(NTF)和羧基末端片段(CTF)。 PEN-2是γ-分泌酶成熟所必需的; APH-1稳定复合物和nicastrin被认为在底物结合中发挥作用。已经在PS1中鉴定了200多种AD相关突变,其中大多数导致Aβ42/Aβ40比率升高。
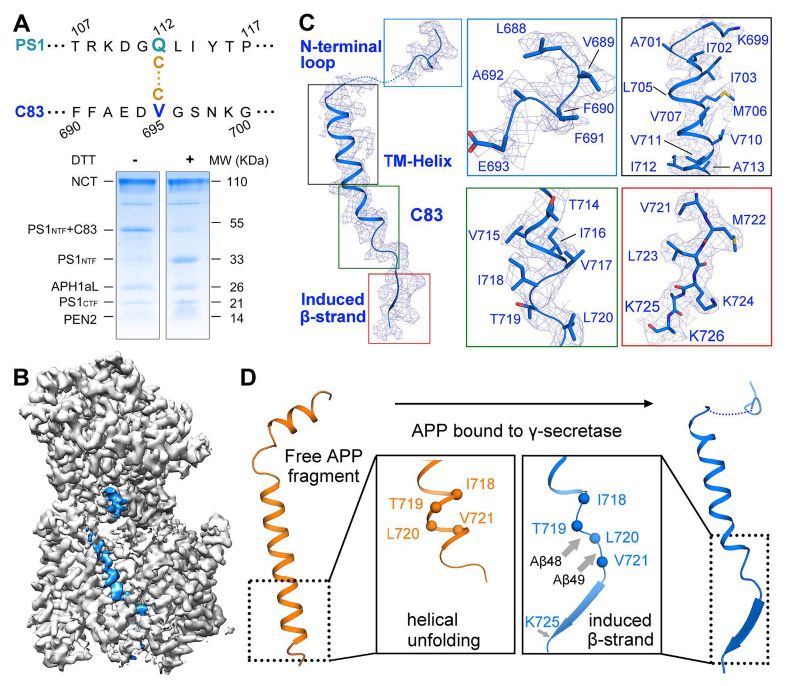
人类γ-分泌酶与跨膜APP片段的复合物的冷冻电子显微镜(cryo-EM)结构
普遍存在的淀粉样蛋白假说假定淀粉样蛋白寡聚体直接促成AD的发展,使γ-分泌酶的抑制成为AD治疗的潜在治疗策略。不幸的是,也许是因为它们也抑制Notch切割,γ-分泌酶*制剂抑**会引起严重的副作用,而对AD患者没有任何明显的临床益处。在这里,施一公报告人类γ-分泌酶与跨膜APP片段的复合物的冷冻电子显微镜(cryo-EM)结构,分辨率达到2.6Å。 PS1和底物之间的β-折叠对于γ-分泌酶的蛋白水解活性是必需的。该结构与γ-分泌酶 - Notch复合物的结构比较揭示了可用于开发底物特异性*制剂抑**的不同特征。

人γ-分泌酶识别APP-C83
与淀粉样蛋白前体蛋白结合的人γ-分泌酶的结构为γ-分泌酶连续底物切割的螺旋解旋模型提供了强有力的支持。 更重要的是,该结构允许通过γ-分泌酶比较APP和Notch识别以及AD相关突变的合理化。 因此,该结构用作发现γ-分泌酶的底物特异性*制剂抑**和理解γ-分泌酶的生物学功能以及AD的疾病机制的重要框架。
原文链接:
http://science.sciencemag.org/content/early/2019/01/08/science.aaw0930?rss=1
8

在1977年,Phillip Sharp和Richard Roberts俩个研究组独立发现了剪切这一过程,紧接着,1979年, Steitz研究组发现五种称为U1,U2,U4,U5和U6 snRNA的富含尿苷的小核RNA(snRNA)和7种12-35kDa的蛋白质(snRNPs)。之后, Steitz等研究组发现U1 snRNA的5'末端序列被识别为与5'剪接位点(5'SS)互补,并且snRNP被部分纯化。纯化的U1snRNP在体外特异性结合到5'SS上,并且U1snRNP的消耗抑制了体外剪接。随后,证实了多个snRNPs参与前mRNA剪接。

施一公
剪接测定的发展使得剪切反应的描绘成为可能。 发现ATP和镁(Mg2 +)对于腺病毒前体mRNA的体外剪接是必不可少的。 通过分支点序列(BPS)中的腺苷核苷酸和5'SS的5'末端的鸟嘌呤核苷酸之间的连接形成内含子套索结构,得到了生物化学证实。
前体mRNA剪接是由剪接体催化的,剪接体是一种高度动态和复杂的分子机器,它含有前体mRNA,U1,U2,U4 / U6和U5 snRNPs以及许多非snRNP蛋白。 U1和U2 snRNP分别与内含子的5'剪接位点(ss)和分支位点(BS)相互作用,同时为U4 / U6.U5 tri-snRNP的稳定整合铺平了道路,产生了剪接体B复合物。然而,尽管tri-snRNP引入了必需的催化组分,但是剪接体B复合物仍然需要转化成催化活性复合物,这一过程需要广泛的结构重排。通过解开U4 snRNA的U4 / U6双链体(通过RNA解旋酶Brr2)启动活化, U6随后与U2(U2 / U6螺旋Ia和螺旋Ib)以及内部茎环(U6 ISL)自由地形成短双链体。最终在剪接体激活期间建立的催化RNA-RNA网络与II组自我剪接内含子的催化核心非常相似。

剪切过程
随后通过RNA解旋酶PRP2将所得的活化的但是预催化的B(Bact)复合物转化为催化剪接体(命名为B *)。在人类中,B-to-B *转换也需要AQR RNA解旋酶的ATP酶活性,这在酵母酿酒酵母的剪接体中是不存在的。这表明人类剪接体中催化活化所需的构象重排比酵母中的那些更复杂。 B *复合物催化剪切的第一步,产生切割的5'外显子和内含子3'外显子套索中间体,产生剪接体C复合物。额外的RNP重排将C复合物转化为C *复合物,然后催化第二步剪接,并且5'和3'外显子的连接形成mRNA并释放内含子作为套索。
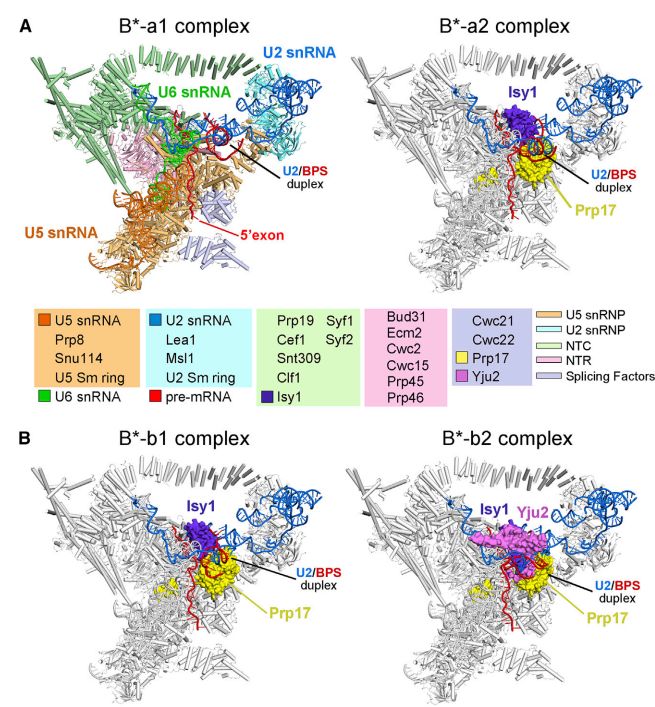
来自酿酒酵母的催化活化的剪接体(B *复合物)的冷冻电子显微镜结构
2015年,通过单粒子冷冻电子显微镜(cryo-EM)分析确定剪接体的第一个近原子分辨率结构,报道了来自S. pombe的ILS复合物。从那时起,已经阐明了13种冷冻-EM结构,大部分分辨率在3.3和5.8之间,已经阐明了来自酿酒酵母的组装剪接体的七种不同状态,人类剪接体的7种不同状态的11种这样的结构。在剪接体的八种已知功能状态中,仅B *复合物在结构上保持未表征。
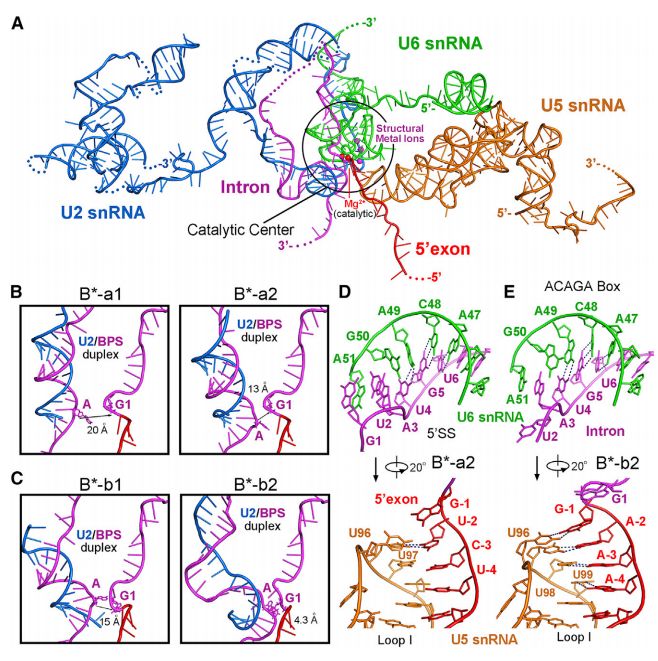
酿酒酵母B *复合物中的RNA元件
在这项研究中,研究人员报告了来自酿酒酵母的B *复合物的冷冻-EM结构。该研究得到了酿酒酵母的两种不同前mRNA上组装了B *复合物,并确定了四种不同B *复合物的冷冻EM结构,总分辨率为2.9-3.8Å。 U2核小RNA(snRNA)和分支点序列(BPS)之间的双链离散地远离5个B *复合物中的5'-剪接位点(5'SS),其缺乏步骤I剪接因子Yju2和Cwc25。 将Yju2募集到活性位点使U2 / BPS双链体进入5'SS附近,BPS亲核试剂位于距催化金属M24Å处。
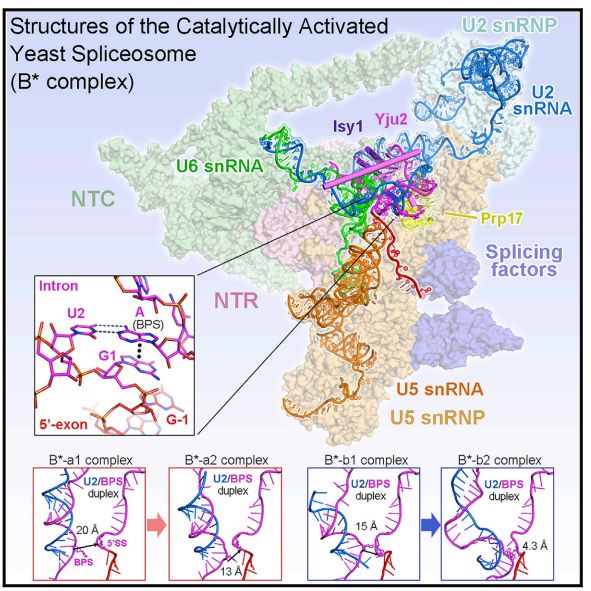
结构总结
该分析揭示了Yju2和Cwc25在分支中的功能机制。 不同前mRNA上的这些结构揭示了在主要功能状态下剪接体的底物特异性构象。这些构象状态的比较揭示了对支化反应的机理见解。
9/10



植物也有一系列防御机制,如抗性基因(R基因)介导的疾病抗性。R蛋白在病原体感染后被激活介导效应子触发的免疫(ETI)并导致局部程序性细胞死亡,称为过敏反应(HR)(见下图)。根据结构域组成,R基因至少可被分为五组。其中,含有核苷酸结合位点(NBS)和C末端富含亮氨酸的重复结构域(LRR)的NBS-LRR家族是最大的。
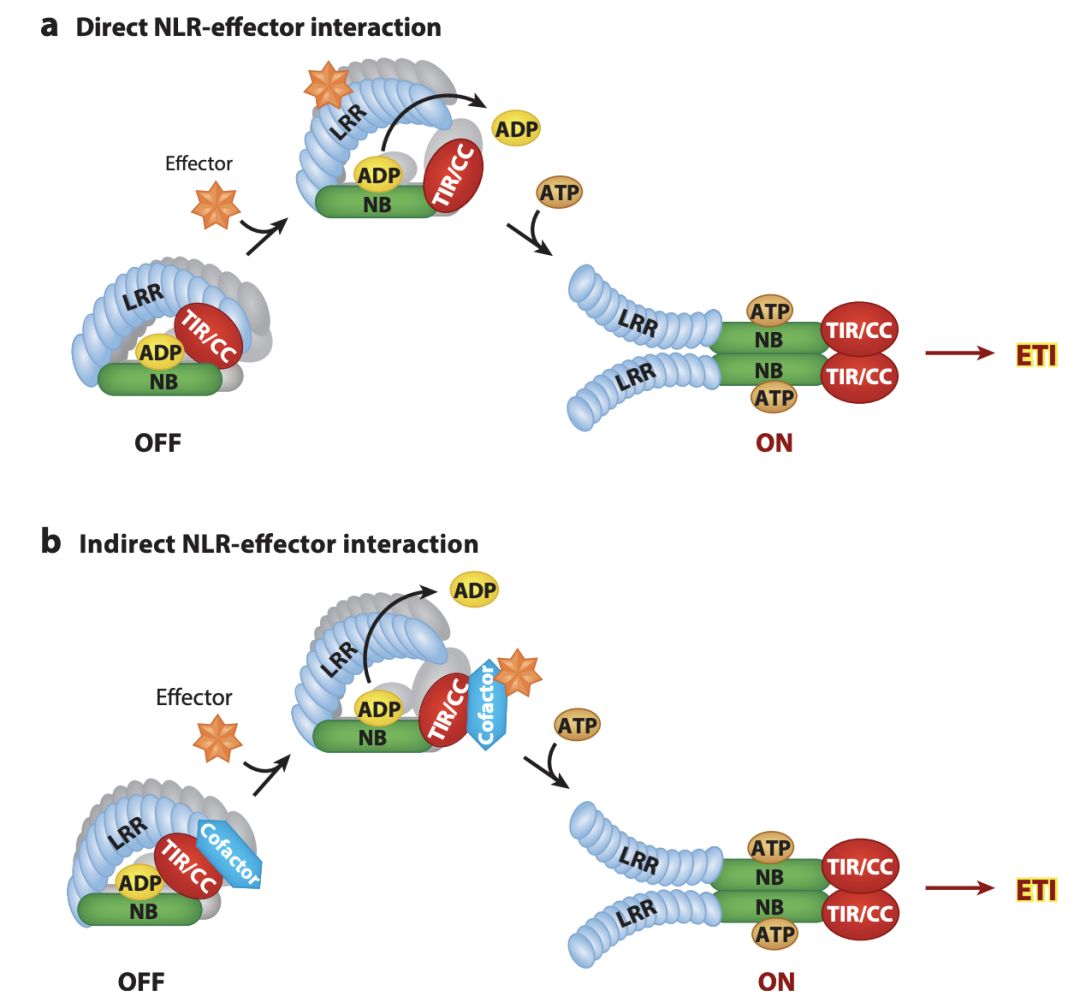
图. NLR-效应子识别模式导致效应子触发的免疫(ETI)
早在2015年,来自中科院遗传发育所的周俭民课题组在Cell Host & Microbe杂志上发表题为“The Decoy Substrate of a Pathogen Effector and aPseudokinase Specify Pathogen-Induced ModifiedSelf Recognition and Immunity in Plants”的研究论文,该研究表明激酶PBL2能被来自Xanthomonas 的效应蛋白AvrAC尿甘化后触发免疫。因此,PBL2是充当诱饵并用来检测AvrAC。同时AvrAC的识别还需要ZRK家族的RKS1假激酶和NOD样受体ZAR1。此外,ZAR1与RKS1形成稳定的复合物,当PBL2被AvrAC尿苷酰化时,其特异性地被募集,触发ZAR1介导的免疫(如下图)。
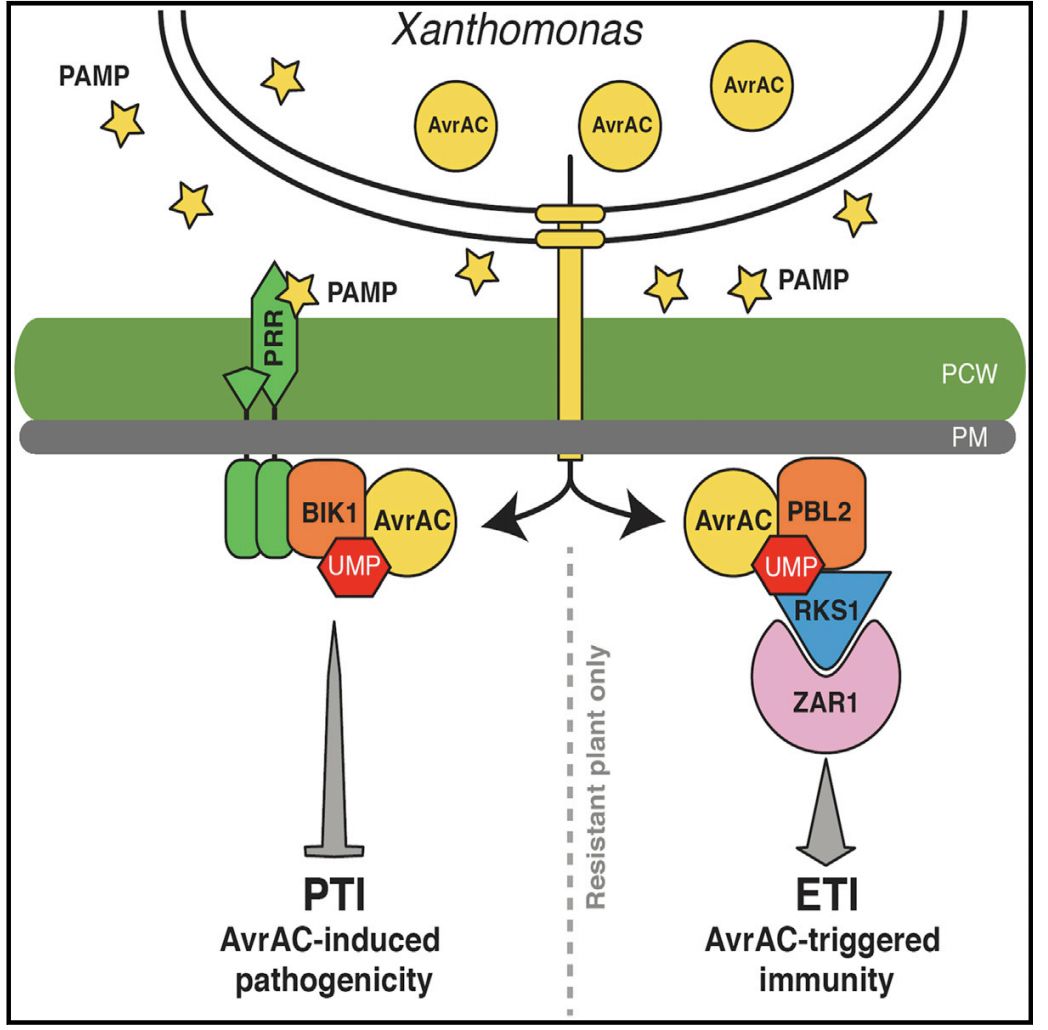
图. AvrAC被识别和起始ETI免疫的模型
然而,上述研究中,仍然具有很多问题需要解决,如PBL2如何激活ZAR1-RKS1复合体的机制不太清楚,同时NLR的ADP-和ATP-结合形式分别对应于“关闭”和“开启”状态,但是ADP如何从NLR释放以与ATP交换的机制仍然难以捉摸。此外,植物NLR在活化后如何寡聚化成大蛋白复合物仍然是未知的 。
在第一项研究中,研究者在共同表达了ZAR1与RKS1,并解析了其复合体在ADP结合状态下的冷冻电镜结构。这一代表ZAR1处于“静息状态”的结构表明,RKS1的异二聚体只与ZAR1的富亮氨酸重复(LRR)结构域进行结合,而对这种结合起到关键作用的氨基酸在同一家族中趋于保守。
随后,研究人员们在这个复合体中引入了单尿苷酰修饰(mono-uridylylated)的PBL2,并发现它与RKS1的结合会造成构象的显著变化,将ADP排出ATP结合位点。在没有ATP存在的情况下,这一复合体能处于激活的过渡状态。因此,该研究揭示了ZAR1-RKS1识别PBL2UMP和PBL2UMP激活ZAR1的机制。
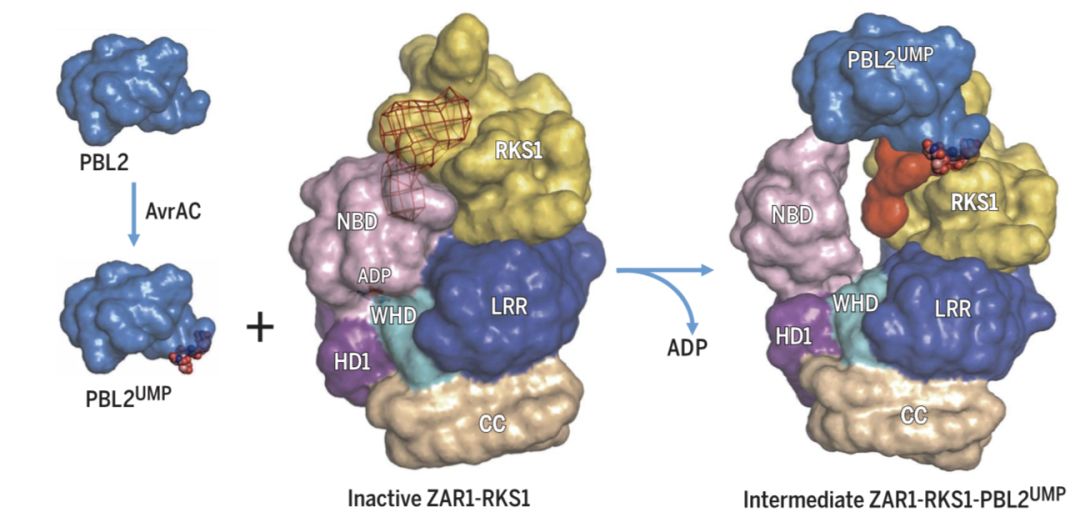
在第二项研究中,研究者又往ZAR1-RKS1-PBL2(有单尿苷酰修饰)的复合体中添加了dATP,并获取了冷冻电镜结构。有趣的是,在dATP的作用下,这一复合体会进一步形成五聚体。研究人员们发现,这种五聚体的氨基端会微微翘起,形成一个漏斗状的结构。他们猜测,这一结构可能会在细胞膜上制造孔洞,协助ZAR1行使其功能。当然,这一猜想还有待进一步的证实。因此,该研究证明了植物中的NLR在免疫激活过程中类似动物中的NLR进行多聚化。
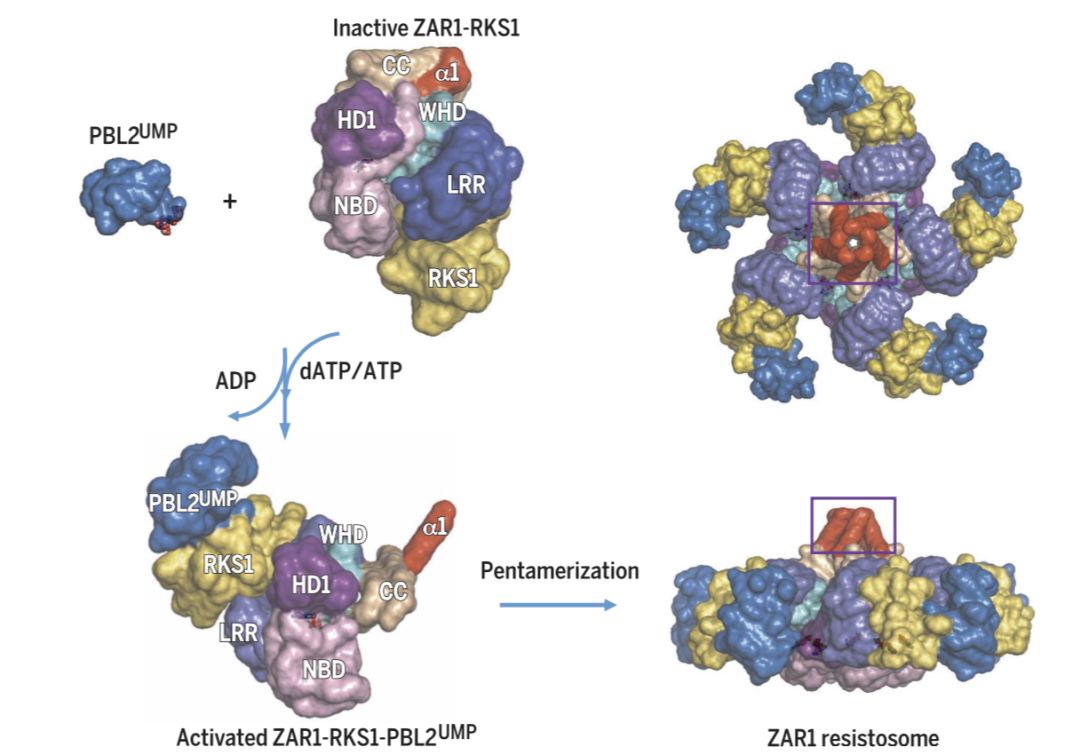
综上所述,这两项研究成功地组装了ZAR1-RKS1-PBL2UMP复合物(抗病小体),阐明了抗病蛋白从静息状态经过中间状态最终形成抗病小体的生化过程,揭示了抗病小体的工作机制。抗病小体具有重新调动防御系统的能力,并在植物细胞膜上发出自杀指令,让受到感染的植物细胞与细菌同归于尽,从而保护其它健康细胞。该项工作填补了人们25年来对抗病蛋白认知的空白,为研究其它抗病蛋白提供了范本。研究还发现,植物抗病小体的组装方式、结构与功能,与动物免疫中的炎症小体有着惊人的相似,展现了在不同生命形式中,进化对免疫形成的力量。

原文链接:
Jizong Wang et al., (2019), Ligand-triggered allosteric ADP release primes a plant NLR complex, Science, DOI: 10.1126/science.aav5868
Jizong Wang et al., (2019), Reconstitution and structure of a plant NLR resistosome conferring immunity, Science, DOI: 10.1126/science.aav5870
11

长春花RLK1样(CrRLK1L)家族的受体激酶(RKs)已成为植物繁殖,生长和对环境反应的重要调节因子。内源性快速碱化因子(RALF)肽已被提议作为几种CrRLK1L成员的配体。然而,这种看法的机制是未知的。
在这里,研究人员报道RALF23诱导CrRLK1L FERONIA(FER)和LORELEI(LRE)-LIKE GLYCOSYLPHOSPHATIDYLINOSITOL(GPI)-ACHORED PROTEIN 1(LLG1)之间的复合物以调节免疫信号。结构和生化数据表明,对RALF23反应具有遗传重要性的LLG1或相关的LLG2直接结合RALF23以使RALF23-LLG1 / 2-FER复合物组装成核。RALF23的保守N末端区域足以通过LLG1 / 2/3进行生化识别,并且结合分析表明,可以以类似方式感知共享该保守N末端区域的其他RALF。结构数据还显示RALF23识别由LLG1 / 2/3的构象灵活的C-末端侧控制。
该研究工作揭示了GPI锚定蛋白与植物遗传学上不相关的RK一致的植物肽感知的意外机制,这提供了一个分子框架,通过CrRLK1L RK和GPI锚定 的LRE / LLG家族蛋白质之间的不同异源复合物的感知,提供了一种分子框架来理解RALF多肽如何调节多个过程。
参考信息:
https://www.nature.com/articles/s41586-019-1409-7
12

L型氨基酸转运蛋白1(LAT1;也称为SLC7A5)以钠和pH非依赖性方式催化大的中性氨基酸的跨膜转运。 LAT1是氨基酸 - 多胺 - 有机超家族的反向转运蛋白,它还催化甲状腺激素,药物和激素前体如L-3,4-二羟基苯丙氨酸穿过膜的渗透。已经在广泛的肿瘤细胞中观察到LAT1的过表达,因此它是抗癌药物的潜在靶标。
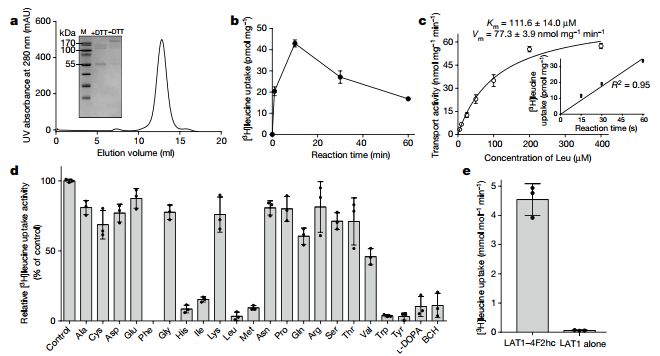
体外表征LAT1-4F2hc复合物的转运活性
LAT1形成与4F2细胞表面抗原的重链异聚氨基酸转运复合物(4F2hc;也称为SLC3A2)-a II型膜糖蛋白,其用于LAT1的稳定性必不可少的。尽管对LAT1-4F2hc复合物进行了广泛的研究,并对细菌中的同源物进行了结构测定,但LAT1和4F2hc之间的相互作用以及该复合物的工作机制仍然很大程度上未知。
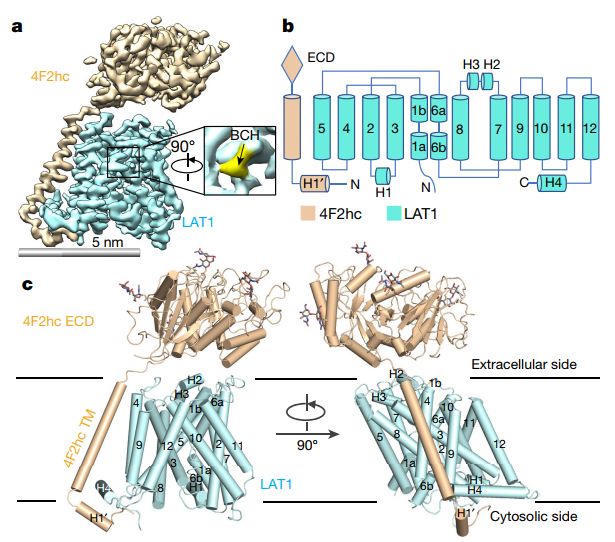
人源LAT1-4F2hc复合物的结构
在这里,研究人员报告了人源LAT1-4F2hc的单独及LAT1-4F2hc与*制剂抑**2-氨基-2-降冰片烷羧酸复合的冷冻电子显微镜结构,其分辨率分别为3.3Å和3.5Å。 LAT1表现出向内开放的构象。除了二硫键结合外,LAT1还在细胞外侧,膜内和细胞内侧与4F2hc广泛相互作用。
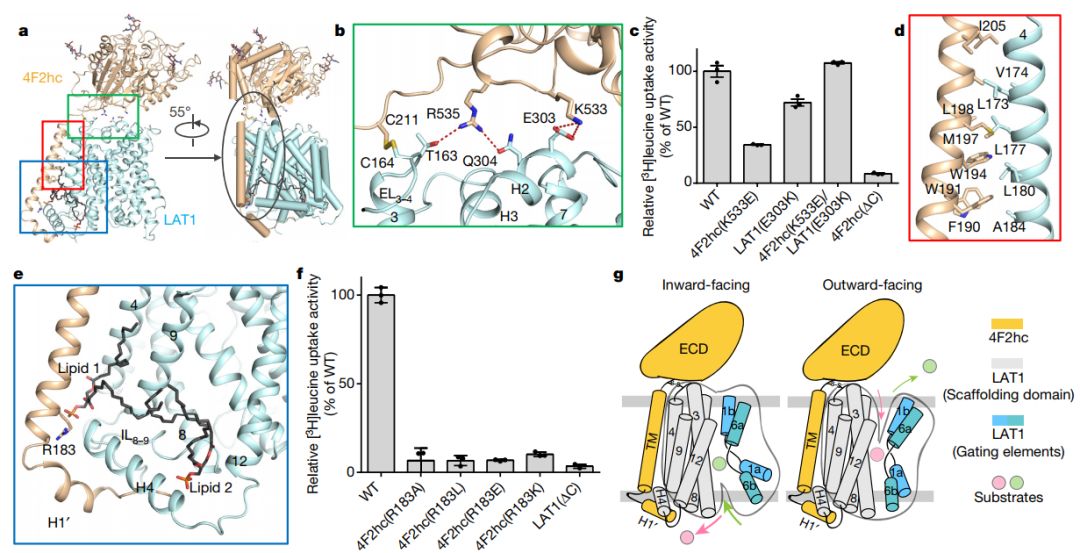
4F2hc和LAT1之间的相互作用
生化分析表明4F2hc对于复合物的转运活性至关重要。总之,该研究阐明了LAT1-4F2hc复合体的结构,并提供了对其功能及其可能与疾病相关的机制的见解。
参考消息:
https://www.nature.com/articles/s41586-019-1011-z