整理:肿瘤资讯
来源:肿瘤资讯
晚期三阴性乳腺癌(mTNBC)患者预后较差,主要的治疗方案为化疗,白蛋白紫杉醇——凯素(Abraxane®)单药一线治疗是国内外指南推荐的一线治疗方案。近年来,免疫治疗在mTNBC患者中开展了多项研究,在既往I期研究中观察到免疫检查点*制剂抑**Atezolizumab单药治疗的初步疗效,但疗效有限,有待进一步提高。临床前和IB期临床研究提示,白蛋白紫杉醇联合Atezolizumab具有协同作用,相比于单药,疗效更优。在近期落幕的2018年ESMO大会主席论坛上报道了III期IMpassion130研究结果,进一步证实了白蛋白紫杉醇联合Atezolizumab的协同作用。目前,白蛋白紫杉醇已经成为免疫治疗的最佳拍档,联合免疫治疗在晚期肺鳞癌中也取得了显著的疗效,并于近期获批用于晚期肺鳞癌一线治疗。
TNBC接受免疫检查点*制剂抑**Atezolizumab单药治疗,疗效有待提高
TNBC是指一类ER、PR和HER2均不表达的乳腺癌,约占乳腺癌总体人群的10%-17%。化疗是TNBC最主要的系统性治疗方案,国际指南推荐单药紫杉类或蒽环类作为mTNBC的一线治疗。近年来,随着对TNBC患者分子生物学研究的不断深入和新药的发展,针对晚期TNBC患者开展了多项新药探索,包括PARP*制剂抑**、PI3K/AKT/mTOR通路*制剂抑**、雄激素受体拮抗剂、免疫治疗等。在TNBC患者中,PD-L1表达主要见于肿瘤浸润淋巴细胞而非肿瘤细胞,可以抑制抗肿瘤免疫。因此,抗PD-1/L1治疗可能是一个有效的治疗策略。Atezolizumab单药在人体的第一个临床研究PCD4989g中,入组了mTNBC患者队列,评估了Atezolizumab治疗mTNBC的安全性和疗效。I期研究中,115例可进行ORR评估。RECIST评估的ORR为10%,接受Atezolizumab一线和二线及以上治疗的患者,ORR分别为24%和6%。在总体人群中,RECIST评估的mPFS为1.4个月;中位OS为8.9个月,1年、2年和3年的OS率分别为41%、19%和16%。总体而言,Atezolizumab单药mTNBC患者的疗效有限,免疫联合治疗模式有望改善mTNBC的ORR和OS。
白蛋白紫杉醇——凯素(Abraxane®),治疗三阴性乳腺癌的骨架药物
目前,国内外开展了多项关于mTNBC化疗的研究。其中值得一提的是白蛋白紫杉醇用于mTNBC的tnAcity研究,这一随机II期研究评估了以白蛋白紫杉醇为基础的联合方案治疗mTNBC一线治疗。入组患者随机分为白蛋白紫杉醇联合卡铂、白蛋白紫杉醇联合吉西他滨和吉西他滨联合卡铂三组。研究结果显示,白蛋白紫杉醇联合卡铂组所取得的PFS最长(mPFS分别为7.4个月,5.4个月,6.0个月),且风险-获益比最佳。目前,在TNBC一线治疗和新辅助治疗中,白蛋白紫杉醇已经逐渐成为化疗和新药联合应用的骨架药物。
由复旦大学附属肿瘤医院胡夕春教授牵头的CBCSG006研究,证实了GP方案治疗mTNBC的疗效,为国际乳腺癌的诊疗增加了“中国数据”。为了优化TNBC化疗方案,GAP研究(CBCSG018)顺势而出,研究旨在对比白蛋白紫杉醇联合顺铂和吉西他滨联合顺铂的疗效,研究结果值得期待。
IMpassion130研究:Atezolizumab联合白蛋白紫杉醇治疗mTNBC,疗效显著提高
在近期ESMO大会上重磅发布的IMpassion130研究中,评估了Atezolizumab联合白蛋白紫杉醇Abraxane®治疗mTNBC。主要终点为研究者评估的PFS和OS,包括ITT人群和PD-L1>=1%患者亚组。
研究共入组902例患者,入组患者1:1随机分配接受Atezolizumab联合白蛋白紫杉醇或安慰剂联合白蛋白紫杉醇,每组各分配451例患者,定义为ITT人群。PD-L1阳性亚组患者占369例(40.9%,其中Atezolizumab联合白蛋白紫杉醇组和安慰剂联合白蛋白紫杉醇组分别为185例和184例)。结果显示,在ITT人群中,Atezolizumab联合白蛋白紫杉醇组对比安慰剂联合白蛋白紫杉醇组,显著延长PFS,mPFS分别为7.2个月和5.5个月,见图A。在PD-L1阳性亚组中,Atezolizumab联合白蛋白紫杉醇组对比安慰剂联合白蛋白紫杉醇组,同样观察到显著更低的进展或死亡风险,mPFS分别为7.5个月 vs 5.0个月,见图B。此外,在大多数亚组患者中,Atezolizumab联合白蛋白紫杉醇组的PFS显著更优。

图A. ITT人群中,两组PFS对比
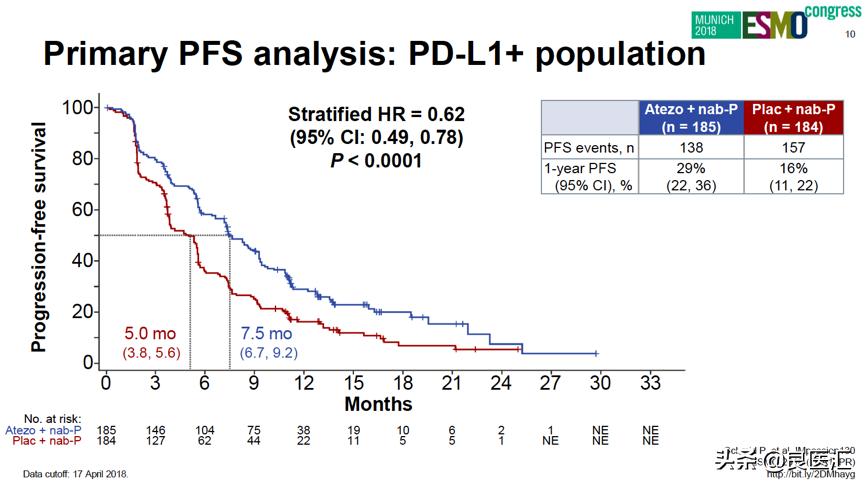
图B. PD-L1阳性患者中,两组PFS对比
在ITT人群中,Atezolizumab联合白蛋白紫杉醇组和单用白蛋白紫杉醇组的ORR分别为56.0%和45.9%,mDOR分别为7.4个月和5.6个月;在PD-L1亚组中,两组的ORR分别为58.9%和42.6%,mDOR分别为8.5个月和5.5个月,见下图2。IMpassion130研究结果证实,Atezolizumab联合白蛋白紫杉醇,可以显著改善Atezolizumab单药治疗疗效,在PD-L1阳性患者中,获益更显著。
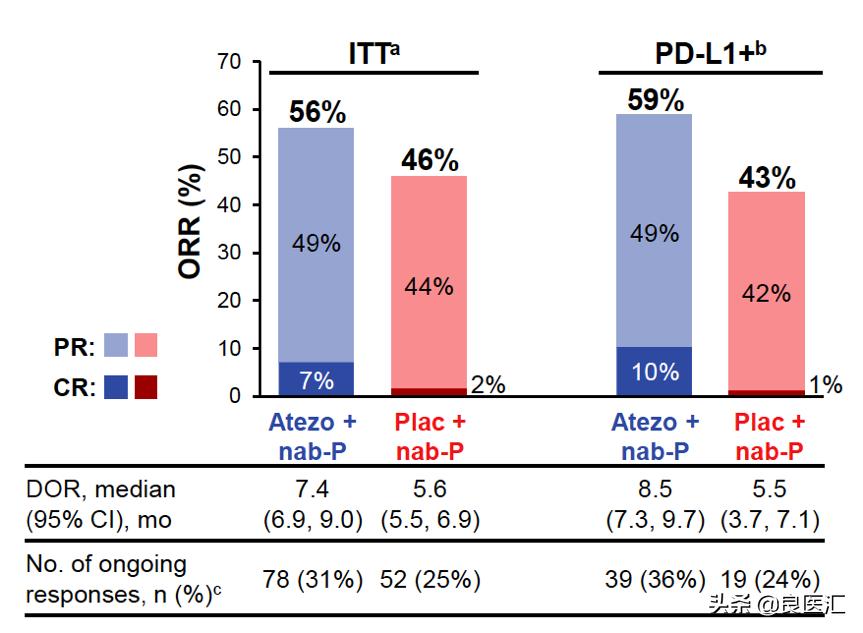
图2. ITT人群和PD-L1阳性患者中,两组ORR对比
白蛋白紫杉醇——凯素(Abraxane®),免疫治疗联合的最佳伴侣
在使用免疫检查点*制剂抑**时,可能需要其他药物来帮助引爆免疫系统,提高治疗疗效。虽然很多化疗药物具有免疫抑制作用,但仍有一些化疗药物具有引爆宿主免疫系统的作用,激发抗肿瘤T细胞反应。紫杉类是实体瘤常用的化疗药物,适用于乳腺癌、肺癌、胰腺癌等多个瘤种。紫杉类药物通过稳定微管蛋白抑制细胞分裂起作用,同时具有脂多糖模拟物作用,可以激发巨噬细胞介导的肿瘤细胞*伤杀**作用。紫杉类还可能可以引发长期的免疫活化效应,增加肿瘤浸润淋巴细胞(TILs);在乳腺癌中,TILs增高与化疗更好的疗效相关。此外,紫杉类药物还是较强的免疫活化剂,可以激活CD8+T细胞,降低免疫抑制细胞,如调节性T细胞作用。在晚期乳腺癌中,紫杉类药物治疗还可以通过增加自然*伤杀**细胞活性或抑制骨髓起源的抑制细胞实现抗肿瘤效应。紫杉类药物可以调节免疫系统的多个功能,包括招募淋巴细胞、促进免疫增强的细胞因子释放,如IL-12、IFNΥ、TNFα和GMCSF,这些都有可能增加免疫治疗的抗肿瘤活性。
在包括乳腺癌在内的IB期研究中发现,Atezolizumab介导的免疫治疗效应并不会被同时使用的白蛋白紫杉醇抵消。在IMpassion130研究设计时,一些回顾性研究结果提示,紫杉醇治疗时使用的糖皮质激素预处理,可能会影响免疫治疗的抗肿瘤疗效。白蛋白紫杉醇则可以克服这一困境,既不需要使用激素,同时具备调节免疫的功能,因此在IMpassion130研究中,选择白蛋白紫杉醇作为联合伴侣,并成功取得阳性结果,较Atezolizumab单药显著提高疗效。
多项免疫联合白蛋白紫杉醇的研究正在开展
目前乳腺癌免疫治疗的研究正如火如荼开展。其中,免疫治疗联合白蛋白紫杉醇的研究众多,总结见下表。
表1. 抗PD-1单抗联合白蛋白紫杉醇正在进行的研究
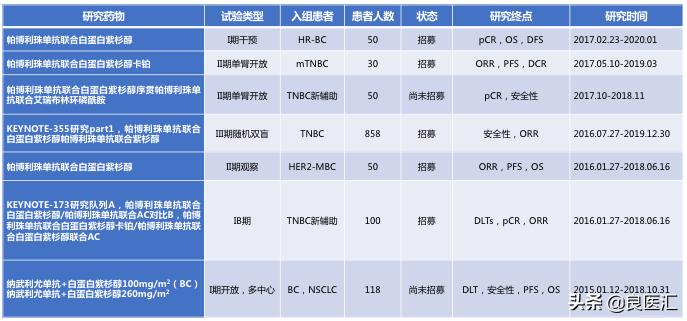
表2. 抗PD-L1单抗联合白蛋白紫杉醇正在进行的研究
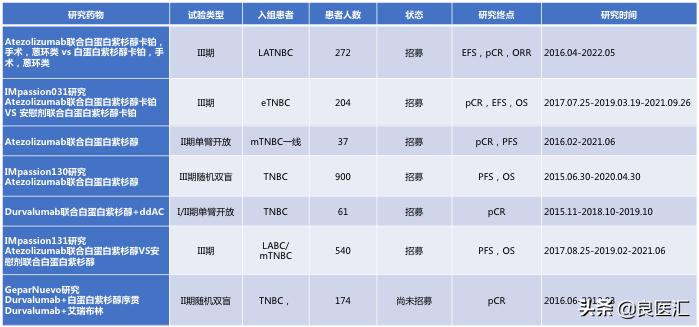
总结
白蛋白结合型紫杉醇以纳米微粒白蛋白为载体,改变了助溶剂,相比于传统紫杉类药物,提高疗效的同时亦减轻了毒性。目前,白蛋白紫杉醇已经成为TNBC化疗的基石类药物。基础研究显示,白蛋白紫杉醇与免疫治疗联合,具有协同作用机理,且白蛋白治疗前,无需常规使用激素,不会降低免疫治疗的疗效。IMpassion130研究从临床研究角度,进一步证实了免疫治疗联合白蛋白紫杉醇的卓越疗效,为TNBC一线治疗带来新选择。目前,多项白蛋白紫杉醇联合免疫治疗的研究正在开展,白蛋白紫杉醇作为免疫治疗最佳联合伴侣,正在乳腺癌患者治疗中书写新的历史。此外,白蛋白紫杉醇已经成为免疫治疗的最佳拍档,联合免疫治疗在多个其他瘤种中开展相关研究。以晚期肺鳞癌为例,KEYNOTE-407研究证实了白蛋白紫杉醇联合免疫治疗的显著疗效,并于近期获批用于晚期肺鳞癌一线治疗。
参考文献
1. Long-term Clinical Outcomes and Biomarker Analyses of Atezolizumab Therapy for Patients With Metastatic Triple-Negative Breast Cancer. JAMA Oncol. doi:10.1001/jamaoncol.2018.4224 Published online September 2018.
2. Atezolizumab and Nab-Paclitaxel in Advanced Triple-Negative Breast Cancer. This article was published on October 20, 2018, at NEJM.org.
3. nab-Paclitaxel Plus Carboplatin or Gemcitabine vs Gemcitabine Plus Carboplatin as First-Line Treatment for Patients With Triple-Negative Metastatic Breast Cancer: Results From the tnAcity Trial. Ann Oncol. 2018 Aug 1;29(8):1763-1770.
版权声明
版权属肿瘤资讯所有。欢迎个人转发分享,其他任何媒体、网站如需转载或引用本网版权所有内容,须获得授权,且在醒目位置处注明“转自:良医汇-肿瘤医生APP”。