体外诊断医疗器械法规(IVDR) 于2017年5月5日正式发布,并 于2022年5月26日实施。 自实施之日起, IVDR将取代原体外诊断医疗器械指令(IVDD)。
在IVDR法规中第10条第8点对质量管理体系提出了明确要求: 制造商应确保采取必要流程,使系列产品的生产符合本法规的要求。
应及时充分考虑产品设计或特性的更改和协调标准或产品符合性所声明的CS的更改。以与风险等级和器械类型成正比例的方式,器械(非性能研究用途器械)制造商应以最有效的方式确立、记录、实现、维护、不断更新和不断改善一个能确保器械符合本法规规定的质量管理体系。
其中, 质量管理体系应至少包括以下方面:
1、法规符合性战略,包括符合性评估流程的遵守和系统所涵盖的器械的变更管理
2、确定适用的通用安全与性能要求,寻找满足这些要求的选项
3、管理职责
4、资源管理,包括选择和管理供应商和分包商
5、风险管理
6、性能评估,根据第56条和附录XIII的规定,包括上市后的PMPF
7、产品实现,包括策划、设计、研发、生产和服务提供
8、UDI,验证所有相关器械的UDI分配,并确保根据第26条提供的信息一致性和有效性;
9、上市后监督系统,建立、实施和维护上市后监管体系;
10、与主管机构、公告机构、其他经济运营商、客户和/或其他利益相关人沟通
11、事故报告&FSCA:警戒情况下的严重事件和现场安全纠正措施的报告流程
12、CAPA管理:纠正措施和预防措施的管理及其有效性的验证
13、监视和测量:产品、数据分析和产品改进的监督和评估流程

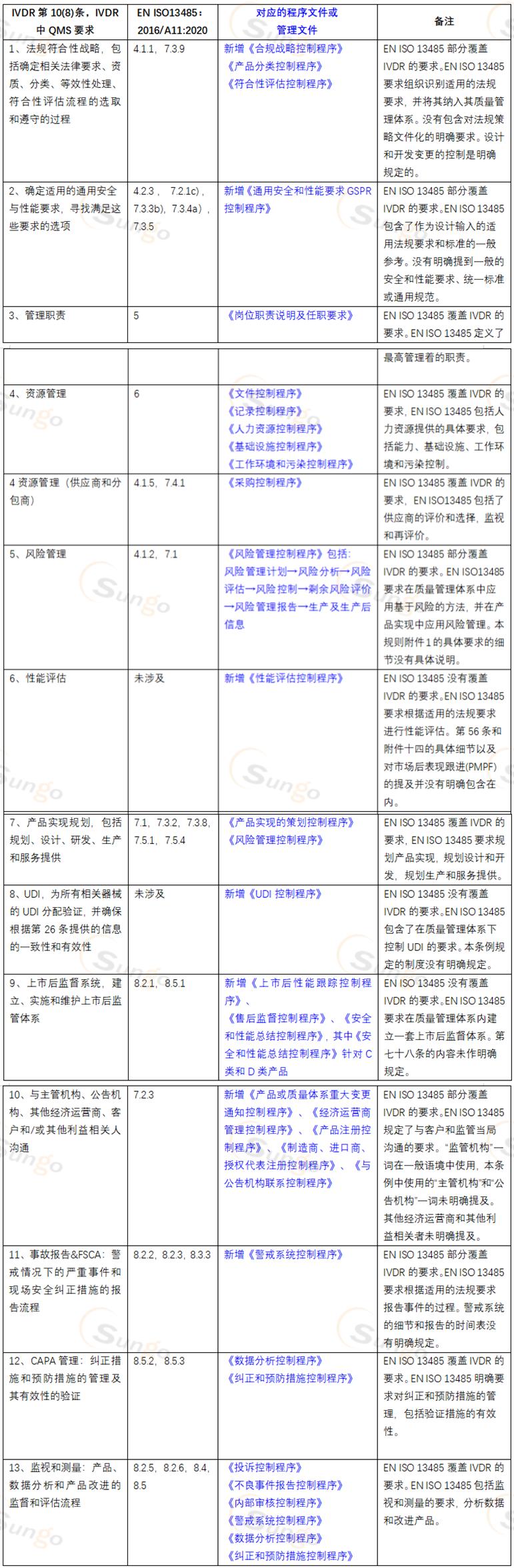
我们结合EN ISO13485:2016/A11:2021及IVDR法规要求,对IVDR下质量管理体系管控进行了梳理,具体要求如下:
在整个IVD领域, 涉及公告机构介入的产品数量从IVDD监管体系下的0%~20%增加至80%~90%。
随着公告机构介入量的增加, 意味着绝大多数的体外诊断器械,在欧盟的市场准入将要 告别原先“自我宣告”的模式,取而代之的将 是一个实质性的认证过程。
质量管理体系作为认证过程中一个重要考核点, 各大医疗器械注册商都需要积极建立一套符合IVDR法规要求的质量管理体系来应对最新法规的要求。