本文由brainnews脑科学世界团队原创编译,转载请联系授权。
Greengard遗产: 留给后人新的领域去拓展,科学奖与传承
纵观历史长流,科学的发展是由众多很小的发现逐渐累积的。但在这所有的发现中,最重要的是那些突破性的、开启新领域的发现。经济学上有个说法叫帕累托法则(Pareto principle,俗称二八法则),即80%的土地为20%富人所有。科学上也有类似的现象,即80%的大文章由20%的精英科学家发表。在诺贝尔奖获得者中该比例更高。当然,这也会进入一个“富人越来越富”的循环。精英科学家获得更多的资助、招募更优秀的学生、发表更多的文章,这是科学上的马太效应(Matthew Effect in Science)。
不过,精英科学家之所以成为精英科学家,是因为做出了突破性的发现。通常这类开创新领域的发现是以技术突破为主,比如CRISPR基因编辑技术、光遗传学等,其次是概念、认识上的突破。Greengard的研究属于后者,俗称paradigm-shifting(范式转换)的发现。Greengard基本上在每一个方向上的研究都是paradigm-shifting的发现。以磷酸化/去磷酸化化学反应为主的细胞信号通路介导的“神经传递慢反应”,这一Greengard刚建立实验室时提出的观念,从最初被同行嘲笑到现在已经写入教材成为常识性的知识。
神经传递慢反应的“慢”是相对神经传递快反应而言的。从神经递质(如谷氨酸)结合离子型受体,通道打开,离子跨膜传输形成电流,细胞电压变化,整个反应发生在1毫秒之内;而由代谢型受体(比如多巴胺受体)介导的慢反应则耗时几百毫秒,甚至几分钟。但对于化学反应而言,几百毫秒到几分钟的“慢”反应仍然是很“快”的反应,故一开始Greengard的同行都不接受他的观点。
但Greengard的研究为我们开启了全新的一个世界,让我们认识到 这个“慢”的磷酸化/去磷酸化反应下游的多个效应物,包括:
1)离子通道,通过磷酸化修饰改变离子通道传输离子的能力,从而影响电导(G,电阻的倒立1/R,通道打开,电阻下降,电导上升)和动作电位(参考上文);
2)离子泵,在动作电位时,离子顺着细胞内外浓度差传输之后,需要通过离子泵逆浓度差传输回去,恢复浓度差,而对离子泵的磷酸化修饰则可通过改变离子浓度来影响细胞活性;
3)神经递质受体,包括离子型和代谢型受体(快和慢神经传递都受影响),对受体的磷酸化修饰可以一方面直接影响受体活性,另一方面影响受体插入细胞膜和从细胞膜内吞,从而改变受体的多少,两个影响都可改变突触的强弱,即突触可塑性;
4)基因表达,包括对神经递质受体基因表达的影响,从而影响受体的多少。
在调控突触可塑性方面,改变受体活性的影响较快,受体的入膜和内吞的影响较慢持续时间较长,受体基因表达的影响最慢持续时间最长。突触可塑性目前认为是学习和记忆的基础,Greengard 的好友Eric Kandel在这方面有重大贡献。总之,基本上这里提到的每一个研究都是开创一个新的领域。
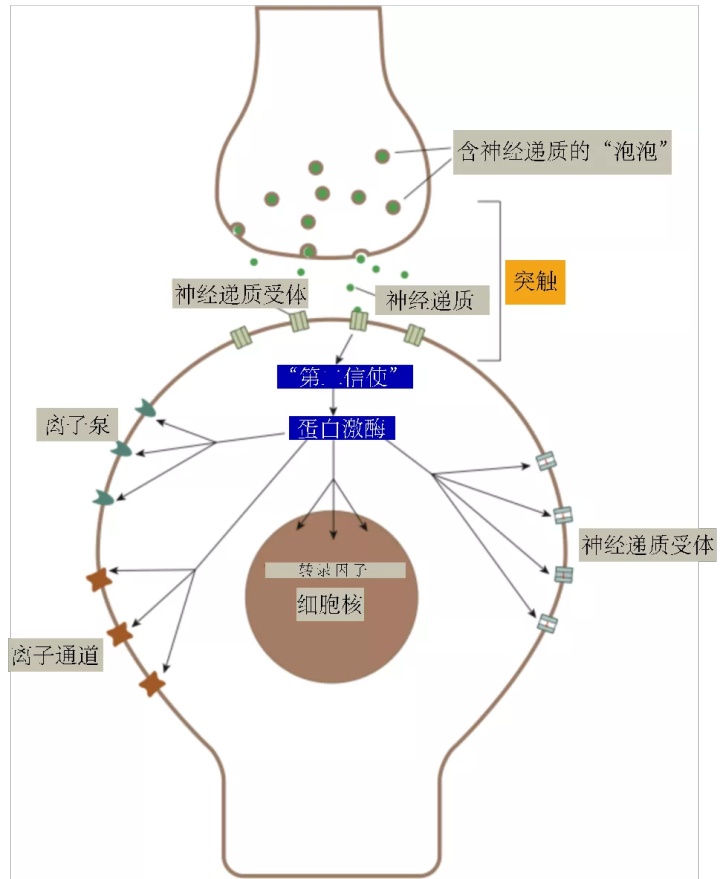
图22. 神经传递慢反应的“第二信使”及下游效应58(作者汉化)。
最终Greengard与发现多巴胺的Carlsson、研究学习和记忆的神经分子机制的Kandel共享了2000年诺贝尔生理学或医学奖。2004年,Greengard将他的诺奖奖金用于成立Pearl Meister Greengard Prize,纪念他因难产而死的母亲。Greengard直到上大学才知道他生母的事情,对于生母Pearl Meister Greengard,他没有任何记忆、照片和信息,他希望这个奖能够证明他母亲的存在。
该奖由洛克菲勒大学每年一次颁发给女性生物学家,用来支持女性科学家。获奖者中已有三人后来获诺贝尔奖,包括去年因CRISPR技术而获诺贝尔化学奖的Jennifer Doudna。获奖者中还有中科大天才班毕业生、著名华人生物物理学家庄小威。今年10月1日,mRNA疫苗技术发明人之一Katalin Karikó也被授予该奖。

图23. 千禧年诺贝尔生理学或医学奖的三位得主。(图片来源自诺奖官网截图)
Greengard的小儿子Leslie有医学和计算机科学双博士学位,两人曾合作建立多巴胺信号通路数学模型59。
Greengard还培养了许多优秀的学生,除了上面提到的,还有Eric Nestler,读博期间主要研究cGMP信号通路和Synapsin I。据Nestler回忆,第一次去找Greengard的时候,秘书叫他敲门然后直接进去。他进去后,只看到两只大哈士奇盯着他,却不见Greengard。原来Greengard躺在办公桌后面的地板上看文献,他背不太好,所以经常是躺地上办公。Nestler现为纽约西奈山医学院的学术院长、脑研究所主任。Greengard后来养了只大伯恩山犬,叫Alpha。当有客人来他办公室的时候,Alpha就会第一个冲过去自我介绍。不熟悉Greengard的人往往会吓一跳。但Alpha很温顺,从来不乱叫。 Greengard的博后Richard Huganir,主要研究cAMP激活的激酶通过磷酸化神经递质受体和离子通道来调控神经细胞活性。在Huganir师从Greengard的第二年,Greengard从耶鲁大学搬到了洛克菲勒大学(Rockefeller)。后来Huganir有了两个孩子,纽约的消费太高,Huganir也想独立做学习和记忆相关的研究,于是Greengard把他推荐给了Synder。Huganir现任约翰斯·霍普金斯大学Solomon Snyder神经科学系系主任。华人神经科学家中,美国凯斯西储大学(Case West Reserve University)神经科学系主任梅林、密西根大学叶冰、香港科技大学夏军、美国国立卫生研究院药物滥用研究所(NIDA)的Da-Ting Lin等均曾师从Huganir。Nestler和Huganir也都曾先后担任神经科学学会SfN主席。 Greengard的博士Marina Picciotto,博士期间克隆了CaMKI基因,现为耶鲁大学教授,主要研究尼古丁成瘾的机制,Picciotto还是神经科学学会会刊 The Journal of Neuroscience 现主编。Greengard的博后、华人科学家Linda C. Hsieh-Wilson研究磷酸化修饰对肌动蛋白、AMPA受体活性和突触可塑性的影响,现为加州理工大学(Caltech)教授,研究蛋白糖基化修饰对神经功能的影响。 博后Mary Kennedy研究CaMKII,现在同为加州理工大学教授,主要研究突触后支架蛋白PSD和突触可塑性。博后Daniele Piomelli同样研究CaMKII,现在为内源性*麻大**素研究领域的领袖。Greengard还培养了很多优秀的科学家,不再一一介绍。 2019年4月13日,Greengard去世,享年93岁。Greengard将一生都奉献给了科研,他没有担任任何系主任、院长等职务,他认为行政工作会影响他对科研的投入(显然,他的两个弟子Nestler和Huganir没有听取他的意见)。Greengard直到去世前仍活跃在实验室,包括晚上和周末,通常是和学生一对一改文章。 写作是科学家的基本技能之一,上文提到的哈佛神经生物学创系主任Kuffler在学术领域涉猎很广,在各方面都有很高成就,只是他的文章笔者读起来感觉有点难,也可能是他的研究本身比较复杂或要传达的信息较多(当然笔者的写作也很糟糕,没有资格去评价像Kuffler这样的大师)。 但他的学生Hubel和Wiesel的文章则简洁、清晰、优美,绝对可以作为学术写作范文来反复阅读(Hubel和Wiesel的文章还有个特点,就是参考文献大部分都是他们自己的文章,这就是耕耘20多年开创一个领域的典型)。不过即便优秀如Hubel和Wiesel,他们最初的写作也曾遭到他们的导师Kuffler的无情摧残60。所以写作是个需要导师指导并勤加练习的技能。 Greengard改文章的风格和他的师爷Brodie颇相似。Brodie通常是晚上八九点约学生来家里改文章,Brodie爱人提供食物,逐字逐句改,查字典,大声朗读,直到每个字都准确,每一句听过去都优美。一对一改文章也是Greengard和学生互相深入了解彼此的最佳时候,基本上是一半工作一半聊天。 Greengard是幽默、笑话、八卦大师,他有时候会和学生挖苦一下竞争对手、为他们的文章被自己超越而感到幸灾乐祸、并自信自己的文章将是篇杰作。他也曾为自己没能共享1994年G蛋白信号通路的诺贝尔奖而悲伤,通常同一类研究不会再给一个奖,不过好在Greengard 的悲伤并没有持续太久,6年后他因慢神经传递的信号传导而获诺奖。 Greengard一直工作到生命的最后一秒,周六早上,在家读文献时突发心脏病去世。这天他原本准备和实验室博后程嘉讨论她的文章。程嘉现为 Cell 杂志编辑,她的博士导师颜震曾经也是Greengard的博后,参与DARPP-32的研究,现为纽约州立大学布法罗分校(SUNY Buffalo)教授。下期会介绍颜震读博期间做的一个结合多巴胺受体和纹状体通路的研究,补齐多巴胺功能的最后一块缺口。
未完待续
现在我们知道多巴胺受体是G蛋白偶联的受体GPCR,一类结合多巴胺后激活神经细胞(一型受体),另一类结合多巴胺后抑制神经细胞(二型受体)。我们也知道纹状体SPN细胞有两条投射通路,一条直接通路促进运动(Go),另一条间接通路抑制运动(NoGo)。那么多巴胺一型/二型受体和直接/间接通路又有什么关系呢,多巴胺如何通过影响直接/间接通路来调控运动?颜震做的研究是什么呢?我们下回分解。
参考文献:
1. Waldeyer W. Ueber einige neuere Forschungen im Gebiete der Anatomie des Zentralnervensystems. Dtsch Med Wochenschr (1891) 17:1213. doi:10.1055/s-0029-1206893
2. Foster M, Sherrington CS: A Textbook of Physiology. 3. The Central Nervous System, ed 7. London, MacMillan, 1897.
3. Bennett MR: The early history of the synapse: from Plato to Sherrington. Brain Res Bull 1999; 50: 95–118.
4. HODGKIN AL, HUXLEY AF, KATZ B. Measurement of current-voltage relations in the membrane of the giant axon of Loligo. J Physiol. 1952 Apr;116(4):424-48. doi: 10.1113/jphysiol.1952.sp004716. PMID: 14946712; PMCID: PMC1392219.
5. HODGKIN AL, HUXLEY AF. Currents carried by sodium and potassium ions through the membrane of the giant axon of Loligo. J Physiol. 1952 Apr;116(4):449-72. doi: 10.1113/jphysiol.1952.sp004717. PMID: 14946713; PMCID: PMC1392213.
6. HODGKIN AL, HUXLEY AF. The components of membrane conductance in the giant axon of Loligo. J Physiol. 1952 Apr;116(4):473-96. doi: 10.1113/jphysiol.1952.sp004718. PMID: 14946714; PMCID: PMC1392209.
7. HODGKIN AL, HUXLEY AF. The dual effect of membrane potential on sodium conductance in the giant axon of Loligo. J Physiol. 1952 Apr;116(4):497-506. doi: 10.1113/jphysiol.1952.sp004719. PMID: 14946715; PMCID: PMC1392212.
8. HODGKIN AL, HUXLEY AF. A quantitative description of membrane current and its application to conduction and excitation in nerve. J Physiol. 1952 Aug;117(4):500-44. doi: 10.1113/jphysiol.1952.sp004764. PMID: 12991237; PMCID: PMC1392413.
9. Dale H.H. and Ewins AJ. (1914) Choline esters and muscarine. Proc. Physiol. Soc. 48,24-25.
10. Dale, H.H. The action of certain esters and ethers of choline, and their relation to muscarine. J. Pharmacol. Enp. Ther., 1914, 6: 147-190.
11. Loewi O: Über humorale Übertragbarkeit der Herznervenwirkung. I. Mittei‐lung. Pflügers Arch Ges Physiol 1921; 189: 239–242
12. Loewi O: Über humorale Übertragbarkeit der Herznervenwirkung. I. Mittei‐lung. Pflügers Arch Ges Physiol 1922; 193:201-213.
13. Dale HH. Otto Loewi, 1873-1961. Biogr. Mems Fell. R. Soc. 8: 67–89
14. Karczmar AG. The Otto Loewi Lecture. Loewi's discovery and the XXI century. Prog Brain Res. 1996;109:1-27, xvii. doi: 10.1016/S0079-6123(08)62084-1. PMID: 9009689.
15. Loewi O. "An Autobiographic Sketch." Perspectives in Biology and Medicine, vol. 4 no. 1, 1960, p. 3-25. Project MUSE, doi:10.1353/pbm.1960.0006.
16. American Chemical Society National Historic Chemical Landmarks. Carl and Gerty Cori and Carbohydrate Metabolism. http://www.acs.org/content/acs/en/education/whatischemistry/landmarks/carbohydratemetabolism.html
17. von Euler U. (1992) Discoveries of Neurotransmitter Agents and Modulators of Neuronal Functions. In: Worden F.G., Swazey J.P., Adelman G. (eds) The Neurosciences: Paths of Discovery, I. Birkhäuser Boston. https://doi.org/10.1007/978-1-4684-6817-5_10
18. Cannon WB. THE ARGUMENT FOR CHEMICAL MEDIATION OF NERVE IMPULSES. Science. 1939 Dec 8;90(2345):521-7. doi: 10.1126/science.90.2345.521. PMID: 17819668.
19. Brooks CM, Eccles JC. An electrical model of central inhibition. Nature, 159, 760-764, 1947.
20. Eccles JC. The synapse: from electrical to chemical transmission. Annu Rev Neurosci. 1982;5:325-39. doi: 10.1146/annurev.ne.05.030182.001545. PMID: 6122420.
21. Carlsson A. Treatment of Parkinson's with L-DOPA. The early discovery phase, and a comment on current problems. J Neural Transm (Vienna). 2002 May;109(5-6):777-87. doi: 10.1007/s007020200064. PMID: 12111467.
22. Barger G, Dale HH. Chemical structure and sympathomimetic action of amines. J Physiol. 1910 Oct 11;41(1-2):19-59. doi: 10.1113/jphysiol.1910.sp001392. PMID: 16993040; PMCID: PMC1513032.
23. BARGER, G. & EWINS, A.J. Some phenolic derivatives of β-phenylethylamine. J. chem. Soc., 1910; 97, 2253–2261.
24. Mannich, C. and Jacobsohn, W. Über Oxyphenyl-alkylamine und Dioxyphenylalkylamine. Ber.Deut.Chem.Ges., 1910; 43, 189-197
25. Blaschko, H. K. F. (1985). Ulf Svante von Euler. 7 February 1905-10 March 1983. Biographical Memoirs of Fellows of the Royal Society, 31, 145–170.
26. Sir Bernard Katz. The History of Neuroscience in Autobiography. SfN.
27. BROCK LG, COOMBS JS, ECCLES JC. The recording of potentials from motoneurones with an intracellular electrode. J Physiol. 1952 Aug;117(4):431-60. doi: 10.1113/jphysiol.1952.sp004759. PMID: 12991232; PMCID: PMC1392415.
28. Langer SZ, Pinto JE. Possible involvement of a transmitter different from norepinephrine in the residual responses to nerve stimulation of the cat nictitating membrane after pretreatment with reserpine. J Pharmacol Exp Ther. 1976 Mar;196(3):697-713. PMID: 4607.
29. Sulzer D, Joyce MP, Lin L, Geldwert D, Haber SN, Hattori T, Rayport S. Dopamine neurons make glutamatergic synapses in vitro. J Neurosci. 1998 Jun 15;18(12):4588-602. doi: 10.1523/JNEUROSCI.18-12-04588.1998. PMID: 9614234; PMCID: PMC6792695.
30. Tritsch NX, Ding JB, Sabatini BL. Dopaminergic neurons inhibit striatal output through non-canonical release of GABA. Nature. 2012 Oct 11;490(7419):262-6. doi: 10.1038/nature11466. Epub 2012 Oct 3. PMID: 23034651; PMCID: PMC3944587.
31. Kim JI, Ganesan S, Luo SX, Wu YW, Park E, Huang EJ, Chen L, Ding JB. Aldehyde dehydrogenase 1a1 mediates a GABA synthesis pathway in midbrain dopaminergic neurons. Science. 2015 Oct 2;350(6256):102-6. doi: 10.1126/science.aac4690. PMID: 26430123; PMCID: PMC4725325.
32. Ren J, Qin C, Hu F, Tan J, Qiu L, Zhao S, Feng G, Luo M. Habenula "cholinergic" neurons co-release glutamate and acetylcholine and activate postsynaptic neurons via distinct transmission modes. Neuron. 2011 Feb 10;69(3):445-52. doi: 10.1016/j.neuron.2010.12.038. PMID: 21315256.
33. Liu Z, Zhou J, Li Y, Hu F, Lu Y, Ma M, Feng Q, Zhang JE, Wang D, Zeng J, Bao J, Kim JY, Chen ZF, El Mestikawy S, Luo M. Dorsal raphe neurons signal reward through 5-HT and glutamate. Neuron. 2014 Mar 19;81(6):1360-1374. doi: 10.1016/j.neuron.2014.02.010. PMID: 24656254; PMCID: PMC4411946.
34. Johnson MD. Synaptic glutamate release by postnatal rat serotonergic neurons in microculture. Neuron. 1994 Feb;12(2):433-42. doi: 10.1016/0896-6273(94)90283-6. PMID: 7906530.
35. Yang B, Sanches-Padilla J, Kondapalli J, Morison SL, Delpire E, Awatramani R, Surmeier DJ. Locus coeruleus anchors a trisynaptic circuit controlling fear-induced suppression of feeding. Neuron. 2021 Mar 3;109(5):823-838.e6. doi: 10.1016/j.neuron.2020.12.023. Epub 2021 Jan 20. PMID: 33476548.
36. Kaneko T, Akiyama H, Nagatsu I, Mizuno N. Immunohistochemical demonstration of glutaminase in catecholaminergic and serotoninergic neurons of rat brain. Brain Res. 1990 Jan 15;507(1):151-4. doi: 10.1016/0006-8993(90)90535-j. PMID: 1967973.
37. Bean BP. The action potential in mammalian central neurons. Nat Rev Neurosci. 2007 Jun;8(6):451-65. doi: 10.1038/nrn2148. PMID: 17514198.
38. Tsiang-Tung Chang. The History of Neuroscience in Autobiography. SfN.
39. Feng TP. Looking back, looking forward. Annu Rev Neurosci. 1988;11:1-12. doi: 10.1146/annurev.ne.11.030188.000245. PMID: 3284437.
40. Snyder, S. Dr Julius Axelrod, 1912–2004. Neuropsychopharmacol 30, 1764–1766 (2005). https://doi.org/10.1038/sj.npp.1300799
41. Pert CB, Snyder SH. Opiate receptor: demonstration in nervous tissue. Science. 1973 Mar 9;179(4077):1011-4. doi: 10.1126/science.179.4077.1011. PMID: 4687585.
42. Sabatini DM, Erdjument-Bromage H, Lui M, Tempst P, Snyder SH. RAFT1: a mammalian protein that binds to FKBP12 in a rapamycin-dependent fashion and is homologous to yeast TORs. Cell. 1994 Jul 15;78(1):35-43. doi: 10.1016/0092-8674(94)90570-3. PMID: 7518356.
43. SUTHERLAND EW, RALL TW, MENON T. Adenyl cylase. I. Distribution, preparation, and properties. J Biol Chem. 1962 Apr;237:1220-7. PMID: 13918525.
44. Miyamoto E, Kuo JF, Greengard P. Adenosine 3',5'-monophosphate-dependent protein kinase from brain. Science. 1969 Jul 4;165(3888):63-5. doi: 10.1126/science.165.3888.63. PMID: 17840687.
45. Sanes J. Paul Greengard (1925-2019). Neuron. 2019 May 22; 102(4): 718-720
46. Livet J, Weissman TA, Kang H, Draft RW, Lu J, Bennis RA, Sanes JR, Lichtman JW. Transgenic strategies for combinatorial expression of fluorescent proteins in the nervous system. Nature. 2007 Nov 1;450(7166):56-62. doi: 10.1038/nature06293. PMID: 17972876.
47. Kuo JF, Greengard P. Cyclic nucleotide-dependent protein kinases. IV. Widespread occurrence of adenosine 3',5'-monophosphate-dependent protein kinase in various tissues and phyla of the animal kingdom. Proc Natl Acad Sci U S A. 1969 Dec;64(4):1349-55. doi: 10.1073/pnas.64.4.1349. PMID: 4393915; PMCID: PMC223291.
48. Kuo JF, Greengard P. Cyclic nucleotide-dependent protein kinases. VI. Isolation and partial purification of a protein kinase activated by guanosine 3',5'-monophosphate. J Biol Chem. 1970 May 25;245(10):2493-8. PMID: 5445796.
49. Schulman H, Greengard P. Stimulation of brain membrane protein phosphorylation by calcium and an endogenous heat-stable protein. Nature. 1978 Feb 2;271(5644):478-9. doi: 10.1038/271478a0. PMID: 628428.
50. Nestler EJ, Greengard P. Protein phosphorylation in the brain. Nature. 1983 Oct 13-19;305(5935):583-8. doi: 10.1038/305583a0. PMID: 6312325.
51. McAfee DA, Schorderet M, Greengard P. Adenosine 3',5'-monophosphate in nervous tissue: increase associated with synaptic transmission. Science. 1971 Mar 19;171(3976):1156-8. doi: 10.1126/science.171.3976.1156. PMID: 4322706.
52. Kebabian JW, Greengard P. Dopamine-sensitive adenyl cyclase: possible role in synaptic transmission. Science. 1971 Dec 24;174(4016):1346-9. doi: 10.1126/science.174.4016.1346. PMID: 4332627.
53. Kebabian JW, Petzold GL, Greengard P. Dopamine-sensitive adenylate cyclase in caudate nucleus of rat brain, and its similarity to the "dopamine receptor". Proc Natl Acad Sci U S A. 1972 Aug;69(8):2145-9. doi: 10.1073/pnas.69.8.2145. PMID: 4403305; PMCID: PMC426888.
54. Kebabian JW, Calne DB. Multiple receptors for dopamine. Nature. 1979 Jan 11;277(5692):93-6. doi: 10.1038/277093a0. PMID: 215920.
55. McAfee DA, Greengard P. Adenosine 3',5'-monophosphate: electrophysiological evidence for a role in synaptic transmission. Science. 1972 Oct;178(58):310-2. doi: 10.1126/science.178.4058.310. PMID: 4346045.
56. Tsien RW, Giles W, Greengard P. Cyclic AMP mediates the effects of adrenaline on cardiac purkinje fibres. Nat New Biol. 1972 Dec 6;240(101):181-3. doi: 10.1038/newbio240181a0. PMID: 4343950.
57. Richard Tsien. The History of Neuroscience in Autobiography. SfN.
58. Greengard P. The neurobiology of slow synaptic transmission. Science. 2001 Nov 2;294(5544):1024-30. doi: 10.1126/science.294.5544.1024. PMID: 11691979.
59. Barbano PE, Spivak M, Flajolet M, Nairn AC, Greengard P, Greengard L. A mathematical tool for exploring the dynamics of biological networks. Proc Natl Acad Sci U S A. 2007 Dec 4;104(49):19169-74. doi: 10.1073/pnas.0709955104. Epub 2007 Nov 21. Erratum in: Proc Natl Acad Sci U S A. 2008 Apr 15;105(15):5945. PMID: 18032599; PMCID: PMC2148263.
60. Hubel DH, Wiesel TN. Early exploration of the visual cortex. Neuron. 1998 Mar;20(3):401-12. doi: 10.1016/s0896-6273(00)80984-8. PMID: 9539118