ALG-000184 是一款由 Aligos Therapeutics 开发用于慢性乙型肝炎治疗的具有皮摩尔效力的泛基因型 II 型衣壳组装调节剂(CAM-E),是ALG-001075 的前药。
目前 ALG-000184 正处在 Phase 1期(ALG-000184-201研究)期临床试验阶段,这项研究是一项多部分、双盲、随机、安慰剂对照研究,旨在评估健康志愿者和慢乙肝患者中单次和多次递增剂量 ALG-000184 的安全性、药代动力学和抗病毒活性。
ALG-000184-201研究目前已进行至第四部分研究。第一部分和第二部分分别是在健康志愿者中进行的双盲、随机、安慰剂对照研究,旨在评估单递增剂量和多递增剂量在健康志愿者中的安全性、耐受性和药代动力学。
第三部分是在目前未治疗/未经治慢性乙型肝炎患者中进行的随机、双盲安慰剂对照研究,这项研究包含四个队列,每个队列10名受试者,其中8名用药,2名安慰剂,受试者将每天用药一次,共28天,各受试者条件及用药方案如下:队列 1:HBeAg 阴性慢乙肝患者 100 mg 药物/安慰剂;队列 2:HBeAg 阴性慢乙肝患者 50 mg 药物/安慰剂;队列 3:HBeAg 阴性慢乙肝患者 10 mg 药物/安慰剂;队列 4:HBeAg 阳性慢乙肝患者 100 mg 药物/安慰剂。在此前的各种会议场合已有部分数据公布,感兴趣的可前去本号考古。
第四部分是在目前未治疗的慢性乙型肝炎患者中进行的安全性、耐受性、药代动力学和抗病毒活性研究,研究中受试者每日一剂 ALG-000184 ,共48周。该项研究目前正在进行中。队列1和队列2中受试者按4:1的比例随机分配到ALG-000184+恩替卡韦(ETV)或安慰剂+ETV,为期12周,然后是36周的ALG-000184+ETV。队列1和队列2中分别评估100毫克和300毫克的 ALG-000184。队列3开放标签的评估了300毫克ALG-000184单药治疗,目前也正在进行中。截至目前获得的所有三个队列的数据都将在本次2023欧肝会上公布。
截至目前,已有25名受试者参加了第1队列(100毫克,N = 11)和第2队列(300毫克,N = 14)试验,分别已用药24周和16周。所有受试者均为亚洲人,大多数为女性(52%),平均年龄33.2岁,BMI 22.3 kg/m2,HBV基因型为B或C。大多数受试者基线(BL)ALT低于1.2 × ULN。
研究药物的耐受性良好;没有严重的不良事件(AEs),也没有因AE而停药。所有治疗中出现的AE都是1级或2级,只有一个ALT升高的4级AE,尽管继续用药,但情况有所改善,ALT委员会评估认为不是由于药物毒性引起的。没有关于实验室、心电图或生命体征的等临床关切的报告。
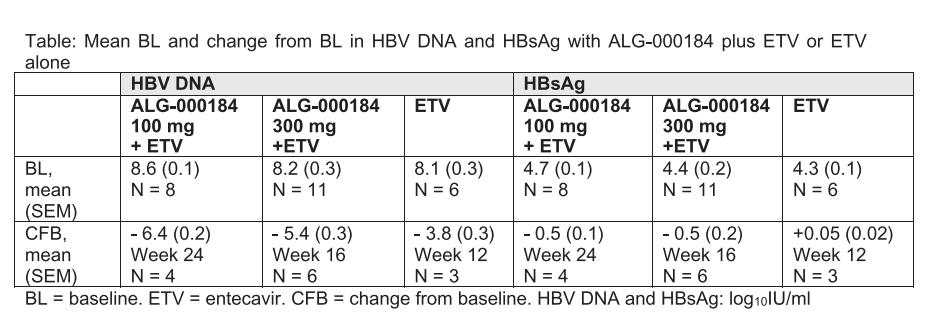
第一天的PK情况与早期健康志愿者的研究结果一致。HBV DNA 和 HBsAg 的平均BL和从BL开始的变化见表。HBsAg 水平在单独使用ETV中没有变化,但100mg ALG-000184+ETV 至少22周内最大下降0.7 log10 IU/ml,在300mg ALG-000184加ETV至少14周内最大下降1.0 log10 IU/ml。
研究认为,ALG-000184加ETV用药长达24周,耐受性良好,表现出可预测的PK,并导致与单独使用ETV相比,HBV DNA和HBsAg大幅降低。重要的是,ALG-000184加ETV的用药方案导致了HBsAg的剂量依赖性和临床相关的下降,表明ALG-000184在功能性治愈的联合治疗方案中具有潜在的作用。
来源:肝脏时间(HeparSpace)