
文|唐文采飞扬
编辑|唐文采飞扬
GO和r-GO作为二维纳米材料,具有独特的物理和化学特性,使其在生物医学、电子器件和能源储存等领域具有广泛的应用潜力。
然而,随着其应用范围的扩大,人们对其潜在的毒性效应产生了担忧,因此,进行全面的体外毒理学评估是确保GO和r-GO的安全应用的关键。

石墨烯基纳米材料(GO 和 rGO)的细胞毒性评估
使用改进版乳酸脱氢酶(LDH)测定法对GO和r-GO的细胞毒性进行了初步评估,该方法基于细胞内LDH水平的定量,而不是LDH的释放。
LDH的释放可以显示细胞膜的损伤,这是坏死的标志,改进的LDH(m-LDH)测定法只提供样品中存活细胞数量的信息,而不作为坏死的指标。
然而,这种修改允许在分析之前去除过量的纳米颗粒,从而减少碳基纳米材料的干扰风险。
因此,m-LDH测定法被认为是迄今为止评估这类材料细胞毒性最可靠的方法,从对GO和r-GO的评估结果显示,毒性与时间和浓度有关,并与细胞类型和物理化学特性相关。
短时间暴露(3小时)不会导致显著的毒性,无论是对于材料还是细胞类型,然而,从24小时开始,可以观察到材料之间的差异。
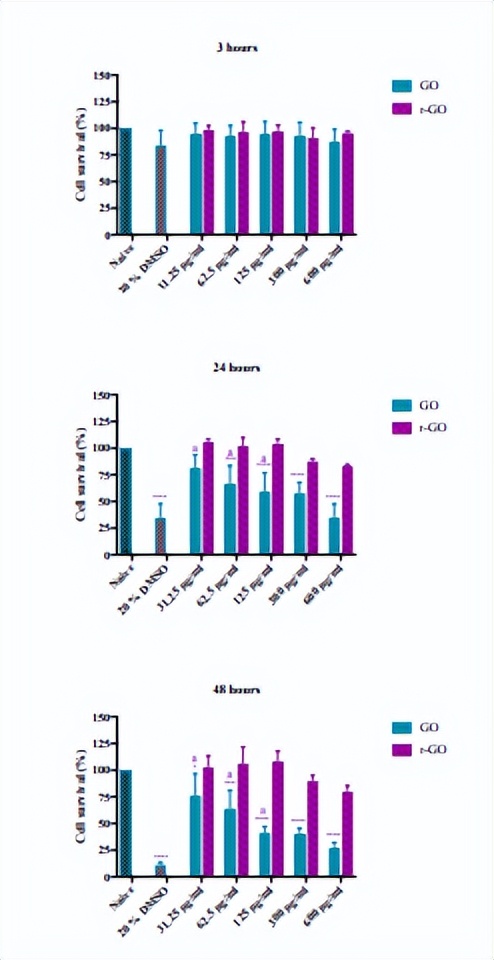
对于MRC-5细胞,随着时间和GO浓度的增加,细胞存活率下降,最高浓度条件下的细胞存活率分别为12.9±35%和5.2±27%。
将细胞暴露于高达300µg/ml的GO浓度中24小时,对所有处理产生类似的效果(约70-60%的细胞存活率)。
然而,48小时后,除了最低两个浓度外,其他浓度的细胞存活率均高于LD50。
相反,暴露于r-GO并没有对细胞存活率产生显著影响,对所有浓度和时间点的处理,细胞存活率保持在80%的毒性阈值附近。

对于A549细胞,GO和r-GO显示非常相似的细胞毒性谱,对于这两种材料,细胞毒性随着浓度和时间的增加而逐渐增加。
尽管r-GO的毒性几乎与MRC-5的结果一致,但与健康细胞相比,GO对癌细胞的影响较弱。
事实上,在24小时和48小时后,与MRC-5细胞相比,A549细胞在600µg/ml的条件下的存活率高出一倍。

最常用的细胞毒性测定方法存在一些限制,因此寻找替代方法来确认细胞毒性数据。
在所有用于研究细胞存活的检测方法中,基于发光的测定方法是唯一没有报道与碳基材料干扰的方法。
然而,关于金属纳米颗粒干扰的报道表明,使用这种测定方法可能存在问题,此外,干扰光线并不是唯一要考虑的因素。
事实上,代谢测定(如MTT)可能由于碳基材料与不溶*福性**尔马唑蓝晶体的相互作用导致假阴性(低毒性)结果。

考虑到所有这些因素,对一种新的发光测定方法RealTime-GloTM MT进行了研究,以评估其用于石墨烯纳米材料研究的适用性。
这种特殊的细胞存活测定方法测量活细胞的还原潜能,因此不允许去除纳米材料,这使得该测试方法特别适用于干扰的研究。
在该测定方法中,信号是通过将还原的MT底物从细胞扩散到周围培养基中产生的,底物与荧光酶结合,产生的发光信号与活细胞数量相关。
在最初的实验中,仅使用GO,因为它相对于r-GO具有更好的分散性。
即使在考虑到终点、敏感性和毒性机制的差异时,经过3小时暴露后得到的细胞存活结果已经表明可能存在干扰,因为这种短暂的暴露时间与GO的显著毒性无关。
相比之下,RealTime-GloTM MT细胞存活结果显示,即使暴露于低浓度的GO(31.25 µg/ml),细胞存活率也下降了50%。

值得注意的是,即使在更高的浓度和48小时处理时间下,使用改进的LDH测定法评估细胞毒性时也没有观察到这种水平的毒性。
众所周知,基于代谢的测定法可能会高估某种物质对细胞代谢的影响,而不会对细胞存活性产生影响,因为这些测定法将代谢活性作为细胞存活性的间接指标进行分析。
然而,RealTime-GloTM MT测定法观察到的GO对A549细胞的明显细胞毒性,在所有时间点上,31.25至125 µg/ml的浓度范围内,与m-LDH测定法数据相比,超出了RealTime-GloTM MT测定法的预期高灵敏度。

为了澄清与m-LDH测定法数据的差异,进行了另一个实验,在这个实验中,细胞与测定试剂一起培养,并在24小时后测量荧光强度。
在确定了基线后,不同浓度的GO被加入孔中,并立即测量荧光强度,结果显示,在加入GO后荧光强度显著下降,在浓度为15.6和125 µg/ml时,平均信号分别减少了25%和95%。
综合所有这些结果,可以推测GO与基于荧光的测定法存在干扰现象,尽管从未报告过,但这在一定程度上是可以预料的,因为碳纳米材料会干扰荧光,这是一个紧密相关的现象。
此外,GO与测定法中的试剂之间的相互作用也不可忽视,很可能需要修改荧光测定法,引入额外的步骤以去除纳米颗粒,类似于对LDH测定法所需的操作。
石墨烯纳米材料的细胞相互作用
在确定了石墨烯衍生物在肺细胞中可能会引起细胞毒性的作用后,我们要探究的问题是细胞毒性是由内吞作用还是与细胞质膜的相互作用所致。
一些研究表明,石墨烯纳米颗粒的进入是导致其观察到的细胞毒性的原因,而其他研究则表明,石墨烯进入细胞可以输送治疗药物而不对细胞造成损害。
纳米颗粒进入细胞需要不同的能量依赖的内吞作用过程,内吞作用途径有多种类型,包括噬菌作用,可以将大颗粒(>500 nm)主动内吞到噬菌细胞中。
此外,内吞作用根据纳米颗粒的大小被分为多种机制,即微噬作用(<500 nm)、依赖衣蛋白的内吞作用(约120 nm)、依赖洞窟蛋白的内吞作用(约60 nm)和衣蛋白与洞窟蛋白独立的内吞作用(约60 nm)。
A549和MRC-5等非噬菌细胞能够摄取小颗粒,研究中石墨烯衍生物的平均尺寸主要小于200 nm,预计它们在MRC-5和A549细胞中的内吞将通过非噬菌细胞内吞机制进行。
有些纳米颗粒有通过细胞质膜的被动扩散进入的潜力,例如,碳纳米管据报道可以通过穿透细胞质膜进入细胞。
荧光染色通常用作研究纳米颗粒被细胞摄取的方法,然而,信号猝灭使得这种方法不适用于石墨烯纳米材料。
Al-Jamal和Kostarelos提出了一种基于流式细胞仪对光散射变化进行定性评估的替代方法。
具体而言,该方法基于碳基纳米材料与细胞的结合,导致颗粒度增加,从而转化为侧向散射轮廓的变化。
尽管侧向散射方法无法区分细胞吸附和细胞对纳米颗粒的内吞作用,但该方法已成功用于研究碳纳米管、氧化锌、二氧化钛和银纳米颗粒的摄取,并且预计能够提供有关石墨烯纳米材料与细胞相互作用的有用信息。
在这个实验中,细胞接触到最高浓度为125 µg/ml,因为在更高浓度下石墨烯衍生物表现出的高细胞毒性可能导致细胞计数较低。
经过实验得知,侧向散射轮廓的缺乏变化表明纳米材料与MRC-5和A549细胞之间的相互作用可以忽略不计。
这在一定程度上对细胞毒性数据提出了挑战,特别是在MRC-5细胞的情况下,在125 µg/ml的GO处理48小时后观察到的低细胞存活率暗示细胞与纳米材料之间存在一定的相互作用。
GO 和 r-GO 细胞毒性的机制评估
将细胞暴露于细胞毒性物质可能导致不同类型的细胞死亡,其中一种例子是称为坏死的非意外性细胞死亡。
坏死过程表现为细胞迅速肿胀和细胞膜完整性丧失,导致细胞内物质释放到周围环境中。
坏死细胞死亡并不是细胞唯一的死亡方式,细胞也可能经历凋亡,这是一种高度调节的细胞自杀过程。
凋亡的特征包括细胞质萎缩、细胞膜脱落、细胞核浓缩和明确的碎裂,除了凋亡和坏死外,自噬是另一种细胞死亡机制。
自噬是一种回收系统,可以分解异常蛋白质团、细胞质成分和损坏的细胞器,然而,无限制的自噬可能导致非凋亡性细胞死亡。
有报道称,自噬功能的破坏导致细胞损伤并引起细胞死亡,这被认为是纳米材料毒性的潜在机制之一。

纳米颗粒毒性的机制已经得到广泛研究,据报道,不同类型的纳米材料可以通过在许多生物系统中产生活性氧自由基(ROS)来诱导毒性。
过量产生的ROS会导致氧化应激,这是一种导致细胞信号传导不受控制、细胞运动变化、基因毒性、致癌性、自噬和凋亡等不同毒性终点的情况。

结论:
对于GO而言,与细胞的物理相互作用似乎比r-GO更为显著,这反映在两种细胞系的细胞信号蛋白上有显著影响。
纳米颗粒能够与细胞膜受体相互作用,因此可以调节信号转导途径,因此,GO纳米片与细胞膜受体的结合可能导致信号事件的失调。
GO passively转位进入细胞是观察到的细胞事件的可能触发因素,但还需要进一步的工作来证实这一点。
Chang等人提出,GO的形状(类似片状结构)可能会阻塞A549细胞表面的通道,从而干扰物质的交换。
该研究还显示,GO进入A549细胞的能力较差,因此,细胞膜对物质交换的阻滞可能是GO导致不同细胞信号通路失调的间接效应。
关于GO纳米片的间接作用的另一个可能性是它们从培养基中吸收营养物质,引起氧化应激和细胞饥饿,进而诱导自噬,许多研究者报道了这一现象。
综上所述,GO而不是r-GO可以导致肺细胞系中的细胞信号通路失调,这种能力可能具有临床意义,同时也可能揭示与GO毒理效应相关的机制。
参考文献:
1.石墨烯对植物的生理毒性效应研究进展. 翁轶能;蒋楠;李佳欣;应祉凝;都韶婷.应用生态学报,2020
2.石墨烯材料与蛋白质的相互作用. 王晓娟;刘真真;陈奇;王小强;黄方.化学进展,2019
3.氧化石墨烯在生物医学领域的应用. 杜夏夏;舒刚;陈宗艳.功能材料,2018
4.石墨烯的制备、功能化及应用. 宗路艳;常旭;吴惠霞;杨仕平.上海师范大学学报(自然科学版),2016
5.石墨烯和氧化石墨烯对细胞脂膜破坏作用研究. 涂育松;方海平.中国科学:物理学 力学 天文学,2016