面肌痉挛(HFS)是一种以第七颅神经支配的面部肌肉不自主收缩为特征的运动障碍。这种疾病的特点是面部表情肌肉的不自主性、强直性收缩,通常单侧起病,开始于眼眶周围的肌肉,并逐渐进展到口周、颈阔肌和其他面部表情的肌肉。
虽然传统上被认为是一种良性疾病,但它可能会导致患者的焦虑情绪增加以及社交障碍,在严重的情况下,甚至会因非自愿闭眼而导致患者功能性失明。该疾病的平均患病率为11/10万,男女比例约为2:1(女性患病率为14.5/10万,男性患病率为7.4/10万)。

一、发病机制
面肌痉挛(HFS)是一种面神经支配的相应的肌肉阵发性的不由自主的痉挛。对于HFS的病因及发病机制,目前尚不清楚,从上世纪以来相关的各种理论不断被各国学者所提出,其中被人们广泛接受的有两种观点:“周围学说”以及“中枢学说”。
虽然可以阐释其中一部分的病因,但没有办法用单独的其中一种理论来解释HFS的具体发病机制。目前显微血管减压术(MVD)被认为是目前临床上可以治愈HFS最可行的手段。
1.周围学说
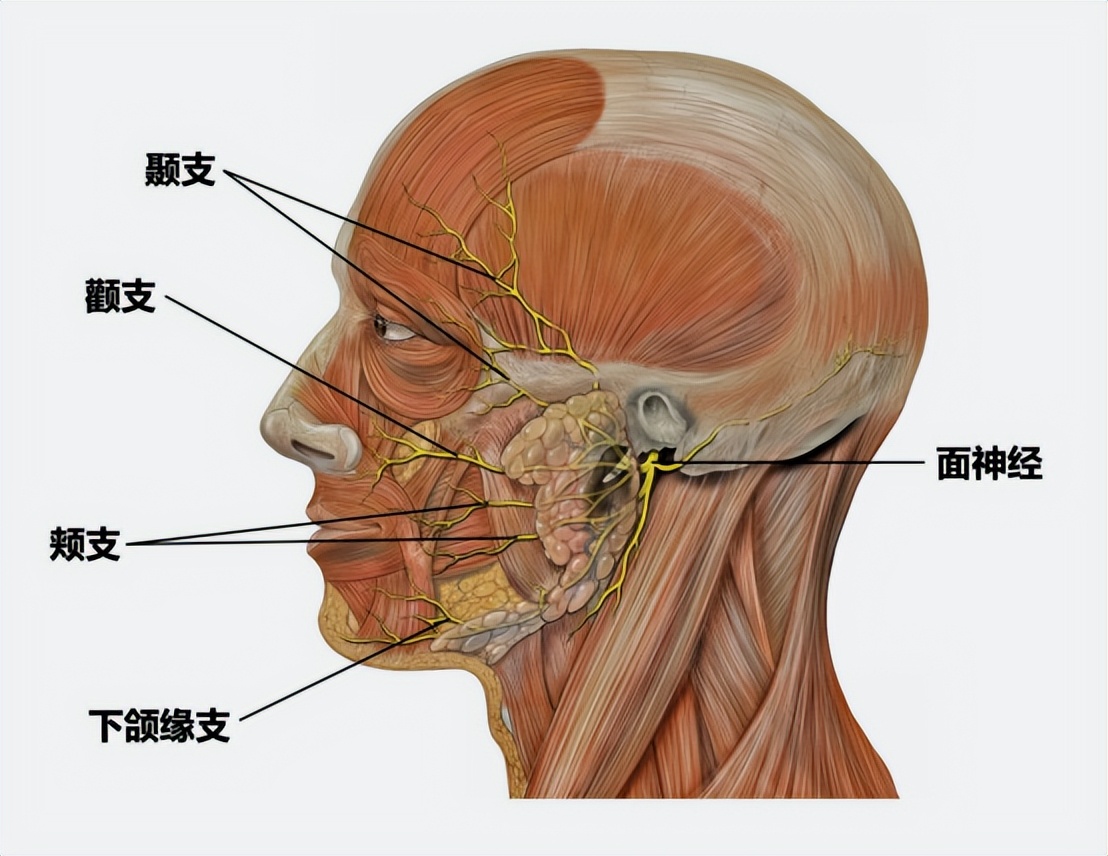
HFS患者的面神经出脑干区(REZ)受到血管的压迫是目前接受程度最高的病因。外周学说认为面神经REZ段由于是移行区,这个部位被施万细胞包裹的不完全,甚至该节段仅被蛛网膜包裹,缺乏分隔纤维和神经外膜的束间结缔组织。
这些特性导致了该部位对于血管压迫的耐受性降低,REZ段长时间的被邻近的责任血管所压迫而导致了损伤,并进一步的导致了神经产生了脱髓鞘以及一系列的病理改变,在一些轴突发生了暴露的面神经纤维束和纤维束之间产生了跨越神经突触从而传递扩散的异位神经电活动,最后导致脸部以及眼睑等部位的肌肉发生抽动。
而责任血管对REZ的压迫从而引起的脱髓鞘改变则是导致痉挛的异常动作电位的根源。但这一学说仍存在一些目前尚无法解释的问题,术中并未将已经发生了脱髓鞘改变的面神经纤维束相互分离开,仅仅是将责任血管分离后即可使异常肌反应波(AMR)和相应的抽动表现马上缓解,这与周围学说的观念不尽相同。
2.中枢学说
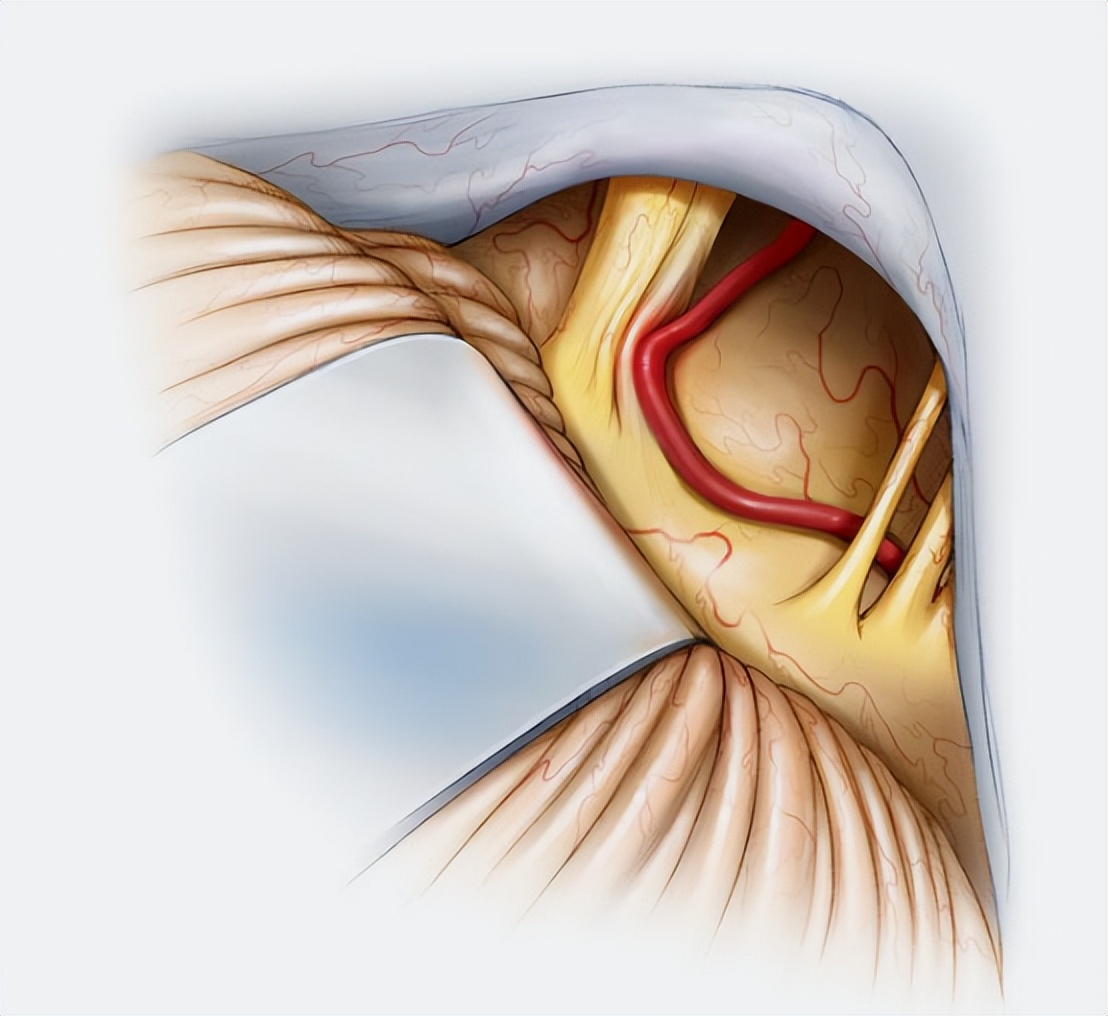
中枢学说则认为,REZ段由于受到了相应的责任动脉的压迫,并随着血管的搏动并产生逆行传导的神经冲动,这一过程促使面神经核的兴奋性逐渐增高,并逐渐的发生相应的功能和结构上的变化,并最终会形成向下传导的冲动,引起临床症状的发生。
但这一学说也有无法解释的现象,根据该学说的原理,即使在分离责任血管后,面神经核的高兴奋性并不会立即下降,但大部分患者在显微血管减压术(MVD)术后症状会即刻缓解。
3.交感学说
我国学者提出的交感学说认为,面肌痉挛患者的责任血管在与REZ和面神经根的长时间接触中,动脉的外膜和面神经均会产生损伤;这会导致责任动脉外膜中包含的交感神经裸露。

同时面神经也产生了脱髓鞘病变;裸露的交感神经产生的神经递质传导至面神经,从而诱发面神经产生相应的动作电位,进一步导致了HFS症状的出现。但交感学说的原理尚不能解释部分患者在术后症状不能即刻缓解的现象。
二、原发性面肌痉挛的诊断
HFS的诊断主要基于临床识别。此外,需要详细的病史和神经系统检查,以排除任何可能的继发性因素。目前,可用的诊断检查包括肌电图检查,以排除面神经损伤引起的去神经支配。
以及脑部MRI检查,以排除脑干附近的脱髓鞘或占位性病变。区分原发性和继发性HFS是正确指导治疗策略的基础。事实上,虽然针对原发性HFS的治疗可以减少患者的症状,并最终导致临床症状的持续改善。

但在继发性HFS中,重点应该首先是确定和治疗原发疾病。需要对眼睑痉挛、迟发性运动障碍、心因性HFS、累及面部肌肉的局灶性皮质癫痫发作以及面神经损伤后的连带运动进行鉴别诊断。
三、治疗方案
1.药物治疗
大量的药物已经被研究和发现对于面肌痉挛具有一定的疗效。这些药物包括氯硝西泮、加巴喷丁和卡马西平等抗惊厥药物,以及巴氯芬、抗胆碱药和氟哌啶醇等其他药物。但口服药物最大的局限性是疗效不一致,并且会产生包括以眩晕为主以及其他包括镇静、疲劳等相关的并发症。
2.肉毒素治疗
我国采用注射A型肉毒素(BTX-A)治疗肌肉痉挛已有数十年的时间。肉毒素是一种源自肉毒梭菌的生物毒素。它在神经与肌肉接头的突触前区起作用,通过抑制了钙介导的乙酰胆碱的释放,从而避免下游冲动的产生,导致神经麻痹。
并使神经产生的相应电活动没有办法顺利的传递到肌肉,从而减弱肌肉的收缩力,以此来缓解肌痉挛的症状。目前肉毒素在面肌痉挛、肌张力障碍等一系列疾病的临床治疗中均有被使用。
尽管肉毒素注射疗法的有效率高达97%,但它仍存在有一些局限性。它面临着每隔三个月到六个月进行一次重复给药的情况,并随着给药次数的增加,肉毒素的有效期会越来越短。
尽管它的安全性被广泛接受,但也存在相关不良反应的报道,包括面部轻瘫、复视和上睑下垂等,主要的长期副作用是面部不对称。关于系统性不良反应,在肉毒素注射后24小时内,约有14%的患者出现流感样症状(BoNT-A治疗患者约1.7–20%,BoNT-B治疗患者约5–55%)。
总的来说,肉毒素注射治疗面肌痉挛短期内可达到良好的效果,是一种安全有效的治疗方法,但存在复发率高的问题,预后情况也有待改善。
3.MVD治疗
1977年由Jannetta首次提出了采用MVD来治疗面肌痉挛,这是一种通过解除面神经根受压来提供持久症状缓解的手术干预。但因为面肌痉挛并不会危及生命,MVD也存在相关的风险,在决定是否进行手术之前,需要权衡疗效和安全性。

由于听力损失等并发症发生率较低,并且随着术中技术和监测水平的不断提高,MVD仍然是HFS患者的首选治疗方法。几乎在所有病例中都被证实面神经存在血管压迫。
目前MVD手术对面肌痉挛症状的总缓解率可达85%-90%。大约33%的患者在经过延迟治愈后可获得缓解,这其中12%的人延迟治愈的周期在1年左右。
对于MVD术后复发,在经过长期随访后发现只有约1%–2%的患者会出现复发,其他所有患者的缓解都是永久性的。至于并发症,永久性面神经麻痹的风险约为1%–2%,非功能性听力下降的发生率为2%–3%,后组颅神经出现功能障碍的风险为0.5%–1%,死亡率为0.1%-0.3%。
在大多数病例中,只要术中水密缝合硬脑膜以及封堵开放的乳突气房,脑脊液漏的发生率可以降低不到2%。MVD对几乎所有原发性HFS患者都是一种有效的治疗方法。
由于HFS的MVD是功能性手术,因此仔细考虑其潜在风险以及避免并发症的方法至关重要。当考虑MVD失败时,推荐的做法是等待一年后再考虑再次手术,因为许多患者可能会从延迟治愈中受益。这一点尤为重要,因为重复手术会导致更高的并发症发生率。
四、面肌痉挛与神经
面肌痉挛(HFS)是日常生活中一种发病率较高的疾病。表现为面神经支配的相应的肌肉阵发性的不由自主的痉挛。这种痉挛或抽动常常先从眼轮匝肌开始出现,并随着时间的进展渐渐地扩散到面部相应的一些表情肌和口轮匝肌。
面神经核和面神经根出脑干区(REZ)的慢性刺激被认为是HFS的主要病理生理机制。Jannetta等人既往的研究提示REZ受到后颅窝相应的血管的压迫是导致HFS发生的主要原因,并提出了从解决病因而根治疾病的显微血管减压术(MVD)。
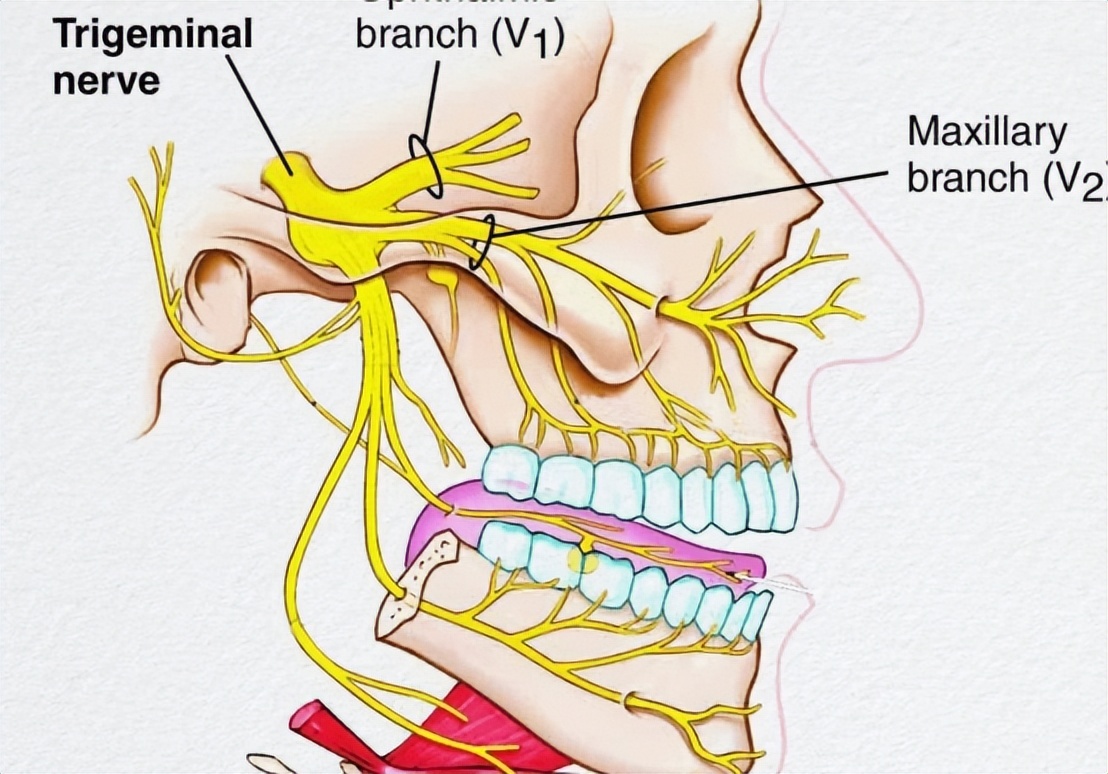
后颅窝中的血管,例如小脑前下动脉、小脑后下动脉、前庭动脉等,是导致REZ受压的最常见的责任动脉。但血管神经产生压迫的机制尚不明确,有文献报道面肌痉挛患者的后颅窝更加拥挤,这可能导致血管神经冲突。
根据KwanPark等人发明的分级方法进行分类,HFS患者的神经受压特征分为三个等级。1级:REZ上无压痕或轻微压痕;2级:REZ区存在中度压痕;3级:REZ区存在严重压痕或变色。
五、结语
综上所述,自从面肌痉挛疾病被人们报道以来,在过去的数十年中,关于面肌痉挛的发病机制及治疗手段的研究不断呈现。对于HFS的发病机制目前仍无定论,周围学说、中枢学说、交感学说均无法完美的解释面肌痉挛的病因。
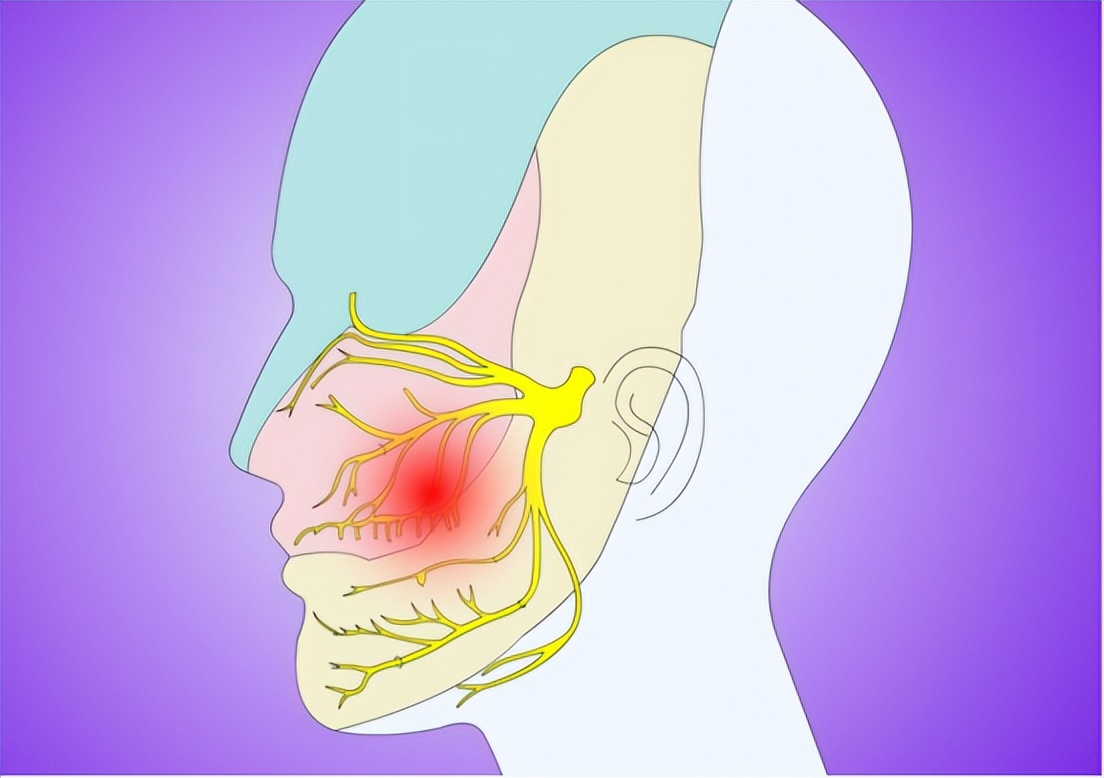
尽管具体的发病机制仍不清楚,但神经受到了责任血管的压迫仍是目前被临床上认可的病因,我们期待对面肌痉挛的发病机制做更深一步的研究。目前显微血管减压术被认为是治疗HFS最有效的手段。
但MVD也存在出现死亡、面瘫、听力下降、脑脊液漏等并发症的风险,内镜、神经电生理等一系列新技术的出现能否有效降低并发症发生率以及提高手术有效率是我们进一步研究的方向。对于不愿或无法行手术治疗的患者,采用肉毒素局部的注射在短期内可以产生良好的疗效。