编译:李皓静来源:肿瘤资讯
免疫疗法大潮出现之前,表观遗传学一度被认为是一个重要的抗肿瘤研究方向。EZH2是表观遗传学中最为成熟的靶点,目前EZH2*制剂抑**的抗肿瘤研究大多还处在细胞和动物试验水平。作为EZH2*制剂抑**先行者,Tazemetostat已在弥漫大B细胞淋巴瘤(DLBCL)、滤泡性淋巴瘤(FL)等多种肿瘤中展现出不俗潜力。法国学者将目光聚焦于Tazemetostat在复发/难治的B细胞非霍奇金淋巴瘤(NHL)和晚期实体肿瘤中的安全性和疗效,研究结果近期发表在Lancet Oncology上。
研究背景
约10-25%的FL和生发中心DLBCL患者中存在Zeste基因增强子人类同源物2(EZH2)突变。EZH2对生发中心B细胞分化起到关键作用,其突变可介导二甲基化的H3K27向三甲基化的H3K27转化。在DLBCL的生发中心B细胞样亚型小鼠模型中,EZH2突变抑制在BCL2过表达的情况下导致生发中心增生和加速的淋巴瘤形成。有研究表明,在EZH2突变DLBCL中,EZH2小分子*制剂抑**可降低体内H3K27me3浓度,重新激活沉默的EZH2靶基因,并起到抑制肿瘤增殖的作用。
此外,INI1表达缺失的实体瘤对EZH2具有致癌依赖性。 INI1是一种有效的肿瘤抑制基因,是SWI/SNF复合物的核心组分,调控细胞分化、增殖。INI1缺失破坏了SWI/SNF复合物的功能,导致EZH2异常激活,H3K27me3增加,导致多种肿瘤抑制因子的转录受到抑制和致癌信号传导通路的上调。
Tazemetostat(EPZ-6438)是一种高选择性EZH2*制剂抑**,在EZH2突变B细胞非霍奇金淋巴瘤(NHL)、INI1阴性恶性横纹肌样瘤和SMARCA4阴性恶性肿瘤的体外和异种模型中显示出抗肿瘤活性。
我们进行了首次人类第一阶段试验,以评估安全性,药代动力学,药效学和每日两次口服tazemetostat - 一类EZH2*制剂抑**的患者的初步活性, 复发或难治性B细胞非霍奇金淋巴瘤(NHL)和局部晚期或转移性实体瘤。
方法
该研究为一项多中心,开放性、I期剂量爬坡临床试验。入组患者为复发或难治性B细胞NHL和晚期实体瘤患者。
入组标准
1. 年龄在18岁或以上;
2. ECOG评分≤1分,预期寿命至少3个月;
3. 器官功能能够耐受治疗,具体标准为:血清总胆红素≤1.5倍正常值上限(ULN),天冬氨酸转氨酶或丙氨酸转氨酶≤3.0倍ULN,中性粒细胞绝对值≥0.75×109/L,血小板计数≥75×109/L,血红蛋白≥9g/ L,血清肌酐正常或肌酐清除率≤150ml/min,INR≤1.5倍ULN,部分凝血活酶时间≤1.5倍ULN。
排除标准
1. 患者在3周内接受过任何抗癌治疗,4周内接受过大手术,或者在首次使用tazemetostat前30天内接受过任何试验药物;
2. 不能服用口服药物;
3. 已知存在软脑膜或脑转移瘤,脑转移瘤病史;
4. 有明显的心血管损伤;
5. 严重感染或免疫功能低下。
研究设计
该研究采用传统3+3法,起始剂量为100mg日两次口服,后续剂量阶梯分别为200mg,400mg,800mg和1600mg。研究终点为疾病进展或出现不能耐受的毒副反应。
该研究的主要目标:根据受试者报告的剂量毒性、实验室参数和其他安全性、药代动力学参数明确药物的最大耐受剂量或II期试验推荐剂量。
结果
2013年6月13日至2016年9月21日,该研究共入组64例患者,包括21例B细胞NHL和43例晚期实体瘤,其中有13例INI1阴性或SMARCA4阴性。63/64(98%)例在入组前有1个月内发生疾病进展。
不良反应
服用tazemetostat的64例患者在第1周期中耐受性良好,并且后续治疗中未观察到新增不良事件。
最常见的不良事件为乏力(35例[55%],其中21例[33%]与治疗相关),另外还有贫血、厌食、肌肉痉挛、恶心和呕吐,多为轻至中度。3级或更严重的治疗相关不良事件并不常见(23例),主要为血小板减少、中性粒细胞减少、血压升高和肝损伤(转氨酶或胆红素升高)。
12例(19%)患者因治疗后出现不良事件而中断用药,其中最常见的不良事件为血小板减少。共2例患者出现严重治疗相关不良事件,包括1例中性粒细胞减少和和1例贫血和血小板减少。7例(11%)出现致命不良反应,但都与治疗无关。
该研究未达到定义的最大耐受剂量。基于不良事件,药代动力学,药效学和临床效力的综合评估,推荐的阶段2剂量为每日两次800mg。
药代动力学
Tazemetostat的中位达峰时间Tmax为给药后1-2小时,平均半衰期t1/2为3-4小时。
第一周期的第15天,在不同的剂量组中,均观察到Tazemetostat的Cmax 和AUC0–12 呈剂量依赖式增加。但重复给药后,AUC0–12 h出现剂量依赖性下降。在800mg组中,与给药第1天相比,第15天的AUC0–12 h减少了42%。
分别在用药前和用药后对32名患者参加剂量爬坡和剂量扩增队列的受试者进行皮肤活检,发现在皮肤棘层上中H3K27me3表达出现剂量依赖性减少。
对4例患者分别在给药前和用药4周后进行肿瘤组织活检,发现与基线相比,有3例(75%)观察到肿瘤组织中EZH2介导的组蛋白甲基化的靶向抑制。
研究者还在治疗前、治疗中和1例INI1阴性实体瘤患者进展后进行了RNA和外显子测序。RNA测序表明治疗前与治疗中对比,EZH2表达减少4倍,并观察到已知SWI / SNF复合物和EZH2靶基因的差异表达(一些基因上调,一些下调)。外显子组测序未检测到EZH2的特异性耐药突变。
疗效
截至2016年11月11日,21例B细胞NHL患者中有8例出现客观反应,其中3例达到CR,5例达到PR,其中3名患在后续治疗中肿瘤进一步缩小,并且分别在用药9个月、22个月和24个月时达到CR。观察到首次反应的中位时间为3.5个月,中位反应持续时间(定义为从达到CR或PR到出现PD或因任何原因导致死亡的时间)为12.4个月(图A)。
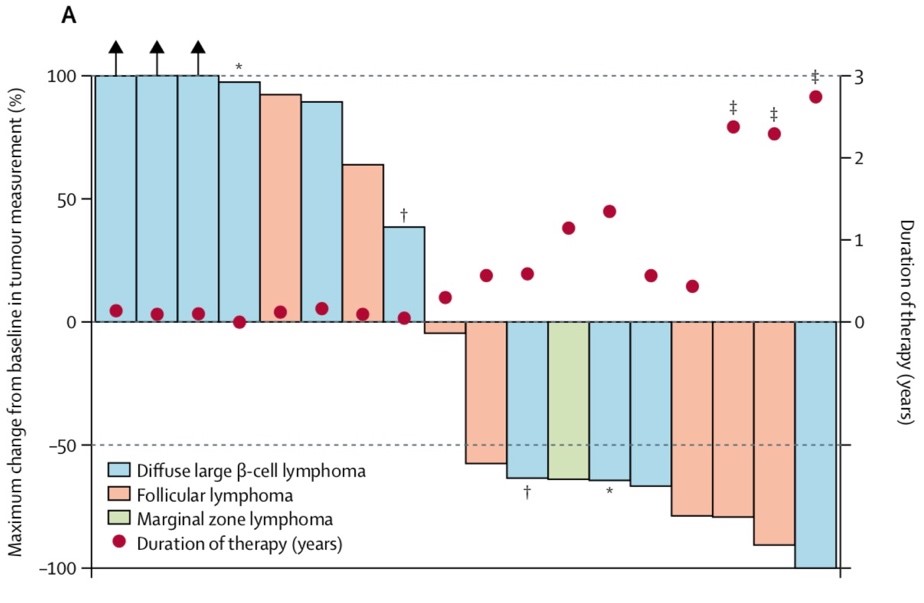
图A 21例B细胞非霍奇金淋巴瘤患者疗效评价
在43例实体瘤患者中,共13例INI1阴性或SMARCA4阴性,其中2例达到了客观反应,5例取得临床获益(SD或更好)。相比之下,其余30例实体瘤患者中只有1例(3%)取得临床获益(图B)。
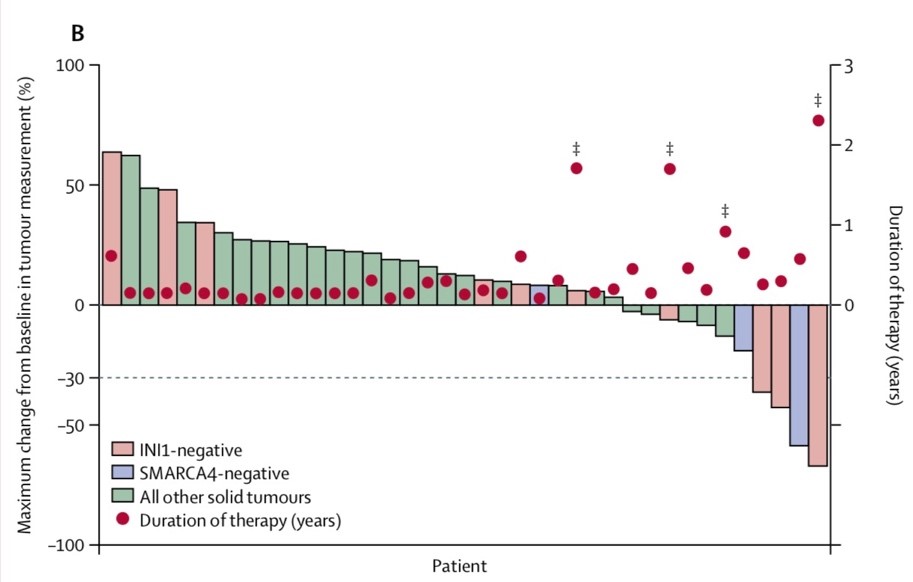
图B 43例晚期实体瘤患者疗效评价
结论
Tazemetostat在后续II期临床试验中的推荐剂量为800mg,每日两次口服。
该试验首次探讨了EZH2抑制对复发或难治性B细胞非霍奇金淋巴瘤和晚期实体瘤患者的疗效和安全性。结果显示,Tazemetostat在难治性B细胞非霍奇金淋巴瘤和晚期实体瘤(包括上皮样肉瘤)中显示出良好的安全性和抗肿瘤活性。
参考文献
Tazemetostat, an EZH2 inhibitor, in relapsed or refractory B-cell non-Hodgkin lymphoma and advanced solid tumours: a first-in-human, open-label, phase 1 study.The Lancet. Oncology 2018 Apr 9
责任编辑:肿瘤资讯-Amiee 版权声明版权属肿瘤资讯所有。欢迎个人转发分享,其他任何媒体、网站如需转载或引用本网版权所有内容,须获得授权,且在醒目位置处注明“转自:良医汇-肿瘤医生APP”。
欲了解更多血液肿瘤、淋巴瘤相关资讯,与全国各地血液肿瘤、淋巴瘤医生交流与讨论,请扫描以下二维码,添加肿瘤资讯小助手-Dinna微信,备注“血液肿瘤”!