欢迎关注凯莱英药闻
2022 年 6 月 7 日,礼来公布了lebrikizumab 针对中度至重度特应性皮炎( AD )患者治疗一年(52周)的疗效和安全性分析数据,3 期临床试验(ADvocate 1 和2)的新数据显示,在使用16周lebrikizumab单药治疗获得临床缓解的患者中,继续采用每2周或4周使用一次的维持治疗,80%的患者能在一年内维持皮肤症状清除和瘙痒缓解。

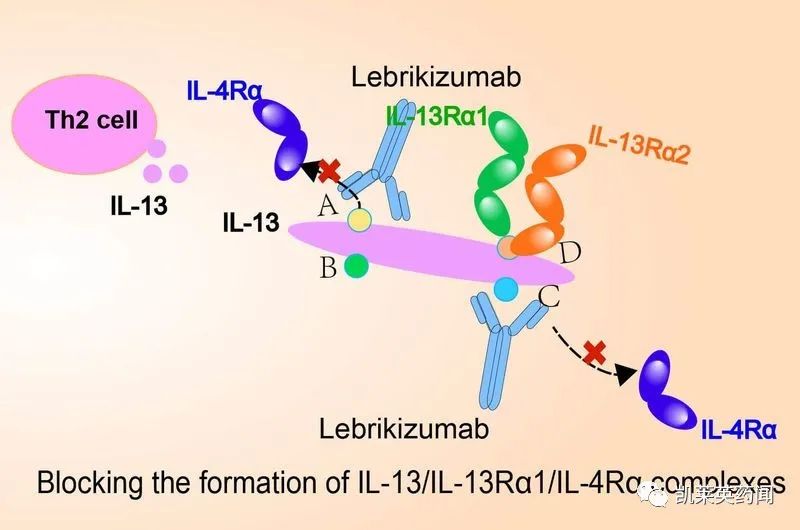
Lebrikizumab 是针对中度至重度AD开发的白细胞介素 13 (IL-13)*制剂抑**,它以高亲和力与IL-13 蛋白结合,以特异性阻止 IL-13Rα1/IL-4Rα(2 型受体)的形成,从而阻断通过 IL-13 的下游信号传导途径。在AD患者中,IL-13蛋白(疾病的中心致病介质)过度表达,通过促进辅助性T细胞2(Th2)细胞炎症,从而驱动AD病理生理学的多个方面,导致皮肤屏障功能障碍、瘙痒、感染、皮肤区域变硬增厚。此前,美国FDA已授予lebrikizumab治疗中重度AD成人和青少年患者(12岁至18岁以下,体重≥40公斤)的快速通道资格。礼来拥有lebrikizumab除欧洲以外的全球独家权益(包括美国),Almirall拥有该药在欧洲开发AD适应症的权益。
ADvocate 1 和ADvocate 2 是为期 52 周的随机、双盲、安慰剂对照、平行组、全球性 3 期研究,旨在评估 lebrikizumab 作为成人和青少年患者(12 至 18 岁以下且体重至少 40 公斤)的单一疗法治疗中度至重度 AD。在 16 周的治疗期,患者最初接受 lebrikizumab 500mg,两周后接受 lebrikizumab 250mg或安慰剂;在36周的维持期,每2周或 4 周接受一次 lebrikizumab 或安慰剂。主要终点由研究者全球评估(IGA)评分测量,评分为清晰皮肤(0)或几乎清晰皮肤(1),与基线相比减少至少2个点,16周时湿疹区域和严重程度指数(EASI-75)评分基线变化至少75%,EASI衡量疾病的程度和严重程度。关键的次要终点是通过IGA、EASI、瘙痒数值评分量表测量的瘙痒引起的睡眠损失和皮肤病学生活质量指数。
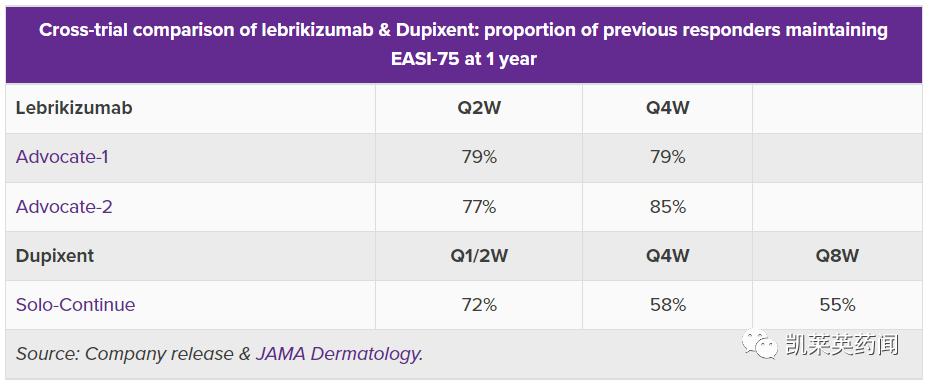
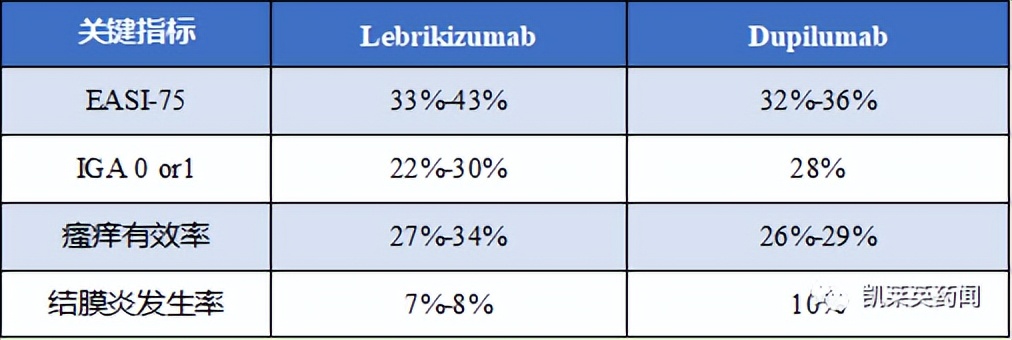
根据2022年3月公布的数据,对比lebrikizumab和Dupixent(dupilumab)的临床数据,可知lebrikizumab有望挑战dupilumab的治疗地位。
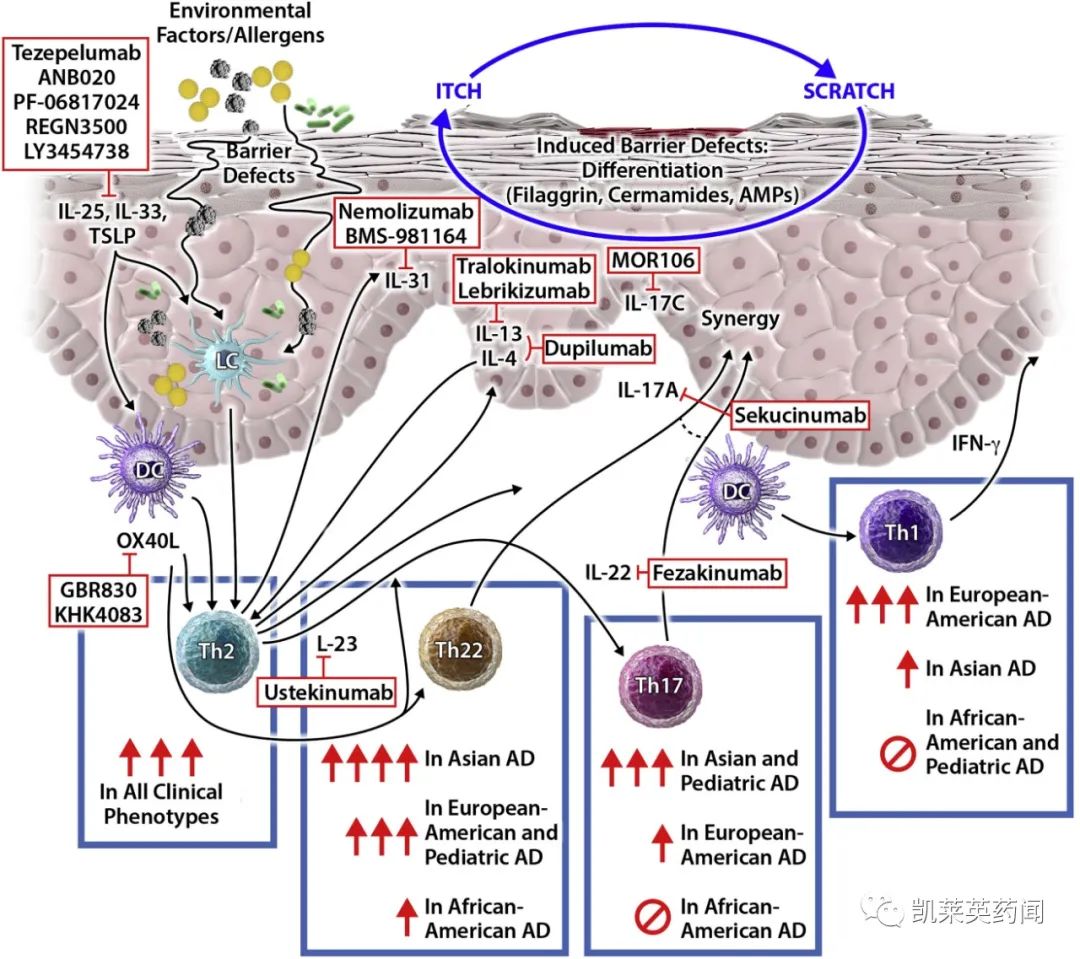
AD是一种常见的慢性、复发性炎症性皮肤病,其特点是反复的剧烈瘙痒和抓挠,从而导致皮肤开裂、呈鳞片状和渗液。全球大约80%的AD病例通常始发于婴儿期或儿童期,在各国儿童的患病率从2.7%到20.1%不等,其余病例则在成年期发生,患病率从2.1%到4.9%不等。在中国,据估计,AD的患病率为2460.18/100000,近几十年来,AD患者的数量增长了25.65%。中国成年人和青少年的患病率分别大约为4.6%和2.5%。在个体之间的症状表现各异,给患者带来了沉重的身体、心理和经济负担。
2021年,Dupixent销售额达到52.49亿欧元,同比增长52.7%,远远高于行业预测值。据Global Data市场调研数据显示,全球特应性皮炎治疗市场的规模将从2021年的62亿美元持续增长至2028年的242亿美元。期待lebrikizumab能为AD患者带来更多的治疗选择!