HBeAg血清学转换作为慢乙肝患者的满意的治疗目标,之前被广泛的用作各个研究的主要疗效指标。但是随着慢乙肝临床治愈概念的普及,HBsAg清除成为了慢乙肝患者追求的主要目标及各项研究的主要疗效指标。
早前有荟萃分析表明获得HBeAg血清学转换的慢乙肝患者15年内的肝癌发生率仅为2.58%,但是并未区分患者是通过何种治疗方式获得的HBeAg血清学转换。
近日,《BMC Gastroenterology》发表一项韩国的最新研究表明:NA治疗发生HBeAg清除的慢乙肝患者肝癌发生风险仍较高。

研究方法
这是一项回顾性队列研究,数据均来自韩国的三级医院。2006年1月至2016年12月期间,接受NA(ETV或TDF)一线药物治疗的1256例HBeAg阳性患者中,203例患者发生HBeAg清除(16.2%)。本研究纳入获得HBeAg清除的这203例患者,≥18岁,HBsAg和HBeAg阳性≥6个月。获得HBeAg清除的患者中仅有12例在巩固治疗>12个月后停药,其余191例患者均继续治疗来追求HBsAg清除。研究的主要疗效指标为肝癌发生率和HBsAg清除率。
患者基线
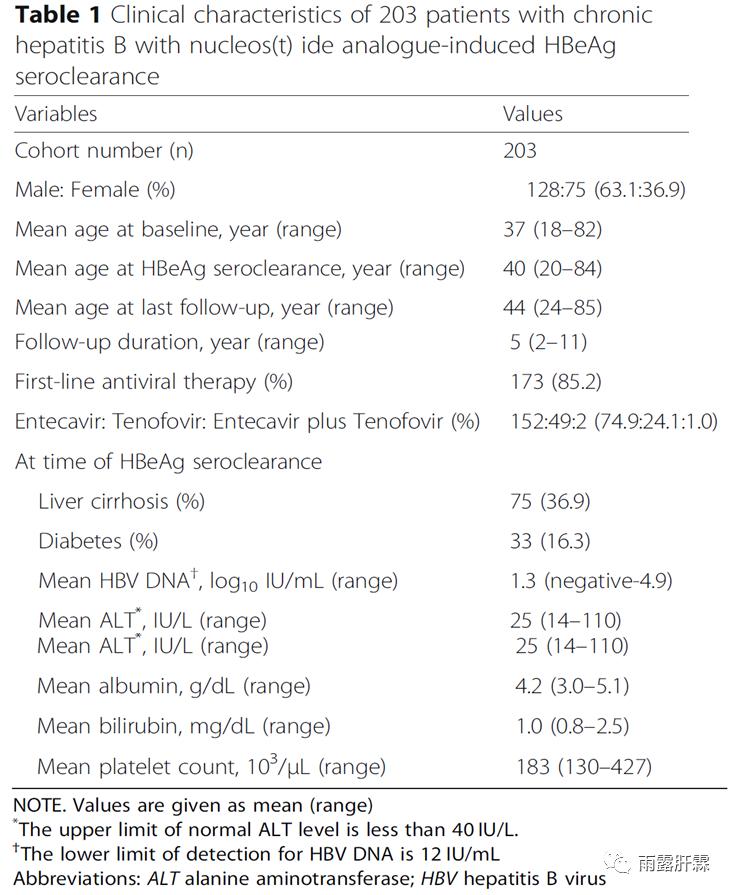
入组患者203例,男性128例(63.1%),基线中位年龄37岁,平均随访5年,173例(85.2%)患者接受ETV或TDF一线药物治疗,获得HBeAg清除时的肝硬化患者占36.9%。

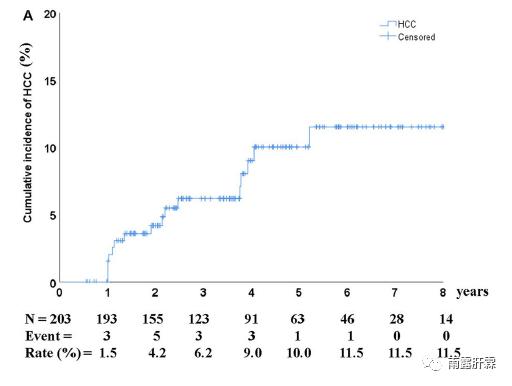
NA治疗获得HBeAg清除的患者随访5年的肝癌发生率高达7.9%

NA治疗获得HBeAg清除的患者平均随访5年,共有16例(7.9%)患者发生肝癌。随访1、3、5和8年的肝癌累积发生率分别为1.5%、6.2%、10.0%和11.5%。

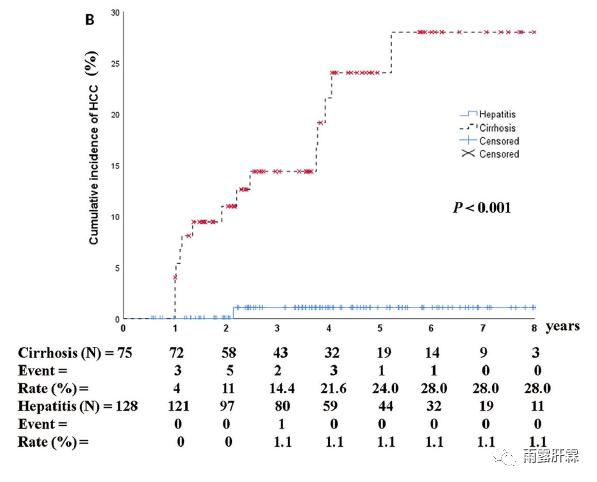
HBeAg清除时肝硬化患者的肝癌累积发生率显著更高

HBeAg清除时的肝硬化患者肝癌的累积发生率从HBeAg清除后1年的4%上升到8年后的28.0%,显著高于无肝硬化的慢乙肝患者(P<0.001)。
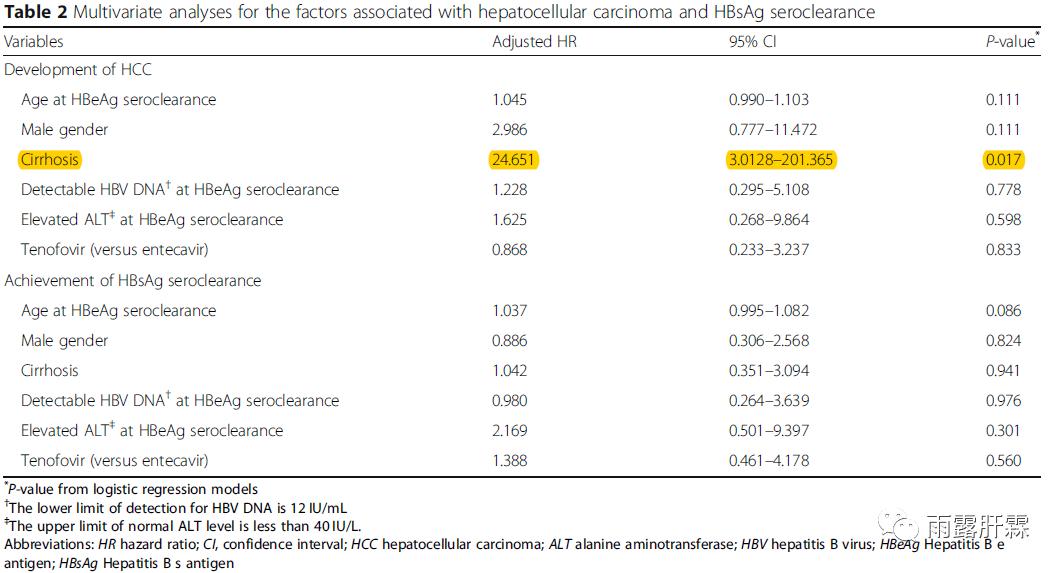
多因素分析显示:HBeAg清除时肝硬化的存在是肝癌发生的唯一相关因素 (P=0.003)。且研究未发现NA治疗获得HBeAg清除后与HBsAg清除的相关因素。

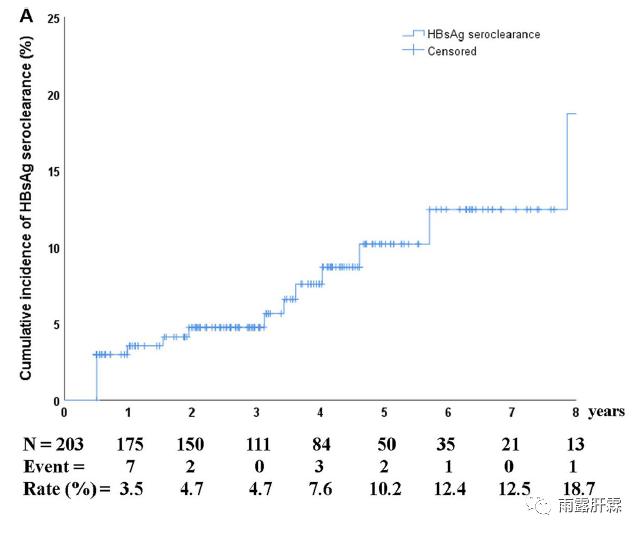
NA治疗获得HBeAg清除后随访5年的累积HBsAg清除率仅为7.9%

NA治疗获得HBeAg清除后平均随访5年,共有16例患者获得HBsAg清除(7.9%),其中13例患者获得HBsAb。HBeAg清除后的1、3、5和8年,累积的HBsAg清除率分别为3.5%、4.7%、10.2%和18.7%。
总结
本研究入组的NA治疗获得HBeAg清除的患者中,平均随访5年的肝癌发生率仍高达7.9%,高于之前荟萃分析发现HBeAg血清学转换后15年内肝癌发生率的2.58%。可能是因为:
1. 荟萃分析包含了自发和不同抗病毒治疗获得HBeAg血清学转换的各类研究,因此可能NA获得的HBeAg清除与通过自发或PEG IFNα获得HBeAg清除的机制不同,从而对肝癌发生率的影响不同。
2.HBeAg清除和HBeAg血清学转换对肝癌的发生风险的影响不同。
另外本研究提到NA治疗获得HBeAg清除后平均随访5年的HBsAg清除为7.9%,但我们知道NA治疗获得HBeAg清除的概率较低,本研究为16.2%,而这些人群再NA治疗平均5年后HBsAg清除率为7.9%,那么NA长期治疗后获得HBsAg清除的概率仅为1.3%。因此NA治疗后不仅HBeAg清除和HBsAg清除率较低,肝癌发生率也相当高,即便是获得了HBeAg清除。要想获得更高的HBsAg清除率并更好的降低肝癌发生风险,则需联合核苷类药物和长效干扰素来治疗。
参考文献:
Lee HW, Lee JI, Kim S, et al. Cumulative incidence of hepatocellular carcinoma and hepatitis B surface antigen Seroclearance after Nucleos(t) ide analogue-induced hepatitis B e antigen Seroclearance[J]. BMC Gastroenterol, 2020, 20(1): 113.
本文转自:雨露肝霖