头颈癌是上气消化道、唾液腺和甲状腺异质性恶性肿瘤的集合。全球范围内,每年有83万人被诊断为头颈部肿瘤,有43万人死于该病,头颈部鳞状细胞癌(HNSCC)占所有头颈部肿瘤的90%,可见于于不同的解剖部位(图1)。大约75%的HNSCC与*草烟**和酒精有关,少数HNSCC是由人乳头瘤病毒(HPV)感染引起
由于外科手术和综合治疗的发展和进步,HNSCC患者的局部控制率和生活质量有所提高,但近几十年来总体生存率并未大幅提高,约有一半的患者在 1~ 5 年内死亡,因此 5年生存率仍很低,主要原因是肿瘤的复发或转移,而复发性或转移性 HNSCC 常无法进行手术治疗,放化疗效果也差。近年来,靶向治疗和免疫治疗的发现为复发性或转移性 HNSCC 患者带来了新希望。本文总结了HNSCC近年来在化疗、靶向治疗和免疫治疗的研究进展。
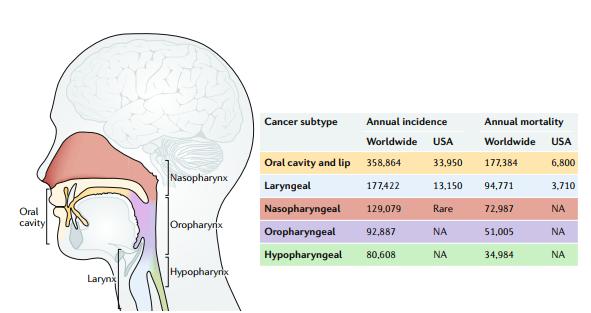
图1 HNSCC不同发病部位
01 化疗
在过去的三十年中,研究者们付出了很大努力去探索放疗中增加系统治疗对HNSCC患者的影响。一项含93项研究的Meta分析发现,与放疗相比,同步放化疗的5年OS获益率提高了6.5%。在该研究中,联合顺铂单药治疗与同期放化疗疗效相同。
每3周在第1、22、43天给予高剂量顺铂(100mg/m2),同时常规分割放疗7周以上,或在第1和22天进行加速分割放疗,或辅助放疗6周以上,仍然是标准治疗。
低剂量顺铂 vs 高剂量顺铂
每周低剂量顺铂对比高剂量有几个优点,包括易于给药和降低毒性,尽管被广泛使用,但之前仅在小样本前瞻性试验中对其进行过评估。Quon等人开展的一线研究显示,低剂量(20mg/m2)放射增敏在不可切除HNSCC中并不发挥作用,低剂量放射增敏不充分不仅增加了毒性,也没有改善生存率,但生存率没有统计学差异。
Noronha等人在一项单中心随机试验中,评估了给予300例III/IV期HNSCC患者每周低剂量顺铂(30 mg/m2)和每3周高剂量顺铂(100 mg/m2)同时放疗的疗效,结果显示,高剂量的2年局部控制率更优。
此外,更重要的变量是累积剂量还是最高剂量是仍有待解答,RTOG 0129研究评估了加速放疗期间给予两剂100 mg/m2顺铂(累积200 mg/m2)与常规放疗期间给予三剂100 mg/m2顺铂(累积剂量300 mg/m2)的疗效,结果无明显差异。
每周给予40-50 mg/m2可能改善患者疗效,目前正在进行临床研究。
02 靶向治疗
EGFR抗体
EGFR过表达见于90%HNSCC患者中,EGFR高表达与较差生存相关。西妥昔单抗是一种IgG1单克隆抗体,竞争性地*制剂抑**EGFR配体与EGFR受体的结合,而改变肿瘤细胞生长所需的EGFR依赖的信号通路。西妥昔单抗已FDA批准用于HNSCC的多个适应证。西妥昔单抗治疗复发或转移性HSNCC患者的有效率为13%,EXTREME研究显示,在复发和/或转移性HNSCC患者的一线化疗中加用西妥昔单抗可提高缓解率、无进展生存期(PFS)和总生存期(OS),中位OS为10.1个月vs 7.4个月(P = 0.04)。
在局部晚期患者中,与单纯放疗(29.3个月)相比,西妥昔单抗联合放疗可改善OS达49.0个月(P = 0.03)。
值得一提的是,许多其他EGFR抗体,例如帕尼单抗(panitumumab)、zalutumumab、吉非替尼、阿法替尼或拉帕替尼在HNSCC患者中都没有表现出显著的临床活性。
EGFR抗体+放化疗的临床研究产生了不同的结果,III期RTOG研究未能证明西妥昔单抗+顺铂+放疗可改善患者的临床结局,而在另一项研究中,nimotuzumab+放疗+每周顺铂(30mg/m2)可改善患者的PFS和无病生存期(DFS)。
其他靶向药物
癌症基因组图谱(TCGA)分析了HNSCC中的不同基因组亚型,数据显示,在HPV阴性HNSCC患者中广泛存在TP53和CDKN2A的缺失(图2)。在HPV+ HNSCC中存在TRAF3、PIK3CA和E2F1的缺失和突变。总的来说,HNSCC中最有潜力的靶点包括PI3K信号通路蛋白和细胞周期蛋白依赖性激酶4/6。
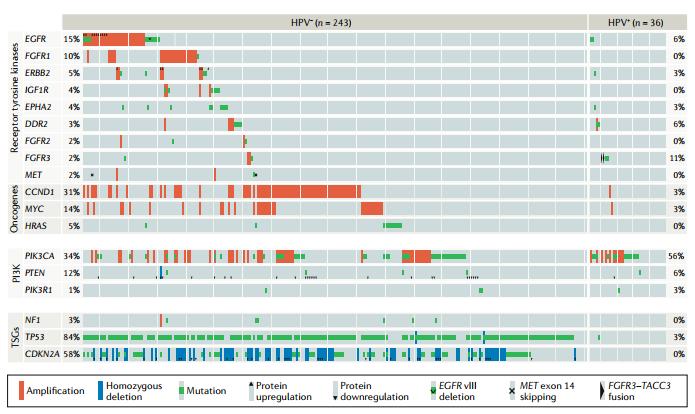
图2 HNSCC中潜在的驱动基因(TCGA)
03 免疫治疗
在过去10年里,HNSCC治疗领域最显著的进展是免疫治疗。
2016年,FDA批准了首个PD-1抗体用于治疗铂类难治性复发/转移性HNSCC。Ib期KEYNOTE-012和其扩展队列均显示出了帕博利珠单抗的持久应答(表1),加速了帕博利珠单抗的获批。不久后,在CheckMate 141研究中,纳武利尤单抗改善了复发/转移性HNSCC患者的OS和QOL,纳武利尤单抗组和化疗组的1年OS率分别为36%和16.6%,基于此,纳武利尤单抗也获FDA批准。
表1 HNSCC中的PD-1抗体的临床研究
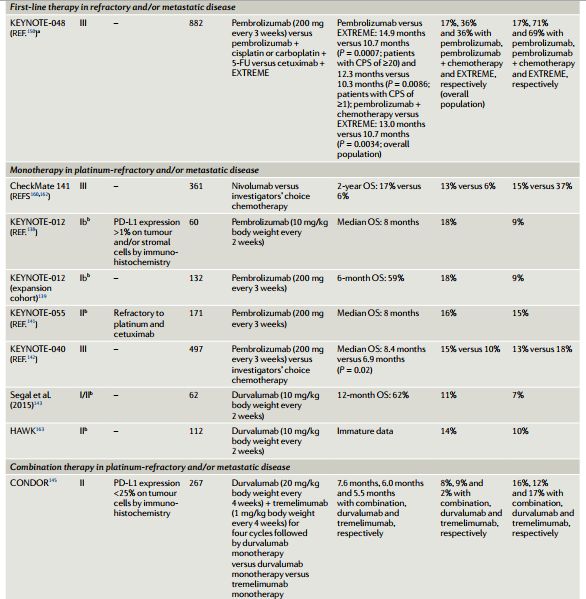
II期KEYNOTE-055和III期KEYNOTE-040研究进一步确认了帕博利珠单抗的疗效。在KEYONTE-040研究中,497例铂类难治性或复发/转移性HNSCC随机分配接受帕博利珠单抗和标准治疗,帕博利珠单抗明显改善了OS,两组中位OS分别为8.4个月和6.9个月(P=0.016)。但是,纳武利尤单抗和帕博利珠单抗仅在少数人群中有持久的生存获益。
德瓦鲁单抗用于HNSCC的研究正在进行中,在一项I/II期研究中,德瓦鲁单抗在晚期患者中的客观缓解率为11%。
生物标志物和免疫治疗
PD-L1在50% ~ 60%的HNSCC中表达,是HNSCC中抗肿瘤免疫逃避机制的重要构成。数据显示,PD-1+调节性T细胞更容易浸润HPV+ HNSCC肿瘤细胞。PD-L1阳性率可用多种评分方法测定。肿瘤比例评分(TPS)是PD-L1染色肿瘤细胞百分比,综合阳性评分(CPS)是PD-L1+肿瘤细胞和免疫细胞与肿瘤细胞总数的比值。
生物标志物筛选已在几个研究中体现出重要性,CheckMate 141研究中,在PD-L1 CPS≥1%患者中,纳武利尤单抗和化疗组的中位OS分别为8.7个月和4.6个月,而在<1%患者亚组中,两组的中位OS为5.7个月。
III期KEYNOTE- 048研究纳入了825名患者,评估了帕博利珠单抗单药或联合和EXTREME方案(西妥昔单抗+5 -氟尿嘧啶+顺铂或卡铂)用于复发/转移性HNSCC一线治疗的疗效。中期数据分析显示,与EXTREME方案相比,帕博利珠单抗单药可显著改善PD-L1 CPS≥20或>1患者的OS,而联合治疗可改善未经选择患者的OS(表2)。
其他实体瘤中,肿瘤突变负荷也与免疫治疗应答相关,在HNSCC中的价值正在探索中,此外,HPV+可能是另一个潜在的生物标志物,CheckMate 141研究中,HPV+ HNSCC对PD-1抗体应答更好。
免疫联合放疗
几项I/II期研究在局部晚期HNSCC患者中探索了与PACIFIC研究类似治疗模式的疗效(NCT02252042、NCT02586207、NCT02819752、NCT02707588、NCT02289209)。
2018 ASCO年会上的一项II期研究显示,与纳武利尤单抗相比,立体定向放射治疗+纳武利尤单抗并不能改善复发/转移HNSCC患者的OS。
双免疫治疗
大部分患者对HNSCC对PD-1抗体单药没有应答,为提高应答率,正在进行多项临床研究。
NCT02551159和NCT027451570研究中探索了PD-1+CTLA-4在HNSCC中的活性。II期CONDOR研究中,tremelimumab+德瓦鲁单抗在复发/转移性HNSCC患者中已观察到一定的疗效。
关于治疗性疫苗在HNSCC中的活性也在进行临床研究。其他方法比如HPV多肽疫苗或共刺激制剂(Toll样受体、OX40、CD40L和CD13)也正在研究中。
在Active8研究中,195例患者随机分配接受EXTREME±Toll样受体8激动剂Motolimod,结果并无差异,但在HPV+ HNSCC亚组中,Motolimod+EXTREME明显改善PFS和OS,分别为7.8个月vs 5.9个月(P=0.046),15.2个月 vs 12.6个月(P=0.03)
04 小结
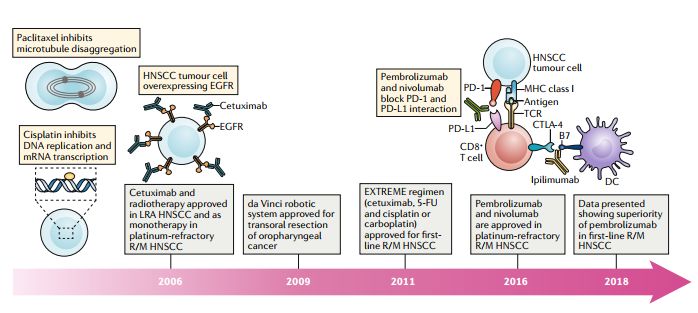
图3 HNSCC中的主要研究进展
参考文献:
1. Cramer JD, Burtness B, Le QT,et al.The changing therapeutic landscape of head and neck cancer. Nat Rev Clin Oncol. 2019 Nov;16(11):669-683. doi: 10.1038/s41571-019-0227-z. Epub 2019 Jun 12.
2. Vermorken JB, Mesia R, Rivera F, et al. Platinum-based chemotherapy plus cetuximab in head and neck cancer. N Engl J Med. 2008 Sep 11;359(11):1116-27. doi: 10.1056/NEJMoa0802656.