转载自:国际肝病
编者按
据世界卫生组织发布的2020年全球最新癌症负担数据,肝癌位居我国癌症新发病例第五位,是我国第二大癌症致死病因[1],防治形势依然严峻。但令人欣喜的是,首个获批的肝癌一线免疫联合方案(阿替利珠单抗联合贝伐珠单抗,简称“T+A”)于2020年走入临床,为患者带来新生。相比以往系统治疗方案,除有效性外,高安全性亦是“T+A”的重要优势。那么对比当前同类方案呢?安全性优势能否赢得额外生存获益? 北京大学肿瘤医院肝胆胰外科一科主任邢宝才教授 应本刊邀请,就此分析当前免疫联合治疗进展,并着重介绍安全性之于患者获益的重要性。
中位OS突破2年:相比全球,“T+A”更适合中国肝癌患者
目前晚期肝癌的整体治疗有效率明显提升,免疫联合相对靶向单药提升到了30%~40%的水平。免疫联合治疗主要包括PD-1/L1*制剂抑**联合抗血管生成靶向药物,抗血管药物又分为抗VEGF类和小分子TKI类药物两种。目前有三项联合方案研究备受关注:帕博利珠单抗联合仑伐替尼的Ib期研究(KEYNOTE-524)、卡瑞利珠单抗联合阿帕替尼的II期研究(RESCUE)和“T+A”的III期研究(IMbrave150)。
“T+A”是其中唯一获得高级别循证医学证据III期研究支持的联合方案,被美国NCCN、欧洲ESMO、中国CSCO等一系列国内外权威肝癌诊疗指南或规范推荐为一线用药,于2020年在我国以及全球多个国家和地区获批上市,成为目前晚期肝癌一线免疫联合疗法中唯一获批的方案。
据IMbrave150研究最新数据,尽管中国患者基线特征相比全球患者具有更多不利预后因素,但中国亚群“T+A”组患者中位OS相比全球率先突破2年(图1),提示“T+A”方案可能更适合中国患者。
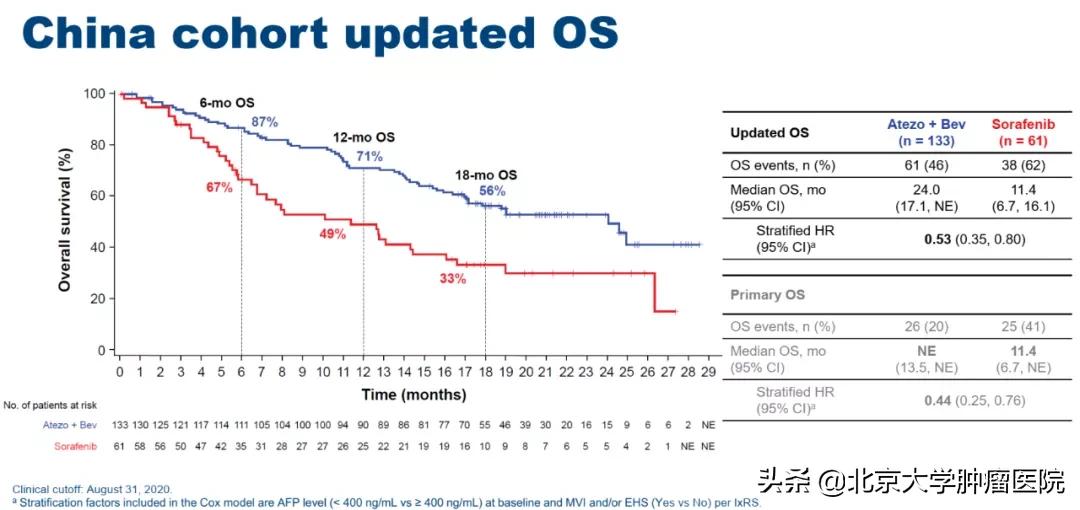
图1. IMbrave150研究:中国亚组OS分析[2]
总之,目前肝癌治疗首选联合治疗,“T+A”相比其他免疫联合方案在有效性和安全性上均有较大优势,而且患者治疗时可以正常生活和工作。所以, "T+A"方案势必将在中国肝癌患者中发挥重要的作用。
更低AE、更好耐受:“T+A”安全性优势较其他免疫联合方案突出
在应用药物治疗肿瘤时,一方面需要关注药物治疗的有效性,另一方面也应该关注药物的安全性,同时还需要关注药物对患者生活质量的影响。
在备受瞩目的三个联合方案中,卡瑞利珠单抗联合阿帕替尼和帕博利珠单抗联合仑伐替尼的3级及以上治疗相关AE分别为77.4%[3]和67%[4],即有2/3~3/4患者应用后出现严重毒副反应,对患者生活质量影响很大;而“T+A”的3级及以上治疗相关AE为45%(图2),患者耐受性更好,尤其是体弱、肝功能差的患者。 从治疗完成率上看,“T+A”相比其他方案的突出安全性优势将使更多患者完成治疗。
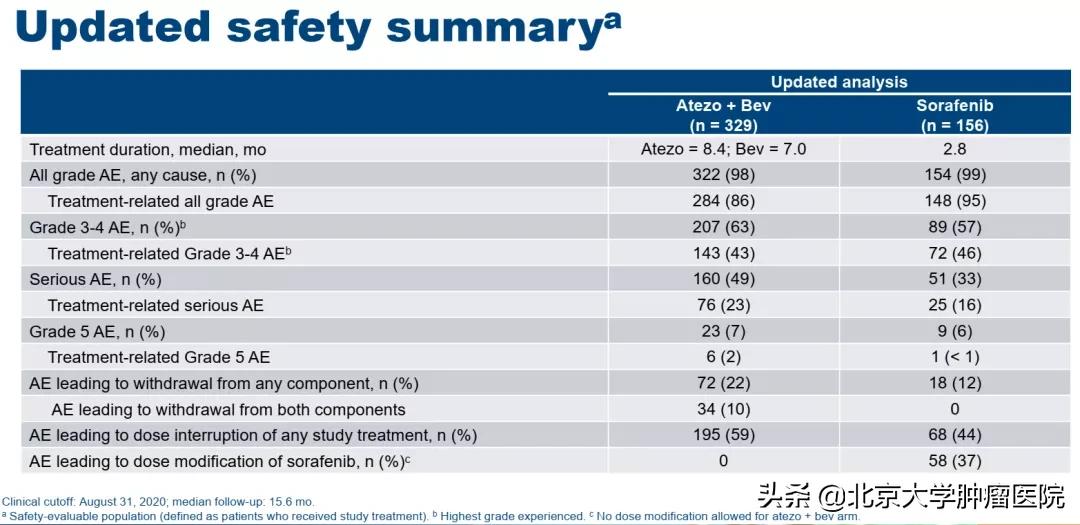
图2. IMbrave150研究:安全性分析[2]
此外,“T+A”方案中的贝伐珠单抗最早上市用于肠癌,在进入中国市场后,至今已有十余年,积累了丰富的临床用药经验。作为抗血管生成药物,其可能对手术出血有些影响,但若不行手术仅用于晚期系统治疗,则基本无副作用,总体安全性好,无消化道和骨髓抑制方面的AE发生。
更多切除、更长生存:“T+A”高安全性为不可切除患者赢得转化治疗机会
肝癌早期没有明显的不适表现,患者一旦出现不适,再做检查,大多数确诊时即为中晚期。我国初诊可能获得手术切除机会的患者仅20%~30%[5],换言之70%~80%的肝癌患者初诊即没有手术机会。外科切除可延长生存,是肝癌治疗的重要手段,晚期HCC可通过转化治疗来获得切除的机会。
既往索拉非尼的ORR约为3%,应用索拉非尼治疗无法实现转化。“T+A”等免疫联合方案的ORR明显提高,使晚期HCC患者通过药物治疗实现转化变为可能,例如根据RECIST 1.1标准,“T+A”方案的ORR达到了30%(图3),是现有同类免疫联合方案中较为理想的方案。
此外,转化并非一次用药就能实现,患者通常需要持续多个治疗周期。 “T+A”的高安全性和良好耐受性为患者完成足量治疗提高了可能性,进而为转化治疗赢得更多机会。
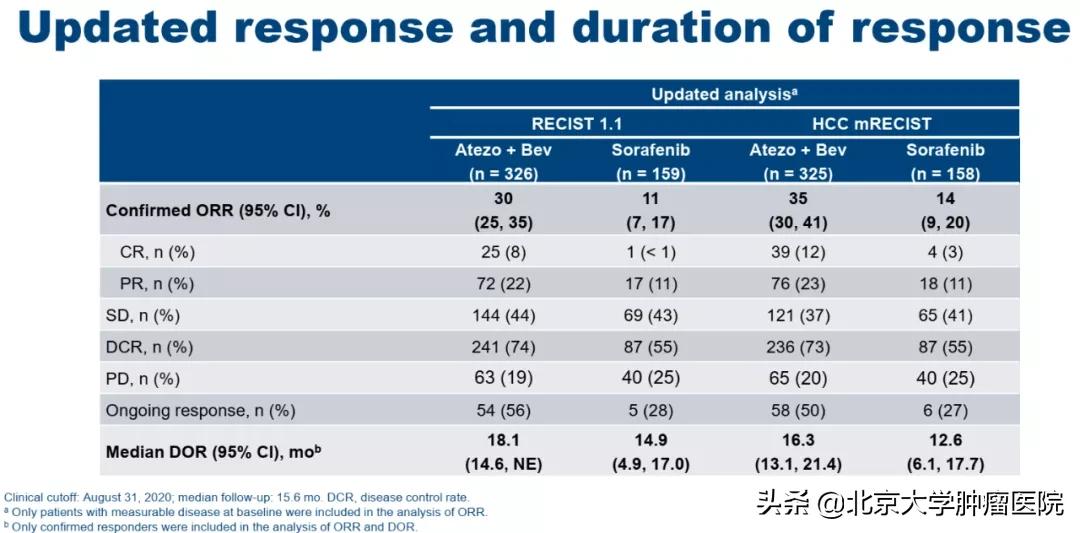
图3. IMbrave150研究:ORR和DOR分析[2]
追求更高生活质量:患者报告结局(PRO)为肝癌临床研究注入新指标
对于肝癌患者而言,除了活得更久,活得更好也十分重要。IMbrave150研究的全球高质量患者报告结局(PRO)结果显示, “T+A”组患者报告的生活质量的恶化时间较对照组索拉非尼延长两倍有余 (图4),对患者生活质量影响小。“T+A”提供了一个很好的契机,即关注肝癌患者的生活质量需求,肿瘤临床研究理念因此发生变化。
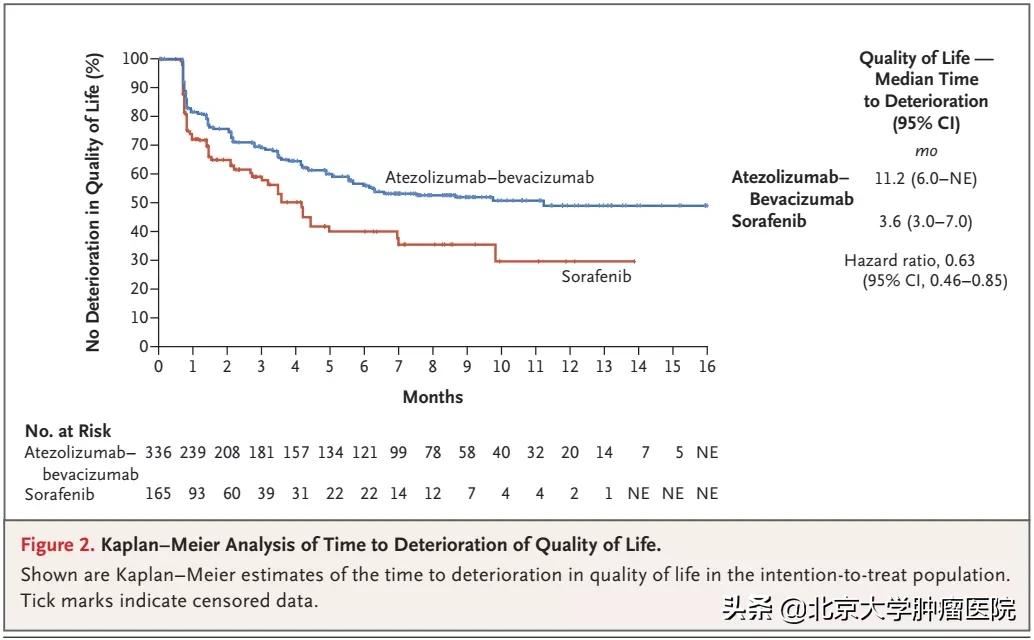
图4. IMbrave150研究:生活质量恶化时间的Kaplan-Meier分析[6]
邢宝才教授表示,临床用药选择由多种因素综合决定,包括药物有效性、副作用、生活质量影响等因素。通常临床研究都是关注OS、PFS和ORR这些客观临床指标,很少有文献报道PRO。 IMbrave150研究为此做了很好的示范,PRO作为临床结局的指标,正逐渐被人们认可和重视,相信此后在中国肿瘤临床研究中PRO会受到更多关注。
相信,随着以“T+A”为代表的免疫联合治疗的应用,不可切除肝癌的整体治疗有效性和安全性将得到大幅提升。基于这样的背景,PRO等关注患者生存质量的指标将会越来越受重视。
小结
综上,选择“T+A”治疗可带来多重获益:①可显著延长不可切除HCC患者的生存期;②安全性良好,使患者能够耐受并完成治疗;③可以实现转化,使部分患者获得手术治疗机会;④不影响患者正常生活,使患者拥有高生活质量。尽管目前HCC药物进步离期望还有一定距离,但“T+A”的问世使我们信心倍增,期待更多更有效药物或治疗方法的出现,以更好地治疗患者,造福我国广大肝癌患者。

专家简介
邢宝才教授
主任医师,博士生导师
北京大学肿瘤医院肝胆胰外一科主任
中华医学会外科学分会肝脏外科学组全国委员
中国医师协会结直肠肿瘤分会肝转移委员会主任委员
中国抗癌协会大肠癌专委会肝转移学组副组长
中国医师协会外科分会MDT专委会副主任委员
中国医促会肝脏外科分会副主任委员
中国研究型医院协会肿瘤外科委员会副主任委员
参考文献:(可上下滑动查看)
[1] https://www.iarc.fr/faq/latest-global-cancer-data-2020-qa/
[2] Finn RS, Qin S, Ikeda M, et al. IMbrave150: updated overall survival data from a global, randomized, open-label Phase III study of atezolizumab + bevacizumab vs sorafenib in patients with unresectable hepatocellular carcinoma. ASCO-GI 2021. A267.
[3] Xu J, Shen J, Gu S, et al. Camrelizumab in Combination with Apatinib in Patients with Advanced Hepatocellular Carcinoma (RESCUE): A Nonrandomized, Open-label, Phase II Trial. Clin Cancer Res. 2021 Feb 15;27(4):1003-1011.
[4] Zhu AX, Finn RS, Ikeda M, et al. A phase Ib study of lenvatinib (LEN) plus pembrolizumab (PEMBRO) in unresectable hepatocellular carcinoma (uHCC). ASCO2020. Poster#4519.
[5] 中华人民共和国国家卫生健康委员会医政医管局.原发性肝癌诊疗规范( 2019年版)[J].临床肝胆病杂志,2020,36 (2) :277-292.
[6] Finn RS, Qin SK, Ikeda M, et al. Atezolizumab plus Bevacizumab in Unresectable Hepatocellular Carcinoma. N Engl J Med. 2020 May 14;382(20):1894-1905.
来源:《国际肝病》编辑部