来自日本东京大学的Kazuko yamaguchi-shinozaki专注于研究干旱期间各种基因的表达。她对干旱诱导基因的表达谱进行了整体分析,并分析了它们在拟南芥中的功能。尤其是DRE结合蛋白DREB1/CBF和DREB2在冷干旱响应基因表达中起转录激活作用。

下面从她重要文献中归纳总结她的研究*法大**:
方法一:诱导处理分离快速胁迫响应基因
用脱水胁迫10小时后从8日龄植物中分离的poly A RNA构建cDNA文库。用从未受胁迫的植物中分离的poly ARNA制备的cDNA差异筛选cDNA文库。并用从植物中分离的poly A RNA制备的cDNA脱水胁迫10小时36个斑块与来自10小时脱水植物的32P标记的cDNA产生更强的杂交信号。在体内切除36个噬菌体克隆的质粒区域并用于转化大肠杆菌细胞。使用限制性图谱和cDN*片A**段的边界DNA序列分析来自所得质粒的cDN*片A**段。
为了在分子水平上了解早期植物对脱水胁迫的反应,从1小时脱水的拟南芥植物的cDNA文库中分离出27个cDNA克隆。基于Southern印迹杂交将这些克隆分成16个ERD组。ERD由两个cDNA克隆(10和73)组成,这些克隆具有任何ERD克隆中最长的插入片段。这些cDNA的部分测序表明,10和73个克隆均来自同一基因的mRNA(未发表的观察)。在这里,我们报告ERD1克隆编码与来自大肠杆菌的ATP依赖性Clp蛋白酶的ATP结合亚基和来自酿酒酵母的HSP104同源的蛋白质。
1. 用与rd29基因3'侧翼区相对应的DN*片A**段进行RNA凝胶印迹分析,分析这些基因的特异性表达。rd29A基因在脱水开始后20分钟内诱导,2小时后强烈表达。相比之下,rd29B mRNA在脱水2小时后才累积到可检测的水平。10小时检测到的RD29B mRNA的最高水平大约是2小时时RD29AmRNA水平的十分之一。RD29A mRNA在暴露于低温(4°C)后5小时内诱导,并在至少24小时内检测到(图1)。然而,RD29b mRNA在24小时内没有积累。RD29A mRNA在高盐处理开始后1小时内检测到,脱水情况也是如此,在5小时内达到最大值(图1)。相比之下,rd29B是在高盐处理后~2h诱导缓慢。作为对照,当植物从琼脂转移到水中时,检测到rd29A mRNA快速但微弱的表达(图1)。因此,RD29a mRNA似乎是由植物从低渗透势的生长条件转移到高渗透势的生长条件,反之亦然。热应激对RD29基因的诱导均无影响。RD29A和RD29B基因在拟南芥基因组上相邻,在脱水、低温、高盐或外源脱落酸(ABA)处理条件下诱导表达。RD29A至少有两个顺式作用元件,一个参与ABA对脱水的相关反应,另一个由渗透势的变化引起,rd29B含有至少一个顺式作用元件,参与ABA反应缓慢的诱导。我们在转基因拟南芥和*草烟**中分析了rd29A基因启动子提出了一种新的顺式作用的脱水反应元件(DRE),含有9bp的TACCGACAT,参与了rd29A对脱水或高盐条件的首次快速反应,DRE也参与低温诱导。在脱水、高盐、低温条件下,不同顺式作用元件在rd29A的两步诱导和rd29B的缓慢诱导中起作用。使用酵母单杂交筛选分离编码DRE-/CRT-结合蛋白,CBF/DREB1(C-重复结合因子/DRE-结合蛋白1)和DREB2的cDNA。这些蛋白质含有在ERF(乙烯响应元件结合因子)和AP2蛋白质中发现的保守DNA结合结构域。这些蛋白质特异性结合DRE/CRT序列并激活由DRE/CRT序列驱动的基因的转录。

为了阐明在渗透胁迫条件下与DREB2A基因相关的转录机制,我们产生了DREB2A启动子的一系列截短和碱基取代的变体,并分别评估了它们的转录活性。我们发现距离转录起始位点约-100bp的ABRE和偶联元件3(CE3)样序列对于DREB2A的脱水反应性表达是必需的。将我们的瞬时表达分析与酵母单杂交和染色质免疫沉淀(ChIP)分析表明ABRE结合蛋白1(AREB1),AREB2和ABRE结合因子3(ABF3)bZIP转录因子可以ABRE依赖性方式结合并激活DREB2A启动子。与渗透胁迫处理相比,外源ABA应用仅诱导DREB2A转录物的适度积累。然而,发现渗透胁迫诱导的DREB2A表达在几种ABA缺陷型和ABA不敏感型突变体中显着受损。这些结果表明,除了ABA非依赖性途径外,ABA依赖性途径在DREB2A的渗透胁迫响应表达中起积极作用。
拟南芥脱水反应元件结合蛋白2A(DREB2A)作为转录激活因子起作用。增加对渗透压和热应激的耐受性;然而,其表达也导致生长迟缓和繁殖减少。为了避免这些不利影响,预计DREB2A的表达受到严格调控。我们鉴定了DREB2A的短启动子区域,其在非应激条件下抑制其表达。酵母单杂交筛选相互作用因子鉴定生长调节因子7(GRF7)。GRF7与DREB2A启动子结合并抑制其表达。在人工miRNA沉默系和GRF7的T-DNA插入系中,与非胁迫条件下的野生型相比,DREB2A转录增加。先前未发现的顺式元件,靶向GRF7的顺式元件(TGTCAGG),通过电泳迁移率变动分析鉴定为DREB2A的短启动子区域中GRF7的靶序列。GRF7敲除植物的微阵列分析显示突变植物中的大量上调基因也对渗透胁迫和/或脱落酸有响应。这些结果表明GRF7作为广泛的渗透胁迫响应基因的阻遏物起作用,以防止在正常条件下的生长抑制。脱水反应元件结合蛋白2A(DREB2A)作为拟南芥干旱和热胁迫耐受性的关键转录因子,并诱导许多干旱和热胁迫诱导基因的表达。
尽管DREB2A表达本身是由应激诱导的,但DREB2A的翻译后调节(包括蛋白质稳定化)是其转录活性所必需的。称为负调节结构域(NRD)的DREB2A的30-a a中心区域的缺失将DREB2A转化为称为DREB2A-CA的稳定且组成型活性形式。然而,这种稳定化和活化的分子基础仍然未知十年。在这里,我们确定BTB/POZ和MATH域蛋白(BPMs),基于Cullin3(CUL3)的E3连接酶的底物衔接子,作为DREB2A相互作用蛋白。我们观察到DREB2A和BPM在细胞核中相互作用,并且DREB2A的NRD足以与BPM相互作用。BPM敲低植物在热和干旱胁迫条件下表现出增加的DREB2A积累和DREB2A靶基因的诱导。遗传分析表明,BPM表达的消耗通过DREB2A稳定赋予增强的耐热性。因此,BPM-CUL3 E3连接酶可能是导致NRD依赖性DREB2A降解的长期寻找的因子。通过对DREB2A稳定性的负调控,BPMs调节热应激反应并防止过量DREB2A对植物生长的不利影响。此外,我们在各种转录因子中发现了BPM识别基序,这暗示了BPM介导的蛋白水解通过加速转录因子的更新对不同细胞反应的一般贡献。
我们用DREB1A的cDN*片A**段作为探针筛选了拟南芥基因组DNA文库,并分离了DREB1A和2个相关基因DREB1B(=CBF1)和DREB1C。它们以8.7kb区域中的B,a,C顺序排列。拟南芥染色体4。使用基因特异性探针的Northern印迹分析显示3个DREB1基因主要由冷胁迫诱导,但不是由叶,根和茎中的渗透胁迫诱导。在所有3个基因的启动子区域中发现了几个保守序列。由DREB1启动子驱动的β-葡糖醛酸糖苷酶(GUS)报告基因在转基因拟南芥植物中通过低温在转录水平诱导。
2. 从一个命名为ERD1的cDNA克隆中获得了该序列,从拟南芥的1小时脱水植物的cDNA文库中分离。该克隆(3150bp)含有946个氨基酸残基的开放阅读框,其与Clp ATP依赖性的调节亚基具有大于34%的序列同一性。大肠杆菌中的蛋白酶,蛋白序列含有推定的叶绿体靶向信号N端。Southern印迹分析表明在拟南芥中存在另外的ERD1相关基因。ERD1基因的表达受脱水胁迫强烈诱导,但不受热,冷或重金属胁迫的诱导。此外,ERD1基因表达不受植物生长调节剂(如生长素,细胞分裂素,脱落酸和赤霉酸)处理或饥饿胁迫10小时的强烈影响。已显示erd1基因响应于水分胁迫和黄化而上调。使用与拟南芥中的萤光素酶(LUC)报道基因融合的erd1启动子区进行启动子研究以鉴定所涉及的推定的顺式元件。结果表明,负责脱水和黄化过程中基因表达的顺式元件分别位于erd1启动子的两个不连续部分。碱基取代分析显示-599至-586的14bp区域和-466至-461的myc识别基序对于在脱水植物中诱导LUC活性是必需的。另一方面,碱基取代分析显示,黄化诱导的增加需要脱落酸响应元件(ABRE)样序列(从-199到-195)和ACGT序列(从-155到-152)。这些结果表明erd1启动子含有两种不同的调节系统,其参与脱水应激和黑暗诱导的衰老的上调。
使用酵母单杂交系统,我们分离了编码ZFHD1转录激活因子的cDNA,其特异性结合ERD1的62bp启动子区域,其含有ZFHDR。体外和体内分析均证实ZFHD1与ZFHDR特异性结合,并且ZFHD1的表达由干旱,高盐度和脱落酸诱导。ZFHD1的DNA结合和激活域分别位于C端同源域和N端锌指域。过表达ZFHD1的转基因植物的微阵列分析显示几种胁迫诱导基因在转基因植物中上调。转基因植物表现出较小的形态表型并且具有显着的干旱胁迫耐受性改善。使用酵母双杂交系统,我们检测到ZFHD1和结合NAC蛋白的NACRS之间的相互作用。此外,ZFHD1和NAC基因的共过表达将转基因植物的形态表型恢复到接近野生型状态,并增强拟南芥T87原生质体和转基因拟南芥植物中ERD1的表达。
3. 在对应于拟南芥脱水反应基因的9个cDNA克隆(命名为RD)中,进一步分析了两个克隆RD19和RD21。Northern印迹分析显示RD19和RD21 mRNA均未被脱落酸诱导。RD19和RD21 mRNA合成均不响应冷或热应激。另一方面,在高盐条件下强烈诱导RD19和RD21 mRNA的转录,这表明对应于RD19和RD21的基因可以通过植物细胞的渗透势的变化诱导。由两个RD cDNA编码的推定蛋白RD19和RD21具有半胱氨酸蛋白酶(CysP)催化位点典型的氨基酸(aa)序列。RD21和RD19似乎含有在蛋白质分泌中起作用的信号肽。RD21包含类似于C端延伸肽的氨基酸序列。系统发育树分析表明,推定的RD21和RD19蛋白是完全不同类型的CysP。基因组Southern分析显示每个基因家族包含至少两个不交叉杂交的成员。
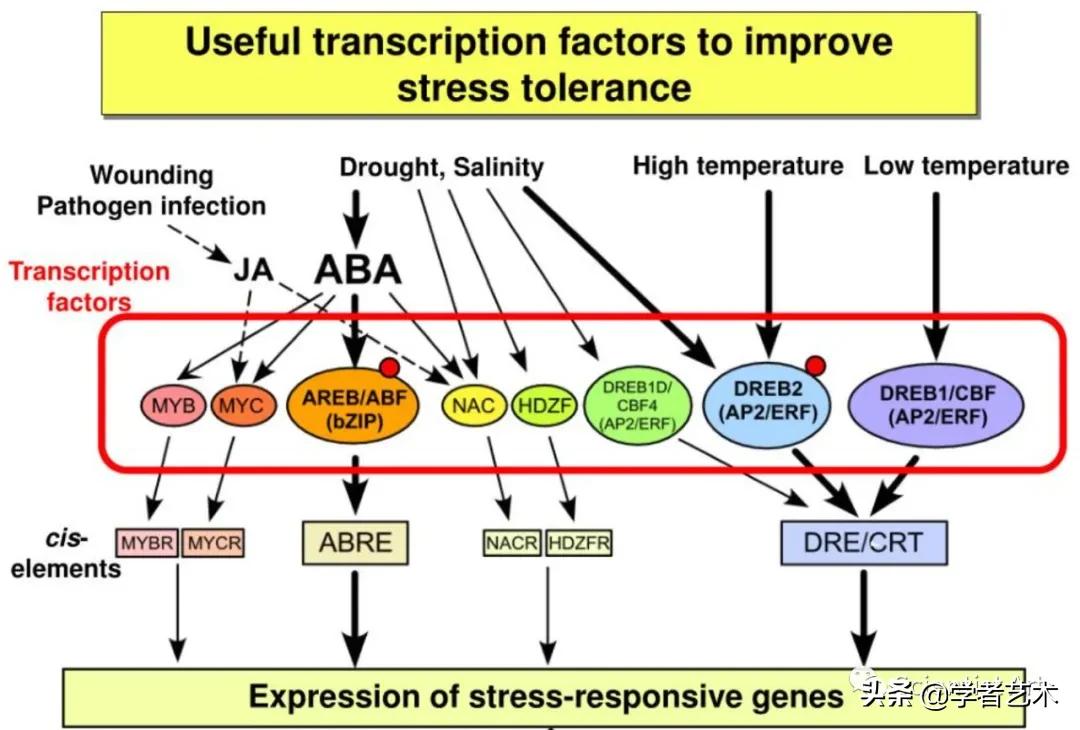
4. 对从拟南芥的1小时脱水植物的cDNA文库中分离的两个cDNA克隆(命名为ERD10和EDR14)进行测序和表征。预测的ER10和ERD14多肽对Glu(分别为19.62%和21.08%)和Lys(分别为16.15%和18.38%)具有组成偏倚,并且都缺乏Trp和Cys残基。从两种cDNA推导的氨基酸序列与II组LEA(晚期胚胎发生丰富)蛋白质非常相似,这是一类在胚胎发生晚期积累并且其基因表达由植物激素脱落酸(ABA)诱导的蛋白质。基因组Southern印迹分析表明存在ERD10相关基因。在脱水1小时内强烈诱导ERD10和ERD14的基因的表达,并且在脱水24小时期间检测到升高的转录物水平。erd10和erd14基因的冷诱导表达的Northern印迹分析揭示了两步诱导过程。早期诱导发生在1小时内,二次诱导发生在冷应激开始后5小时。ABA的施加诱导了两种基因的表达,但2,4-D,BA,ABA和GA3的应用不影响这些基因的表达。在抽苔植物中,在茎,茎叶,根和花中检测到ERD10和ERD14转录物,但它们的水平在种子形成期间降低,并且在成熟后期的种子中仅检测到低水平的转录物。
5. 从1-h-脱水拟南芥中分离的cDNA克隆ERD5(早期响应脱水)编码脯氨酸(Pro)脱氢酶(ProDH)的前体,其是参与Pro转化为谷氨酸的第一步的线粒体酶。当植物脱水时,erd5(ProDH)基因的转录物是不可检测的,但是当植物随后再水化时,大量的转录物积累。在含有L-或D-Pro的培养基中在低渗条件下孵育的植物中也观察到转录物的积累。我们分离了ProDH基因推定启动子区域的1.4kb DN*片A**段。由1.4-kb ProDH启动子驱动的β-葡糖醛酸糖苷酶(GUS)报告基因不仅通过再水化诱导,而且通过低渗透压和L-和D-Pro在转基因拟南芥植物中以显着水平诱导。ProDH基因的启动子在生殖器官如花粉和雌蕊以及转基因植物的种子中指导强GUS活性。当转基因植物暴露于低渗透压和Pro溶液时,在营养组织如叶脉和根尖中检测到GUS活性。在低渗透压下转基因植物萌发期间GUS活性增加。讨论了促代谢与应激反应和发育的生理方面之间的关系。ProDH也由L-Pro和低渗透压诱导。补液下ProDH表达的诱导似乎是由累积的Pro和低渗透压引起的。我们分析了位于ProDH转录起始位点(启动子区域)5'的DNA区域,以鉴定参与L-Pro诱导和低渗透压诱导的转基因*草烟**(Nicotiana tabacum)和拟南芥植物表达的顺式作用元件。我们发现,ProDH启动 子中 的9 bp序列ACTCATCCT对于响应L-Pro和低渗透压的ProDH的有效表达是必需的。此外,ACTCAT是核心顺式作用元件,我们称之为促渗或低渗反应元件(PRE),这是ProDH的L-Pro反应和低渗反应表达所必需的。微阵列和RNA凝胶印迹分析显示21个L-Pro诱导型基因在其启动子区域具有前序列。这些结果表明,前序列在L-Pro应答基因表达中起重要作用。从拟南芥脱水制备的cDNA文库中分离和表征δ1-吡咯啉-5-羧酸酯(P5C)合成酶(cAtP5CS)(一种参与脯氨酸生物合成的酶)的cDNA。Southern印迹分析表明,拟南芥中仅存在一个拷贝的相应基因(AtP5CS)。来自拟南芥的P5CS蛋白(AtP5CS)的推导氨基酸序列显示出与来自Vigna aconitifolia的P5CS的74%同源性。Northern印迹分析显示P5CS基因是通过脱水,高盐和ABA处理诱导的,而不是通过热处理或冷处理诱导的。此外,由于先前在拟南芥中的处理,观察到脯氨酸的同时积累。还从拟南芥中分离出P5C还原酶(cAtP5CR)的cDNA,并进行Northern印迹分析。脱水或高盐胁迫未在很大程度上诱导AtP5CR基因。这些观察结果表明,在渗透胁迫下,AtP5CS基因在拟南芥脯氨酸的生物合成中起主要作用。6-bp序列ACTCAT充当顺式作用元件,参与拟南芥脯氨酸脱氢酶(ProDH)基因的低渗透压和脯氨酸反应性表达。搜索植物顺式作用元件的数据库显示ACTCAT序列类似于被bZIP转录因子识别的GCN4基序[ATGA(C/G)TCAT]。为了鉴定用于调节ProDH的转录因子,我们检查了拟南芥bZIPs是否作为ACTCAT序列的转录因子起作用。瞬时表达分析显示,S组bZIPs,AtbZIP11/ATB2,AtbZIP44,AtbZIP2/GBF5和AtbZIP53中的四种蛋白质形成ATB2亚组,其激活由ACTCAT序列驱动的GUS报告基因的表达,而其他bZIP和不同的家族。植物转录因子没有。在低渗条件下,ATB2亚组的反式激活活性增强。在凝胶迁移率变动分析中,ATB2亚组的重组蛋白与ACTCAT序列特异性结合。RNA凝胶印迹分析表明,AtbZIP2/GBF5和AtbZIP53以及ProDH的表达是由低渗透压诱导的。此外,我们显示sGFP::AtbZIP11/ATB2融合蛋白位于细胞核中。这些结果表明,ATB2亚组可作为拟南芥低渗透诱导型ProDH的转录激活因子。
6. 从脱水植物中分离的拟南芥RD26 cDNA编码NAC蛋白。RD26基因的表达不仅由干旱诱导,而且由脱落酸(ABA)和高盐度诱导。RD26蛋白位于细胞核中,其C末端具有转录活性。过表达RD26的转基因植物对ABA高度敏感,而RD26抑制的植物不敏感。微阵列分析的结果显示ABA-和胁迫诱导型基因在RD26过表达植物中上调并在RD26抑制植物中被抑制。此外,RD26在拟南芥原生质体中激活其靶基因的启动子。这些结果表明RD26在植物的非生物胁迫下在ABA诱导型基因表达中起转录激活因子的作用。
7. 在拟南芥中,脱水反应基因rd22的诱导由脱落酸(ABA)介导,但该基因在其启动子区域中不包括对应于共有ABA反应元件(ABRE)RYACGTGGYR的任何序列。rd22启动子的顺式调节区通过监测在用rd22的5'缺失启动子和GUS编码区之间构建的嵌合基因融合体转化的转基因*草烟**植物的叶中β-葡糖醛酸糖苷酶(GUS)报告基因活性的表达来鉴定。对应于rd22启动子的-207至-141位的67bp核苷酸片段赋予对无应答启动子上的脱水和ABA的响应性。67bp片段含有一些转录因子如MYC,MYB和GT-1的识别位点序列。rd22 mRNA的积累需要蛋白质合成的事实提高了rd22的表达可能受这些反式作用蛋白质因子之一调节的可能性,所述反式作用蛋白质因子的从头合成由脱水或ABA诱导。我们仔细分析了转基因*草烟**植物中rd22启动子的67bp区域,发现第一个MYC位点和MYB识别位点在脱水诱导的rd22基因表达中起顺式作用元件的作用。使用67bp区域作为探针,通过DNA配体结合筛选分离编码MYC相关DNA结合蛋白的cDNA,并命名为rd22BP1。rd22BP1cDNA编码一个68 kD的蛋白质,该蛋白质在MYC相关转录因子中具有基本区域-螺旋-环-螺旋亮氨酸拉链基序的典型DNA结合结构域。rd22BP1蛋白特异性结合67 bp片段中的第一个MYC识别位点。RNA凝胶印迹分析显示rd22BP1基因的转录由脱水胁迫和ABA处理诱导,并且其诱导先于rd22。我们已经报道了编码MYB相关蛋白ATMYB2的干旱和ABA诱导型基因。在使用拟南芥叶原生质体的瞬时反式激活实验中,我们证明rd22BP1和ATMYB2蛋白均激活与β-葡糖醛酸糖苷酶报道基因融合的rd22启动子的转录。这些结果表明rd22BP1(MYC)和ATMYB2(MYB)蛋白在rd22基因的脱水和ABA诱导表达中起转录激活剂的作用。
方法二:同源搜索激酶和膜受体
1. 由于真核细胞中的蛋白激酶具有高度保守的区域(Hanks和Quinn,1991),PCR可以与对应于那些保守区域的简并寡核苷酸一起使用以分离编码推定的蛋白激酶的cDNA。使用该策略,我们分离了含有来自拟南芥的蛋白激酶的部分序列的PCR扩增的DN*片A**段。其中包括编码酪蛋白激酶II,促分裂原活化蛋白激酶和钙依赖性蛋白激酶保守区的DN*片A**段。然后我们分离并鉴定了与PCR片段相对应的cDNA(Mizoguchi et al,19931994;Urao et al.,1994)
2. 从拟南芥中克隆编码Ca(2+)依赖性,钙调蛋白非依赖性蛋白激酶(CDPK)的两个cDNA克隆cATCDPK1和cATCDPK2,并测定它们的核苷酸序列。Northern印迹分析表明,对应于ATCDPK1和ATCDPK2基因的mRNA由干旱和高盐胁迫快速诱导,但不受低温胁迫或热胁迫诱导。用外源脱落酸(ABA)处理拟南芥植物对ATCDPK1或ATCDPK2的诱导没有影响。这些发现表明,环境渗透势的变化可以作为诱导ATCDPK1和ATCDPK2的触发因素。由ATCDPK1和ATCDPK2编码的推定蛋白质分别含有1479和1488bp的开放阅读框,命名为ATCDPK1和ATCDPK2,并且在氨基酸序列水平显示52%的同一性。ATCDPK1和ATCDPK2与大豆CDPK显示出显着的相似性(分别为51%和73%)。两种蛋白质都含有典型的丝氨酸/苏氨酸蛋白激酶的催化结构域和与钙调蛋白的Ca(2+)结合位点同源的调节结构域。基因组Southern印迹分析表明在拟南芥基因组中存在一些与ATCDPK1和ATCDPK2相关的其他基因。发现在大肠杆菌中表达的ATCDPK2蛋白相对于组蛋白底物优先磷酸化酪蛋白和髓鞘碱性蛋白,并且需要Ca 2+进行活化。
3. 我们在这里描述了编码蛋白激酶的cDNA的克隆和表征,该蛋白激酶与丝裂原活化蛋白激酶(MAPK)激酶激酶(MAPKKK或MEKK)家族的成员具有高度序列同源性;该cDNA命名为cATMEKKI(拟南芥MAP激酶或ERK激酶1)。推定的ATMEKK1蛋白的催化结构域与MAPKKK的催化结构域的氨基酸序列(例如来自粟酒裂殖酵母的Byr2,来自酿酒酵母的Ste11,来自酿酒酵母的Bck1,来自小鼠的MEKK和来自*草烟**的NPK1)。在过表达ATMEKK1的酵母细胞中,蛋白激酶在响应交配信息素时取代Ste11。在该研究中,通过Northern印迹分析检查三种蛋白激酶的表达:ATMEKK1(结构上与MAPKKK相关),ATMPK3(结构上与MAPK相关)和ATPK19(结构上与核糖体S6激酶相关)。这三种蛋白激酶的mRNA水平在触摸,寒冷和盐度胁迫下显着同时增加。这些结果表明,被认为响应各种细胞外信号的MAP激酶级联不仅在翻译后水平而且在植物的转录水平上受到调节,并且植物中的MAP激酶级联可以在存在下转导信号中起作用。
4. 磷脂酰肌醇-4-磷酸5-激酶(PIP5K)磷酸化磷脂酰肌醇-4-磷酸以产生磷脂酰肌醇-4,5-二磷酸作为两种第二信使,肌醇-1,4,5-三磷酸和二酰基甘油的前体,并且作为调节剂参与信号转导和细胞骨架组织的许多细胞蛋白。尽管PIP5K在许多生理过程中发挥了如此重要的作用,但仍有许多关于其与植物的关联尚待阐明。在针对已知酵母和哺乳动物PIP5K cDNA的拟南芥表达序列标签数据库中搜索,我们鉴定了两个克隆,其部分编码相同的拟南芥PIP5K,并分离出编码我们命名为AtPIP5K1的蛋白质的相应全长cDNA。在大肠杆菌中表达的重组AtPIP5K1在体外具有PIP5K活性。由于一些结构和生化差异,AtPIP5K1未被归类为I型或II型PIP5K.AtPIP5K1mRNA的表达通过用干旱,盐和脱落酸处理拟南芥植物而快速诱导,这表明AtPIP5K11参与水分胁迫信号转导。这些数据提供了磷酸肌醇信号级联与植物水分胁迫反应之间密切联系的证据。
5. 为了探索涉及植物细胞渗透调节的新候选转运系统,我们关注在转录组中缺水胁迫和/或ABA处理下上调的应激反应膜因子(Maruyama等,2009)。从这些中,我们选择了KUP/HAK/KT家族K+转运蛋白基因KUP6,它对缺水胁迫有反应(Maruyama等,2009)。最近发现该基因在ABA的拟南芥悬浮细胞中上调(Böhmer和Schroeder,2011)。在这里,我们证明了KUP钾转运蛋白家族在脱落酸(ABA)和生长素的控制下在此过程中起重要作用。我们为K(+)摄取转运蛋白6(KUP6),KUP8,KUP2/短下胚轴3和ABA反应性钾外排通道,保卫细胞向外整流K(+)通道(GORK)产生拟南芥多个突变体。三重突变体kup268和kup68-gork表现出增强的细胞扩增,表明这些KUP负调节膨胀依赖性生长。在突变体中使用(86)放射性钌离子((86)Rb(+))的钾吸收实验表明这些KUP可能参与拟南芥根中的钾流出。突变体显示生长素响应增加并且在侧根生长中对生长素*制剂抑**(1-N-萘基邻苯二甲酸)和ABA的敏感性降低。在缺水胁迫期间,kup68-gork损害ABA介导的气孔关闭,kup268和kup68-gork降低干旱胁迫的存活率。蛋白激酶SNF1相关蛋白激酶2E(SRK2E)是ABA信号传导的关键组分,与KUP6相互作用并磷酸化,表明KUP功能通过ABA信号复合物直接调节。我们提出KUP6亚家族转运蛋白通过平衡细胞生长中的钾稳态和干旱胁迫反应而成为渗透调节的关键因素。
6. 已经从拟南芥中分离出编码单体小GTP结合蛋白家族的新型Rab蛋白AtRabα的全长cDNA克隆。AtRabα具有210个氨基酸,计算分子量为23.3kDa。发现来自日本莲花的Rab1x和Rab1y具有最高的同源性。基因组DNA的Southern印迹分析表明AtRab-α由单拷贝基因编码。Northern印迹分析显示AtRabα mRNA的表达富含茎和根,但在叶和花中较差,这与其他拟南芥Rab基因的表达模式不同。
7. HsfA3是过表达DREB2A的转基因植物中上调最多的热诱导基因之一。本研究中,HsfA3表达谱分析和HsfA3反式激活分析表明HsfA3的表达受HS下DREB2A的直接调控。使用过表达HsfA3的转基因植物的微阵列分析还显示HsfA3的过表达诱导许多热诱导基因。此外,我们显示HsfA3过表达的耐热性增加,并且HsfA3 T-DNA标记的突变体的耐热性降低。这些结果表明,HsfA3调节DREB2A应激调节系统下游转录级联中许多热诱导基因的表达,并在DREB2*级A**联控制下获得耐热性。TsHsfA1d的部分核定位可能在常温下诱导转基因植物中AtHsfA1d调节子的表达。我们还发现过表达AtHsfA1d的转基因拟南芥植物比野生型植物更耐热,并且上调了HsfA1d调节子的表达,如在TsHsfA1d过表达植物中观察到的。我们建议TsHsfA1d和AtHsfA1d的产物作为拟南芥热应激反应的正调节剂起作用,并且可用于改善其他植物的热应激耐受性。
方法三:全基因分析
1. 全长cDNA对于拟南芥基因组后测序时代植物基因的功能分析至关重要。最近,已经开发了cDNA微阵列分析用于表达谱的全局和同时分析的定量分析。我们已经制备了含有大约7000个独立的全长cDNA组的全长cDNA微阵列,以分析干旱,寒冷(低温)和高盐度胁迫条件下基因随时间的表达谱。与对照基因相比,冷,干旱和高盐度处理后53277和194个基因的转录物分别增加超过五倍。我们还鉴定了许多高度干旱,冷或高盐度胁迫诱导基因。然而,我们基于维恩图分析观察到这些应激反应基因表达的强关系,并发现22个应激诱导基因对所有三种应激都有反应。通过在应激反应基因诱导期间分析它们的表达模式来鉴定显示不同表达谱的几个基因组。冷诱导基因从其表达谱中分为至少两个基因组。DREB1A被包括在冷处理后2小时表达达到峰值的组中。在鉴定的干旱,冷或高盐度胁迫诱导基因中,我们发现了40个转录因子基因(相当于所有鉴定的胁迫诱导基因的约11%),表明各种转录调控机制在干旱,寒冷或高盐度胁迫中起作用。信号转导途径。我们使用含有约7000个拟南芥全长cDNA的全长cDNA微阵列,并鉴定了152个再水化诱导基因。维恩图分析显示补液诱导基因与脯氨酸诱导型和水处理诱导型基因的关系。在152个补液诱导基因中,有58个基因在其启动子区域包含与脯氨酸和低渗透压诱导基因表达有关的ACTCAT序列,这表明ACTCAT序列是参与补液诱导基因表达的主要顺式作用元件,并且一些新的顺式作用元件参与补液诱导的基因表达。补液诱导和补液抑制基因的功能分析揭示了它们不仅在从胁迫状态释放中的功能,而且在植物生长的恢复中的功能。
研究这些潜在的用途: