同种异体细胞疗法比自体细胞疗法更能媲美分子药物,也是细胞治疗行业一直在追求的一种通用商业化模式。12月8日,我国人源异体脐带间充质干细胞治疗活动性狼疮肾炎提交临床试验申请,12月6日,FDA批准了同种异体NK1R+人间充质干细胞治疗缺血性心力衰竭的IND申请,11月底FDA授予一种同种异体抗CD19 CAR-T细胞疗法(CB-010)再生医学高级疗法和快速通道认定......从制造和商业角度来看,同种异体细胞治疗产品尤其具有吸引力,同时可以满足不适合自体细胞治疗的患者需求。本文简要梳理同种异体细胞疗法临床前和临床研究注意事项,以供参考。
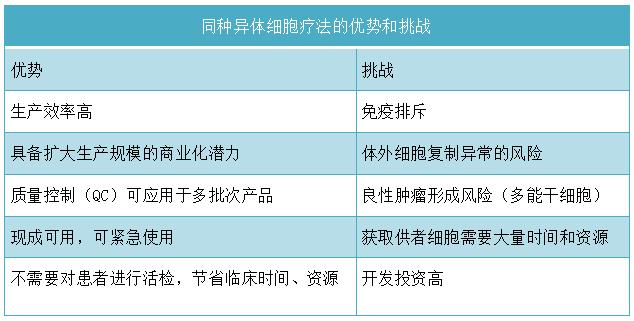
一、临床前研究注意事项
1.1 保证异体供者材料与患者相匹配
自体细胞产品或采用异体供者材料生产的需与患者配型使用的产品,一旦发生混淆或差错,造成供者材料或细胞产品与患者之间的不匹配,可能会对患者产生危及生命的严重后果。
1.2 GMP生产管理中,对供者材料留样
自体和异体供者材料一般应当保存留样,稀缺的供者材料如需调整留样要求或不保存留样的,应书面说明其合理性。
1.3 免疫细胞治疗产品药学研究
病原微生物筛查方面,同种异体供者应至少符合国家对于献血的相关规定,如筛查供者是否存在人类免疫缺陷病毒、乙型肝炎病毒、丙型肝炎病毒、梅毒螺旋体等感染。根据产品实际情况,还可增加相应的检测项目,对于一些特定产品,有明确风险且有明确病毒检测要求的则需要进行检测,如T细胞治疗产品的供者除上述病原微生物外,还建议进行人巨细胞病毒、人EB病毒、人类嗜T淋巴细胞10病毒的筛查。同种异体供者还需考虑窗口期对病原微生物筛查的影响。
除病原微生物检测外,根据临床使用和生产需求,可增加对供者的筛查项目,例如对于同种异体来源的产品,建议适时评估包括多态性的分型,例如血型、供者和受者之间主要组织相容性抗原(Ⅰ类和/或Ⅱ类 HLA)的匹配,在某些情况下可能需关注次要组织相容性抗原,明确并建立分型程序和标准。
对于同种异体治疗产品,在开展人源病毒检测时,应关注供者处于感染窗口期的可能,适时开展二次取样和检测。
建议对异体来源的细胞产品选择适用的方法进行免疫学反应检测。
二、临床研究注意事项
2.1 受试者保护
在受试者的选择中,还应关注,如果患者将来需要通过细胞、组织或器官移植治疗该或其他疾病,异体细胞治疗产品诱导产生的抗体可能会影响到移植的成功率。
2.2 异体来源的干细胞疗法
对于异体来源的干细胞相关产品,反复给药可能诱导机体产生免疫应答,进而降低重复给药的有效性或增加安全性风险。因此,确证性试验的临床终点还应关注疗效的持续时间,建议根据目标人群的疾病特点和临床获益评价标准,设置足够的观察期以评价受试者的长期获益。
无论细胞来源如何,标准化生产都是必要的,以满足多批次或不同制备地点的质量控制标准的一致性。
目前,国内新药临床研究综合服务一体化的第三方机构仍为数不多,提供新药和细胞治疗产品临床试验申请、临床研究、注册上市、上市后研究等全流程咨询与服务的CRO,将能最大程度帮助申办方在研发过程中减少风险、降低成本、缩短研发周期,从而加快药品获批上市。
十多年来,兴德通用强大的注册能力和执行能力,帮助申办方完成了几十个新药注册与上市,积累了丰富的项目经验。兴德通也辅助了不少改良型新药、仿制药、中药顺利上市,多个细胞治疗产品顺利获得中国药监机构颁发的IND批件,同时,兴德通团队也有附条件批准上市药物及新冠治疗药物等经典案例。
作为“专精特新”临床CRO企业,兴德通始终保持高效专业的水平,帮助申办方有效应对药物研发与注册过程中的各类问题,被业界誉为“临床研究综合服务一体化的中国创新型CRO”。此外,兴德通还在信息化和数字化建设上不断创新,自主开发多个临床试验用系统,保障临床试验数据质量,加速新药注册与上市。
相对于其他较为成熟的疗法,由于细胞成分的复杂性和可变性增加以及载体介导的基因工程步骤的重要性,良好生产规范细胞疗法的合规制造比许多其他生物药物更具挑战性。兴德通现已形成完善的细胞治疗产品开发咨询与服务业务,已制定细胞治疗产品不良事件监测计划、风险控制计划、质量控制计划等,保障受试者权益。兴德通细胞临床研究中心主要解决细胞药物开发面临的痛点和难点(GMP厂房规划、细胞制备工艺、SOP制定等),帮助企业少走弯路,促进成果转化,加快细胞治疗产品上市。
兴德通可提供涵盖细胞治疗产品开发的全产业链服务:
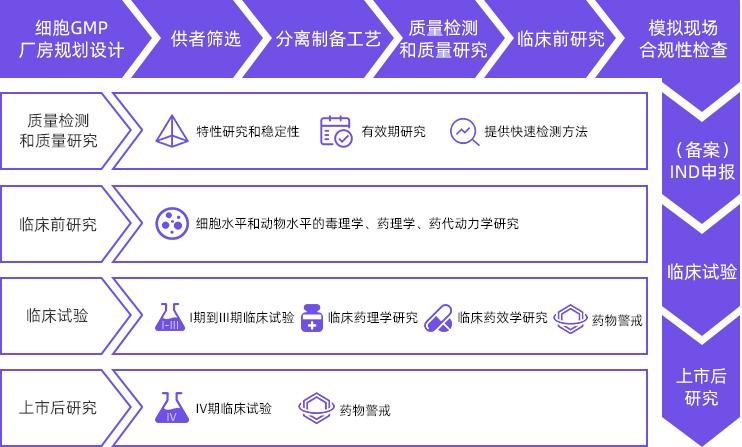
本文参考资料:
1.Commercial manufacture of cell therapies,I.B. Wall, D.A. Brindley, in Standardisation in Cell and Tissue Engineering
2.《免疫细胞治疗产品药学研究与评价技术指导原则(试行)》2022
3.《人源性干细胞及其衍生细胞治疗产品临床试验技术指导原则(征求意见稿)》2022
4.《免疫细胞治疗产品临床试验技术指导原则(试行)》2021
5.《细胞治疗产品研究与评价技术指导原则(试行)》2017
6.《细胞治疗产品生产质量管理指南(试行)》2022