文丨粉墨叔叔
编辑丨粉墨叔叔
前言
动物的再生能力差异很大。在光谱的一个极端,涡虫和水生动物被认为能够完美再生,将裂变与再生相结合以实现无性繁殖。另一个极端是缺乏再生的生物体或仅限于上皮和血液等组织中的生理细胞周转。在这两个极端之间是各种各样的动物,它们再生不完全。
例子包括非洲爪蟾蛙,用图案不佳的尖刺代替截肢,蜥蜴用软骨代替尾巴的骨椎,以及再生腿部的蟑螂若虫,与未受伤的腿相比,腿部在神经,肌肉组织和气管方面存在微小但一致的差异。
在某些情况下,包括经过充分研究的蝾螈腿和斑马鱼鳍,再生会产生外观正常的器官,这些器官可能带有细微的缺陷。在大多数再生情况下,尚不清楚再生器官的细胞组成、详细形态和功能是否完全恢复。
在甲壳类动物Parhyalehawaiensis中解决这个问题,这是一个实验系统,其中腿通常在截肢后1至2周内再生。再生的Parhyale腿在截肢后的第一次蜕皮中比对照腿小,但在随后的蜕皮中逐渐恢复大小。在随意检查时,再生的腿在腿段形态以及肌肉和运动神经元的存在方面看起来与未受伤的腿相同。
尽管如此,Parhyale腿部再生和腿部发育在其全局基因表达动力学上存在差异,这表明在胚胎中产生腿和在成年阶段再生腿的过程可能不同。使用显微解剖学观察、机械感觉测定和单核转录组学来解决再生腿在形态、感觉功能、细胞类型多样性和分子谱方面是否与未受伤的腿不同。
外部感觉器官的多样性和分布
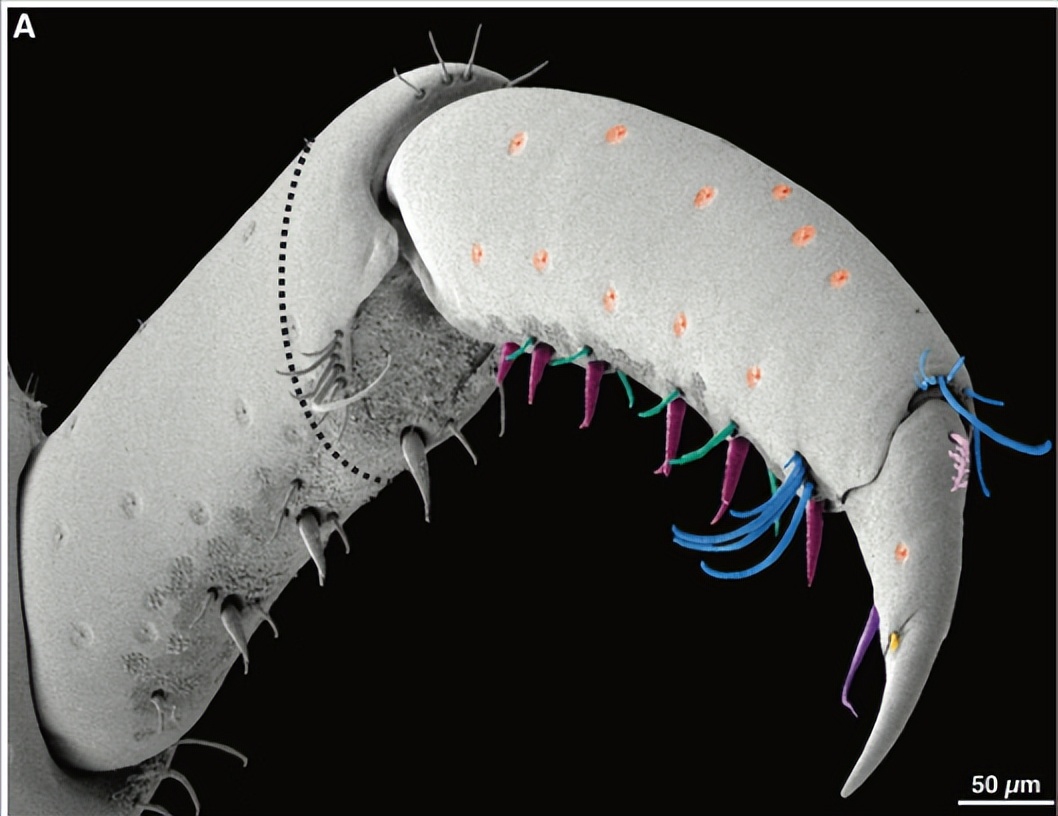
这些结构为以高精度评估再生的准确性提供了精美的标记,因为它们的详细形态和空间模式在个体之间是复杂且可重复的。类似于昆虫感觉刚毛,setae由几个细胞组成,并根据其类型和功能,它们复杂而刻板的外部形态使即使是微小的缺陷也可以轻松检测。
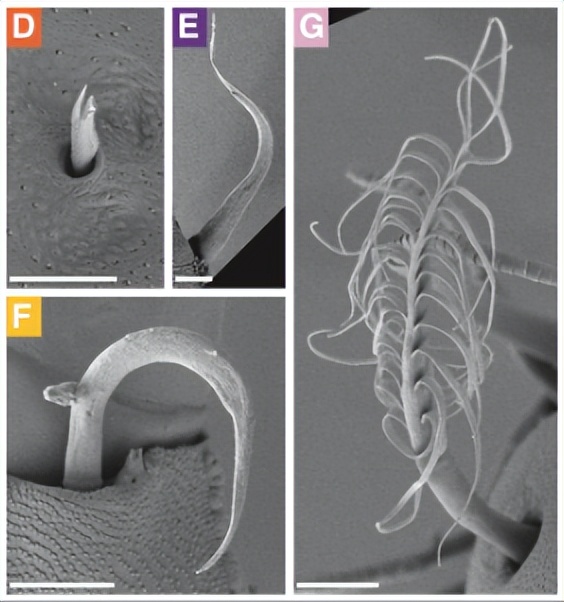
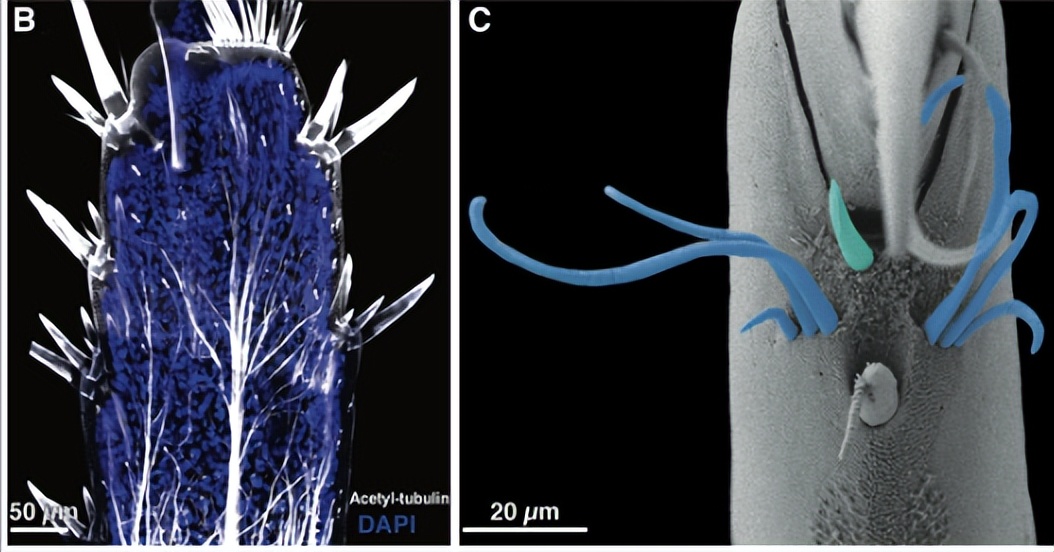
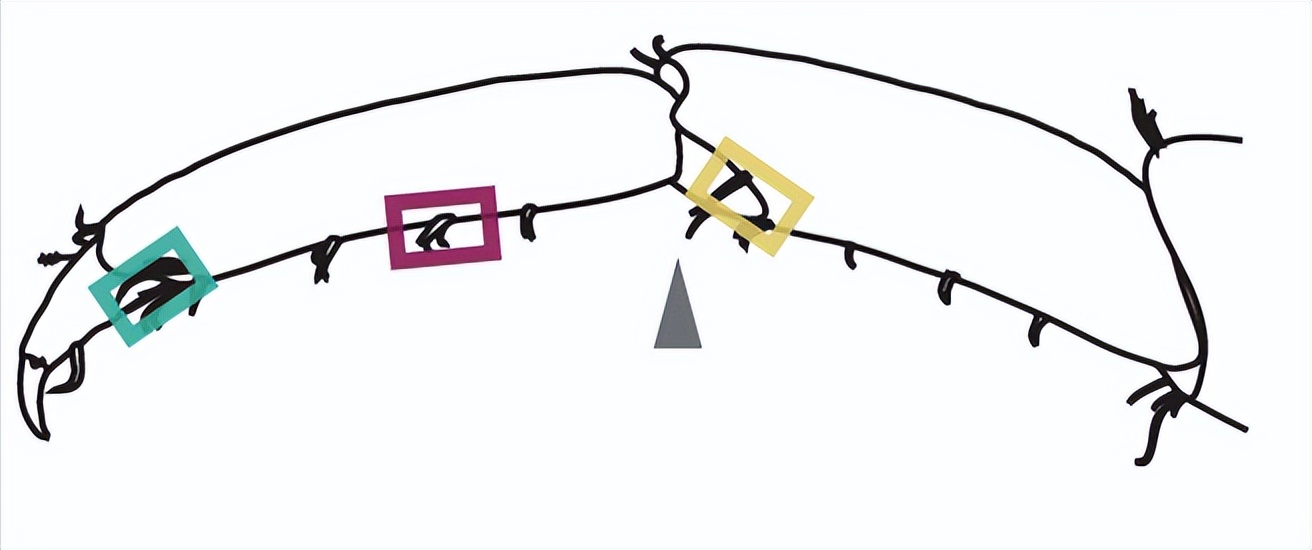
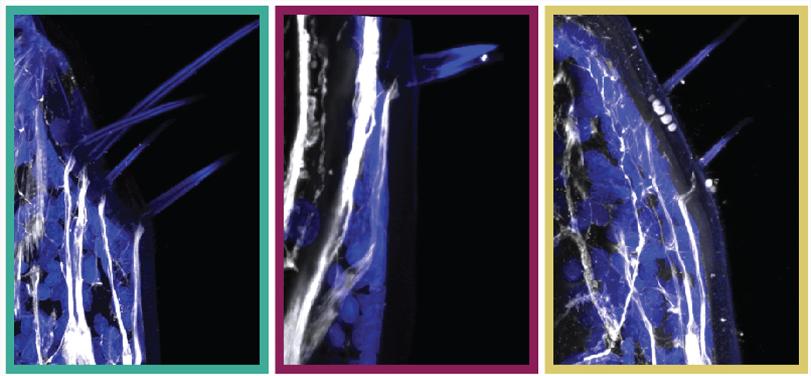
扫描电子显微镜对未受伤的Parhyale腿的最远端的三个部分显示具有不同形态的八种类型的setae。标记神经轴突的乙酰化α-微管蛋白的免疫染色显示,所有神经支配,正如感觉器官所预期的那样。
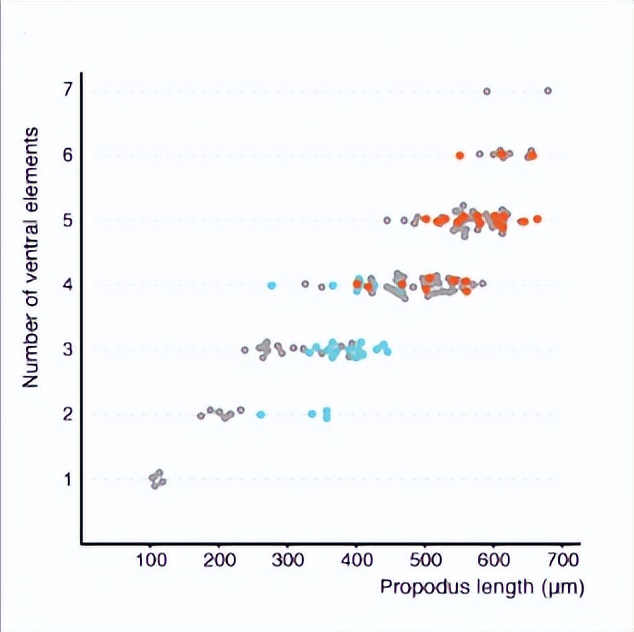
每种组型在T5和T1胸腿上都有特定的分布,要么作为刻板位置的单个seta,要么以特定空间模式排列的setae组。在后一种类型中,setae的数量取决于孔的大小。这些可重复的空间排列的唯一例外是微片,它们在角质层表面间隔,没有明显的保守模式。
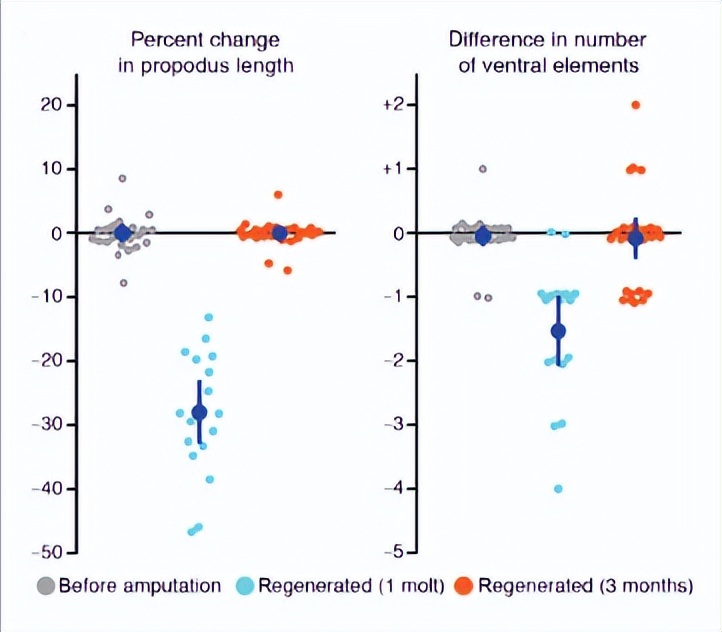
为了尽量减少遗传、环境和生理影响,比较了来自同一个体的再生腿和对照腿之间的固定模式。在再生腿中,所有群落类型的详细形态和空间分布均未改变。在刻板位置中发现的独特setae在其原始位置始终如一地再生。
数量可变的组型在再生后的第一次蜕皮时数量较少,但在随后的蜕皮中完全恢复。这反映了腿的大小,最初在再生腿中较小,但后来反弹以匹配对照的大小。
细胞类型的多样性和相对丰度
考虑到这些微解剖特征的忠实恢复,细胞组成和多样性是否在再生腿中表现出类似的高保真度。Parhyale腿由多种分化的细胞类型组成,包括表皮,肌肉,神经元,肌腱,神经胶质细胞以及可能的其他未知细胞。
为了表征这种多样性,建立了成年Parhyale腿的单核转录谱。这种方法从所有细胞类型中回收细胞核,并克服了由差异解离和细胞存活引起的单细胞方法中的偏差,这在被硬外骨骼包围的动物中尤其成问题。
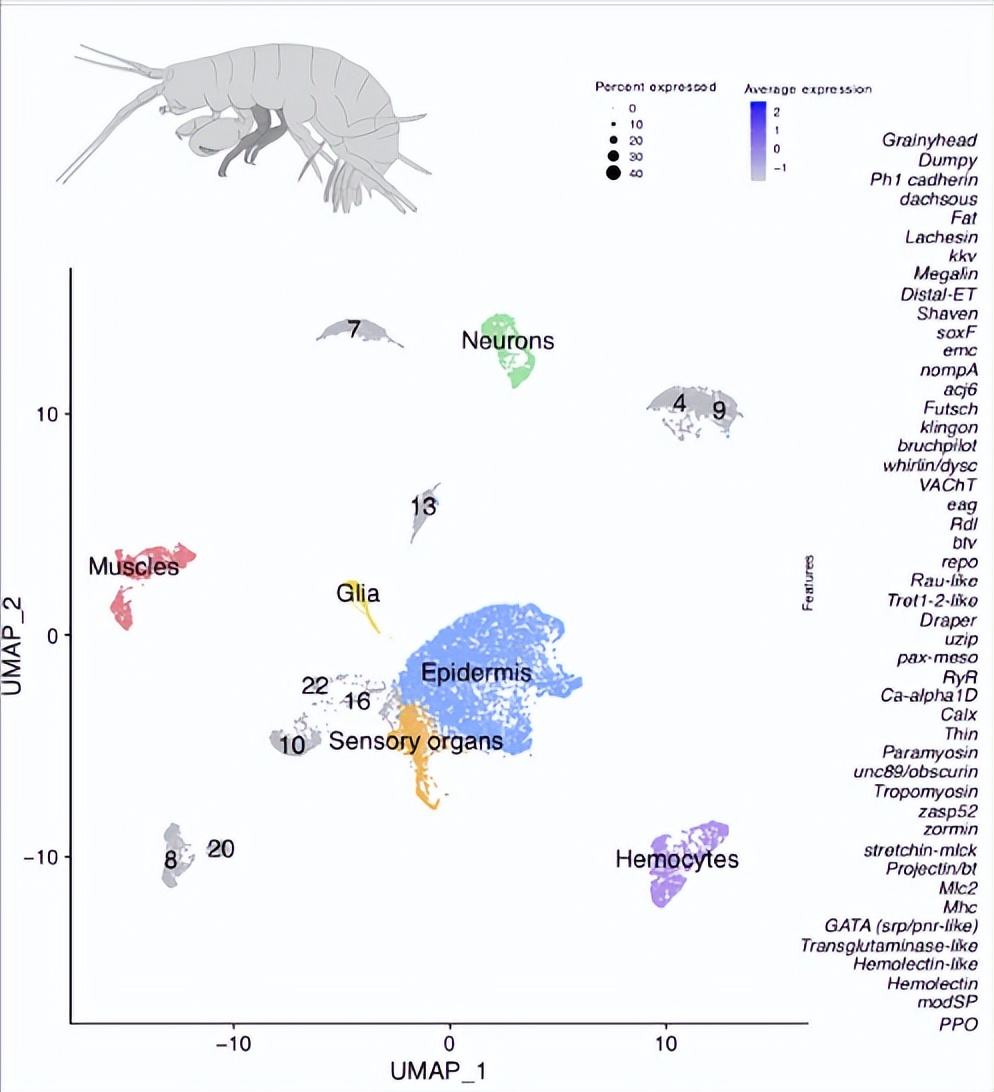
从成年Parhyale的T9459和T4腿获得了5个细胞核的snRNAseq数据。将读数映射到注释基因的内含子序列,以最大程度地减少细胞裂解引起的环境细胞质RNA的污染。降维和聚类分析将这些细胞核分离成定义明确的簇,代表具有不同转录谱的细胞类型或细胞状态。
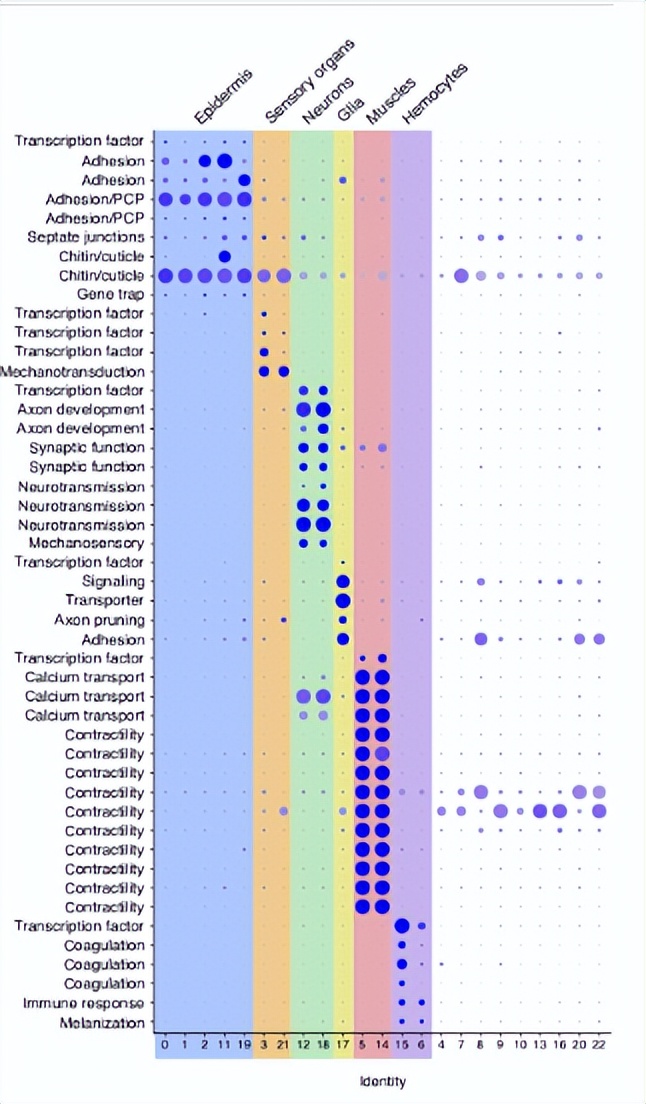
使用已知的细胞类型标记基因,基因本体分析以及与果蝇腿中获得的单细胞RNAseq谱的比较,能够识别对应于表皮,肌肉,神经元和血细胞的细胞簇。还初步确定了对应于神经胶质细胞、毛滴虫细胞和其他有助于感觉器官的支持细胞的簇。其余未鉴定的簇可能对应于甲壳类动物腿中已知或以前未描述的细胞类型。
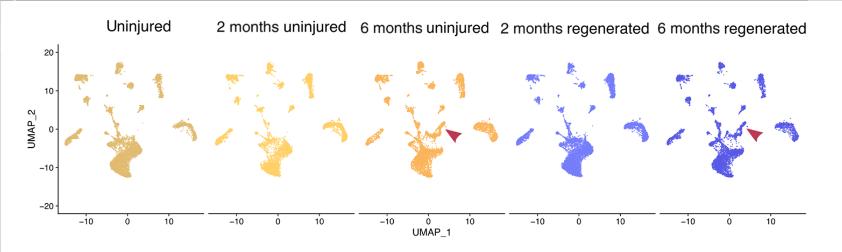
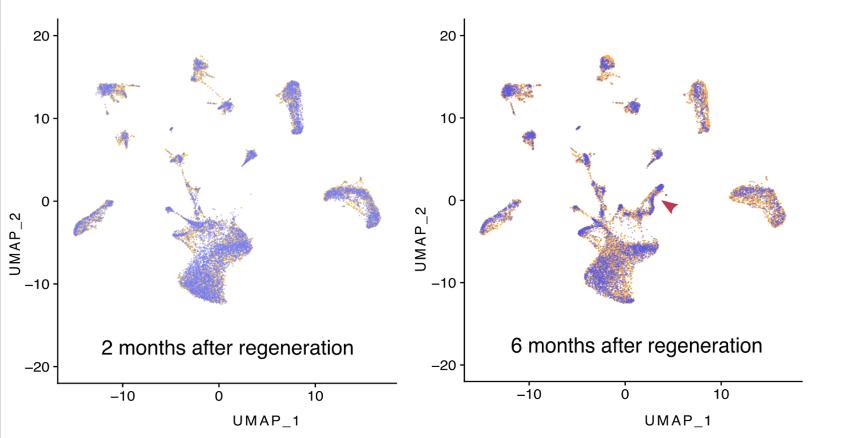
为了探测再生后的细胞组成,在截肢后约2个月和6个月对再生的成年腿进行了snRNAseq。为了解释遗传、环境和生理对核转录组的影响,将再生腿部的snRNAseq数据与同时从同一个体收集的对侧未受伤腿的数据进行了比较。分析是在集成数据集上重新执行的,将数据投影到新的均匀流形近似和投影上。
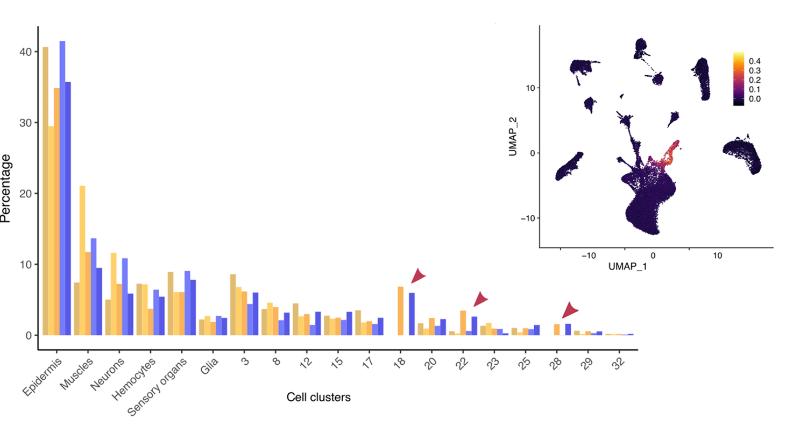
在这两个实验中,再生的腿具有与其对侧对照相同的细胞簇,包括对应于主要已鉴定细胞类型的所有簇,次要簇以及对应于尚未鉴定的细胞类型的簇。每个簇的顶部标记基因在实验中显示出一致的表达水平,无论是在未受伤的腿还是再生的腿中。
发现再生和对侧对照腿中所有簇的细胞比例相似[使用线性模型,方差分析P值为>0.08或替代方法。功效分析表明,能够检测到所有主要细胞簇的相对丰度的两倍差异,以及大多数次要细胞簇的三到四倍差异。
为了以更高分辨率探测细胞类型的恢复,需要确定scRNAseq数据是否允许区分特定神经元细胞类型丰度的差异,为此对神经元细胞进行了单独的聚类分析。这揭示了八个子集群由特定表达谱定义,可能代表不同的神经元细胞类型。果蝇机械感觉和味觉神经元顶部标志物的表达无助于清楚地识别Parhyale神经亚型。
为了评估分析的稳健性,测试了不同的数据集成方法和不同的读取映射策略。将RNAseq读段映射到内含子或整个基因组的结果进行比较,以解释Parhyale基因组中不完整的基因注释。这些分析给出了再生和对照腿中一致的细胞聚类和细胞丰度测量。
整合来自单独实验的数据的方法可能无法将实验批次效应与实际生物变异区分开来。为了解决数据集成是否会影响结论,通过简单地聚合它们来分析所有数据集,而无需明确的集成步骤。同样发现从对照和再生腿中恢复的细胞簇没有一致的差异。
这些细胞包括表达蜕皮相关转录本的细胞,大概是从接近蜕皮的个体那里收集的。对这种与蕃皮相关的细胞状态的检测证实了数据集成方法能够检测仅存在于某些数据集中的簇。
细胞类型的转录谱
除了细胞组成之外,通过对所有单核数据集的每个细胞簇进行差异表达分析,比较了未受伤和再生腿之间每种细胞类型的转录谱。发现差异有限,绝大多数代表实验之间的差异,而不是再生腿和对照腿之间的差异。
为了提高灵敏度,使用DESeq2进行了伪体差异表达分析,将对照和再生样品视为重复。发现对照组与再生腿组相比很少有具有簇特异性差异表达的基因,但这些基因中的绝大多数是在单个重复或少数细胞中表达的。
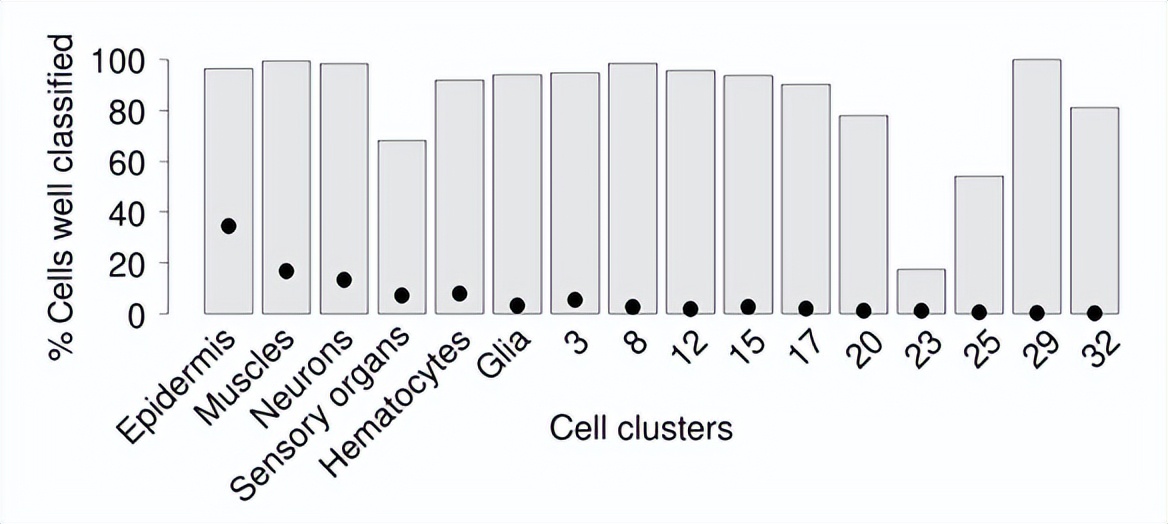
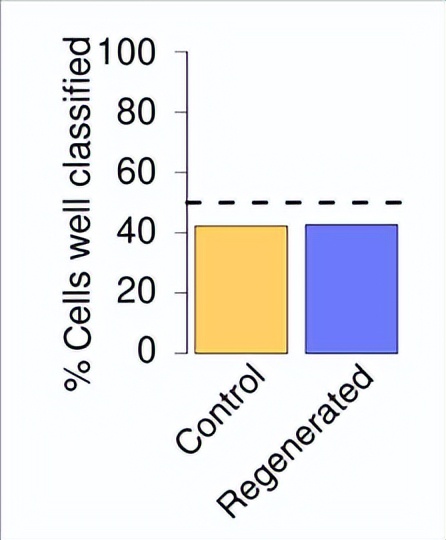
使用机器学习来测试这些转录谱的差异是否足以区分再生腿和对照腿。这种方法能够准确地对不同的细胞类型进行分类,但不能区分再生腿和对照腿的细胞。
结论
数据显示Parhyale的再生腿与未受伤的腿没有区别。这一结论基于对细胞的微观解剖学、感觉功能、细胞组成和分子谱的补充方法。虽然不能排除再生的Parhyale腿存在微妙的图案或功能缺陷,但在目前的形态和分子分辨率水平下,这些腿似乎是截肢前原始腿的完美复制品。
在显微解剖学水平上,尽管得出结论,Parhyale的腿部再生恢复了T4和T5腿尖处外部感觉器官的完整模式和多样性,但尚未探索形态学和显微解剖学的其他方面,内部本体感觉神经元,肌肉,肌腱或肌肉神经支配的模式。
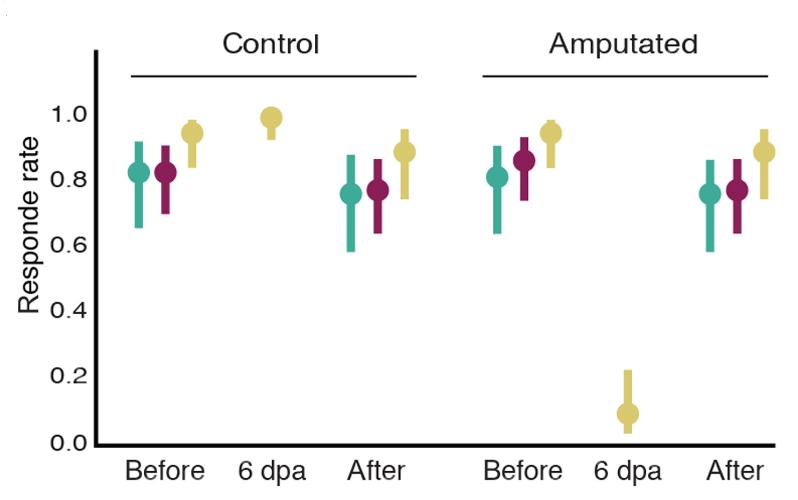
使用行为测定,再生的机械感觉器官对触觉敏感,目前无法探测来自这些器官的感觉信号如何整合到更复杂的行为中。在细胞水平上,所有已鉴定的细胞类型都在再生过程中被回收;如果缺少任何主要细胞类型,这种方法就会发现这种差异。
观察到对照和再生腿之间不同细胞类型的相对比例没有显着差异,随着观察到的样品之间的变化水平,方法的灵敏度仅限于检测任何给定细胞类型丰度的>2倍差异。尽管没有观察到对照与再生腿中细胞的分子谱的显着差异,但认识到在单核研究中探测差异表达具有固有的挑战,例如,灵敏度相对较低。
在Parhyale观察到的非凡保真度提出了关于支撑复杂器官忠实再生的机制的有趣问题。以前的研究表明,相同的调节网络被部署在胚胎和再生成人。最近在Parhyale和海葵的工作表明,发育和再生具有基因表达的不同时间谱。发育和再生可以由不同的全球调控机制驱动,但结合一些用于模式化和细胞分化的共享遗传模块,从而导致保守的结果。
参考文献
C.W.Beck,J.C.IzpisuaBelmonte,B.Christen,超越早期发展:非洲爪蟾作为再生机制研究的新兴模型。戴恩。238,1226–1248(2009).
K.E.McLean,M.K.Vickaryous,一种新型的表态再生羊膜模型:豹壁虎,Eublepharismacularius。BMC开发生物学11,50(2011).
C.Kaars,S.Greenblatt,C.R.Fourtner,蟑螂内股骨结构的模式再生,PeriplanetaamericanaL.J.实验动物。230,141–144(1984).
R.Diogo,E.Nacu,E.M.Tanaka,蝾螈肢体再生真的完美吗?GFP-转基因蝾螈前肢肌肉再生的解剖学和形态发生分析作为再生、发育和进化研究的基础。阿纳特·297,1076–1089(2014).
A.S.Azevedo,S.Sousa,A.Jacinto,L.Saúde,截肢将位置信息重置为再生斑马鱼尾鳍中的近端身份。BMC开发生物学。12,24(2012).