
人胚胎干细胞(ESCs)是一种来自囊胚内细胞团的多能干细胞,可以在体外培养中几乎无限期保持未分化。此外,它们也具有无限增殖的能力。因此,ESCs可以大规模产生具有稳定特性的外泌体(ESC-exos),这是外泌体临床应用的重要因素。此外,ESC微环境已被证实可以抑制癌细胞的致癌表型。
胶质母细胞瘤(GBM)是中枢神经系统最常见的原发性恶性肿瘤,死亡率和致残率均较高。除了耐药性很高,其不良预后的另一个关键原因是血脑屏障(BBB)限制了化疗药物到达肿瘤区域。因此,本文研究团队开发了一种ESC-exos与c(RGDyK)肽偶联,然后通过共孵育加载PTX,可以更有效地将化疗药物传递到癌细胞中,并能显著提高抗肿瘤效果。
技术路线
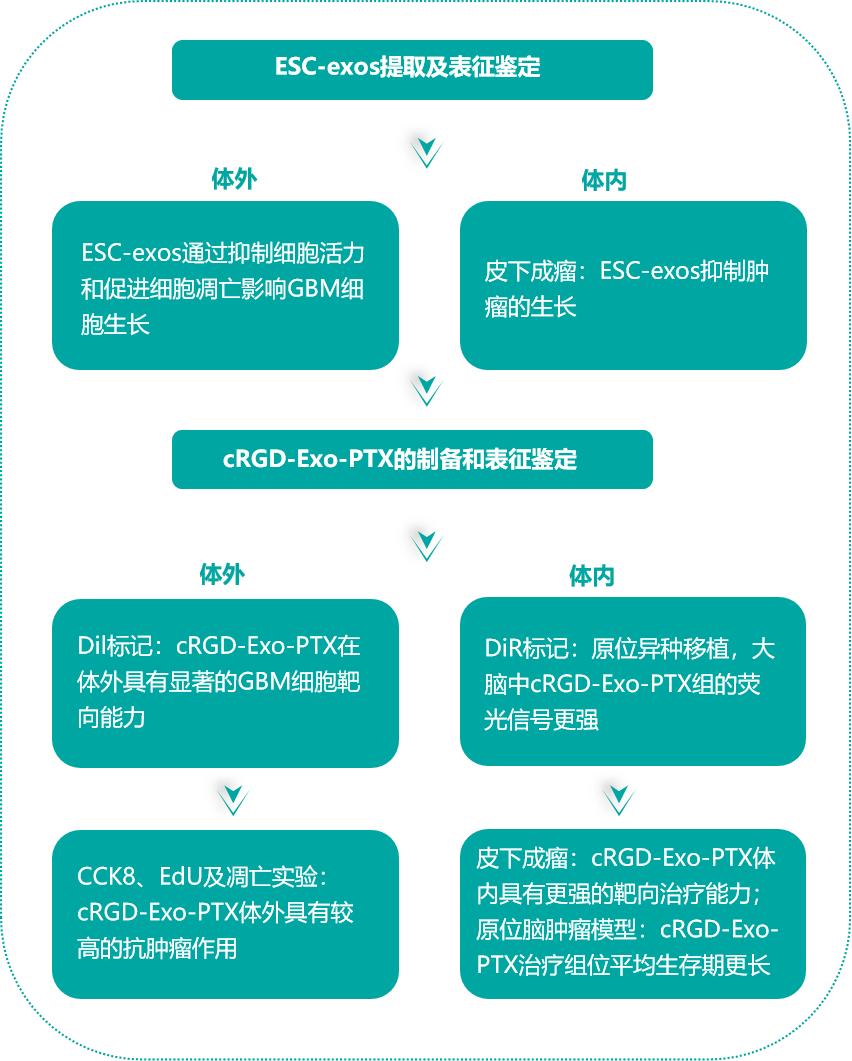
文献思路
1.ESCs和ESC-Exos的表征
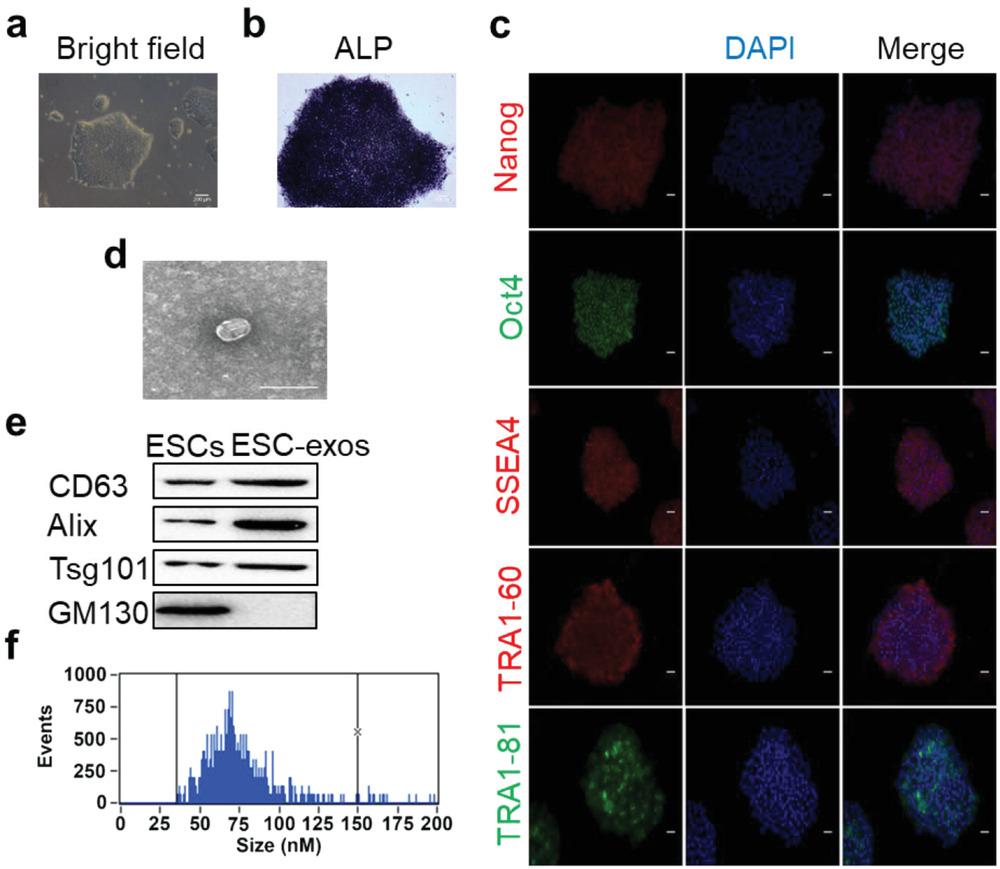
作者在 Matrigel 上培养的 ESC 形成了一个具有尖锐边界的紧凑菌落。免疫染色分析表明,球体中的所有细胞都表达碱性磷酸酶(ALP)和多能性标记分子,包括 Nanog、Oct4、SSEA4、TRA1-60 和 TRA1-81。培养细胞的这些特征与ESCs的特征相一致。之后从细胞培养上清液中纯化 ESC-exos,并通过透射电子显微镜 (TEM)、蛋白质印迹和流动纳米分析仪 (NanoFCM) 对其进行表征。这些数据表明,作者已经成功地从ESCs培养基中提取和纯化了ESC-exos。
2. ESC-Exos在体外和体内均表现出抑胶质母细胞瘤活性。
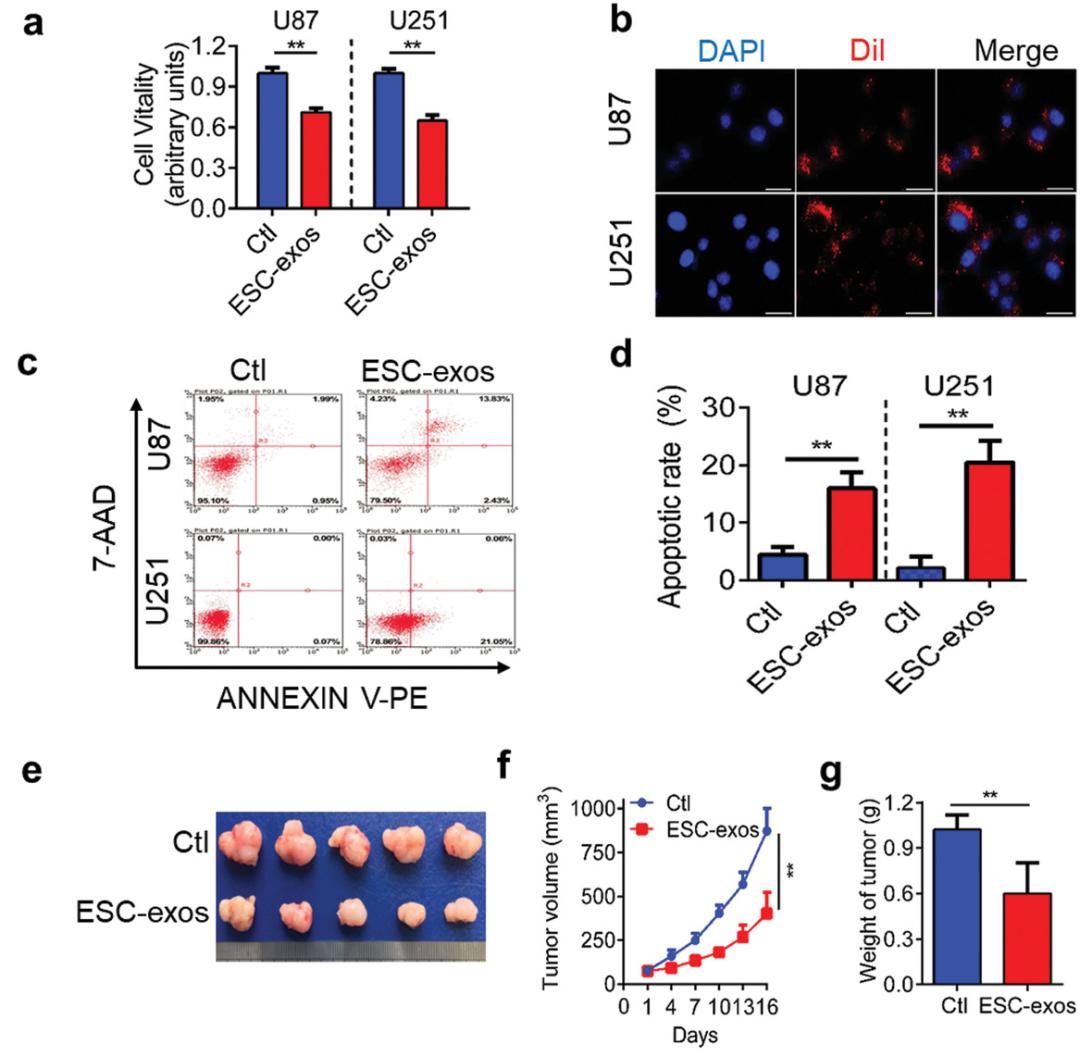
作者为了确认ESC-exos是否具有广泛的抗癌活性,对人GBM细胞系(U87和U251)在含有ESC-exos的培养基中培养48h,细胞活力(CCK-8试验)检测显示,ESC-exos显著降低了这些癌细胞的活力。接下来,作者对ESC-exos用亲脂性荧光染料Dil标记,加入U87和U251细胞培养基中。孵育12h后,ESC-exos被U87和U251有效内化。流式细胞凋亡检测结果显示,与对照组相比,ESC-exos组的凋亡细胞百分比显著增加。这些数据表明,ESC-exos通过抑制细胞活力和促进细胞凋亡影响GBM细胞生长。
作者为了评估ESC-exos是否能够影响体内GBM的生长,进行了裸鼠成瘤实验。在研究结束时,注射ESC-exos的小鼠的肿瘤大小明显小于注射PBS组的小鼠。与PBS治疗组相比,ESC-exos治疗组的肿瘤体重也显著下降。这些数据表明,与PBS组相比,ESC-exos组的肿瘤生长明显受到抑制。
综上所述,这些数据表明ESC-exos在体内外均表现出抗GBM的作用。
3. cRGD-Exo-PTX的制备
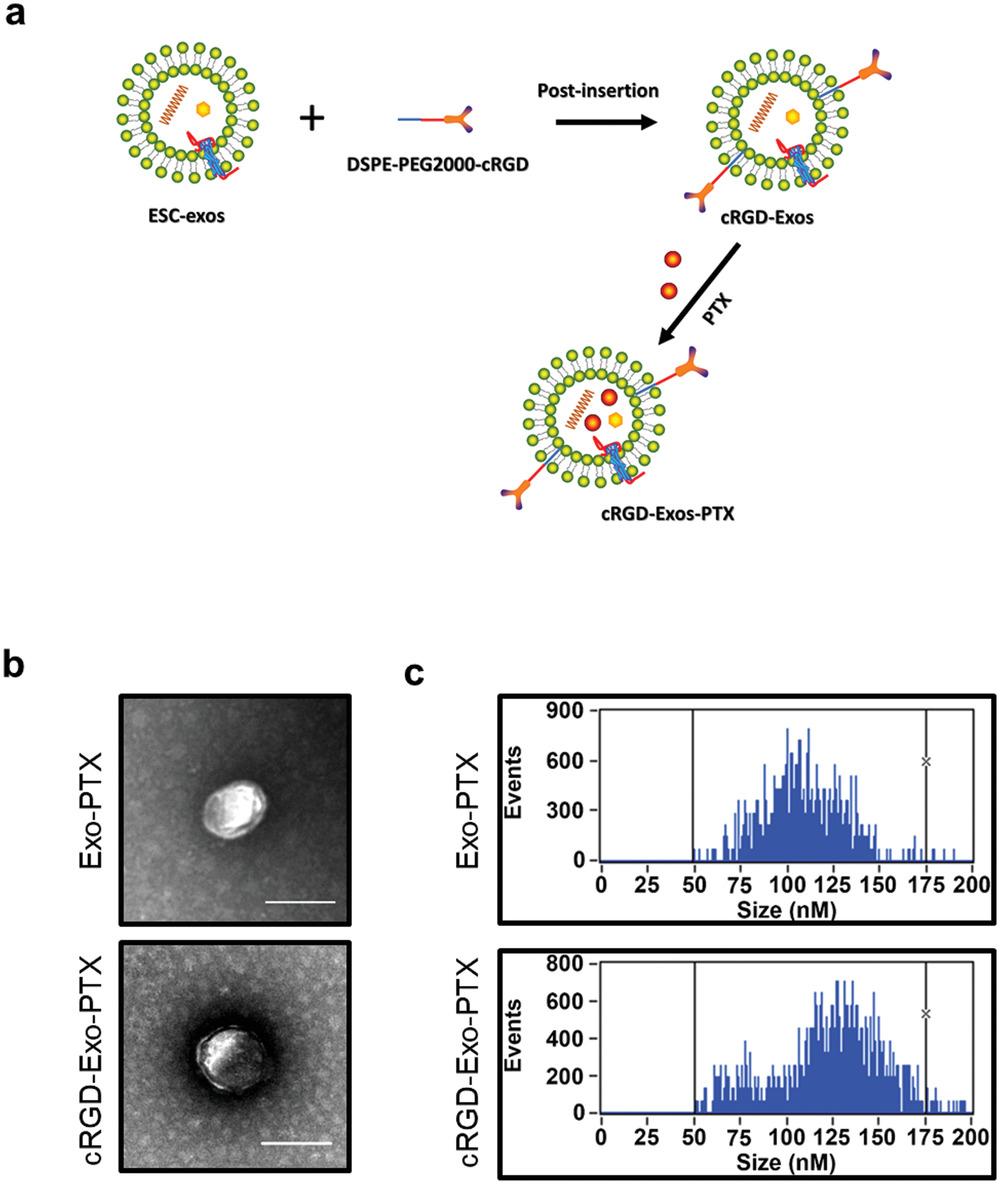
ESC-Exos虽然具有显著的抗GBM作用,然而,静脉注射未经修饰的外泌体的生物分布研究显示,外泌体在肝脏和脾脏器官中快速积累,很少有外泌体被传递到大脑。因此,ESC-exos的靶向特征需要改进才能用于提供针对GBM的治疗。已充分证明,c(RGDyK) 肽结合了针对αvβ3整合素的药物递送系统,用于肿瘤靶向治疗。紫杉醇(PTX)是一种肿瘤细胞有丝分裂*制剂抑**,广泛用于实体瘤的治疗。尽管PTX显示出有效的抗GBM活性,但由于其BBB渗透性低,它不能在体内产生治疗效果。
为了获得适合以下实验的工程化 ESC-exos,作者首先将ESC-exos与 c(RGDyK) 偶联,然后通过共孵育加载 PTX,命名为 cRGD-Exo-PTX。之后,作者通过透射电镜和NTA检测Exo-PTX和cRGD-Exo-PTX形态和粒径。这些结果表明,cRGD-Exo-PTX和Exo-PTX经过修饰和载药后保持了完整性。
4. cRGD-Exo-PTX在体外和体内的靶向能力
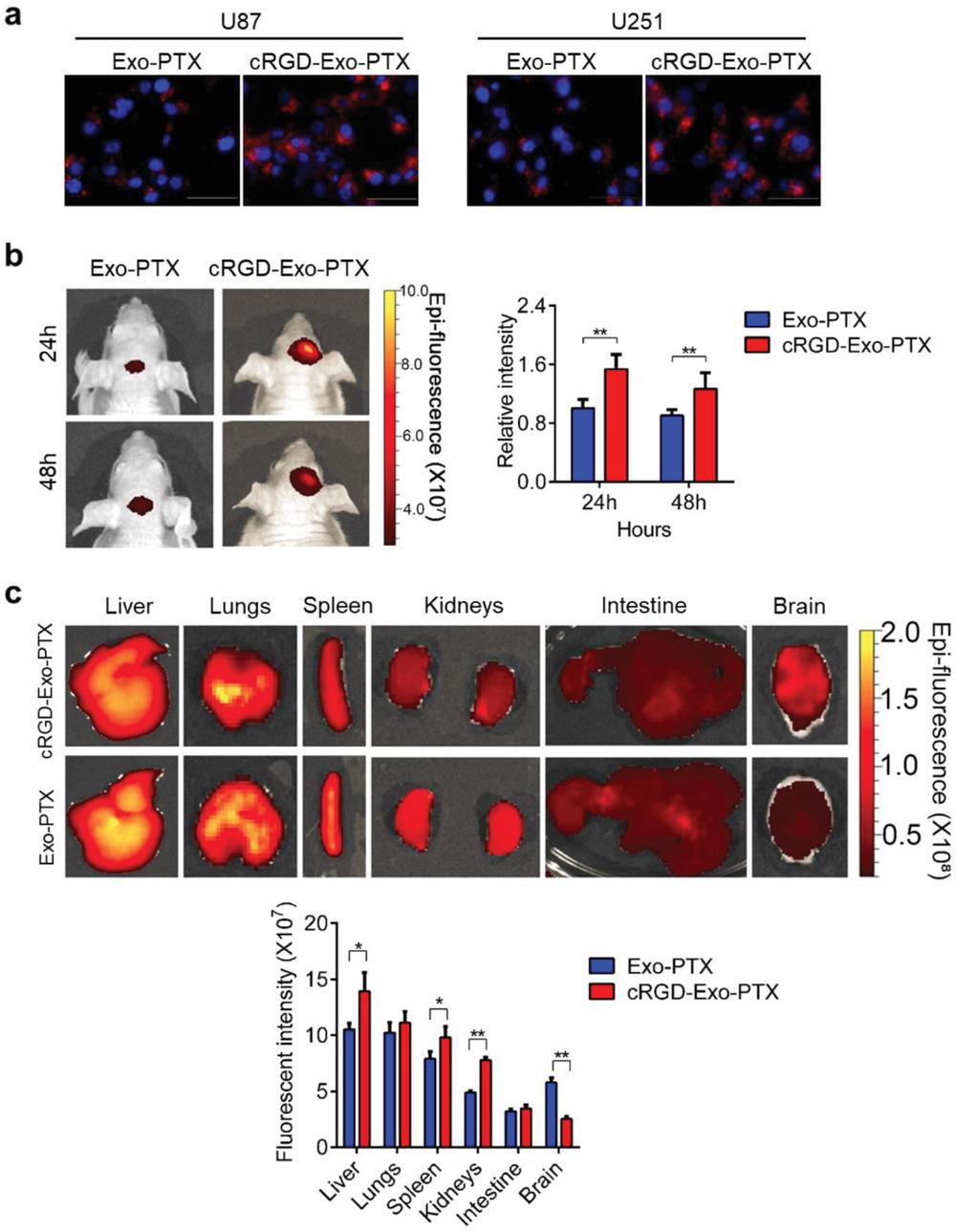
在制备cRGD-Exo-PTX后,作者评估了cRGD-Exo-PTX的靶向能力。U87和U251细胞与Dil标记的Exo-PTX和cRGD-Exo-PTX一起孵育,然后用荧光显微镜观察荧光信号。在与cRGD-Exo-PTX孵育的U87和U251细胞中显示出比与Exo-PTX孵育的细胞更强的荧光信号,这表明cRGD-Exo-PTX在体外具有显著的 GBM 细胞靶向能力。
作者使用原位异种移植物证实了cRGD-Exo-PTX在体内的积累能力。Exo-PTX和cRGD-Exo-PTX分别用DiR标记,然后,在原位植入后1周DiR标记的Exo-PTX或 cRGD-Exo-PTX静脉注射到荷瘤小鼠体内。通过实时成像系统在24h和48 h记录荧光信号的强度。cRGD-Exo-PTX治疗组肿瘤区域的荧光强度显着高于Exo-PTX治疗组。接下来,作者收集主要器官(脑、肝、脾、肺、肾和肠),并进一步检测这些器官中的荧光信号。Exo-PTX组大脑中的荧光比cRGD-Exo-PTX组中的弱。相反,Exo-PTX治疗小鼠的其他器官(肝、脾、肺、肾和肠)的荧光明显强于cRGD-Exo-PTX治疗小鼠。这些结果表明,cRGD-Exo-PTX可以比Exo-PTX更有效地在胶质瘤部位积累,证明了cRGD-Exo-PTX的肿瘤靶向能力。
5.cRGD-Exo-PTX的体外靶向治疗
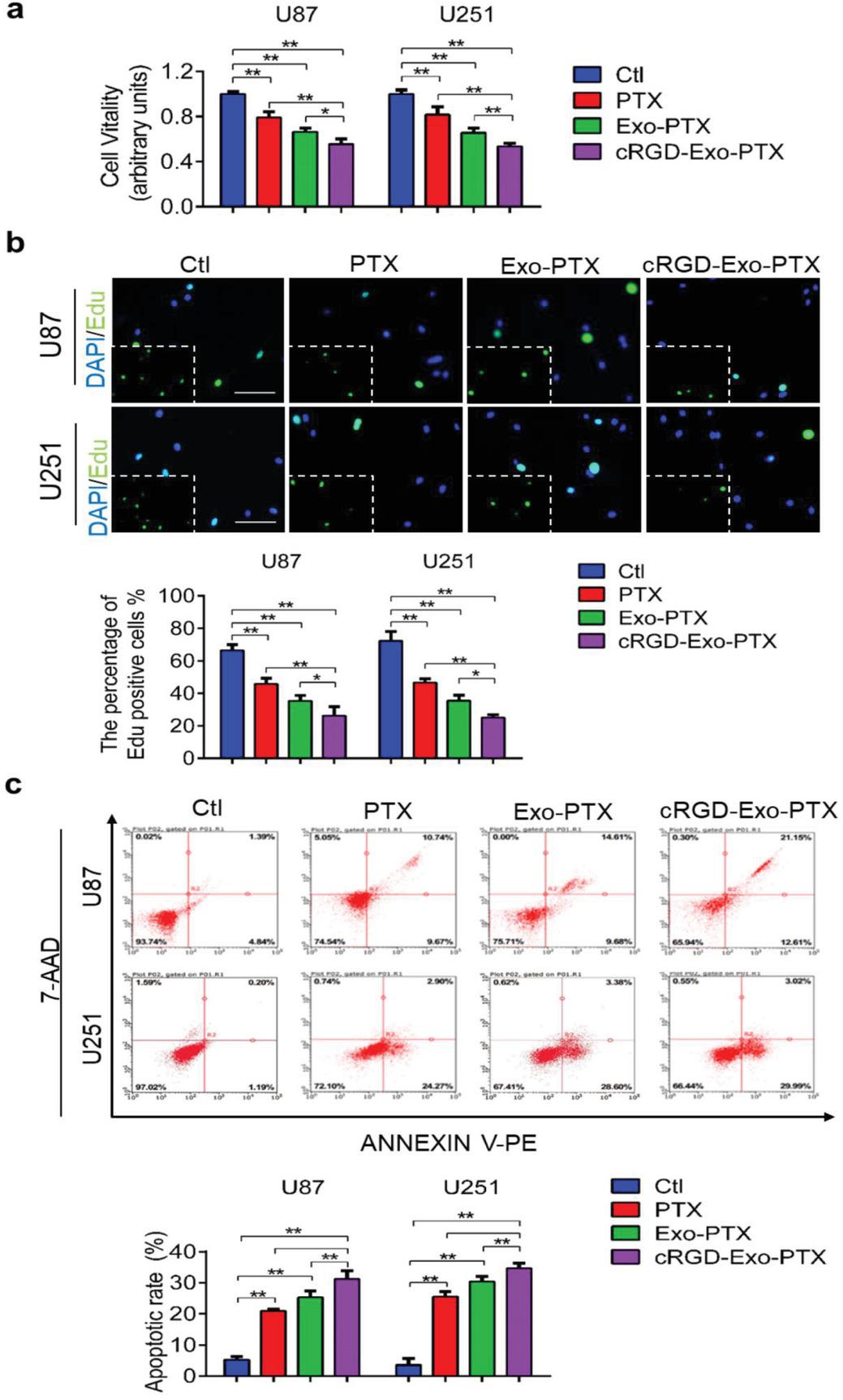
作者在验证了cRGD-Exo-PTX的靶向能力后,通过CCK8和Click-iT EdU测定评估了cRGD-Exo-PTX 对U87和U251细胞的抗增殖作用。U87和U251细胞与PBS、PTX、Exo-PTX和cRGD-Exo-PTX孵育48 h,结果表明,与PBS、PTX和Exo-PTX相比,cRGD-Exo-PTX可以更有效地降低U87和U251的细胞活力。流式凋亡数据显示,与PBS、PTX 和Exo-PTX 处理的细胞相比,使用cRGD-Exo-PTX处理的U87和U251 中凋亡细胞的百分比显著增加。这些结果表明cRGD-Exo-PTX发挥对U87和U251细胞的抑制作用比PTX 和Exo-PTX更强,这证实了cRGD-Exo-PTX在体外的高抗肿瘤功效。
6. cRGD-Exo-PTX的体内靶向治疗
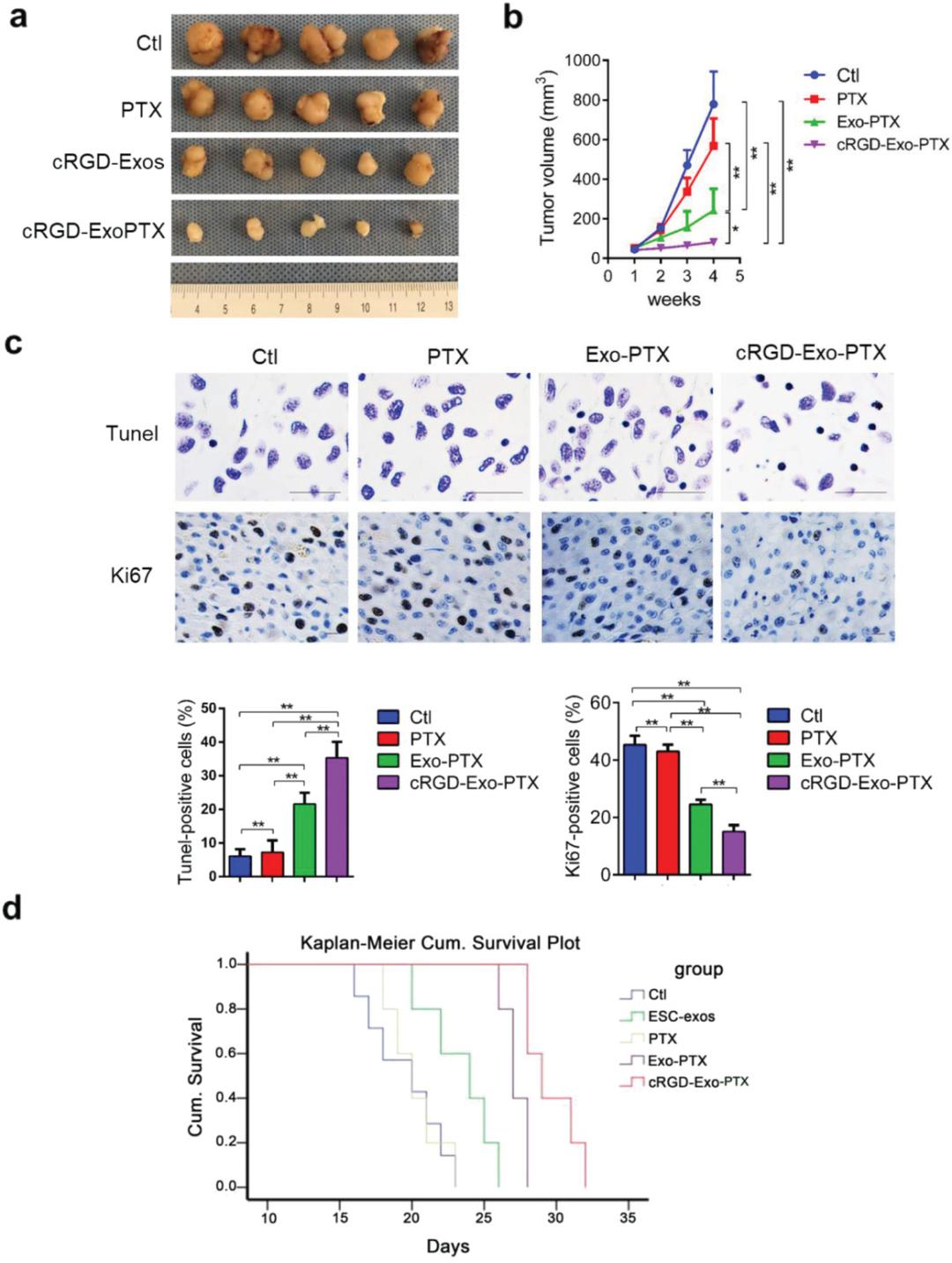
作者观察了cRGD-Exo-PTX对皮下荷瘤小鼠的治疗效果。每隔一天用PBS、PTX、Exo-PTX和cRGD-Exo-PTX对皮下荷瘤小鼠的治疗,持续2周。研究结束时,与PBS、PTX和Exo-PTX组相比,cRGD-Exo-PTX组的肿瘤生长受到显著抑制,此外,与PBS、PTX 和 Exo-PTX相比,cRGD-Exo-PTX处理后Ki67阳性细胞数显着减少,TUNEL阳性细胞数显着增加。
为了评估 cRGD-Exo-PTX 的长期效果,在原位脑肿瘤模型中记录了总生存期。每隔一天用 PBS(对照组,Ctl,125 µL)、ESC-exos(1 × 1011 颗粒/mL;125 µL)、PTX(320 µg/ mL;125 µL)、Exo-PTX (1 × 1011 颗粒/mL;125 µL)和 cRGD-Exo-PTX(1 × 1011 颗粒/mL;125 µL)对小鼠进行尾静脉处理。Kaplan-Meier 生存曲线表明,用 cRGD-Exo-PTX 治疗的原位脑肿瘤小鼠的平均生存期比其他组长得多(图 6d)。
这些结果表明,cRGD-Exo-PTX 在体内具有比 ESC-exos、PTX 和 Exo-PTX 更强的靶向治疗效果。
综述结论
作者在体内外均证实了ESC-exos的GBM抑制作用。将ESC-exos与肿瘤靶向c(RGDyK)肽偶联,并加载PTX,该工程化外泌体被命名为cRGD-Exo-PTX,已被证明具有良好的GBM靶向能力,并提高了PTX在GBM模型中的疗效。
综上所述,作者研究设计了一种新型的GBM靶向外泌体,并为脑肿瘤的治疗提供了一个强有力的工具。