撰文丨萧平
COVID-19流行以来,治疗药物、疫苗和单克隆抗体的开发极大程度改善了COVID-19的管控,但重大的全球公共卫生安全威胁仍然存在 【1】 。 当今,新的SARS-CoV-2变种持续出现,带来新的风险和挑战,与此相对,预防和治疗措施尚不足以应对来势汹汹的疫情蔓延。以地塞米松、瑞德西韦、Molnupiravir、Nirmatrelvir为代表的治疗药物仅能改善特定患者群体的临床表现,REGN-COV2 cocktail等单克隆抗体对病毒新的变体的中和效力降低,而疫苗则受限于效力、成本、可获得性、疫苗耐受变体的出现等诸多问题 【2-5】 。当然,最大的挑战之一依旧在于弱势高风险群体的预防,比如免疫功能低下患者,他们甚至不会对疫苗产生适当的反应。
病毒宿主受体是逻辑上最佳的治疗和预防靶点,正是它们介导了SARS-CoV-2侵入和感染细胞 【6】 。其中,血管紧张素转化酶2 (ACE2) 尤具有吸引力,这种跨膜羧肽酶是SARS-CoV-2的主要受体。它直接结合不同冠状病毒的刺突蛋白,对SARS-CoV-2具有很高的亲和力,在病毒侵入细胞过程中不可或缺,这也是COVID-19主要影响到那些表达ACE2的组织——比如说肺、心血管系统、消化道和胆道——的原因 【7-8】 。
原理上讲,下调ACE2的表达可以阻断病毒的侵入,预防SARS-CoV-2以及潜在的其他冠状病毒的感染。此外,作为宿主细胞蛋白,ACE2的表达不太可能受到病毒突变的影响,因而,调节ACE2表达的干预手段可能对多种SARS-CoV-2变体均有效果 【9-10】 。然而,ACE2的调控机制目前仍不清楚。
2022年12月5日,来自英国Wellcome – MRC剑桥干细胞研究所的 Fotios Sampaziotis 和 Ludovic Vallier 团队在 Nature 在线发表了题为 FXR inhibition may protect from SARS-CoV-2 infection by reducing ACE2 的研究工作, 这一工作报道了FXR信号通路在多种受SARS-CoV-2影响的组织中对ACE2的调控作用,证明了非处方药ZGG和非专利药熊去氧胆酸 (UDCA) 通过抑制FXR信号下调ACE2,降低SARS-CoV-2易感性。进一步地,研究人员通过回顾性登记信息确定了UDCA服药与SARS-CoV-2感染后患者临床结局之间的相关性,并在肝移植受者的独立队列中证实了这些发现。

Ludovic Vallier和Fotios Sampaziotis是胆管类器官培养体系的建立者和开拓者,2021年, Science 发表了二者作为共同通讯作者 (Fotios Sampaziotis同时作为第一作者) 的研究论文,通过胆管类器官在人离体常温灌注器官中的移植,成功利用胆道类器官移植实现了胆道再生 (可参见BioArt往期文章: Science | 胆管类器官移植实现胆道再生) 。作为胆道系统中ACE2表达最高的细胞,胆管细胞和胆管类器*能官**够被SARS-CoV-2感染。意外地,研究人员发现未经胆汁酸 (CDCA) 刺激的胆管类器官在缺失胆囊特征性基因表达的同时,ACE2的水平也大幅下调 (如 图1 所示) ,说明CDCA对于胆管细胞ACE2的表达是必要的。随后,研究人员证明CDCA通过激活胆汁酸受体FXR,直接作用于ACE2的启动子区域,激活其转录。
FXR在多种细胞类型中均有表达,除了胃肠道系统,还可见于肺、体循环中 【11】 ,说明上述发现极有可能是一种普遍存在的调控机制。与之相应地,研究人员在肺类器官和小肠类器官这两种能够被SARS-CoV-2感染的器官模型中,利用FXR的激动剂CDCA、*制剂抑**UDCA或者ZGG,同样证实了FXR对ACE2的正向调控作用 (如 图1 所示) 。
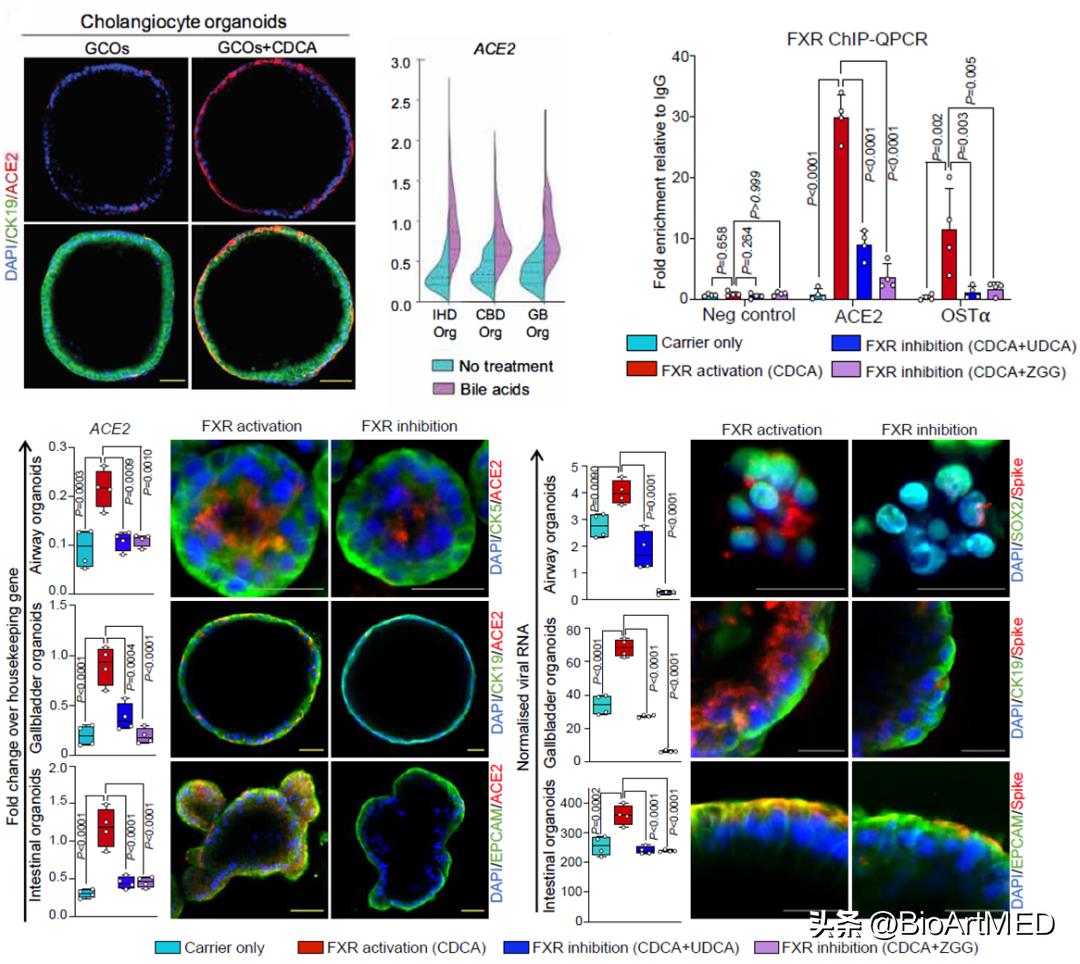
图1 FXR信号参与调控ACE2表达。
特别地,鉴于UDCA这一临床已获批的原发性胆管炎一线用药和非处方药ZGG均能够通过抑制FXR信号,下调多种细胞类型中ACE2的表达,研究人员意识到通过抑制FXR下调ACE2有可能降低SARS-CoV-2的易感性。随后基于上述三种类器官的体外实验证实了这一点。
而后,以FVB/N小鼠和叙利亚黄金仓鼠作为模型,研究人员首先证实了UDCA给药能够下调实验动物鼻腔、呼吸道、胆道以及肠上皮ACE2的水平。随后,通过建立叙利亚黄金仓鼠SARS-CoV-2感染模型,研究人员发现,预先UDCA给药7日能够有效预防仓鼠被SARS-CoV-2感染 (33% infected vs. 100% infected) (如 图2 所示) 。
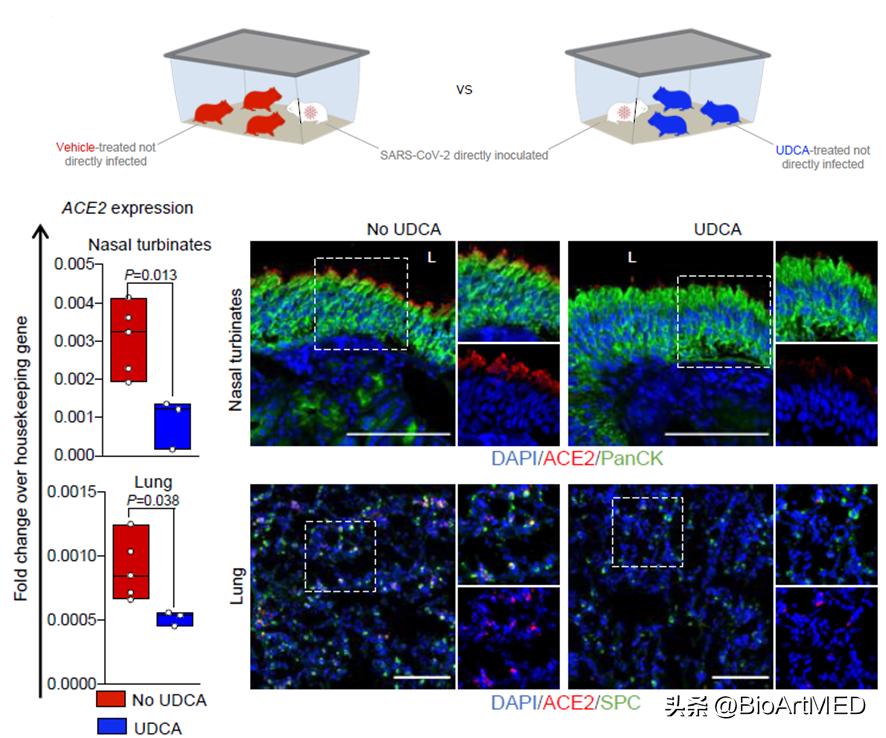
图2 仓鼠SARS-CoV-2感染试验。
紧接着,研究人员建立人肺的离体常温灌注 (ESNP) 和机械通气培养模型,让肺组织在实验过程中更为接近生理情况。同一供体的左肺和右肺被用于一组实验,分别接受或不接受临床剂量的UDCA给药。给药前后的检测发现,UDCA给药降低了肺实质、气道以及肺血管的ACE2水平,以及灌流液中ACE2的酶活性。随后的SARS-CoV-2感染试验同样证明,UDCA预先给药降低了SARS-CoV-2的感染效率。人肝脏ESNP的给药、感染试验再次证实了以上结论。
经过了上述体外、体内、离体实验,研究人员严谨论证了FXR对ACE2的表达调控,以及这一调控具备的SARS-CoV-2预防潜力。继而,研究人员着手招募志愿者,受试者们 (n = 8) 接受标准剂量的UDCA (15 mg/kg/day) 5天,服药前后以及过程中,受试者的鼻腔上皮细胞被采集用以ACE2水平的检测。结果显示,UDCA服药显著降低了受试者鼻腔上皮细胞的ACE2水平 (如 图3 所示) 。此外,UK-PBC患者队列中,UDCA服用与未服用者血浆蛋白组学数据显示,UDCA同更低的血浆ACE2水平相关 (如 图3 所示) 。
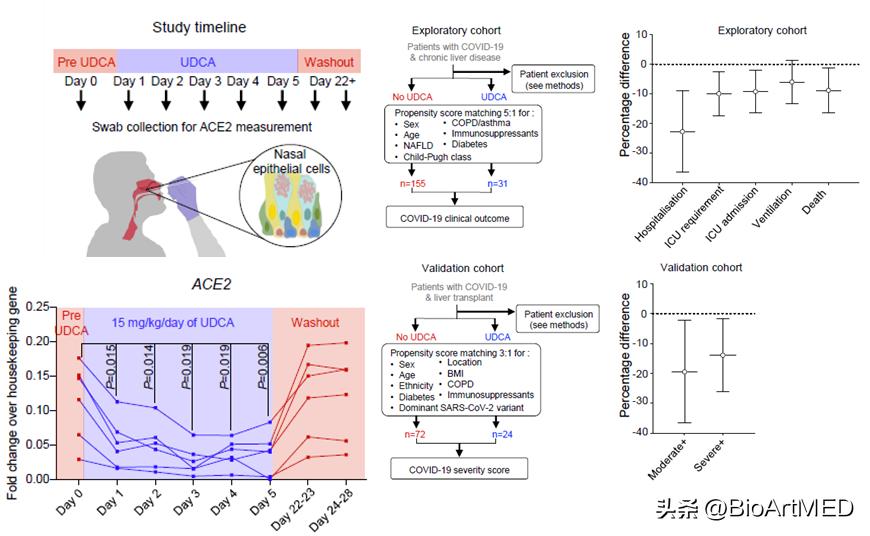
图3 志愿者试验和队列研究分析。
最后,通过分析两个独立的队列——COVID-Hep/SECURE17-Liver和Veterans Outcomes and Costs Associated with Liver disease (VOCAL) ,均发现UDCA服药同更好的SARS-CoV-2预后相关 (如 图3 所示) ,再次增强了这一研究工作结论的可信性。
总结而言, 这一工作发现了FXR在调控ACE2表达方面的新功能,并为靶向这一通路预防SARS-CoV-2感染提供了理论依据和实验证据,为未来的临床试验铺平了道路。
原文链接:
https://doi.org/10.1038/s41586-022-05594-0
制版人:十一
参考文献
[1] Organization., W. H. Therapeutics and COVID-19 LIVING GUIDELINE 3 MARCH 2022. 1–109 (2022).
[2] The RECOVERY Collaborative Group. Dexamethasone in Hospitalized Patients with Covid-19. N. Engl. J. Med. 384, 693–704 (2021).
[3] Beigel, J. H. et al. Remdesivir for the Treatment of Covid-19 — Final Report. N. Engl. J. Med. 383, 1813–1826 (2020).
[4] Cao, Y. et al. Omicron escapes the majority of existing SARS-CoV-2 neutralizing antibodies. Nature 602, 657–663 (2022).
[5] Callaway, E. The unequal scramble for coronavirus vaccines — by the numbers. Nature 584, 506–507 (2020).[6] Gaziano, L. et al. Actionable druggable genome-wide Mendelian randomization identifies repurposing opportunities for COVID-19. Nat. Med. 27, 668–676 (2021).[7] Sungnak, W. et al. SARS-CoV-2 entry factors are highly expressed in nasal epithelial cells together with innate immune genes. Nat. Med . 26, 681–687 (2020).[8] Evangelou, K. et al. Pulmonary infection by SARS-CoV-2 induces senescence accompanied by an inflammatory phenotype in severe COVID-19: possible implications for viral mutagenesis. Eur. Respir. J. 60, (2022).
[9] World Health Organization. WHO Guidelines: Drugs to prevent COVID-19. WHO Guidel. 53, 1689–1699 (2021).[10] Bartoszko, J. J. et al. Prophylaxis against covid-19: Living systematic review and network meta-analysis. BMJ 373, 1–12 (2021).
[11] Sun, L., Cai, J. & Gonzalez, F. J. The role of farnesoid X receptor in metabolic diseases, and gastrointestinal and liver cancer. Nat. Rev. Gastroenterol. Hepatol . 18, 335-347 (2021).