·论著·
引用本文:史鑫, 王向平, 张妍, 等. 原发性硬化性胆管炎的内镜治疗及预后分析[J]. 中华消化内镜杂志, 2022, 39(12): 992-997. DOI: 10.3760/cma.j.cn321463-20210709-00349.
原发性硬化性胆管炎的内镜治疗及预后分析
史鑫1,2 王向平2 张妍1,2 王静怡1,2 王旭2 陈龙2 潘阳林1,2
1西安医学院,西安 710068;2空军军医大学第一附属医院消化内科,西安 710032
通信作者:潘阳林,Email:49255980@qq.com
【摘要】 目的 探讨原发性硬化性胆管炎(primary sclerosing cholangitis,PSC)患者行经内镜逆行胰胆管造影术(endoscopic retrograde cholangiopancreatography,ERCP)的诊疗效果及预后相关因素。方法 纳入2009年5月—2020年5月西京医院接诊的PSC病例。回顾性收集人口学、临床症状、实验室和影像学检查、ERCP诊疗等数据,探讨ERCP治疗人群特点及临床疗效,随访观察疾病进展、无移植生存期和总体生存期等。结果 共纳入74例PSC患者,中位年龄53岁,男性占54.1%(40/74),合并胆管显性狭窄、炎症性肠病和其他自身免疫性肝病患者分别占32.4%(24/74)、18.9%(14/74)和17.6%(13/74),接受ERCP患者占36.5%(27/74)。Logistic回归分析显示,高总胆红素( OR =12.33,95% CI :1.24~122.63, P =0.032)和合并胆管显性狭窄( OR =24.67,95% CI :3.40~178.88, P =0.002)是ERCP诊疗的独立危险因素。ERCP操作和临床成功率均为96.3%(26/27)。截至最后一次随访,患者进展为肝硬化、胆管癌、行肝移植及死亡比例分别为9.5%(7/74)、4.1%(3/74)、5.4%(4/74)和18.9%(14/74)。随访患者( n =54)的五年生存率为83.3%。接受ERCP患者与未接受ERCP患者相比,无移植生存期( P =0.933)和总体生存期( P= 0.608)差异均无统计学意义。瘙痒患者 ( HR =5.30,95% CI :1.50~18.90, P =0.010)无移植生存期更短。结论 PSC患者合并炎症性肠病较少而合并自身免疫性肝病的比例较高。高总胆红素或胆管显性狭窄患者接受ERCP治疗占比更高,其操作及临床成功率满意,但ERCP对长期预后无显著影响。瘙痒患者的无移植生存期较短。
【关键词】 胆管炎,硬化性; 胰胆管造影术,内窥镜逆行; 预后; 无移植生存期
Endoscopic treatment and prognosis of primary sclerosing cholangitis
Shi Xin1,2, Wang Xiangping2, Zhang Yan1,2, Wang Jingyi1,2, Wang Xu2, Chen Long2, Pan Yanglin1,2
1 Xi'an Medical University, Xi'an 710068, China; 2 Department of Gastroenterology, The First Affiliated Hospital of Air Force Medical University, Xi'an 710032, China
Corresponding author: Pan Yanglin, Email: 49255980@qq.com
【Abstract】 Objective To investigate the outcome and prognostic factors associated with endoscopic retrograde cholangiopancreatography (ERCP) in patients with primary sclerosing cholangitis (PSC). Methods PSC patients admitted to Xijing Hospital from May 2009 to May 2020 were included. Data of demographics, clinical symptoms, laboratory and imaging tests, and ERCP consultations were collected to explore the population characteristics and clinical efficacy of ERCP treatment, and to follow up disease progression, transplant-free survival, and overall survival . Results A total of 74 patients with PSC were included in this study, with a median age of 53 years, 54.1% (40/74) male. Patients combined with bile duct dominant stenosis, inflammatory bowel disease (IBD), and another autoimmune liver disease were 32.4% (24/74), 18.9% (14/74), and 17.6% (13/74), respectively, and those undergoing ERCP were 36.5% (27/74). Logistic regression analysis showed that high total bilirubin ( OR =12.33, 95% CI : 1.24-122.63, P =0.032) and bile duct dominant stenosis ( OR =24.67, 95% CI : 3.40-178.88, P =0.002) were independent high-risk factors for ERCP consultation. The operation and clinical success rates of ERCP were both 96.3% (26/27). As of the last follow-up, the proportions of patients progressing to cirrhosis, bile duct cancer, liver transplantation and death were 9.5% (7/74), 4.1% (3/74), 5.4% (4/74) and 18.9% (14/74), respectively. The five-year survival rate of the follow‑up patients ( n =54) was 83.3%. The differences in transplant-free survival ( P =0.933) and overall survival ( P =0.608) between ERCP patients and non-ERCP patients were not statistically significant. Transplant-free survival of those who were companied with pruritus ( HR =5.30, 95% CI : 1.50-18.90, P =0.010) was shorter. Conclusion PSC patients have higher proportion of IBD and less autoimmune liver disease. Higher proportion of patients with higher total bilirubin or bile duct dominant stenosis receive ERCP. While the short-term efficacy of ERCP is satisfactory, the long-term prognosis is still suboptimal. Patients with pruritus have a shorter transplant-free survival.
【Key words】 Cholangitis, sclerosing; Cholangiopancreatography, endoscopic retrograde; Prognosis; Non‑transplantation survival
原发性硬化性胆管炎(primary sclerosing cholangitis,PSC)是一种发病机制尚不明确的进行性慢性胆汁淤积性疾病,其特征为肝内和(或)肝外胆道树的炎症改变[1]。大多数PSC患者最终由于胆管进行性炎症和纤维化,进展为肝纤维化、肝硬化门静脉高压和肝衰竭[2]。目前本病唯一的根治方法是肝移植,但同时也面临着肝源缺乏、移植后并发症及复发等问题。近年来,PSC的内镜减黄、新药探索及预后分析是其研究的热点和重点方向。
PSC在欧美西方国家较为多见,其发病特点和预后情况较为清楚。在我国,PSC属于较为罕见的疾病类型,既往相关的临床报道较早,且绝大多数不超过30例[3‑5]。迄今为止,我国最大的一项有随访资料的PSC研究来自于上海仁济医院的马雄教授团队[5],但研究仅纳入了55例PSC患者,重在探索血清标志物对PSC的鉴别价值和预后影响。因此,我国PSC患者的临床预后研究尚有不足。经内镜逆行胰胆管造影术(endoscopic retrograde cholangiopancreatography,ERCP)是有胆管炎症状特别是合并胆管显性狭窄的PSC患者的重要治疗方法,然而,我国患者ERCP治疗相关的大宗报道极少[6],特别是缺少远期疗效数据。本研究基于当前较大的一组有随访资料的PSC中国人群(74例)展开,旨在探索我国PSC患者的ERCP诊疗特点及影响PSC患者预后的危险因素,也将讨论与西方国家历史数据的差异。
资料与方法
一、研究设计
本研究为单中心回顾性队列研究。纳入所有于2009年5月—2020年5月在西京医院住院治疗的PSC患者。纳入标准:(1)年龄18~80岁;(2)入院初诊确定或疑似PSC。排除标准:(1)恶性胆管狭窄;(2)各种因素导致的继发性硬化性胆管炎;(3)胆囊切除术后、肝移植术后等胆管良性狭窄;(4)妊娠期或哺乳期妇女。PSC诊断标准参照2019年发表于 Gut 杂志的PSC诊断和管理指南[7]。
二、数据采集
收集入组患者入院时的人口统计学资料、症状、首发症状时间、实验室检查(肝功能、血常规、自身抗体、IgG4等)、影像学检查资料[磁共振胰胆管成像术(magnetic resonance cholangiopancreatography, MRCP)、上腹部CT、ERCP胆管造影等]、合并相关疾病情况及治疗情况(ERCP、熊去氧胆酸、激素或免疫*制剂抑**)等。所有患者接受门诊或电话随访,随访的内容包括患者后续治疗、是否进展为肝硬化、是否行肝移植及死亡情况。最后一次随访日期为2020-11-15。
根据术前MRCP和(或)ERCP胆管造影以及胆道梗阻的表现,评估有无胆管显性狭窄,其定义为胆总管直径≤1.5 mm或肝总管直径≤1.0 mm,伴有胆管梗阻的表现,如肝功能异常进行性加重、近段胆管扩张或胆汁淤积[7]。
三、研究终点
鉴于诸多条件限制,本队列后期接受肝移植的病例受限。因此,本研究将无移植生存期作为主要的观察指标。随访研究终点为患者从开始出现症状直至死亡、肝移植或最后一次随访的时间。其他观察指标包括总体生存期、ERCP操作和临床治疗成功率、并发症等。ERCP临床治疗成功的定义为术后2周复查总胆红素水平下降超过30%[8]。
四、统计学方法
使用SPSS 25.0统计软件进行统计学分析。正态分布的计量资料用± s 表示,组间比较采用 t 检验;非正态分布计量资料用 M ( Q 1, Q 3)表示,组间比较采用Wilcox秩和检验。计数资料以例(%)表示,组间比较采用 χ ²检验。使用Logistic回归分析评估PSC患者进行ERCP诊疗的独立危险因素。使用Kaplan‑Meier曲线分析ERCP对患者无移植生存期和总体生存期的影响,通过Cox比例风险模型分析确定终点的危险因素。检验均为双边, P <0.05为差异有统计学意义。
结果
一、患者基线资料
2009年5月—2020年5月,所有住院确诊或疑似PSC的患者共91例,根据排除标准筛除17例,最终纳入74例进行分析(表1)。患者中位年龄为53岁,男性患者占54.1%。约90%患者就诊时存在一项或多项临床症状,主要为黄疸(71.6%)、腹痛(35.1%)、发热(9.5%)和瘙痒(8.1%)。24例(32.4%)患者存在两项及以上症状。首次入院时,56.8%(42/74)患者存在影像学胆管狭窄的表现,其中约1/3合并胆管显性狭窄;有3例(4.1%)患者合并冠心病,4例(5.4%)合并高血压,5例(6.8%)合并糖尿病。实验室检查方面,血清总胆红素升高者60例(81.1%)、碱性磷酸酶升高大于1.5倍上限者57例(77.0%)。自身免疫性肝病和炎症性肠病(inflammatory bowel disease, IBD)是主要的合并疾病。前者共13例(17.6%),包括8例自身免疫性肝炎和5例原发性胆汁性肝硬化。合并IBD患者共14例(18.9%),包括溃疡性结肠炎12例、克罗恩病1例以及未定型IBD 1例。入院时合并肝硬化患者15例(20.3%)。
表1 原发性硬化性胆管炎患者基线资料、ERCP治疗情况及随访结果
|
项目 |
全部患者 ( n =74) |
接受ERCP |
统计量 |
P 值 |
|
|
是( n =27) |
否( n =47) |
||||
|
年龄[岁, M ( Q 1, Q 3)] |
53(34,60) |
57(34,62) |
49(34,57) |
Z =-1.52 |
0.144 |
|
性别(男/女) |
40/34 |
18/9 |
22/25 |
χ ²=2.72 |
0.099 |
|
主要症状[例(%)] |
|||||
|
黄疸 |
53(71.6) |
21(77.8) |
32(68.1) |
χ ²=0.79 |
0.373 |
|
腹痛 |
26(35.1) |
13(48.1) |
13(27.7) |
χ ²=3.16 |
0.076 |
|
发热 |
7(9.5) |
2(7.4) |
5(10.6) |
χ ²=0.00 |
0.964 |
|
瘙痒 |
6(8.1) |
0(0.0) |
6(12.8) |
χ ²=2.23 |
0.135 |
|
其他 |
26(35.1) |
5(18.5) |
21(44.7) |
χ ²=5.15 |
0.023 |
|
合并症[例(%)] |
χ ²=2.77 |
0.964 |
|||
|
冠心病 |
3(4.1) |
1(3.7) |
2(4.3) |
||
|
高血压 |
4(5.4) |
1(3.7) |
3(6.4) |
||
|
糖尿病 |
5(6.8) |
2(7.4) |
3(6.4) |
||
|
实验室检查 |
|||||
|
ALT[IU/L, M ( Q 1, Q 3)] |
83(43,145) |
85(43,198) |
82(38,139) |
Z =-0.72 |
0.469 |
|
TBIL[μmol/L, M ( Q 1, Q 3)] |
72(23,187) |
178(103,219) |
42(16,121) |
Z =-3.96 |
<0.001 |
|
ALP[IU/L, M ( Q 1, Q 3)] |
285(199,605) |
373(227,755) |
261(156,523) |
Z =-1.85 |
0.065 |
|
GGT[IU/L, M ( Q 1, Q 3)] |
253(88,566) |
166(46,383) |
292(99,582) |
Z =-1.20 |
0.106 |
|
相关疾病[例(%)] |
|||||
|
胆管显性狭窄 |
24(32.4) |
19(70.4) |
5(10.6) |
χ ²=0.00 |
<0.001 |
|
炎症性肠病 |
14(18.9) |
1(3.7) |
13(27.7) |
χ ²=6.42 |
0.011 |
|
自身免疫性肝病 |
13(17.6) |
4(14.8) |
9(19.1) |
χ ²=0.02 |
0.877 |
|
肝硬化 |
15(20.3) |
4(14.8) |
11(23.4) |
χ ²=0.78 |
0.376 |
|
随访结局[例(%)] |
|||||
|
进展为肝硬化 |
7(9.5) |
2(7.4) |
5(10.6) |
χ ²=0.00 |
0.964 |
|
胆管癌 |
3(4.1) |
2(7.4) |
1(2.1) |
χ ²=0.25 |
0.620 |
|
肝移植 |
4(5.4) |
0(0.0) |
4(8.5) |
χ ²=1.05 |
0.306 |
|
死亡 |
14(18.9) |
5(18.6) |
9(19.1) |
χ ²=0.00 |
0.947 |
注:ERCP指经内镜逆行胰胆管造影术;ALT指丙氨酸转氨酶;TBIL指总胆红素;ALP指碱性磷酸酶;GGT指谷氨酰转移酶
二、接受ERCP患者的病例特点及疗效
1.病例特点:本队列中有27例患者接受ERCP诊疗,占总数的36.5%。与未接受ERCP患者相比,接受ERCP患者入院时总胆红素水平更高( P <0.001)、合并胆管显性狭窄比例更高( P <0.001)。存在其他症状( P =0.023)、合并IBD患者( P =0.011)则较少接受ERCP减黄治疗(表1)。进一步Logistic多因素分析显示:总胆红素>41 μmol/L( OR =12.33,95% CI :1.24~122.63, P =0.032)与合并胆管显性狭窄( OR =24.67,95% CI :3.40~178.88, P =0.002)是患者接受ERCP诊疗的独立危险因素(表2)。
表2 原发性硬化性胆管炎患者接受ERCP诊疗的多因素Logistic回归分析
|
变量 |
多因素分析 |
||
|
OR |
95 %CI |
P 值 |
|
|
性别(男性) |
1.09 |
00.19~6.17 |
0.925 |
|
症状 |
|||
|
黄疸 |
Ref |
||
|
腹痛 |
5.04 |
0.78~32.73 |
0.090 |
|
发热 |
0.47 |
0.02~18.80 |
0.635 |
|
瘙痒 |
0.47 |
0.02~10.80 |
0.635 |
|
实验室检查 |
|||
|
TBIL>41 μmol/L |
12.33 |
1.24~122.63 |
0.032 |
|
ALP>125 IU/L |
24.69 |
0.78~786.80 |
0.069 |
|
相关疾病 |
|||
|
无 |
Ref |
||
|
胆管显性狭窄 |
24.67 |
3.40~178.88 |
0.002 |
|
自身免疫性肝病 |
3.52 |
0.03~380.94 |
0.598 |
注:ERCP指经内镜逆行胰胆管造影术;TBIL指总胆红素;ALP指碱性磷酸酶;Ref表示参考值
2.治疗情况:所有接受ERCP患者中,治疗性ERCP占96.3%(26/27),治疗主要适应证包括黄疸/急性胆管炎(88.9%,24/27)和胆总管结石(7.4%,2/27)。ERCP操作成功率为96.3%(26/27),其中乳头括约肌切开术12例(44.4%)、鼻胆管引流术15例(55.6%)、球囊扩张术11例(40.7%)、塑料支架置入术9例(33.3%),1例因十二指肠肠腔狭窄操作不成功。临床治疗成功率为96.2%(25/26)。ERCP术后并发症发生率为7.4%(2/27),均为胆道感染,给予抗感染治疗后好转。
3.长期疗效:截至最后一次随访,接受ERCP的PSC患者的中位随访时间为53(1~140)个月,2例患者发展为肝硬化,2例患者发展为胆管癌,5例患者死亡(均为胆管炎相关性),无患者接受肝移植。ERCP术后长期随访的胆管炎复发率为22.2%(6/27),此类患者均多次接受ERCP治疗,后期以临时放置鼻胆管引流为主要治疗方式。与未接受ERCP诊疗相比,接受ERCP诊疗对患者总体生存期( P =0.608)及无移植生存期( P =0.933)无影响(图1、2)。
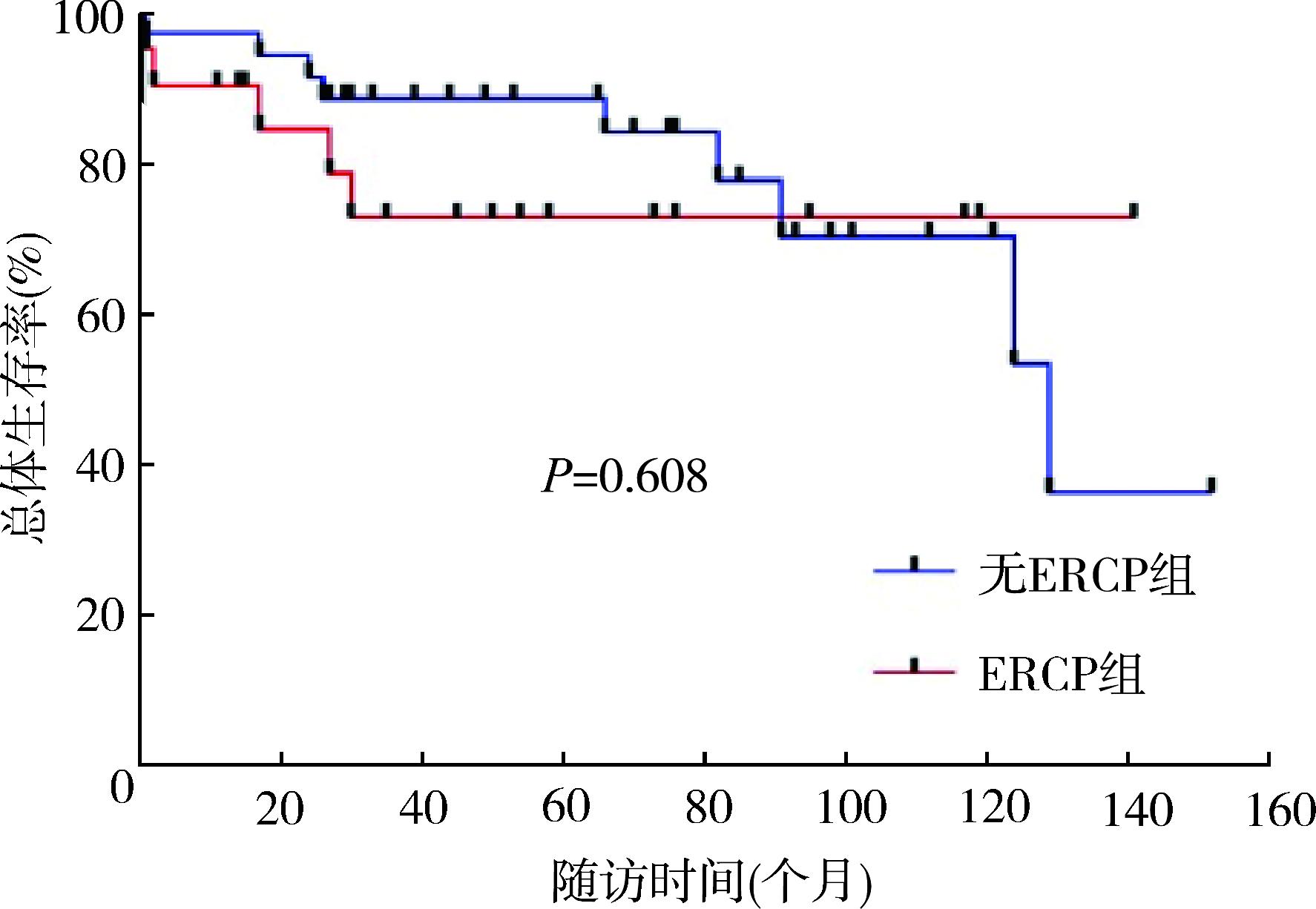
图1 行经内镜逆行胰胆管造影术(ERCP)和未行ERCP的原发性硬化性胆管炎患者总体生存率的Kaplan‑Meier曲线
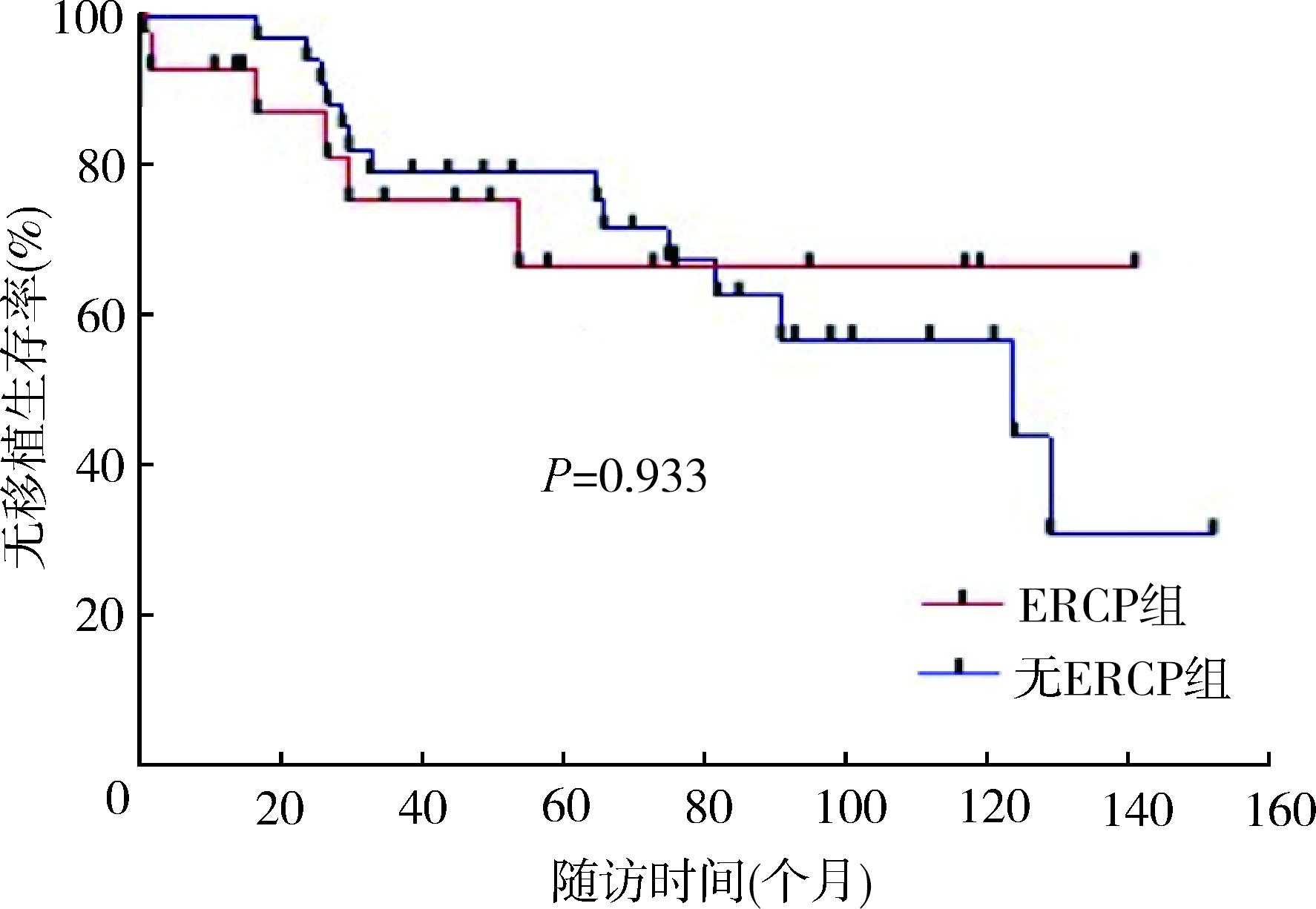
图2 行经内镜逆行胰胆管造影术(ERCP)和未行ERCP的原发性硬化性胆管炎患者无移植生存率的Kaplan‑Meier曲线
三、总体随访及生存、复发分析
1.随访结果:本组所有病例中位随访时间为48(1~152)个月,失访患者20例(27.0%)。截至最后一次随访,7例(9.5%)患者进展为肝硬化,3例(4.1%)患者发展为胆管癌,4例(5.4%)患者接受肝移植,14例(18.9%)患者死亡(胆管炎相关11例、肝硬化相关2例、癌转移相关1例)。在有随访数据的54例患者中,五年生存率为83.3%(图3)。
2.药物治疗情况:63.5%(47/74)患者接受熊去氧胆酸治疗,其中34%的患者持续服用熊去氧胆酸治疗至最后一次随访。另有19例患者接受激素或者免疫*制剂抑**治疗,其中合并自身免疫性肝炎者4例、合并IBD者2例、合并慢性皮疹者1例。
3.无移植生存的危险因素分析:截至最后一次随访,共18例(24.3%)患者死亡或接受肝移植。患者的无移植生存期为85个月。Cox单因素分析结果见表3,进一步行Cox多因素分析显示,瘙痒 (中位生存期94.5个月, HR =5.30,95% CI : 1.50~18.90, P =0.010)是PSC患者无移植生存的独立危险因素。
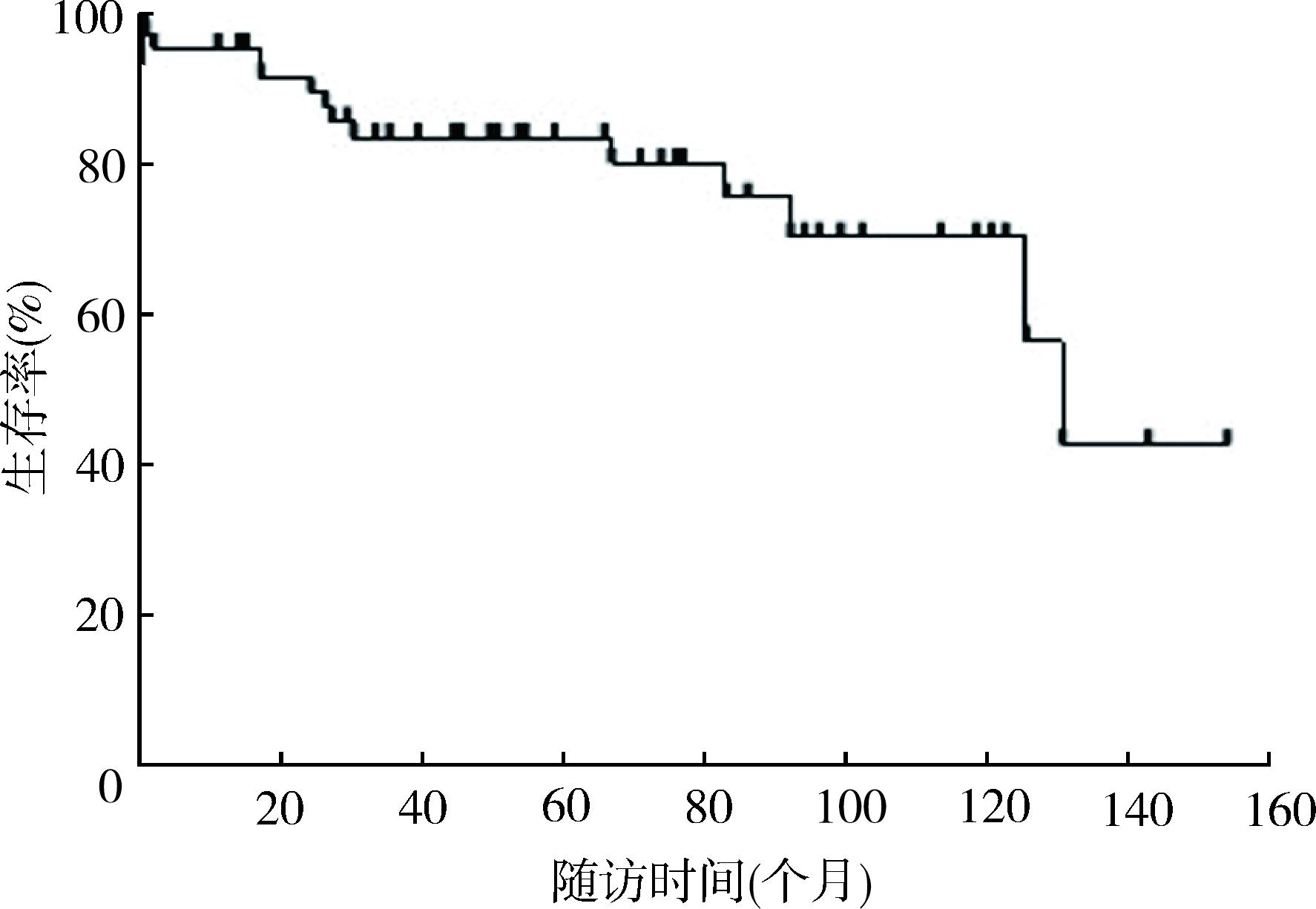
图3 有随访数据的原发性硬化性胆管炎患者总体生存率的Kaplan‑Meier曲线图
表3 原发性硬化性胆管炎患者无移植生存期影响因素的单因素Cox回归分析
|
变量 |
单因素分析 |
||
|
HR |
95% CI |
P 值 |
|
|
年龄(岁) |
1.03 |
0.99~1.06 |
0.101 |
|
性别(男性) |
0.89 |
0.35~2.25 |
0.808 |
|
症状 |
|||
|
黄疸 |
Ref |
||
|
腹痛 |
0.87 |
0.27~2.83 |
0.811 |
|
发热 |
0.75 |
0.09~6.00 |
0.786 |
|
瘙痒 |
5.28 |
1.57~17.59 |
0.007 |
|
合并症 |
|||
|
无 |
Ref |
||
|
冠心病 |
2.43 |
0.31~18.84 |
0.394 |
|
高血压 |
0.82 |
0.11~6.22 |
0.844 |
|
实验室检查 |
|||
|
ALP>185.5 IU/L |
2.81 |
0.64~12.28 |
0.169 |
|
TBIL>20.5 μmol/L |
2.13 |
0.49~9.25 |
0.315 |
|
ALT>50 IU/L |
1.57 |
0.46~5.45 |
0.152 |
|
GGT>60 IU/L |
1.81 |
0.42~7.93 |
0.429 |
|
相关疾病 |
|||
|
无 |
Ref |
||
|
胆管显性狭窄 |
1.74 |
0.58~5.20 |
0.324 |
|
自身免疫性肝病 |
1.41 |
0.17~11.87 |
0.750 |
|
炎症性肠病 |
0.52 |
0.06~4.37 |
0.549 |
|
肝硬化 |
0.95 |
0.24~3.85 |
0.945 |
|
行ERCP |
0.87 |
0.31~2.44 |
0.783 |
|
使用熊去氧胆酸 |
0.83 |
0.32~2.14 |
0.695 |
|
使用激素或免疫*制剂抑** |
0.97 |
0.33~2.84 |
0.953 |
注:ALP指碱性磷酸酶;TBIL指总胆红素;ALT指丙氨酸转氨酶;GGT指谷氨酰转移酶;ERCP指经内镜逆行胰胆管造影术;Ref表示参考值
讨论
与西方国家相比,PSC是我国较为罕见的疾病,目前没有针对性治疗,ERCP仅作为部分PSC患者的姑息性减黄治疗手段,其疗效特别是长期疗效仍是目前关注的重点。在既往报道中,我国PSC人群的长期随访队列均较小,且未见ERCP相关长期疗效的数据。本研究基于本院过去12年间的74例PSC患者队列展开分析,这也是迄今为止我国较大的一组有详细随访数据的PSC相关分析报道。我们的主要发现如下:(1)与西方国家相比,我国PSC患者合并IBD的比例明显偏低(18.9%比70%[9]),而合并自身免疫性肝病的比例较高(17.6%比1%~8%[10]);(2)36.5%(27/74)的PSC患者接受ERCP诊疗,与西方国家报道的数据类似(36%~50%);(3)高总胆红素和合并胆管显性狭窄的患者接受ERCP治疗占比更高,ERCP的操作成功率及短期临床效果均较满意,但似乎不改变患者的长期预后(如总体生存期、无移植生存期等);(4)始发瘙痒患者的无移植生存期较短。
既往发现合并胆管显性狭窄是ERCP治疗较好的适应证[11],本研究接受ERCP的患者合并胆管显性狭窄的比例也更高。本研究发现,合并胆管显性狭窄对患者的无移植生存期无明显影响,这与此前Rupp等[12]研究结果相符。有文献发现,胆管显性狭窄会影响PSC患者肝移植后的生存[13],由于肝源获取受限和可能的经济因素,本研究中接受肝移植的PSC患者较少,因此难以判断胆管显性狭窄与移植后生存的关系。此外既往研究还显示,欧美国家合并IBD患者的总体生存期明显缩短[14],然而基于发病率较低且病例数量有限( n =13),本研究并未分析合并IBD与我国PSC患者总体生存期的关系。
通过术前选择合适的适应证,本研究中ERCP治疗获得了满意的成功率,通过鼻胆管引流、球囊扩张、支架置入等治疗措施,可以快速缓解患者肝功能指标或黄疸症状,改善患者的短期生存质量。有研究显示,与单纯球囊扩张相比,短期支架置入并不增加治疗的有效性[15]。因为病例数较少,我们也未能发现单纯球囊扩张与支架置入患者之间的差异。本研究中部分患者临时放置了鼻胆管以观察术后黄疸的消退情况,如消退效果较好,利用内镜下剪刀剪断鼻胆管,作为一种临时用塑料支架继续发挥短期的狭窄支撑作用,该策略在本研究中的临床效果较好,但尚需与当前单纯球囊扩张的标准治疗进行前瞻性比较。
本研究发现,瘙痒患者的无移植生存期短。瘙痒是PSC的一种常见症状,会导致患者生活质量严重下降甚至致残。对于胆汁淤积性瘙痒且生活质量严重受影响的患者,除了肝移植以外无特殊的治疗方法。本回顾性研究对于瘙痒无法进行系统性评估,主观性较强。瘙痒是否影响PSC患者无移植生存期仍需要大量的前瞻性研究来验证。
在我国,熊去氧胆酸作为PSC的治疗药物使用较多。之前有研究发现熊去氧胆酸可以改善肝功能情况,但不能改善患者无移植生存期;肝硬化是影响患者无移植生存的危险因素[16]。以上皆与本研究的发现一致。肝移植仍是目前PSC唯一有效的根治方法,但由于多方面的原因,我国PSC患者肝移植及再移植率远低于西方国家,因此此组队列PSC患者的无移植生存期尚不理想(85个月比112~180个月[17‑18])。
本研究为单中心回顾性研究,与西方国家相比,本研究队列的样本量仍较少。另外,人群的随访时间偏短,失访率偏高,研究中纳入的人群以西北省份的人群居多,仍局限于当前的一些常规治疗手段。因此,本研究的结果受到上述因素的影响较大,患者的总体生存期欠佳,尚有一定的提升空间。在将来的研究中,在以下若干方面值得进一步探索:(1)将数据库扩充为多中心队列,进行前瞻性随访,获得我国PSC人群更具代表性的数据;(2)基于PSC免疫微环境及基因易感性的基础研究,结合近期在IBD以及自身免疫性肝病等相关疾病治疗的进展,努力探索新的药物治疗方法;(3)ERCP和经皮经肝胆管引流手术作为有效的姑息性减黄手段,尚需进一步优化以使患者获得长期的获益。
总体而言,本研究基于目前我国较大的PSC长期随访队列展开。研究提示相比于西方国家,我国PSC患者合并IBD比例偏低,合并自身免疫性肝病比例较高,而接受ERCP的比例则相当;高总胆红素和胆管显性狭窄者接受ERCP占比较高,ERCP的操作成功率及短期临床效果均较满意,瘙痒患者的无移植生存期较短,而ERCP并未改善患者的长期预后。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明
史鑫:数据收集及整理、论文撰写;王向平:论文修改;张妍、王静怡、王旭、陈龙:统计分析;潘阳林:研究指导、经费支持
参考文献
[1] Silveira MG, Lindor KD. Primary sclerosing cholangitis[J]. Can J Gastroenterol, 2008,22(8):689-698. DOI: 10.1155/2008/824168.
[2] Dyson JK, Beuers U, Jones D, et al. Primary sclerosing cholangitis[J]. Lancet, 2018,391(10139):2547-2559. DOI: 10.1016/S0140-6736(18)30300-3.
[3] 古杰, 蒋文涛, 李江, 等. 肝移植治疗终末期自身免疫性肝病的临床分析[J]. 中华危重病急救医学,2019,31(11):1401-1405. DOI: 10.3760/cma.j.issn.2095-4352.2019.11.017.
[4] 赵新颜, 王婉溦, 欧晓娟, 等. 原发性硬化性胆管炎27例临床病理特点分析 [J]. 中华肝脏病杂志,2010,18(9):685-688. DOI: 10.3760/cma.j.issn.1007-3418.2010.09.010.
[5] Lian M, Li B, Xiao X, et al. Comparative clinical characteristics and natural history of three variants of sclerosing cholangitis: IgG4-related SC, PSC/AIH and PSC alone[J]. Autoimmun Rev, 2017,16(8):875-882. DOI: 10.1016/j.autrev.2017.05.018.
[6] 毕荣欣, 郭全周, 薛志广, 等. 原发性硬化性胆管炎患者经内镜逆行胰胆管造影术后不良事件发病率及危险因素分析[J].临床肝胆病杂志,2015,31(2):189-192. DOI: 10.3969/j.issn.1001-5256.2015.02.011.
[7] Chapman MH, Thorburn D, Hirschfield GM, et al. British Society of Gastroenterology and UK-PSC guidelines for the diagnosis and management of primary sclerosing cholangitis[J]. Gut, 2019,68(8):1356-1378. DOI: 10.1136/gutjnl-2018-317993.
[8] Enns R, Eloubeidi MA, Mergener K, et al. Predictors of successful clinical and laboratory outcomes in patients with primary sclerosing cholangitis undergoing endoscopic retrograde cholangiopancreatography[J]. Can J Gastroenterol, 2003,17(4):243-248. DOI: 10.1155/2003/475603.
[9] Weismüller TJ, Trivedi PJ, Bergquist A, et al. Patient age, sex, and inflammatory bowel disease phenotype associate with course of primary sclerosing cholangitis[J]. Gastroenterology, 2017,152(8):1975-1984.DOI: 10.1053/j.gastro. 2017.02.038.
[10] Kaya M, Angulo P, Lindor KD. Overlap of autoimmune hepatitis and primary sclerosing cholangitis: an evaluation of a modified scoring system[J]. J Hepatol, 2000,33(4):537-542. DOI: 10.1034/j.1600-0641.2000.033004537.x.
[11] 中华医学会消化内镜学分会内镜外科学组, 中国医师协会内镜医师分会, 中国医师协会胰腺病专业委员会. 中国外科ERCP医师培训专家共识意见(2022版)[J].中华消化内镜杂志,2022,39(6):421-429. DOI: 10.3760/cma.j.cn321463- 20220405-00235.
[12] Rupp C, Rössler A, Halibasic E, et al. Reduction in alkaline phosphatase is associated with longer survival in primary sclerosing cholangitis, independent of dominant stenosis[J]. Aliment Pharmacol Ther, 2014,40(11-12):1292-1301. DOI: 10.1111/apt.12979.
[13] Rudolph G, Gotthardt D, Klöters-Plachky P, et al. Influence of dominant bile duct stenoses and biliary infections on outcome in primary sclerosing cholangitis[J]. J Hepatol, 2009,51(1):149-155. DOI: 10.1016/j.jhep.2009.01.023.
[14] Sørensen JØ, Nielsen OH, Andersson M, et al. Inflammatory bowel disease with primary sclerosing cholangitis: a Danish population-based cohort study 1977-2011[J]. Liver Int, 2018,38(3):532-541. DOI: 10.1111/liv.13548.
[15] Ponsioen CY, Arnelo U, Bergquist A, et al. No superiority of stents vs balloon dilatation for dominant strictures in patients with primary sclerosing cholangitis[J]. Gastroenterology, 2018,155(3):752-759. DOI: 10.1053/j.gastro.2018.05.034.
[16] Charatcharoenwitthaya P, Angulo P, Enders FB, et al. Impact of inflammatory bowel disease and ursodeoxycholic acid therapy on small-duct primary sclerosing cholangitis[J]. Hepatology, 2008,47(1):133-142. DOI: 10.1002/hep.21960.
[17] Ravikumar R, Tsochatzis E, Jose S, et al. Risk factors for recurrent primary sclerosing cholangitis after liver transplantation[J]. J Hepatol, 2015,63(5):1139-1146. DOI: 10.1016/j.jhep.2015.07.005.
[18] Herrero JI, Quiñones M, Pérez X, et al. Liver transplant recipients have an increased risk of developing colorectal adenomas: results from a retrospective study[J]. Clin Transplant, 2021,35(1):e14154. DOI: 10.1111/ctr.14154.
DOI:10.3760/cma.j.cn321463-20210709-00349
收稿日期 2021-07-09 本文编辑 朱悦