撰文 | 我的闺蜜老红帽
机体为应对细菌和真菌感染会形成肉芽肿 (Granulomas) ,但是肉芽肿同样也可能导致肉样瘤病 (sarcoidosis) 、铍中毒症 (berylliosis) 和类风湿性关节炎 (rheumatoid arthritis) 等疾病 【1,2】 。肉芽肿所导致的器官纤维化以及损伤病变,是上述疾病的主要原因 【3-6】 。当然,肉芽肿的形成是经进化选择而来,可以将入侵机体的病原体局限在病灶内部,从而帮助免疫系统行使功能,但是,肉芽肿性炎症 (granulomatous inflammation) 也可以弥散开来,且启动因素还不清楚 【7,8】 。肉芽肿结构复杂,内部包含有固有和获得型免疫细胞,以及结构性细胞,如成纤维细胞或内皮细胞等 【2】 。虽然不同肉芽肿的细胞组成类似,但是这些细胞的微解剖分布以及分泌细胞因子谱区别很大。肉芽肿中最为常见的免疫细胞类型为巨噬细胞。它们彼此联系紧密,并可以形成上皮样细胞 (epitheloid cells) 结构,甚至相互融合形成含有多细胞核的巨型细胞。而且,肉芽肿中的巨噬细胞通常处于代谢紊乱状态,从而导致炎症加剧;肉芽肿中的巨噬细胞可以与多种T细胞亚型相互作用,比如蠕虫 (helminth) 感染时,与II型辅助性T细胞 (Th2) 相互作用,罹患肺结核 (tuberculosis) 时,与IFN-r分泌型Th1相互作用,罹患克罗恩病时,与Th1和Th17相互作用。肉芽肿的边界由成纤维细胞所产生的胞外基质 (extracellular matrix) 成分所划定,从而导致纤维化以及器官功能异常。近期工作指出,免疫细胞与结构性细胞之间的相互作用网络,参与维持肉芽肿的结构以及炎症状态,但具体机制仍不算清晰。
近日,来自奥地利CeMM Research Center for Molecular Medicine of the Austrian Academy of Sciences的 Christoph Bock 和 Georg Stary 研究组在 Immunity 上发表题为 Single-cell and spatial transcriptomics reveal aberrant lymphoid developmental programs driving granuloma formation 的文章,就肉芽肿形成机制进行了深入研究。

为了研究肉芽肿形成的分子以及细胞机制,作者之前的工作关注表皮结节病 (cutaneous sarcoidosis) ,这是一类非感染型肉芽肿疾病,是研究肉芽肿形成机制的良好模型。这类肉芽肿的成因可能包含环境刺激、免疫响应异常以及遗传因素。目前来说没有很好的治疗手段,且免疫抑制疗法会带来多种副作用。
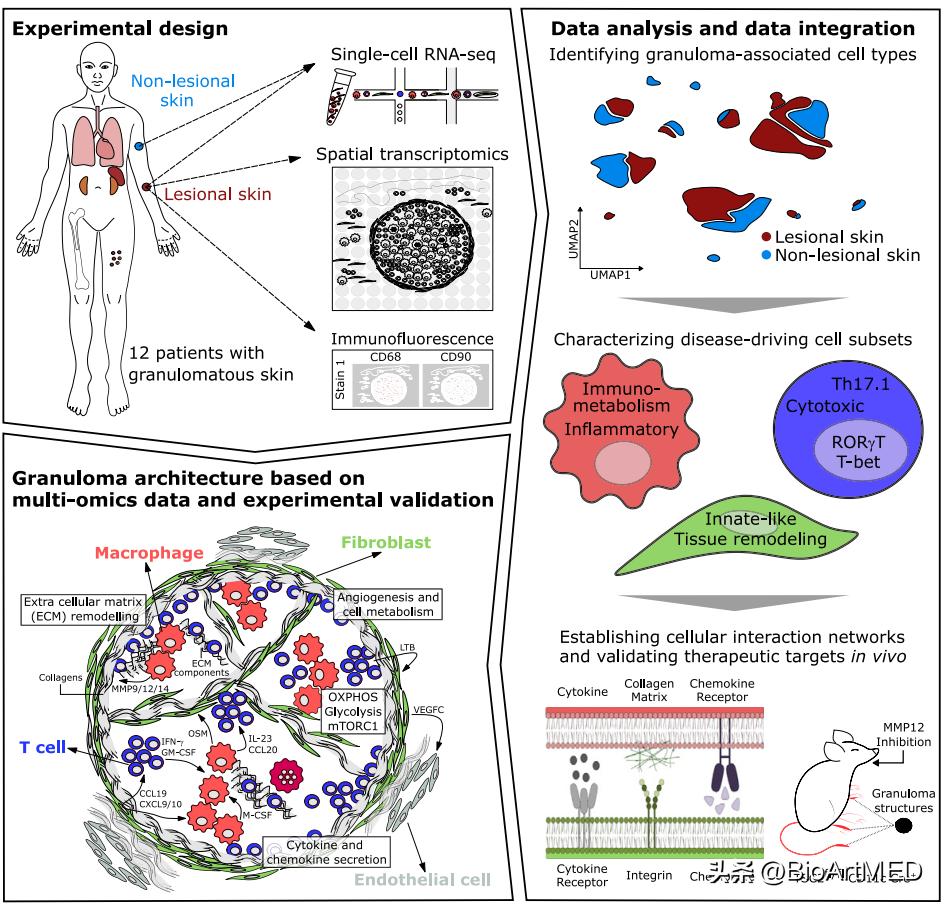
作者这份工作重点关注肉芽肿形成过程中的基因调控图谱以及细胞-细胞相互作用。作者采集了12位结节病患者的样本,通过单细胞RNA测序以及空间转录组学相结合的研究手段,比较肉芽肿与无损皮肤之间差异,深度分析肉芽肿细胞的标志蛋白。作者还发现在肉芽肿中,具有免疫刺激性环境,可以重建调控相关淋巴器官发育的转录图谱。肉芽肿形成所需的空间特征以及相关基因与免疫代谢、细胞因子和趋化因子信号通路以及胞外介质重塑相关。作者所重点解析的肉芽肿相关巨噬细胞、Th17.1细胞以及成纤维细胞,强势参与肉芽肿内细胞-细胞相互作用的旁分泌网络,并且是肉芽肿形成的关键细胞:巨噬细胞进行代谢性重编程、Th17.1进行细胞因子分泌型以及成纤维细胞呈现炎性且具有组织重构表型。在小鼠结核病模型中,通过药物抑制上述某一类通路,就可以有效减缓肉芽肿形成。作者还确定,肉芽肿形成过程中的分子水平变化驱使其形成三级淋巴结构,但是这一结构缺乏整体控制,这也说明肉芽肿可以作为一类异常淋巴器官。
综上所述,作者通过对结核病相关皮肤肉芽肿进行单细胞RNA测序以及空间组学分析发现,肉芽肿形成需要独特的基因调控模式,以及一套病理性巨噬细胞、T细胞和成纤维细胞所构成的细胞网络,并且,肉芽肿可以视作淋巴器官中的异类。
原文链接:
https://doi.org/10.1016/j.immuni.2023.01.014
制版人:十一
参考文献
1. Adams, D.O. (1976). The granulomatous inflammatory response. A re- view. Am. J. Pathol . 84, 164–192.
2. Paga ́ n, A.J., and Ramakrishnan, L. (2018). The formation and function of granulomas . Annu. Rev. Immunol. 36, 639–665. https://doi.org/10.1146/ annurev-immunol-032712-100022.
3. Mornex, J.F., Leroux, C., Greenland, T., and Ecochard, D. (1994). From granuloma to fibrosis in interstitial lung diseases: molecular and cellular interactions. Eur. Respir. J. 7, 779–785. https://doi.org/10.1183/ 09031936.94.07040779.
4. Roda, G., Chien Ng, S., Kotze, P.G., Argollo, M., Panaccione, R., Spinelli, A., Kaser, A., Peyrin-Biroulet, L., and Danese, S. (2020). Crohn’s disease. Nat. Rev. Dis. Primers 6, 22. https://doi.org/10.1038/s41572-020- 0156-2.
5. Saketkoo, L.A., Russell, A.-M., Jensen, K., Mandizha, J., Tavee, J., Newton, J., Rivera, F., Howie, M., Reese, R., Goodman, M., et al. (2021). Health-related quality of life (Hrqol) in sarcoidosis: diagnosis, management, and health outcomes. Diagnostics (Basel) 11, 1–35. https://doi.org/10.3390/diagnostics11061089.
6. Moradkhani, A., Beckman, L.J., and Tabibian, J.H. (2013). Health-related quality of life in inflammatory bowel disease: psychosocial, clinical, so- cioeconomic, and demographic predictors. J. Crohns Colitis 7, 467–473. https://doi.org/10.1016/j.crohns.2012.07.012.
7. Mukhopadhyay, S., Farver, C.F., Vaszar, L.T., Dempsey, O.J., Popper, H.H., Mani, H., Capelozzi, V.L., Fukuoka, J., Kerr, K.M., Zeren, E.H., et al. (2012). Causes of pulmonary granulomas: a retrospective study of 500 cases from seven countries. J. Clin. Pathol. 65, 51–57. https:// doi.org/10.1136/jclinpath-2011-200336.
8. Terziroli Beretta-Piccoli, B., Mainetti, C., Peeters, M.A., and Laffitte, E. (2018). Cutaneous granulomatosis: a comprehensive review. Clin. Rev. Allergy Immunol. 54, 131–146. https://doi.org/10.1007/s12016-017- 8666-8.