*仅供医学专业人士阅读参考
点击右上方“关注”, 准时接收每日精彩内容推送。
过继性T(Treg)细胞是多种自身免疫性疾病的基础,并通过过继细胞疗法加强抗炎诊治。然而,细胞疗法的系统递送通常缺乏针对局部自身免疫性疾病的组织靶向和积累。此外,Treg细胞的不稳定性和可适应性也会诱导表型转变和功能丧失,阻碍临床转译。
浙江大学的顾臻团队等人 开发了一种穿孔微针(PMN),该微针具有良好的机械性能及宽敞的封装腔以支持细胞存活,以及可调节的通道以促进细胞迁移,用于银屑病的局部Treg治疗。相关研究成果以 “Adoptive Treg therapy with metabolic intervention via perforated microneedles ameliorates psoriasis syndrome” 为题,于2023年5月17日发表在 《Science Advances》 上。
研究人员设计了核壳结构的PMN,其特点是 外壳上具有可调通道、所需的机械强度、宽敞的加载腔以及自由的细胞迁移,用于经皮递送具有可持续生存能力的治疗细胞 。

图1 PMN介导的过继性Treg治疗银屑病的设计
为了实现精细的MN设计,使用了立体光刻3D打印技术,并采用“三明治”成型法制造PMN,将两个PDMS模具与其间的生物相容性聚合物挤压在一起,以产生穿孔的MN(图1B)。所得PMN在外壳上有四个矩形通道,针头设计为半径300μm,高度1100μm,中心到中心距离1400μm(图2A)。不同层的截面图证明了PMN的中空结构,表明 其具有规则的外壳结构和宽敞的空腔 (图2、B和C)。

图2 PMN的制造和表征
为了支持亲水培养基,这有助于维持细胞活力,PMN首选不混溶的疏水外壳,以避免在给药过程中出现结构缺陷。除了提供良好的培养环境外,鉴于Treg细胞的不稳定性和可适应性,维持其抑制功能仍然具有挑战性。最近,在Treg细胞的激活状态下,FAO比糖酵解更受青睐。因此,操纵脂肪酸可用性可能是实现Treg代谢编程治疗自身免疫性疾病或癌症的潜在方法。因此,我们通过本体聚合合成了VP和MMA的疏水共聚物作为PMN基质,该共聚物不仅能耐受水细胞介质,而且在酯酶降解过程中还能释放丙酸盐,进一步增强Treg功能。
最后, 确定共聚物聚(VP-co-MMA)中VP与MMA的体积比为7:3,用于制造PMN,其核壳结构即使在内部加载水凝胶(0.376 N /针)也保持了很强的穿透能力,PMN贴片刺穿小鼠皮肤的台锥蓝染*图色**像也证明了这一点 (图2 D、E)。值得注意的是,与广泛使用的3D打印材料(商业化树脂)相比,细胞毒性测试表明对细胞活力的影响微不足道,证明了poly(VP-co-MMA)进一步传递细胞所需的生物相容性(图2)。为了研究脂肪酸从共聚物中的释放行为,我们选择酯酶(100 IU/ml)进行体外释放研究,模拟银屑病感染小鼠皮肤中的炎症微环境。释放谱表明,PMN可以通过酶介导的方式逐渐释放丙酸盐,同时在无酶培养基中保持稳定(图2F)。
为了在PMN系统中装载治疗细胞,应确定合适的培养基以确保细胞存活,从而延长治疗时间窗。选择明胶作为细胞负载基质,可使Treg细胞存活48小时。将2%明胶-RPMI-1640培养基中的Treg细胞(3.6× 105)真空装入PMN阵列(8×8)。 通过在PMN中包埋的羧基荧光素二乙酸丁二酰酯(CFSE)标记的Treg细胞的共聚焦图像可以看到成功的加载(图3A)。 此外,在整个加载过程中,加载2%明胶的细胞活力与RPMI- 1640培养基的细胞活力保持在比较水平(~82%)(图3B)。

图3 由PMN衍生的脂肪酸增强Treg功能。
接下来,我们探索了Treg细胞从PMN的释放行为。壳上的通道被设计成允许细胞在插入释放介质时迅速迁移出PMN,其中大多数细胞在1.5小时内释放(图3C)。从同一层PMN的延时图像可以看出,水凝胶中的迁移速度减慢了(图3 D、E)。因此,考虑到皮肤组织的致密结构,体内释放动力学甚至更慢。通过扫描电子显微镜(SEM)图像观察到,通道结构在应用期间保持不变,表明细胞释放能力恒定。在贴片去除后,Treg细胞也可以在背侧皮肤中存活较长时间。 总之,PMN在体外和体内都具有理想的细胞装载能力和递送效率。
虽然目前对银屑病病因的理解仍然不明确,但在皮肤免疫稳态中描述了异常的自身反应性T细胞活性。具体来说,表达主调控因子Foxp3的抑制性Treg细胞,由于可塑性和不稳定性,可转化为白细胞介素-17 (IL-17)释放T辅助17 (TH17)样Treg细胞,从而进一步加重银屑病综合征。先前的研究表明,Foxp3的不稳定表达可能会抑制Treg细胞的抑制活性,特别是在体外培养和刺激期间。
体外培养结果与之前的研究结果一致,Foxp3的表达在第3天分别下降到43.84(±8.45)%和16.68(±4.32)%,尽管细胞数量分别上升到1.03(±0.12)倍和1.95(±0.22)倍(图3 F、G)。
为了稳定Treg抑制功能,引入了FAO来操纵T细胞代谢。先前的研究表明,脂质氧化增加可以通过Foxp3酰化等机制稳定Foxp3表达,增强Treg抑制功能。为了探究外源脂肪酸对Foxp3稳定性的影响,我们将Treg细胞与丙酸钠在不同培养基*共中**培养。结果表明,在每天更新培养基的情况下,3天后Treg细胞中Foxp3的表达差异不显著(图S13A)。相反,在没有培养基补充的情况下,补充了丙酸钠的有限营养物质从第2天开始引发Foxp3表达升高(图3H),并且在稀疏的营养培养基中培养时,这种升高甚至更早表现出来(图S13B)。这些结果可能归因于脂肪酸和葡萄糖在营养供应方面的竞争以及它们各自在抑制细胞功能和增殖方面的作用(23,24,34)。除了稳定Foxp3表达外,我们进一步评估了脂肪酸对Treg抑制功能的影响。
Treg抑制实验表明,2 mM丙酸钠增强了Treg对常规T细胞(Tcon)的抑制能力,尤其是在Tcon:Treg比例为4:1和8:1时(图3I)。丁酸钠的这种效果更为明显。值得注意的是,共孵育试验表明, 与Tcon相比,Treg细胞更依赖脂肪酸,其中脂肪酸阻碍Tcon增殖,但不阻碍Treg增殖,丙酸钠约为2至4倍,丁酸钠约为6至10倍,具体取决于浓度(图3J) 。
受上述结果的启发,我们进一步验证了PMN衍生的脂肪酸是否可以达到与丙酸钠相似的效果。同样,从第2天开始,Foxp3表达增加,对所有Tcon: Treg比率的抑制能力增强(图3 K、L)。值得注意的是,酯酶介导的逐渐释放可以避免可能对Treg细胞施加渗透应激的富集脂肪酸浓度。
接下来, 研究人员在吡喹莫德诱导的银屑病小鼠模型中评估了Treg细胞负载PMN (Treg-PMN)的治疗效果(图4A) 。选取8 ~ 9周龄的BALB/c雄性小鼠。将小鼠随机分为7组(n = 5 ~ 6),其中1组应用凡士林作为健康对照组(正常),6组应用咪喹莫特诱导牛皮癣。然后,用不同的配方治疗银屑病小鼠,以评估治疗效果:1组不治疗(未治疗)为阴性对照,,其余5组分别给予空白MN (B-PMN)、全身注射Treg (i.v. Treg)、皮内注射Treg (i.d. Treg)、PMMA制成的Treg载孔MN (TregMMN)和聚(vc -co- mma)制成的Treg载PMN (TregPMN)。银屑病的典型临床表现为皮肤表面出现界限清晰、增厚的红斑鳞状斑块,由角质形成细胞不受控制的过度增殖和大量免疫细胞浸润产生。经过6天的治疗,Treg-PMN显著改善了银屑病综合征,未接受治疗的小鼠相比出现严重炎症和角化细胞增生(图4B)。银屑病面积和严重程度指数(PASI)和热图也与从图像中观察到的症状一致,通过PMN给予Treg细胞的整体表现优于其他组(图4 C、D)。

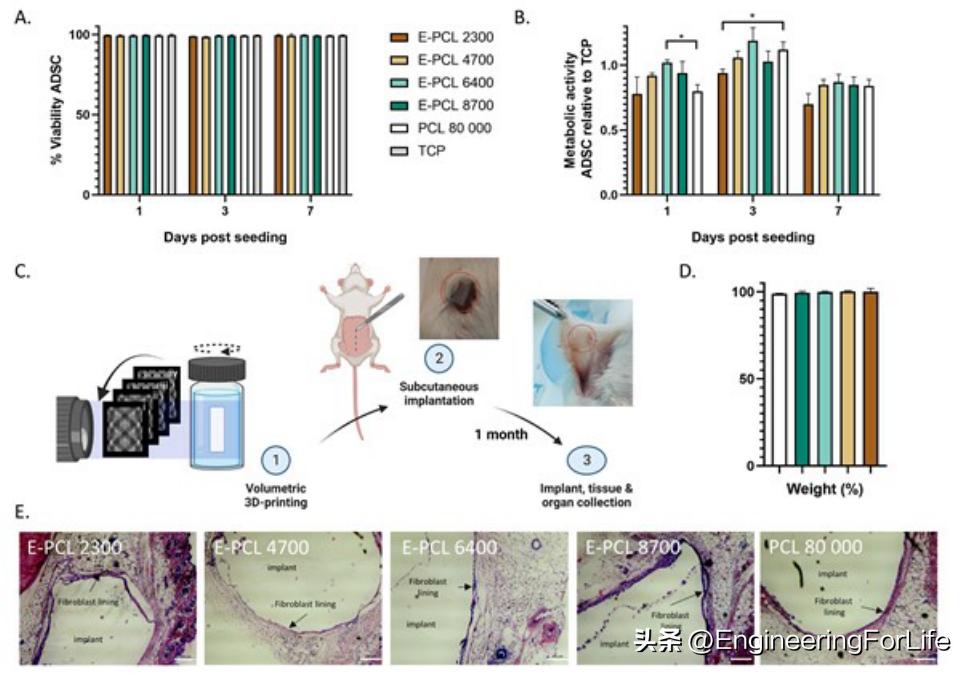
图4 Treg-PMN缓解银屑病
通过监测Treg-PMN组和未治疗组的长期银屑病诱导,进一步排除银屑病复发的可能性。Treg-PMN组抵抗持续使用咪喹莫特,皮肤状况较轻,而未经治疗的牛皮癣组在第12天左右缓慢恢复到正常阶段。这些发现与先前报道的吡喹莫德诱导银屑病小鼠模型的自我恢复一致。
为了进一步研究Treg-PMN的免疫调节作用, 研究人员对MN应用前后免疫环境的演变进行了表征 。PMN给予小鼠8小时后,通过荧光活化细胞分选(FACS)分析证实了Treg细胞的过继转移,其中CD4+ Foxp3+ Treg百分比从5.44%增加到30.2%(图S20)。通过定量逆转录聚合酶链式反应(qRT-PCR)检测几种细胞因子的mRNA表达水平(图4E)。在银屑病恶化期间IL-1β、IL-6和IL-17A的表达显著升高,Treg-PMN治疗后IL-1β、IL-6和IL-17A的表达明显下降。IL-10通常被认为是抗炎和抑制Treg的主要工具,在银屑病进展中高度增加,但在治疗后下降。这种现象也在患者中观察到,研究人员将其归因于IL-10的促炎方面,特别是在CD8+功能和维持中的作用。抑制转化生长因子-β (TGF-β)在银屑病组显著降低,治疗后恢复(P = 0.0723)。IL-23R和IL-12b的表达略有差异,可能与疾病分期有关,皮肤中的表达可以忽略不计。
在第6天进一步评价治疗效果,对所有小鼠实施安乐死,分析免疫群体和细胞因子浓度。FACS和酶联免疫吸附试验(ELISA)显示,通过Treg-PMN治疗,患者从强烈炎症到慢性阶段的整体恢复。结果发现,与未治疗组(6.44%)或B-PMN组(5.08%)相比,给予Treg-PMN的皮肤病变中CD45+细胞显著减少(2.81%)(图5A)。皮内和系统注射Treg细胞的小鼠也有轻度下降,分别为5.58%和4.04%。与未经治疗的银屑病相比,Treg-PMN的中性粒细胞浸润较少,Foxp3+ Treg的百分比较高(图5B)。
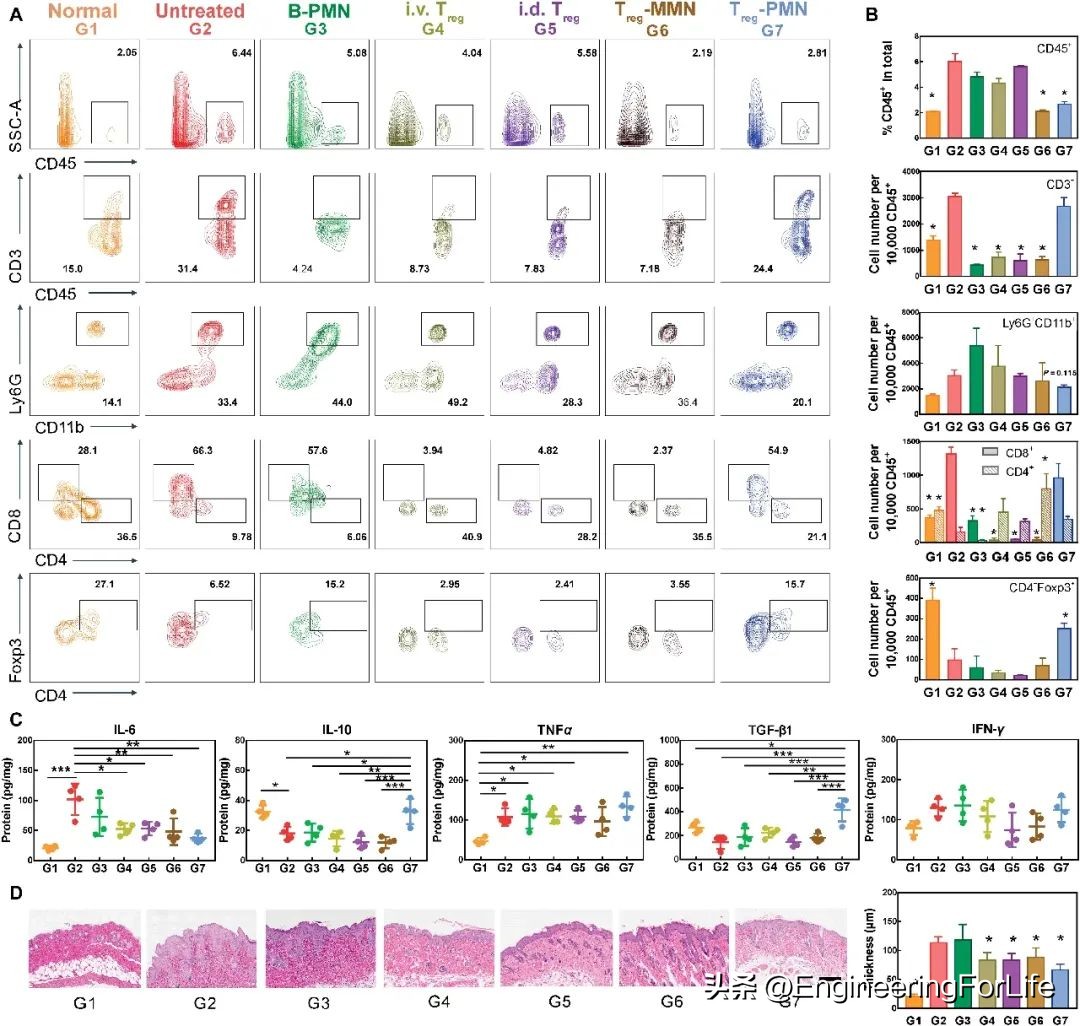
图5 Treg-PMN对银屑病炎症环境的缓解作用
Treg-PMN的改善作用也在细胞因子环境下进行了检测(图5C)。Treg-PMN组IL-10和TGF-β1水平升高,IL-6水平降低,这与Foxp3+ Treg细胞比例较高和整体性能较好是一致的。在所有治疗组中,肿瘤坏死因子-α的中等水平提示慢性银屑病病理。几种银屑病相关细胞因子(干扰素-γ、IL-17A、IL-22和IL-23)的浓度在正常、未治疗的银屑病组和Treg-PMN组中均无统计学意义,这可能是由于它们在银屑病模型恶化的中期过度表达,而在银屑病模型恢复的晚期过度表达(图5C和图S23)。代表性的苏木精和伊红(H&E)染*图色**像也显示Treg-PMN对角质形成细胞过度增殖的改善作用。未经治疗的银屑病组和空白PMN组的背部皮肤角质形成细胞增生从20.58(±3.57)μm增加到118.10(±25.27)μm,而Treg-PMN组的角质形成细胞增生仅增加到66.24(±9.72)μm(图5D)。尽管其他处理均能减轻表皮增厚,但Treg-PMN对表皮增厚的抑制作用显著。此外,研究人员观察到PMN介导的Treg治疗对局部病变的缓解作用强于对全身综合征的缓解作用。
了解更多
关注“EngineeringForLife”,了解更多前沿科研资讯~
