CRISPR基因编辑疗法加快临床应用
01 基因治疗技术有望治愈化学药或生物药无效的疾病
基因治疗是指将外源正常基因导入靶细胞,以纠正或补偿因基因缺陷和异常引起的疾病,以达到治疗目的。基因治疗与常规治疗相比:
常规治疗方法是针对因基因异常而导致的各种症状所作出的疗方案;
基因治疗方法是针对引起疾病的异常基因所采取的治疗手段,能够标本兼制。
Glybera是第一个被西方国家批准的基因治疗药物。该药于2012年10月被欧盟批准用于脂蛋白脂酶缺乏症(LPLD)治疗,2015年上半年首先在德国销售。美国已授予Glybera“孤儿药”资格,预计将于2017年在美国上市。
脂蛋白脂肪酶缺乏症(Lipoprotein lipase deficiency, LPLD)是一种罕见的常染色体隐性遗传病。患者体内脂蛋白脂肪酶缺失或功能异常,血液中的乳糜微粒浓度升高,通常导致急性或复发性胰腺炎。该病目前没有特效药物,临床建议是严格控制饮食中的脂肪含量。
Glybera利用AAV1(腺相关病毒载体)将功能性脂蛋白脂肪酶(LPL)基因递送至骨骼肌细胞,表达脂蛋白脂肪酶。临床试验表明,5名LPLD患者在接受Glybera疗法14周后,血液中的乳糜微粒浓度正常;其中3名患者在接受治疗52周后,血液中的乳糜微粒浓度依然正常。
Glybera在德国的售价为4.1万欧元/瓶,一个典型的LPLD患者需要20-24瓶,总花费80-100万欧元(约合93-117万美元)。LPLD发病率为百万分之一,若欧洲和北美人口按10亿计,则欧美患者人数预计为1000人。若按照每人117万美元的花费计算,Glybera在西方的市场容量为11.7亿美元。
该药的上市标志着基因疗法已不再局限于实验室研究,医药市场的变革时代已经到来。
02 基因编辑技术是基因治疗未来最重要的方向
CRISPR-Cas系统是继ZFN、TALEN之后的第三代基因编辑技术。它的出现推动了基因编辑技术的发展,已经成为当今世界应用最广泛的基因编辑技术,成为生命科学最主要的底层技术之一。CRISPR-Cas9系统主要由Cas9蛋白和单链向导RNA(sgRNA) 所组成,其中Cas9蛋白起切割DNA双链的作用,sgRNA起向导的作用。在sgRNA的向导下通过碱基互补配对原则,Cas9蛋白可对不同的靶部位进行切割,实现DNA的双链断裂。
根据CRISPR-Cas作用模块的数量和种类,CRISPR-Cas系统分为两大类。第一类CRISPR-Cas系统由多个Cas蛋白亚基组成的多蛋白效应复合物和crRNA组成,又可细分为I型、III型和IV型;第二类CRISPR-Cas系统为单一蛋白效应器,又可细分为II型、V型和VI型。目前,已经鉴定的CRISPR-Cas系统中,以第一类CRISPR-Cas系统为主,占比多达90%左右,广泛分布于细菌和古生菌中。由于第一类效应复合物由多蛋白组成,基因编辑过程复杂,实用性不佳。而第二类CRISPR-Cas系统由Cas蛋白发挥DNA或RNA的切割功能,切割靶序列效率高,且单个蛋白易于改造,因而第二类CRISPR-Cas系统被最早开发并广泛应用于基因编辑中。其中,最常用的是Cas9、Cas12a和Cas13a。
图1 Cas9、Cas12和Cas13基因编辑原理图(来源:Molecular Cell)
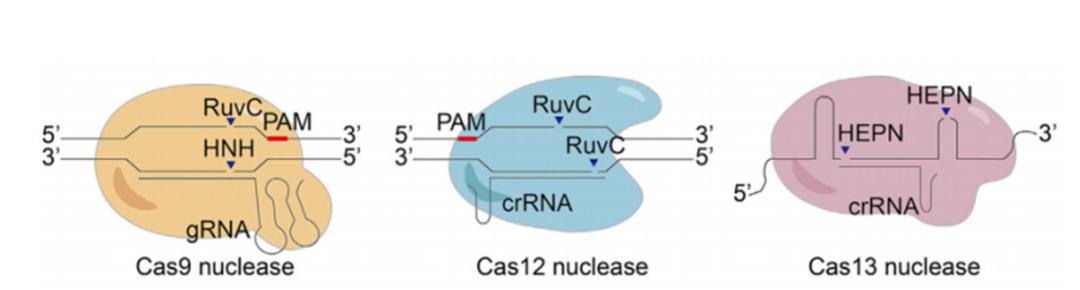
表1 常用Cas蛋白特征
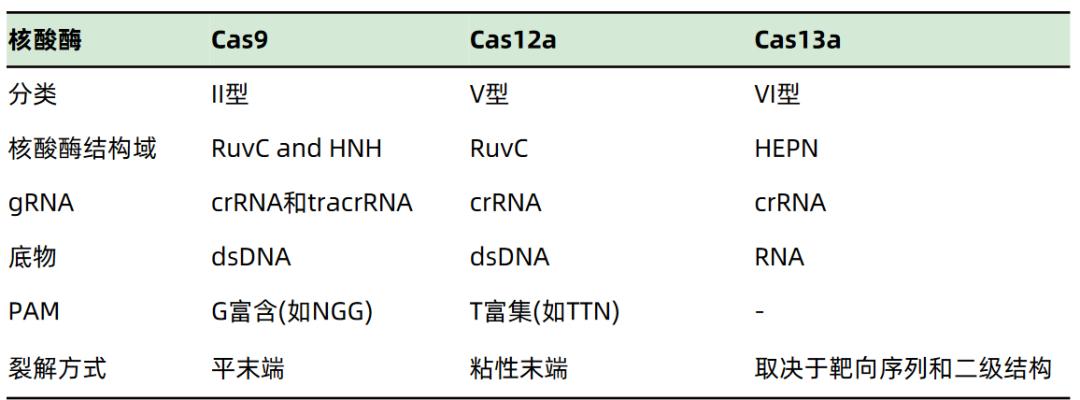
Cas蛋白的固有缺陷限制了CRISPR-Cas系统的应用。PAM序列限制了靶目标的范围,脱靶效应也是CRISPR-Cas系统面临的一大问题,gRNA同靶序列的结合可以允许多个碱基的错配,这导致了基因编辑过程中会发生不可预测的脱靶,由于常用的Cas9、Cas12a和Cas13a大小接近4kb,而递送系统AAV病毒的包装上限约为4.7kb,不利于CRISPR-Cas系统的递送。优化改造Cas蛋白、寻找更小的Cas蛋白、发掘更优的新型系统等成为近年来CRISPR-Cas系统研究的重点方向。
通过合理设计并定向进化开发高保真的Cas9变体,得到高保真蛋白enAsCas12aHF1。新开发的两种Cas9变体SpG和SpRY,不需要特定的PAM来结合和切割DNA序列。
我国辉大基因开发了Cas13X.1(又称Cas13e.1,775氨基酸)和Cas13Y(又称Cas13f,790氨基酸),并于2022年获得美国专利局授予专利,成为我国首个自主研发的、在美国获得专利授权的CRISPR-Cas13基因编辑工具,打破了欧美在基因编辑工具领域的专利垄断。
表2 部分工程化改造的Cas蛋白变体
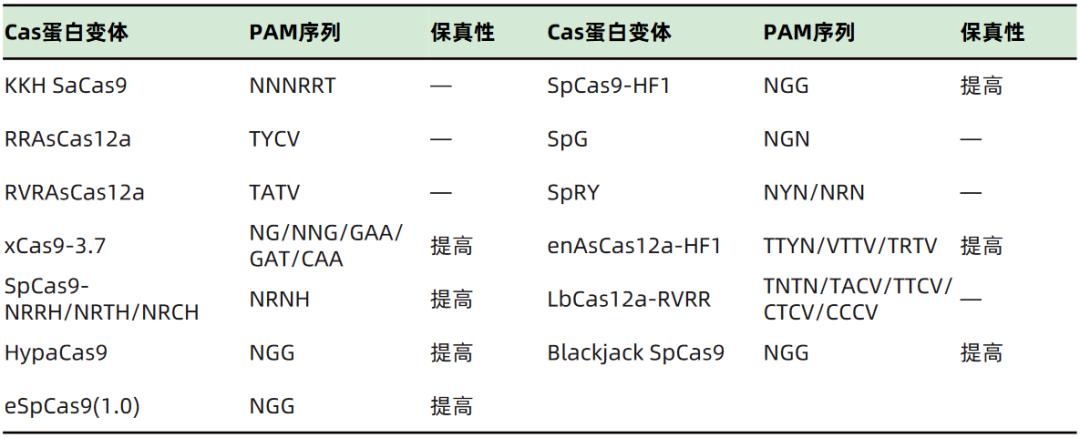
发掘新型Cas蛋白,扩大CRISPR-Cas系统的应用范围。Cas7-11是通过大数据挖掘找到的一类独特的III-E型CRISPR-Cas系统,与传统的多组分效应蛋白复合物不同,该系统具有单一的效应蛋白Cas7-11(由传统的Cas11和Cas7融合而成),具有crRNA加工和序列特异性RNA切割活性,为哺乳动物细胞提供了一种新的RNA敲除工具,其脱靶效应比当前的RNA敲除技术更低。
03 CTX001:首款CRISPR基因编辑疗法上市申请获得受理
2023年1月26日,EMA接受Vertex和CRISPR递交的exagamglogene autotemcel(exa-cel,研发代号CTX001)上市申请,该疗法通过CRISPR/Cas9编辑患者的
CD34+造血干细胞,敲除BCL11A基因红系增强子,以限制性地抑制血红细胞中的BCL11A蛋白表达,从而提升胚胎血红蛋白表达水平,具有一次性治愈潜力。
CTX001获得了FDA授予的再生医学疗法认定(RMAT)、快速通道资格,EMA授予的PRIME认定以及FDA和EMA授予的孤儿药认定。目前在美国已启动上市申请滚动递交,预计将于2023Q1完成。如果获批,CTX001将成为首款获批CRISPR基因编辑疗法。
图2 CTX-001的作用机制
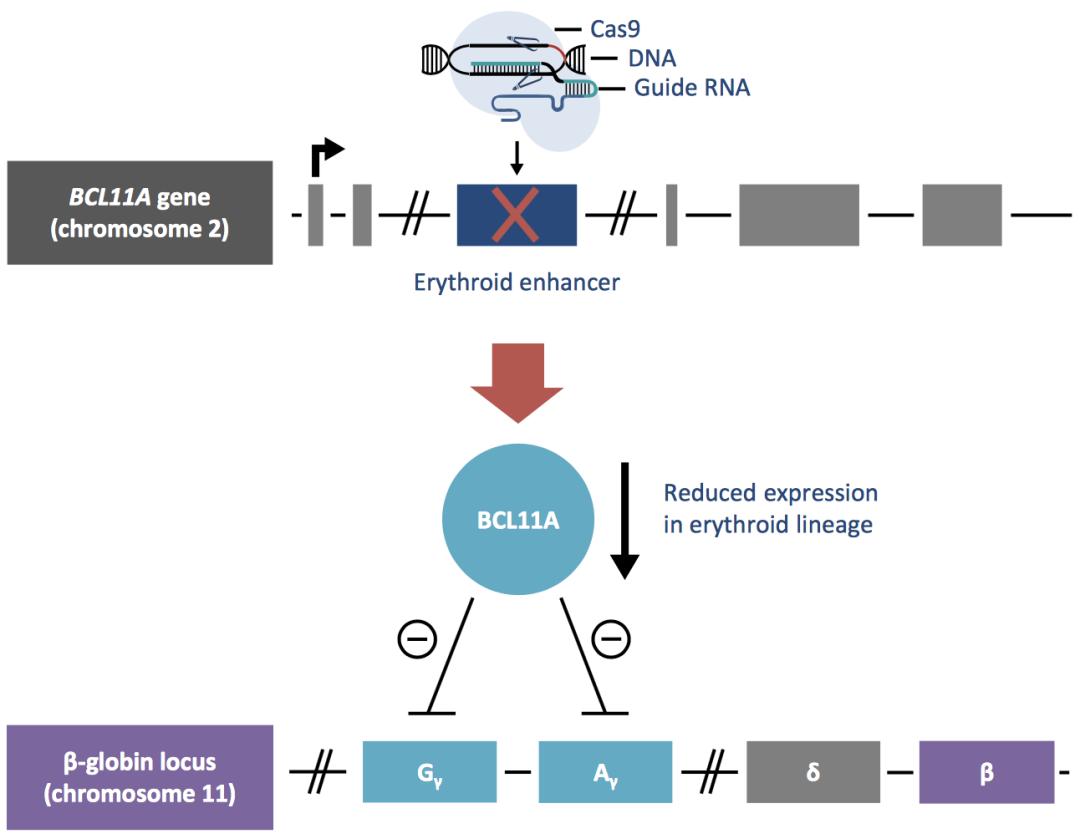
图3 CTX-001的治疗过程
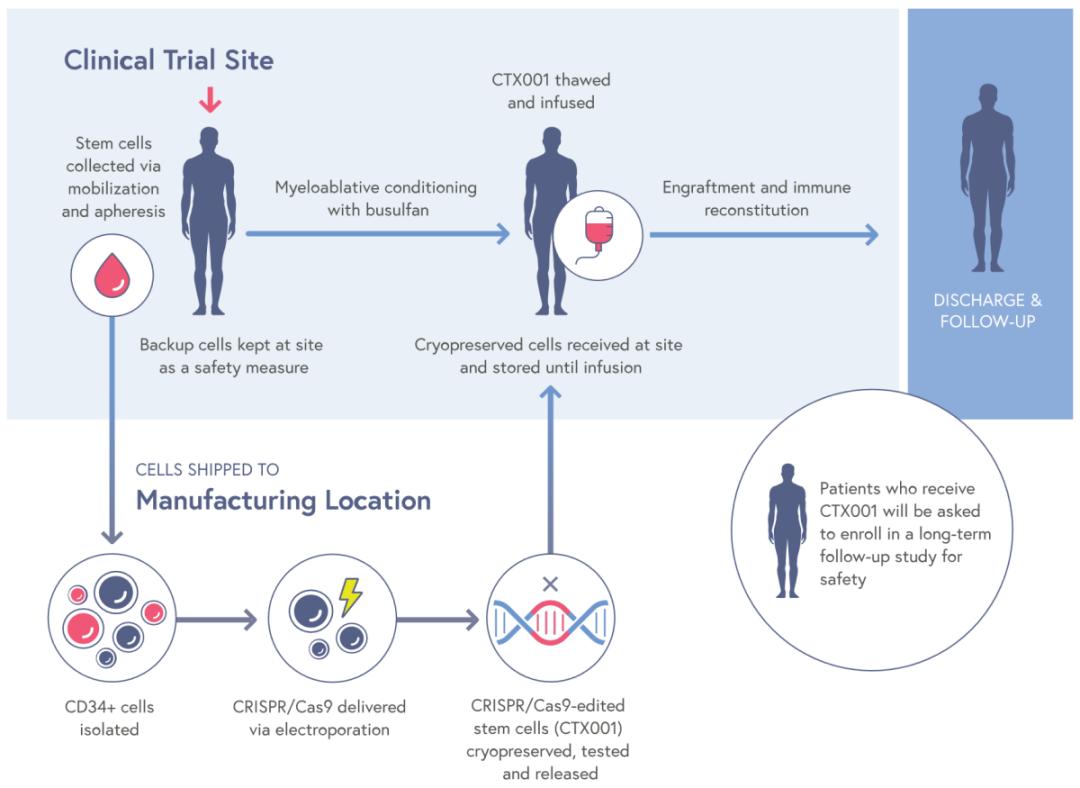
CRISPR和合作伙伴Vertex开展了关键性临床试验CLIMB SCD-121以评估CTX001在严重镰刀型贫血患者中的疗效,共招募了31例12-35岁的严重镰刀型贫血患者,主要终点为至少12个月未发生血管阻塞性危象(Vaso-Occlusive Crisis,VOC)的患者比例。截至2022年2月,中位随访时间为10.2(2.0,32.3)个月。临床试验结果显示,全部31例患者中均未发生任何VOC。血红蛋白中HbF平均占比在输注后提升至40%以上,并且能够长期维持。安全性方面,未发生CTX001相关的SAE。
图4 CLIMB SCD-121临床试验结果
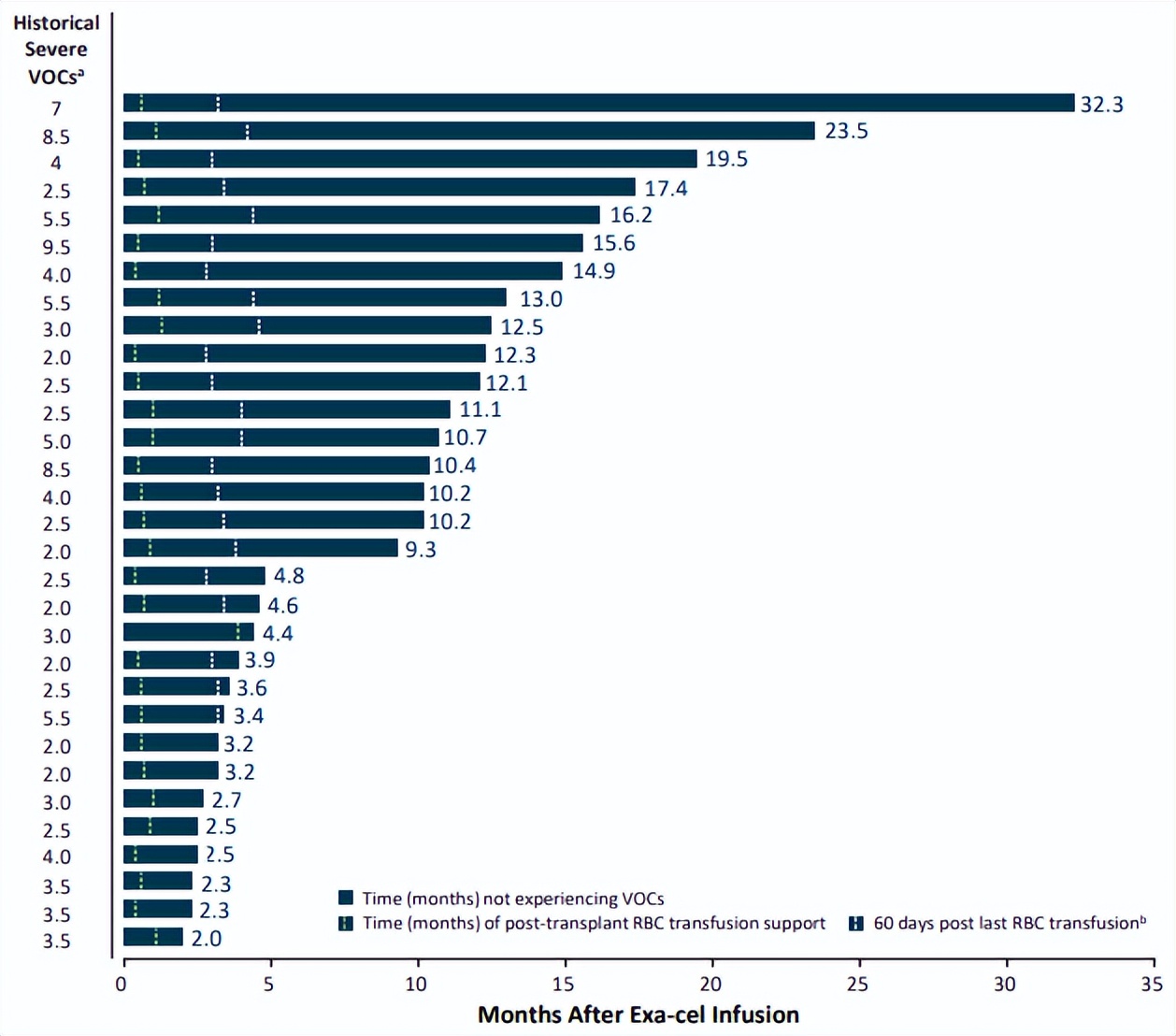
图5 CLIMB SCD-121患者Hb水平随访结果
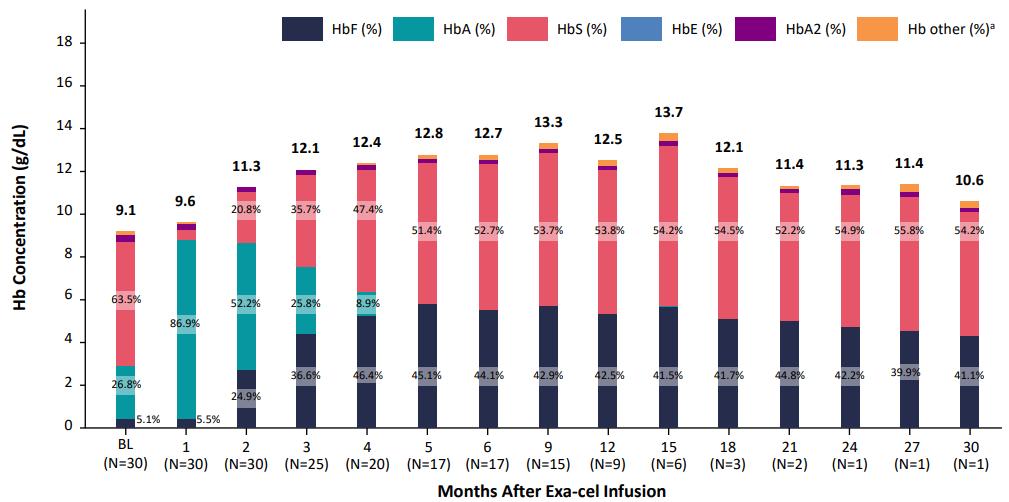
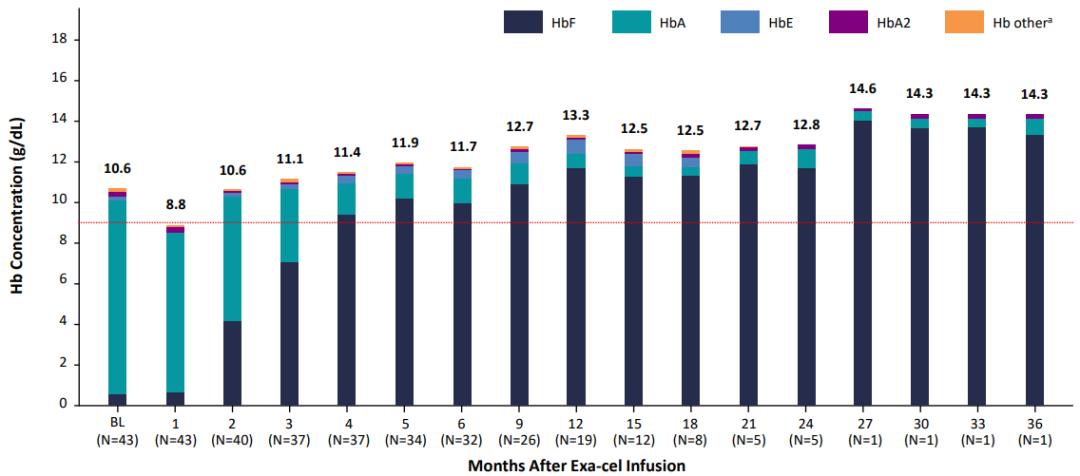
CRISPR和合作伙伴Vertex开展了关键性临床试验CLIMB THAL-111以评估CTX001在地中海贫血患者中的疗效,共招募了44例12-35岁的地中海贫血患者,主要终点为至少持续12个月达到Hb≥9g/dL且不需要红细胞输注的患者比例。截至2022年2月, 中位随访时间为11.9 (1.2, 37.2)。临床试验结果显示,44名地中海贫血患者中有42名停止输注红细胞(持续时间为0.8至36.2个月),两名患者尚未停止输血,但输血量分别减少了75%和89%。Hb平均水平在输注后维持在10 g/dL以上,HbF水平显著提升并且能够长期维持。安全性方面,2例患者发生CTX001相关的SAE,经过治疗后消退。
图6 CLIMB THAL-111临床试验结果
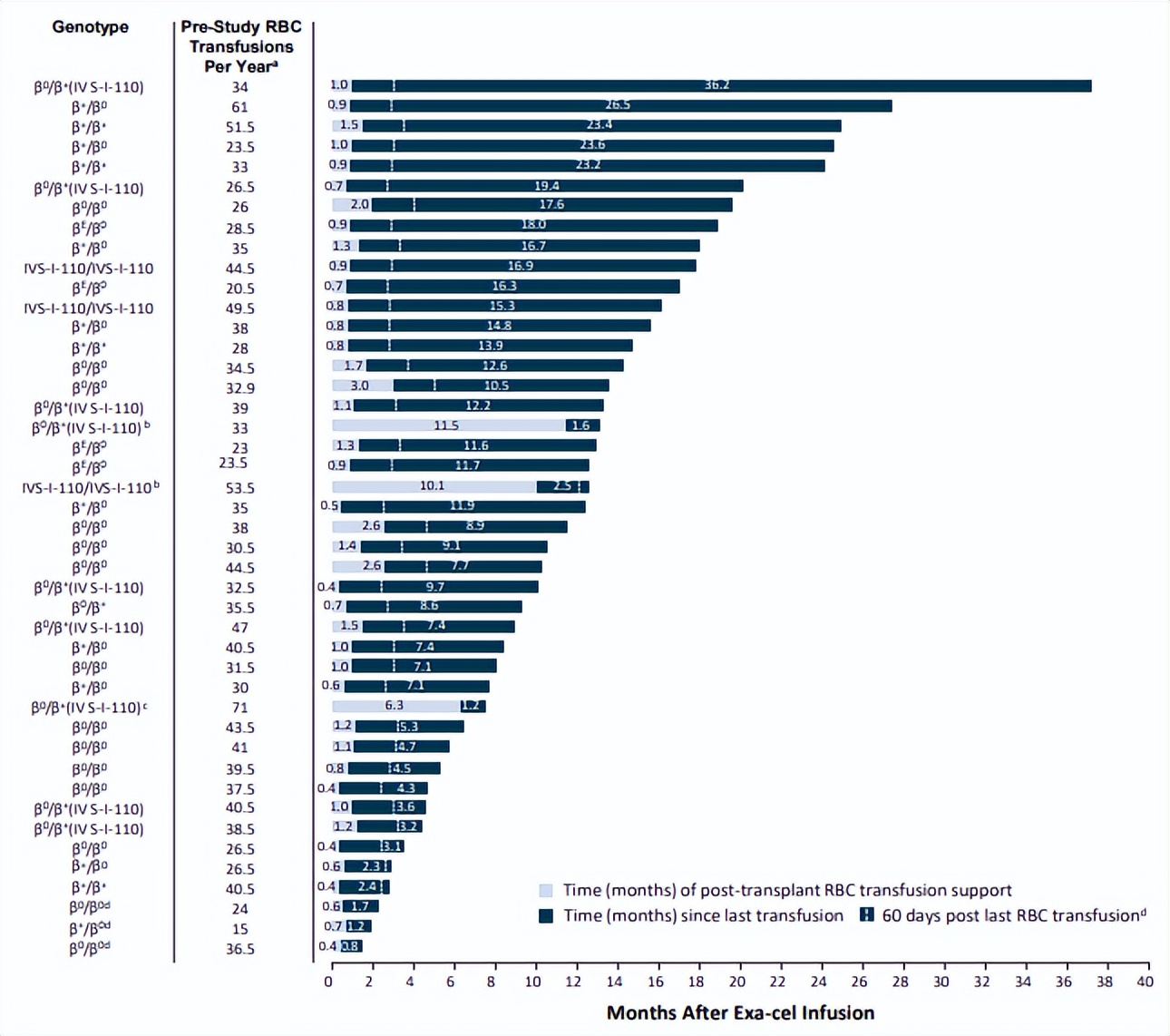
图7 CLIMB THAL-111患者Hb水平随访结果
END
药闻窗