辉瑞制药的Cibinqo(abrocitinib)是一种于2022年1月首次获得FDA批准,用于治疗中重度特应性皮炎的JAK*制剂抑**药物。此前获批用于治疗18岁及以上的成人,现在该药物的补充新药申请已获得FDA批准,用于12至<18岁的青少年。
最新批准的适应症具体为:用于治疗无法通过包括生物制剂在内的其他全身*药性**物得到充分控制,或者不建议使用这些疗法的青少年(12岁至<18岁)难治性、中度至重度特应性皮炎(AD)患者。
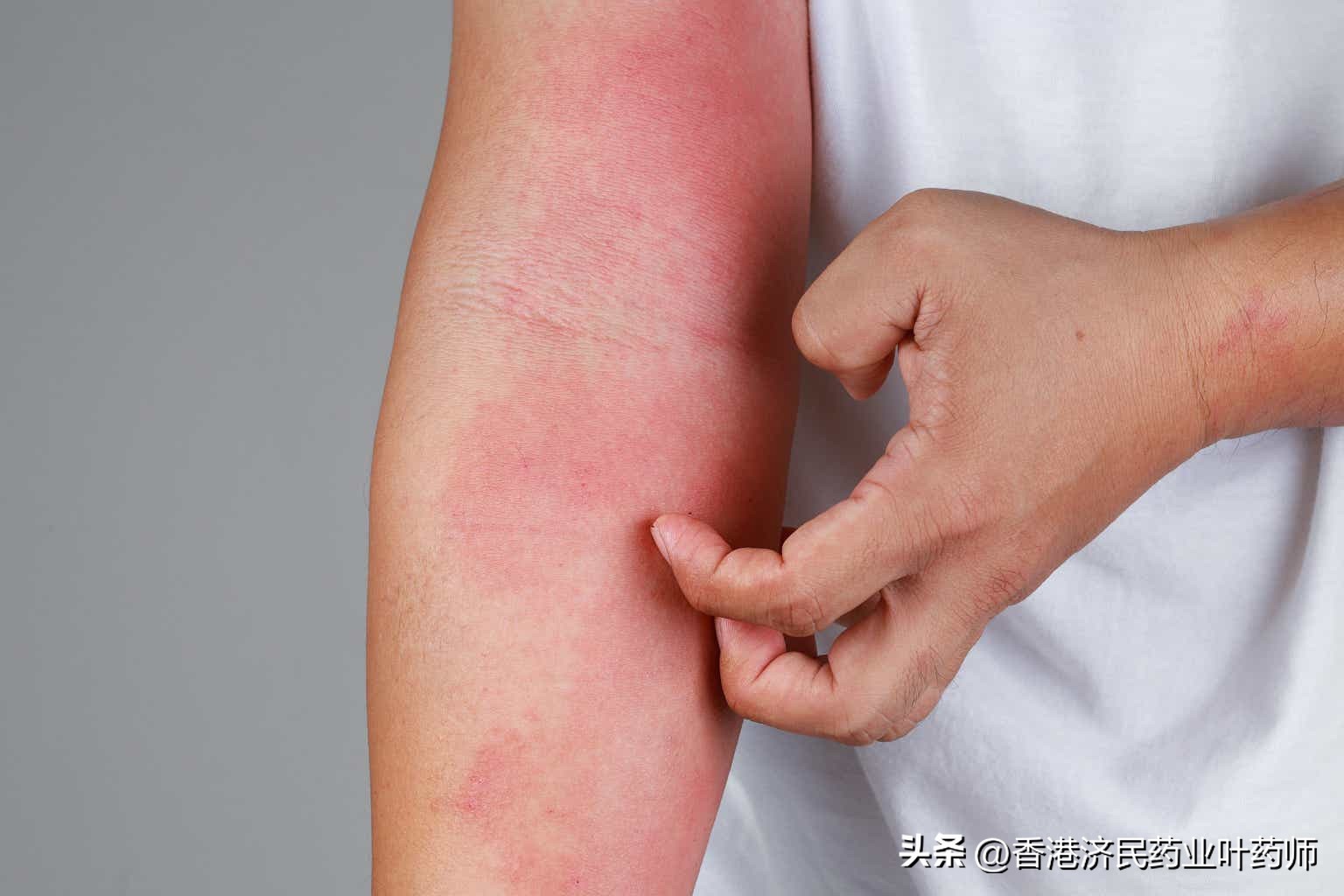
支持扩展用于青少年的临床数据
支持批准标签扩展的数据来自包括124名青少年患者在内的前期研究数据,以及3期JADETEEN研究(NCT03796676),该研究在285名12岁至18岁的中度至重度特应性皮炎患者中比较了口服Janus激酶1(JAK1)*制剂抑**abrocitinib与安慰剂的疗效和安全性。
患者被随机分配接受abrocitinib 100mg、200mg或安慰剂口服,每日一次,持续12周,同时接受背景局部治疗。
共同主要终点是在第12周时研究者的总体评估(IGA)为清除(0)或几乎清除(1)并且与初始相比减少≥2分的患者比例;第12周湿疹面积和严重程度指数(EASI75)评分较初始变化≥75%的患者比例。
来自JADE TEEN的结果显示,分别有39%和46%的患者使用abrocitinib 100mg和200mg治疗达到IGA 0或1应答,而接受安慰剂治疗的患者中这一比例为24%。在第12周,分别有71%和64%的患者接受了100mg和200mg abrocitinib治疗达到了EASI-75应答,而接受安慰剂治疗的患者中这一比例为41%。
此外,与安慰剂相比,接受100mg和200mg abrocitinib治疗的患者在第2周的峰值瘙痒数值评定量表(PP-NRS)评分较初始至少降低4分,分别为13%和25%对比8%。
安全性方面,abrocitinib在青少年中的安全性与之前在成人人群中的研究一致。Cibinqo带有关于与JAK*制剂抑**相关的严重感染、恶性肿瘤、主要不良心血管事件、血栓形成和死亡的可能性的黑框警告。不推荐该治疗与其他JAK*制剂抑**、生物免疫调节剂或其他免疫*制剂抑**联合使用。
其他JAK*制剂抑**药物
Cibinqo是一种口服Janus激酶1(JAK1)*制剂抑**,用于调节参与特应性皮炎病理生理学的多种细胞因子,包括白细胞介素IL-4、IL-13、IL-31、IL-22和胸腺基质淋巴细胞生成素(TSLP)。
其他一些JAK*制剂抑**药物有:辉瑞的药物Xeljanz、艾伯维的Rinvoq和礼来的Olumiant。
其中,只有艾伯维的Rinvoq被批准用于治疗成人和青少年的中度至重度特应性皮炎。事实上,Rinvoq被批准用于治疗五种适应症,类风湿性关节炎、银屑病关节炎、强直性脊柱炎、特应性皮炎和溃疡性结肠炎。
虽然礼来公司的Olumiant被批准用于某些患者的类风湿性关节炎和COVID-19,但未获准用于治疗特应性皮炎。辉瑞的Xeljanz被批准用于某些患者的RA、银屑病关节炎、强直性脊柱炎和溃疡性结肠炎,同样的也未获准用于治疗特应性皮炎。
从Cibinqo(abrocitinib)的相关研究来看,其对皮肤症状清除、瘙痒、疾病范围和严重程度有所改善,随着其标签扩展,为中重度特应性皮炎的青少年患者提供了一种新全身性口服选择。
参考来源:‘FDA Approves Pfizer's Supplemental New Drug Application for Cibinqo® (abrocitinib)’,新闻发布。Pfizer Inc.;2023年2月10日发布。
注:本文旨在介绍医药健康研究,不作任何用药依据,具体用药指引,请咨询主治医师。