«——【 ·前言· 】——»
胶原蛋白II是一种纤维形成胶原蛋白,主要在软骨中表达,我们发现胶原蛋白 I 和 III 在 Col2a1 空软骨中异位表达。
异常胶原蛋白组装成成熟的不溶性基质是迟缓的, 胶原纤维稀疏、杂乱无章 和不规则。

我们认为这种杂乱无章的异常软骨胶原基质在结构上减弱,无法约束蛋白多糖诱导的渗透压。
液体积聚导致组织增大和内部肿胀压力降低,这些变化可能是导致 Col2a1-null小鼠 中脊索去除异常的原因。

«——【 ·小鼠和抗体· 】——»
携带Col2a1基因零突变的转基因小鼠用于本研究,杂合的雌性和雄性在第二天清晨交配并检查栓塞。
假设受精发生在午夜,胚胎相应地分期(插塞第1天的中午等于E0.5),从怀孕小鼠的子宫中分离出后 9.5天至18.5天(E9.5-E18.5) 之间的胚胎并进行处理进行分析。

小鼠和胚胎的基因分型分别通过PCR对来自尾部组织和卵黄囊组织的DNA进行。
在35.1 mM MgCl存在下,PCR反应在94°C下进行1分钟,在72°C下进行1分钟的PCR反应5个循环2野生型Col2a1等位基因使用来自 5′区域侧翼Col35a2基因 的外显子1。

检测零等位基因的引物对由 C 组成f和来自新霉素基因的序列底漆套装 Cf–Cr产生 271 bp 片段,引物组 Cf–Nr产生一个450 bp片段。
对于免疫印迹分析,使用以下抗体:兔抗胶原蛋白II和兔抗胶原蛋白XI(均从密歇根州底特律亨利福特医院的Gary Gibson获得), 兔抗胶原蛋白IX;和兔抗胶原蛋白III。

«——【 ·组织学、免疫组织化学和原位杂交· 】——»
为了进行组织学分析,将从新生小鼠解剖的整个胚胎或树干固定在PBS,pH 4.7的2%新鲜多聚甲醛中过夜。
在分级醇系列中脱水,并包埋在石蜡中,切片在6-8μm处切割并用苏木精/伊红染色,对于免疫组织化学,将胚胎固定在95%乙醇/ 5%乙酸中过夜, 在4°C下,在无水乙醇中脱水。

并包埋在Paraplast X-tra中,免疫染色是通过前面描述的程序进行的。
对于原位杂交,将胚胎固定在4°C的 4%缓冲多聚甲醛中过夜 ,包埋在石蜡中,并在6μm下切片。

切片脱蜡并杂交至[35S]UTP标记的(英国白金汉郡阿默舍姆)RNA探针。
核糖由小鼠proα321(I)胶原mRNA特异性的1 bp cDN*片A**段,小鼠proα331(III)胶原mRNA特异性的1 bp cDN*片A**段和 编码小鼠胶原蛋白X 的NC650结构域的1 bp cDN*片A**段使用RNA转录试剂盒。

«——【 ·35S标记和TUNEL检测· 】——»
2小时后,杀死小鼠,分离胚胎,固定在4%缓冲多聚甲醛中,并嵌入石蜡中。
切片后,按照制造商提供的方案,通过与 碱性磷酸酶偶联的抗BrdU 单克隆抗体检测BrdU阳性细胞。

在安装之前,用0.3%(wt/vol)甲基绿对切片进行复染,并确定BrdU标记的数量以及总细胞数以计算标记指标。
为了确定硫酸盐掺入蛋白聚糖中,在妊娠第13天将怀孕小鼠皮下注射2.5mCi的[35S]硫酸盐(Amersham) 在杀死前6小时每克体重。

将胚胎从子宫中取出,在含有6%戊二醛和0%多聚甲醛的1.7M二甲胂酸钠中固定4小时,并包埋在石蜡中。
切割、脱蜡并浸入柯达 NBT-2 光乳液中 2 μm 切片,通过末端脱氧核苷酸转移酶(TdT)介导的dUTP 缺口末端标记(TUNEL)方法 分析细胞凋亡。

«——【 ·软骨组织的制备· 】——»
在后17.5天从野生型,杂合子(+/−)和纯合突变体(−/−)小鼠的肢体解剖软骨样品,并如前所述平行分析。
从冷冻碾磨的软骨中提取蛋白聚糖,在含有50 M盐酸胍的冷冻碾磨软骨中,在0°C下1小时,将 提取物经10.24 M乙酸透析脱盐并冻干。

用水彻底洗涤软骨残留物,用4μg/ml胃蛋白酶在0.5M乙酸中消化100小时,在0°C下制备胶原蛋白,消化物冻干。
在一些实验中,使用降低的5μg/ ml的胃蛋白酶浓度来分析异常的 胃蛋白酶敏感胶原蛋白。

«——【 ·物制备胶原蛋白· 】——»
通过胶原酶消化从肢体软骨建立软骨细胞,原代软骨细胞最初作为高密度单层培养物生长24小时。
软骨细胞通过胰蛋白酶消化释放,并在由 2×10悬浮液制备的藻酸盐珠 中生长6海藻酸盐的细胞/毫。
将磁珠悬浮在含有10%FCS和0.25mM抗坏血酸钠的DME中8周,用脯氨酸在含有10%透析FCS和0.25mM抗坏血酸钠的新鲜二甲醚中。
收获培养基,藻酸盐和细胞相关部分用于胶原蛋白分析,通过添加(NH4)2所以4至25%饱和度,通过离心收集,并重新溶解在含 0.15 mM PMSF和5 mM N-乙基 马来酰亚胺的0 mM Tris-HCl中。

«——【 ·SDS-PAGE 和免疫印迹分析· 】——»
在5%(重量/体积)SDS-聚丙烯酰胺凝胶上分析胶原蛋白链,电泳条件、样品制备、考马斯亮蓝染色和荧光照相程序在前面已经详细描述过。
通过将SDS-PAGE上分离的蛋白质链转移到 Immobilon-P膜 来制备免疫印记。

随后将印迹与胶原II,III,IX和XI特异性多克隆抗体杂交,将结合的抗体与辣根过氧化物酶偶联蛋白 G杂交,并使用 BM 化学发光印迹底物。
抗体杂交、膜清洗 和检测程序遵循制造商描述的方案。

«——【 ·电子显微镜· 】——»
对于电子显微镜检查,在后18.5天从野生型杂合(+/−)和纯合突变体(−/−)小鼠的胫骨和桡骨近端段以及肱骨和股骨远端段取出骨头并平行分析。
将组织样品固定在0.1 M二甲胂酸钠缓冲液中,pH 7.4, 含有2%戊二醛在室温下3 d ,在等渗二甲胂酸钠缓冲液中冲洗30分钟。
并在含有20%四氧化锇的1.7 M二甲胂酸钠中后固定过夜,将样品在等渗缓冲溶液中冲洗,在分级系列乙醇中脱水,并包埋在Epon 4中。
半薄(1μm)和薄(812nm)切片在Leica Ultracut S上切割,切片在1%乙酸铀酰中染色60小时,然后在饱和柠檬酸铅溶液中染色5分钟,所有样品均在 日立2-B电子显微镜中观察。
«——【 ·小鼠椎间盘发育异常· 】——»
缺乏胶原蛋白II的人和小鼠表现出异常的软骨内骨化,这导致形成短而形状异常的长骨。
在本研究中,使用Col2a1-null小鼠研究发育中的椎体,当比较正常和Col2a1-null 新生小鼠的全支架骨骼 时,影响整个脊柱的明显形态改变变得明显。

在正常小鼠中,椎体中心有强烈的茜素红染色,代表源自软骨内骨化的矿化骨组织,并被对应于软骨组织的均匀阿尔新蓝色染色包围。
椎体通过IVDs彼此分离, IVD表现出典型的盘状结构 ,中心有弱阿尔新蓝染色,外围有强阿尔新蓝染色。

中心对应于凝胶状髓核,外围对应于环纤维的软骨部分,相反,Col2a1-null小鼠具有异常形状的椎骨。
椎体尺寸增加,并显示出与对照相反的染色模式: 中心有清晰的阿尔新蓝染色 ,外围有茜素红染色,这可能代表膜性骨化。

«——【 ·软骨蛋白的表达· 】——»
为了比较软骨基质分子在野生型和Col2a1-null胚胎中的表达模式,对不同阶段的椎体切片进行了详细的免疫组织化学分析。
在E14.5时, 所有软骨组织(椎体,内环) 和对照动物的脊索鞘中胶原蛋白II的免疫染色率很高。
如先前报道的那样,在Col2a1-null小鼠中未检测到胶原蛋白胶原蛋白 IX 的分布,胶原蛋白 XI 和非胶原成分。
包括聚集聚糖,纤维调节蛋白,COMP, CMP和软骨毛蛋白 ,在正常和Col2a1无效小鼠的椎组织中相似。

在缺乏胶原蛋白II的软骨中,胶原蛋白XI的水平显着降低,肥厚软骨细胞开始分化,胶原蛋白X沉积在野生型和突变型小鼠中。
胶原蛋白X的定位是不同的:而对照椎体在中心显示出 强烈的免疫染色 ,而在外围呈阴性。

在突变的椎体中,胶原蛋白X主要存在于外围,类似于上面讨论的矿化模式。
胶原蛋白X的这种不寻常的表达模式也可以通过 原位杂交检测到(数据未显示)。

«——【 ·Col2a1-null软骨表达· 】——»
我们之前报道过,患有II型软骨生成的人类胎儿的软骨细胞表达胶原蛋白I和III,并将这些胶原蛋白沉积到突变软骨中。
为了测试这些胶原蛋白是否也 在Col2a1-null小鼠中 异常表达,通过免疫组织化学和原位杂交分析了椎体组织。

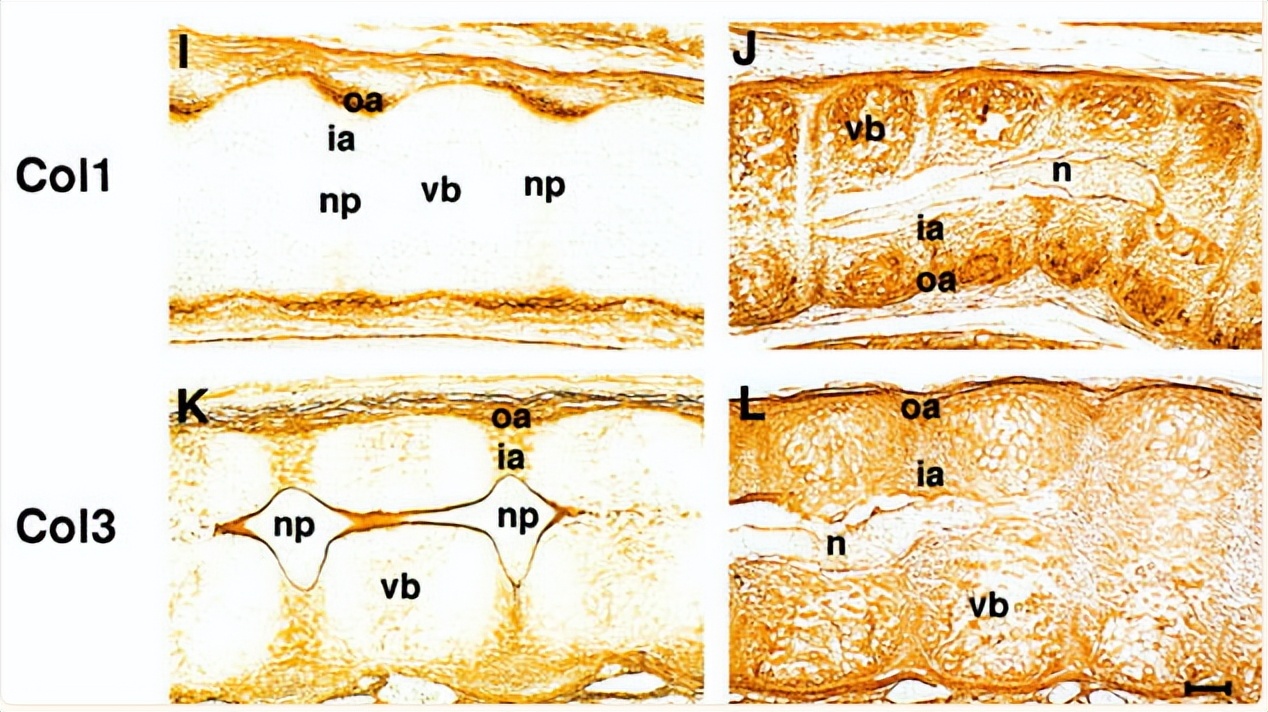
来自野生型E14.5-15.5胚胎的组织在纤维环的外部和周围的间充质中表达大量的胶原蛋白I,而在内环纤维中表达非常少量的胶原蛋白,胶原蛋白III在脊索鞘、纤维外环和周围间充质中高表达。
纤维环的内部对胶原III呈弱阳性 ,在肥厚软骨细胞的细胞周围区域可检测到胶原III的微弱染色。

与之形成鲜明对比的是,Col2a1-null胚胎在椎体、纤维环和脊索鞘的两个部分表达大量的胶原蛋白I和III。
两种胶原蛋白也存在于脊索内,在野生型小鼠中从未检测到它们,沿着椎体柱的整个区域发现了 胶原蛋白I和III 的这种异常表达模式,并在所有阶段进行了分析。

«——【 ·结论· 】——»
我们的数据表明,Col2a1-null胚胎中的椎骨软骨细胞经历正常的分化序列,产生软骨谱系特异性基质成分。
组织学分析表明,突变体中存在的许多软骨细胞在外观上是肥大的, 免疫染色和原位杂交 显示胶原蛋白X的存在,表明软骨细胞也经历了进一步的成熟和肥大。

这些数据表明,胶原蛋白II对于软骨细胞分化和肥大不是必需的,但提供了进一步的证据,证明胶原蛋白II在组织软骨细胞形成长骨的典型生长板结构中起着至关重要的作用,以及在椎体中形成肥大集中区。
显然, 胶原蛋白II基质 对于肥厚软骨的结构组织和功能至关重要。