作者:不二
- 2020.10.09-2020.10.18期间药审中心受理总量为329个,涉及品种209个。
- 17个1类新药申请获CDE受理。
- 新增45个按仿制药质量和疗效一致性评价品种申报的受理号。
1. 在审评阶段
根据健数科技中国药品审评数据,10月9号-10月18号期间共209个(按品种计,下同)药品获CDE承办,包括化药159个,生物制品42个,以及中药9个。
近期CDE承办的申报临床新药,共计17个品种,其中化药10个,生物制品5个,中药2个。另有30个品种提交一致性评价。
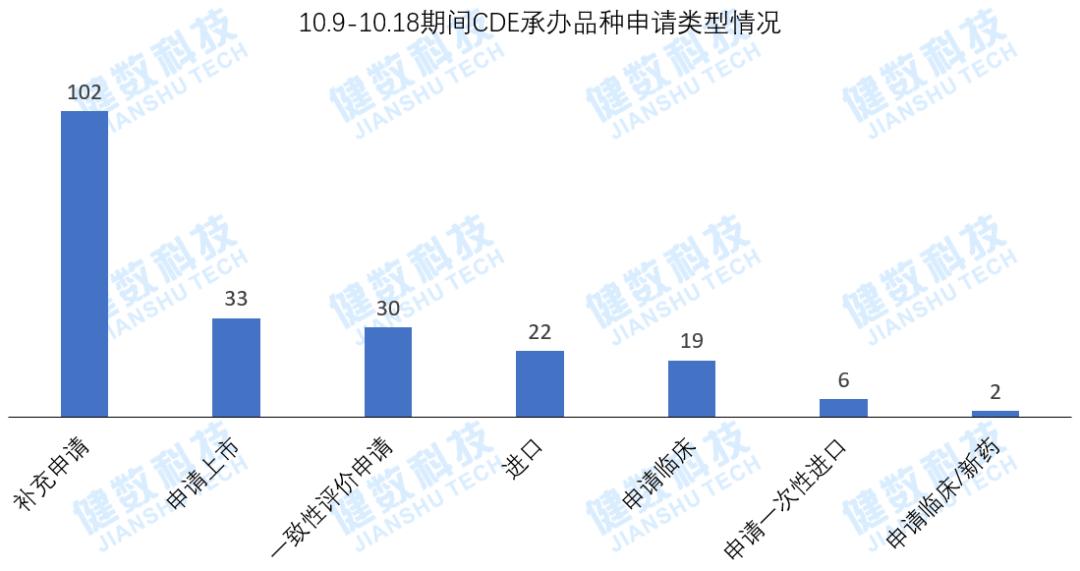
数据来源:健数科技中国药品审评数据库 (备注:按品种统计)
近期受理国产1类新药共计17个受理号,涉及14个品种13家企业。
下表为2020.10.09-2020.10.18新承办的1类新药药物情况。
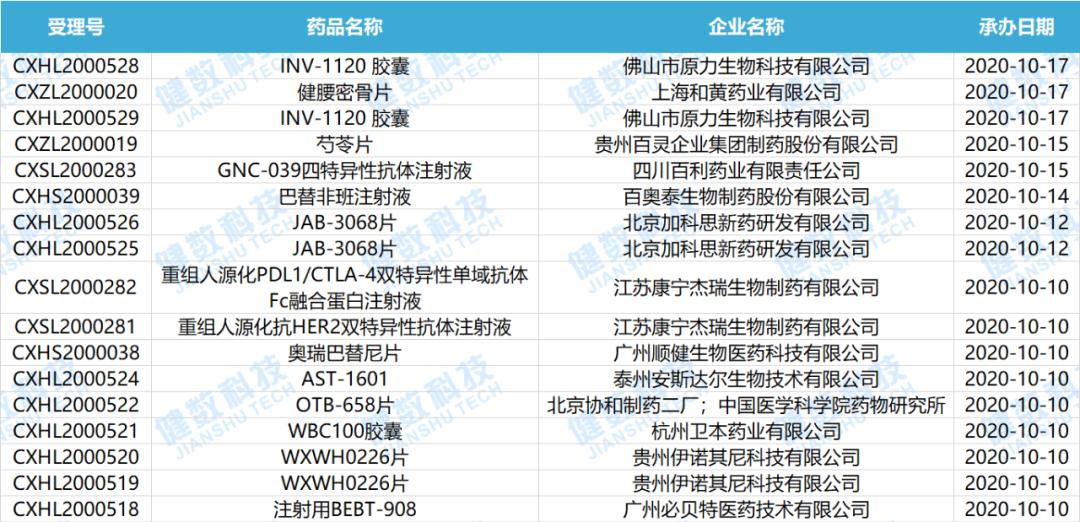
数据来源:健数科技中国药品审评数据库
GNC-039四特异性抗体注射液: 本品为一款四特异性抗体注射液,为1类新药。今年6月,百利药业的另一款1类新药 GNC-038四特异性抗体注射液在我国获批临床 ,适应症为拟用于复发或难治性非霍奇金淋巴瘤(R/R NHL)、复发或难治性急性淋巴细胞白血病(R/R ALL)、难治性或转移性实体瘤的治疗。
巴替非班注射液: 百奥泰巴替非班注射液申报上市。百奥泰1类新药巴替非班注射液 用于PCI围术期抗血栓 的上市申请获CDE受理。巴替非班BAT2094是一种人工合成的血小板糖蛋白IIb/IIIa(即GPIIb/IIIa)受体拮抗剂,可特异性地结合GPIIb/IIIa受体,能通过阻止纤维蛋白原、VonWillebrand因子和其它粘附配体与GPIIb/IIIa的结合来抑制血小板聚集。 用于PCI围术期抗血栓,其临床剂型为静脉给药的注射液。 本品最早于2006年在我国获批临床。
重组人源化抗HER2双特异性抗体注射液(KN026) 和 重组人源化PDL1/CTLA-4双特异性单域抗体Fc融合蛋白注射液(KN046) 是康宁杰瑞自主研发的双特异性抗体创新药,两种药物在单药临床试验中均显示出良好的安全性、耐受性和抗肿瘤疗效。
KN046 ,是 全球首创重组人源化PD-L1/CTLA-4双特异性抗体 ,其 创新设计包括: 采用安全性显著提高的CTLA-4单域抗体;与PD-L1抗体融合组成双特异性抗体;可靶向富集于PD-L1高表达的肿瘤微环境及清除Treg。KN046的临床前和临床试验结果表明可显著减少对人体外周系统可能产生的毒副作用,有望成为突破性肿瘤免疫特效药。在我国,本品的临床试验最快处于2期, 适应症有非小细胞肺癌、晚期不可切除或转移性食管鳞癌、三阴乳腺癌等;
KN026 ,是一种 重组人源化抗HER2双特异性抗体 ,可同时结合HER2的D2和D4两个非重叠表位,相当于同时具备了曲妥珠单抗和帕妥珠单抗的功能。该双抗是基于康宁杰瑞具有自主知识产权的Fc异二聚体平台技术(CRIB)开发。CRIB平台指电荷排斥诱导双特异性(Charge Repulsion Improved Bispecific)平台,可减少同源二聚体的形成,提高产品质量稳定性和收率。
2. 在审批阶段
近期共有21个品种(26个受理号)进入审批阶段。
2020.10.09-2020.10.18在审批阶段药物情况

数据来源:健数科技中国药品审评数据库
贝克生物恩曲他滨替诺福韦片即将获批。 恩曲他滨替诺福韦片原研厂家为吉利德,最早在2004年8月被FDA批准上市(商品名:Truvada ),联合其他抗逆转录病毒药物治疗HIV-1感染,2012年被FDA批准用于预防性传播导致的成人获得性HIV-1感染,是 全球首个HIV预防药物 ,即所谓的 HIV 暴露前预防性治疗 (PrEP) 药物。2019年Truvada全球销售额超过28亿美元。目前国内市场恩曲他滨替诺福韦片获批企业仅有吉利德和正大天晴。
奥赛康注射用右雷佐生即将获批上市。 奥赛康注射用右雷佐生3类仿制上市申请进入“在审批”阶段,有望近期获批上市,成为该品种 首家通过 一致性评价的产品。 注射用右雷佐生 临床上主要用于化疗引起的心*毒脏**性,国内目前只有奥赛康一家企业生产销售该药。
豪森药业沙格列汀片即将获批。 豪森4类仿制药沙格列汀片上市申请已变更为"在审批"状态,预计本月获批上市,成为继奥赛康、正大天晴后该品种第3家获批的仿制药。沙格列汀是一种高效的二肽基肽酶-4(DPP-4)*制剂抑**,用于治疗成人2型糖尿病。原研产品(Onglyza)由百时美施贵宝研发,后被阿斯利康收购,于2011年5月获批进入中国市场,商品名:安立泽。2019年,阿斯利康沙格列汀片全球销售额为5.27亿美元。
丽珠集团注射用丹曲林钠即将获批上市。 丽珠制药厂3类仿制药注射用丹曲林钠进入行政审批阶段,即将获批上市。丹曲林钠是一种突触后肌肉松弛剂,可减轻骨骼肌的收缩,为罕见病恶性高热的有效治疗药物,在美国、欧盟、日本等多个国家和地区均有上市,多为胶囊和注射剂。目前国内仅有2家企业持有丹曲林钠胶囊生产批文,暂无注射用丹曲林钠获批上市。
3. 制证完毕-待发批件
近期共计28个品种(涉及受理号40个)制证完毕-待发批件,有7个品种通过一致性评价。下表是制证完毕的药物情况。
2020.10.09-2020.10.18制证完毕药物情况
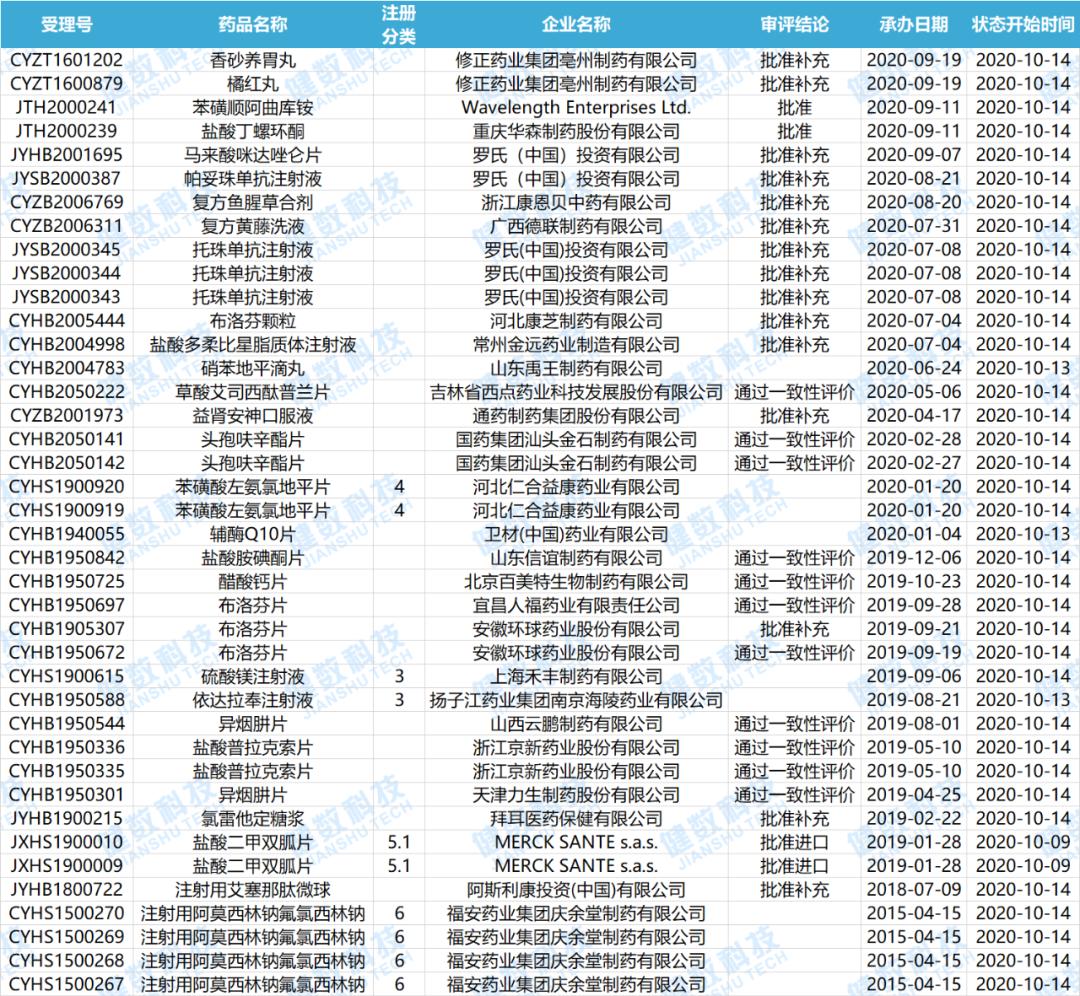
数据来源:健数科技中国药品审评数据库
百美特生物醋酸钙片首家通过一致性评价。 百美特生物醋酸钙片获CDE批准通过一致性评价。醋酸钙片是一种磷结合剂,主要用于预防和治疗终末期肾病高磷血症。国内获批生产销售醋酸钙片的厂家有邦宇制药、赛立克药业、邦宇制药等6家,此前尚未有企业通过一致性评价。
4. 已发件
近期共计38个品种(涉及受理号54个)已发件,其中有14个品种视同通过一致性评价。下表是已 发件 的药物情况。
2020.10.09-2020.10.18已发件药物情况
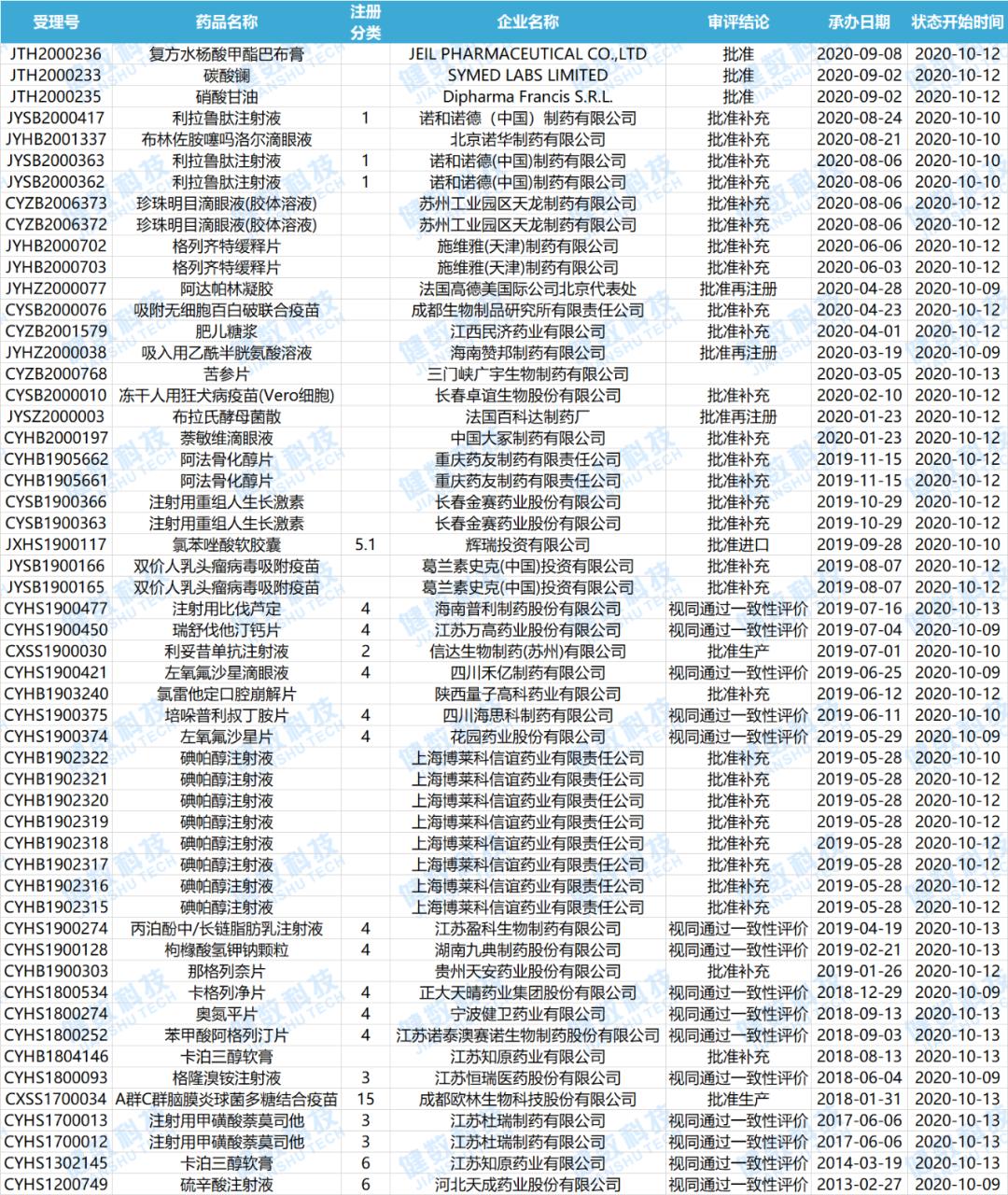
数据来源:健数科技中国药品审评数据库
5. 一致性评价申请
近期有30个品种提交一致性评价申请。
2020.10.09-2020.10.18药审中心一致性评价承办情况
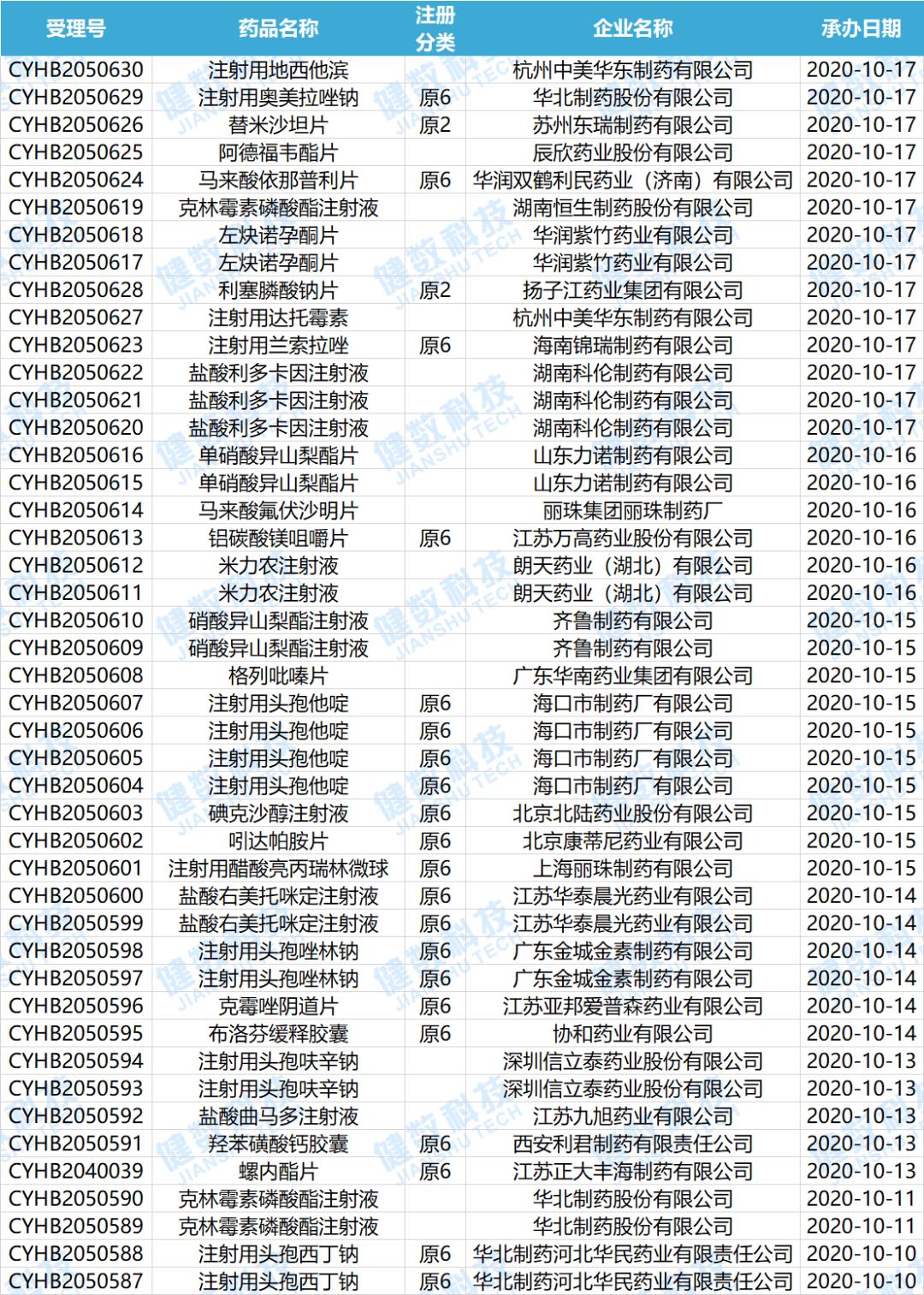
数据来源:健数科技中国药品审评数据库
往 期 精 彩
CDE药审新动态!豪森 1.1 类乙肝新药申报上市
国庆药闻 | 诺贝尔奖持续公布,NEJM呼吁反对的特朗普连任
辉瑞最新研发进展,有望2025年底推出25种新药
【声明】本文为原创文章,首发于微信公众号:健数科技(ID:drugeyes),如需转载请联系授权