
罗氏控股日本药企中外制药近日宣布,日本卫生劳动福利部(MHLW)已批准Tecentriq一个新的适应症:联合化疗(卡铂+依托泊苷)一线治疗广泛期小细胞肺癌(ES-SCLC)成人患者。此次批准,使Tecentriq成为日本批准治疗侵袭性和难治性ES-SCLC的第一种癌症免疫疗法。
小细胞肺癌是一种高侵袭性神经内分泌肿瘤,约占肺癌总数的15%~20%。因其具有恶性程度高、进展快、转移早、预后差等生物学特性,一直以来都是研究者关注的焦点。相关研究表明,若不治疗,小细胞肺癌的中位生存期短于4个月,而治疗后的5年生存率也仅6%。在各类肺癌中,小细胞肺癌的预后最差。
小细胞肺癌分期标准分为局限期和广泛期。广泛期,顾名思义就是它已经超出一侧胸腔外了,比如这个肿瘤已经转移到脑子,转移到骨头或锁骨上淋巴结、对侧的纵膈淋巴结。一般来说,广泛期小细胞肺癌基本都是晚期小细胞肺癌。
关于IMpower133研究
此次批准,基于III期临床研究IMpower133的结果,该研究是证实基于癌症免疫疗法的联合治疗方案一线治疗ES-SLCL能显著改善OS和PFS的第一项III期临床研究。
这是一项多中心、随机、双盲、安慰剂对照研究,在既往未接受化疗(化疗初治)的ES-SCLC成人患者中开展,评估了Tecentriq联合化疗(卡铂+依托泊苷)相对于单用化疗(卡铂+依托泊苷)的疗效和安全性。研究共入组403例患者,这些患者以1:1比例随机分配至两个治疗组,分别接受Tecentriq+化疗(A组)和化疗(B组)。在治疗诱导期,患者接受4个周期(21天/周期)的化疗治疗,之后接受Tecentriq或安慰剂维持治疗,直至疾病进展。
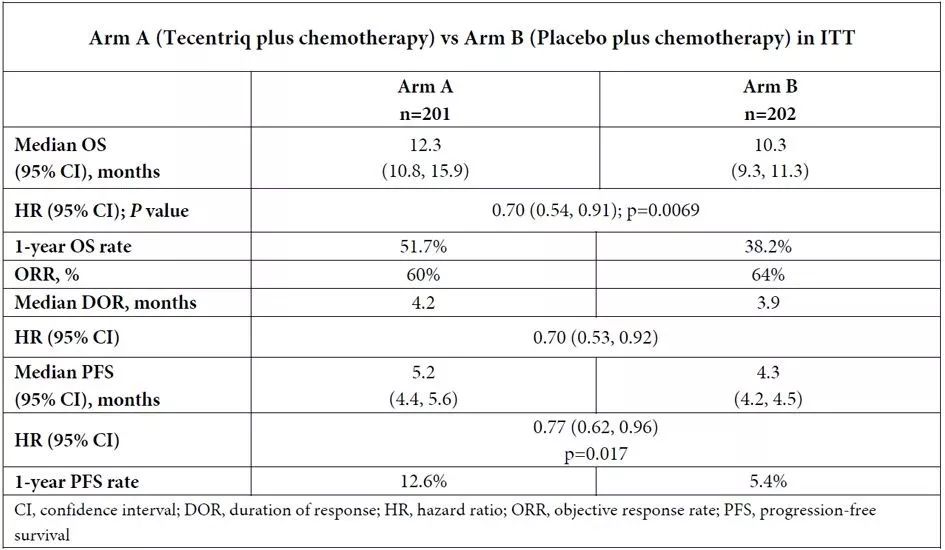
结果显示,在意向性治疗群体中,与B组相比,A组OS显著延长(中位OS:12.3个月 vs 10.3个月;HR=0.70,95%CI:0.54-0.91,p=0.0069)、一年OS生存率大幅提高(51.7% vs 38.2%)。此外,与B组相比,A组疾病进展或死亡风险显著降低23%(中位PFS:5.2个月 vs 4.3个月,HR=0.77,95%CI:0.62-0.96,p=0.017)、一年PFS率提高一倍(12.6% vs 5.4%)。研究中,Tecentriq与化疗联合用药的安全性与Tecentriq已知的安全性一致。
关于Tecentrip
Tecentrip(通用名Atezolizumab,阿特朱单抗,俗称T药)是全球首个获批上市的PD-L1*制剂抑**,也是免疫治疗史上第一个获批用于乳腺癌的免疫药物。
获得批准的适应症及时间:
- 2016年5月18日,获批用于局部晚期或转移性尿路上皮癌。
- 2016年8月18日,获批用于铂类药物治疗后进展以及接受EGFR或靶向药物治疗后疾病进展的转移性非小细胞肺癌。
- 2017年4月17日,获批用于初始治疗不适合顺铂化疗的局部晚期或转移性尿路上皮癌。
- 2019年3月8日,获批联合白蛋白紫杉醇用于一线治疗无法切除的局部晚期或转移性PD-L1阳性的三阴型乳腺癌。
遗憾的是,该药目前尚未在中国上市。
小细胞肺癌治疗盘点
小细胞肺癌的一线治疗方案一直以化疗为主,尽管小细胞肺癌对放化疗敏感,但是小细胞肺癌的倍增时间短,病情进展迅速,早期易出现转移,复发耐药的问题也不可避免的发生,并且以依托泊苷和铂类药物为基础的一线治疗方案多年未曾变化,因此改善小细胞肺癌的治疗一直是临床上需要不断挑战的问题。
目前,已有3款癌症免疫疗法获批治疗SCLC。
2017年美国国家综合癌症网络指南(NCCN)将Opdivo(俗称O药)联合伊匹木单抗作为复发小细胞肺癌三线治疗的推荐方案之一。2018年8月Opdivo获批作为小细胞肺癌的三线疗法,用于接受过铂类药物化疗以及至少接受过一种其他疗法后疾病进展的小细胞肺癌患者,这是近20年来首个获批的小细胞肺癌新药。
2019年3月18日,Tecentriq+卡铂+依托泊苷被FDA批准用于广泛期小细胞肺癌(ES - SCLC)的一线治疗。
2019年6月17日,美国国家食品药品监督管理总局(FDA)正式批准帕博利珠单抗单药用于转移性小细胞肺癌(SCLC)患者的治疗,这些患者接受铂类为基础化疗和至少另一种的治疗方案后仍出现疾病进展。
小细胞肺癌治疗手段有限,预后较差,但临床研究一直在不断地进行,各种新药也不断地涌现。我们期待着这些适应症能在我国获得批准,为小细胞肺癌患者带来更多治疗机会!

撰文&排版 :Cathy参考资料:1. 新浪医药新闻:《罗氏Tecentriq获日本批准 用于一线治疗广泛期SCLC!》2. 丁丁伴你行:《PD-1/PD-L1已上市免疫治疗药物盘点》3. GASTO小细胞肺癌专业委员会:《K药单药获批用于小细胞肺癌三线治疗 | FDA批准SCLC新增免疫治疗盘点》