原创 放疗青咖汇 放疗青咖汇 2022-08-14 19:24 发表于北京

食管癌和胃癌:将免疫治疗纳入当前实践
【翻译】张伟
【审校】杨从容 王 军
河北医科大学第四医院放疗科

【导言】
JCO新近发表的这篇综述主要回顾了在食管癌和胃癌领域,免疫检查点*制剂抑**的Ⅲ期随机临床试验的数据。如基于CheckMate 577试验的辅助纳武单抗治疗,如基于KEYNOTE 590、CheckMate 649和CheckMate 648结果的晚期患者应用一线化疗联合IO。从所有试验中可以看到,化疗仍在晚期患者的一线治疗中发挥着关键作用,即使在经过生物标志物筛选的患者群体中,也不建议一线治疗中不进行化疗,除非患者有医学上不适合细胞毒药物的因素。主要原因是在CheckMate 649和CheckMate 648研究中,单用伊匹木单抗和纳武单抗的队列在治疗早期死亡率增加。由于一线免疫联合化疗的标准化已建立,IO在后线治疗中的作用有所减弱。微卫星不稳定(微卫星高度不稳定)的肿瘤患者代表了对IO更敏感的独特人群,对所有患者进行MSI状态或MMR蛋白表达的检测成为非常重要的一个问题。
(王军)
【引言】
食管癌和胃癌是一种侵袭性肿瘤,显著影响了全球范围内的癌症相关死亡率。2018年,全球癌症相关死亡人数中胃食管癌占120多万,约占所有新确诊癌症的9%。大约50%的上消化道癌症确诊时即为晚期,并且有相当大比例的早期患者在治疗结束后出现复发。全身治疗在这些患者的管理中至关重要。联合化疗在治疗晚期上消化道肿瘤中具有明确作用,但即使采用最积极的治疗方案,总生存期(OS)也只有1年左右。最近,免疫治疗(IO)显示出对上消化道癌症良好的疗效,特别是在疾病早期或与化疗联合使用时。许多改变治疗方式的临床研究已使IO被批准用于治疗EGC。在此,我们将回顾这些关键性的研究,讨论IO生物标志物的选择,并强调该领域现存的一些问题。
【IO生物标志物】
人们一直在努力筛选可受益于IO的上消化道癌症患者。与预测其他癌症对IO的反应类似,PD-L1已成为上消化道肿瘤首选的生物标志物,但其并不完善。许多研究表明,EGC患者肿瘤和免疫细胞上较高的PD-L1表达可以预测肿瘤对IO的反应。然而,食管癌和胃癌中PD-L1的预测价值不如其他疾病那么高,其在上消化道肿瘤临床实践中的应用仍在发展当中。不同的研究使用了不同的评分系统、抗体和阳性阈值,因此很难将所有可用数据结合起来。展望未来,我们迫切需要一种统一且简化的PD-L1检测方法。
目前有两种公认的PD-L1表达评分系统。肿瘤细胞阳性比例评分(TPS)是部分或完全染色的肿瘤细胞相对于样本中所有肿瘤细胞的百分比。联合阳性分数(CPS)指PD-L1染色阳性的细胞数(包括肿瘤细胞、淋巴细胞和巨噬细胞)占样本中存活的肿瘤细胞总数中的百分比。食管腺癌(EGA)和食管鳞癌(ESCC)有不同的PD-L1表达模式。ESCC中PD-L1经常表达于肿瘤细胞,而EGA中PD-L1大多数表达于肿瘤微环境中的细胞上。这表明TPS可能是ESCC中有用的生物标志物,但并不适用于EGA。然而,为简化起见,可以将CPS分析应用于所有上消化道肿瘤,因为CPS评分结果也包含了TPS阳性的肿瘤。
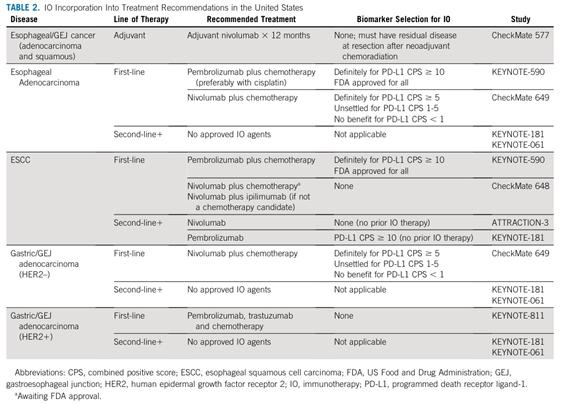
根据评估IO药物的不同,已用相应的检测方法来确定上消化道癌症中的PD-L1状态(表1)。幸运的是,不同抗体之间一致性的数据越来越多,但这些信息仍在不断涌现。更复杂的是,PD-L1阳性阈值在各个试验中并不一致。尽管使用了不同的抗体,帕博丽珠单抗的研究应用的是CPS≥1和10,而纳武单抗的研究使用的临界值为5。肿瘤的空间与时间异质性使检测PD-L1状态更加困难。最可靠的生物标志物可能需要在疾病进展过程中进行多次活检和重复检测。然而,目前尚不清楚如何解释不一致的结果(根据最低还是最高的CPS来决定治疗)。
所有这些问题都强调了上消化道癌症复杂的生物学特性,以及需要继续优化生物标志物PD-L1的检测和找出新的生物预测标志物。目前,DAKO 22C3是检测晚期上消化道癌症中PD-L1 CPS最常用的抗体。PD-L1 CPS治疗阈值取决于肿瘤组织学和治疗周期,后续将会讨论。PD-L1状态并不能指导早期疾病的治疗选择。
除了PD-L1外,上消化道肿瘤还应检测微卫星高度不稳定(MSI-H)和肿瘤突变负荷(TMB)。美国食品药物管理局(FDA)批准帕博丽珠单抗用于错配修复缺陷和/或高肿瘤突变负荷的患者。与其他疾病类似,MSI-H状态是上消化道肿瘤对IO反应的强预测生物标志物。因此,应对所有患者进行MSI状态或MMR蛋白表达的检测。
【IO治疗早期疾病】
多学科方法对于早期上消化道肿瘤达到最佳预后至关重要。食管癌和胃食管交界(GEJ)癌的患者通常采用术前新辅助放化疗。该方法在10年以上的长期生存率中有着13%的绝对优势(38% vs. 25%,P=0.004)。然而远处转移率仍然很高,尤其是在切除时有残留病灶的患者。直到最近,在这种情况下进行辅助全身治疗标准是根据全球Ⅲ期研究CheckMate 577的结果更新的。该研究纳入了1085例腺癌或鳞癌(29%)患者,这些患者在新辅助放化疗完成后切除时有残留病灶(>50%的患者有阳性淋巴结)。患者按2:1的比例随机分配到治疗周期均为1年的辅助纳武单抗组或安慰剂组。纳武单抗组患者无病生存期显著改善(22.4 vs. 11.0个月,HR 0.69),其中ESCC获益最大(鳞癌HR 0.61,腺癌HR 0.75)。无论PD-L1 CPS如何,无病生存期均有所改善,但CPS≥5的肿瘤(29.4 vs. 10.2个月)要比CPS<5的肿瘤获益更多(16.3 vs. 11.1个月)。值得注意的是,与安慰剂相比,与纳武单抗相关的≥3级不良事件(AEs)发生率较低(13% vs. 6%)。基于这些结果,FDA批准对新辅助放化疗后切除时有残留病灶的食管癌和GEJ肿瘤患者进行为期1年的辅助纳武单抗治疗(表2)。这一建议也得到了美国国立综合癌症网络(NCCN)和ASCO指南的认可,无论肿瘤组织学或PD-L1表达如何,所有食管癌和GEJ肿瘤患者都应辅助IO。一项正在进行的Ⅱ/Ⅲ期EA2174研究正在评估术前放化疗加入纳武单抗以及辅助纳武单抗联合伊匹木单抗能否改善在CheckMate 577中观察到的疗效,并具有可接受的毒副作用(ClinicalTrials.gov标识符:NCT03604991;表3)。
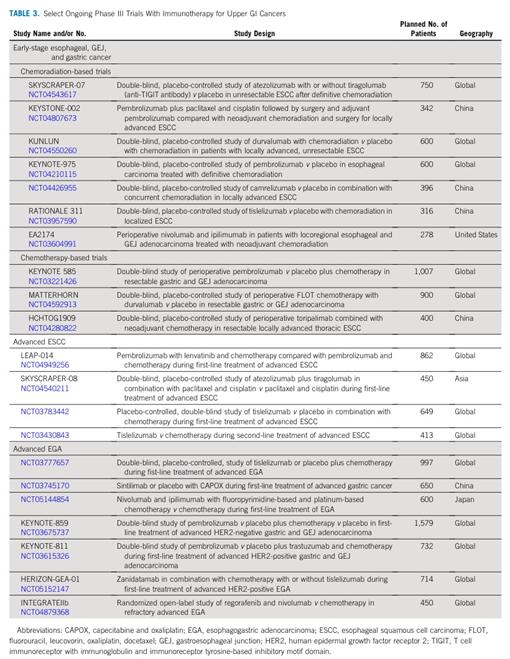
目前,IO并不适用于围术期化疗的上消化道癌症。然而,许多正在进行的试验正在探索IO的益处(表3)。KEYNOTE 585是一项全球Ⅲ期临床试验,评估围术期帕博丽珠单抗联合FLOT(氟尿嘧啶、亚叶酸、奥沙利铂、多西紫杉醇)化疗的益处(ClinicalTrials.gov标识符:NCT03221426)。MATTERHORN试验是一项关于围术期度伐利尤单抗联合FLOT化疗的Ⅲ期研究(ClinicalTrials.gov标识符:NCT04592913)。HCHTOG1909是一项在中国进行的Ⅲ期研究,比较了新辅助特瑞普利单抗联合化疗对比单纯化疗的局部ESCC患者的疗效。
治疗MSI-H上消化道癌症的最佳方法正在探索中。与MSI-H结直肠癌类似,可切除的MSI-H胃癌和GEJ肿瘤可能不会从围术期化疗中获益。在对MAGIC试验纳入的围术期MSI-H肿瘤患者的探索性分析中,MSI-H的肿瘤患者接受单纯手术治疗时预后更好,化疗可能会产生不利影响。在对接受辅助放化疗的MSI-H肿瘤患者的回顾性分析中也发现了类似的结果。而围术期应用IO则显示出了良好的疗效。纳入了32例MSI-H胃癌和GEJ癌患者的前瞻性Ⅱ期GERCORNEONIPIGA研究表明,术前应用纳武单抗和伊匹木单抗显示出了前所未有的59%的病理完全缓解率。这些结果有力支持了在更大规模的研究中进一步探索这种方法的可行性。然而在缺乏前瞻性随机数据的情况下,不建议偏离既定的FLOT治疗标准,特别是对于正在接受治愈性治疗的患者。对于化疗后进展或不适合联合化疗的MSI-H肿瘤患者,新辅助IO正成为一种可行的选择。
【IO治疗晚期EGA】
一线治疗:Her-2阴性
一系列针对晚期EGA的里程碑式研究表明,将IO纳入一线治疗可改善患者的预后(表1)。尽管最佳生物预测标志物仍存在争议,但临床医生应放心地在一线为PD-L1阳性肿瘤患者提供IO联合化疗方案。
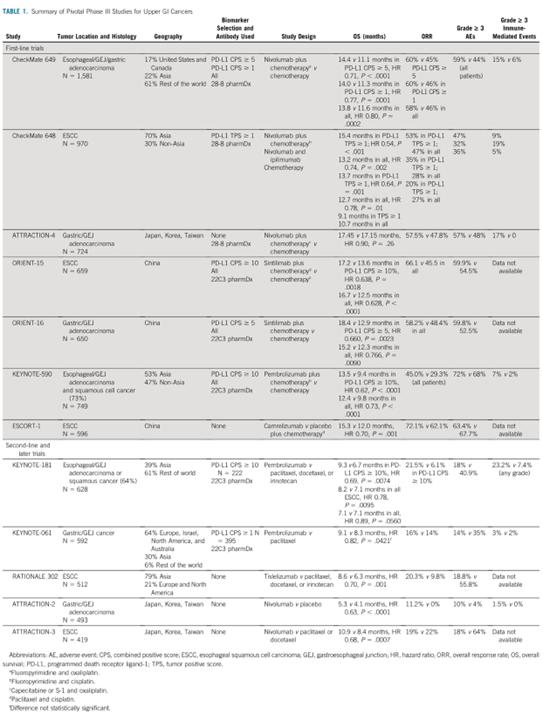
CheckMate 649是FDA批准纳武单抗用于晚期EGA的关键试验。在这项全球Ⅲ期临床试验中,将未经治疗的晚期EGA患者(无已知阳性 HER2)随机分配到单纯化疗组、化疗联合纳武单抗组或纳武单抗联合伊匹木单抗组。PD-L1阳性并不是入组的必要条件。根据CheckMate 032的新数据,在招募期间,主要研究人群修改为包括PD-L1 CPS≥5%的肿瘤患者。将大约1600名患者按1:1的比例随机分配到化疗组(氟嘧啶和奥沙利铂双药)或化疗联合纳武单抗组,该研究证明了加入纳武单抗可使患者获益。纳武单抗延长了PD-L1 CPS≥5%患者的OS(14.4 vs. 11.1个月,HR 0.71)和无进展生存期(PFS;7.7 vs. 6.0个月,HR 0.68)。该研究达到了所有正式的次要终点,包括改善了所有接受治疗患者的OS,但获益主要是由PD-L1 CPS≥5的患者(约60%)推动的,在PD-L1表达较低或阴性的肿瘤患者(17%的患者CPS<1)人群中,HR有所下降。该研究还表明,化疗在一线治疗中不可或缺,单用伊匹木单抗和纳武单抗的队列在治疗早期死亡率增加,无论选择何种生物标志物,OS均没有改善。基于该试验结果,FDA批准纳武单抗联合化疗应用于所有EGA患者的一线治疗。然而,根据NCCN的I类建议,纳武单抗应该用于PD-L1 CPS≥5肿瘤患者(表2)。
两项大型试验KEYNOTE 062和KEYNOTE 590评估了帕博丽珠单抗在上消化道腺癌中的作用。KEYNOTE-062纳入了胃癌和GEJ腺癌患者。虽然与CheckMate 649设计相似,但该试验加入帕博丽珠单抗并没有改善OS。对于这两项研究之间不一致的结果,有许多可能的解释。如生物标志物的选择不同,包括PD-L1 CPS阈值和选择的抗体(KEYNOTE-062中的22C3和CheckeMate 649中的28-8)。化疗方案略有不同,KEYNOTE-062采用基于顺铂的化疗,而CheckMate 649采用基于奥沙利铂的化疗。正在进行的KEYNOTE-859研究采用基于奥沙利铂的化疗,并将讨论不同的化疗方案是否会导致结果不同。此外,CheckMate 649中有13%的食管腺癌患者,而KEYNOTE-062只纳入了胃癌和GEJ肿瘤患者。然而,KEYNOTE 590纳入了符合入组条件的食管腺癌和鳞癌患者。由于73%的入组患者为ESCC,因此该研究结果对这部分患者更有意义。KEYNOTE 590有多个主要终点和亚组分析,因此解释研究结果会更加复杂。然而这项研究最终使FDA批准帕博丽珠单抗与化疗联合用于食管癌的一线治疗,依据是PD-L1 CPS≥10的肿瘤患者的OS有明显改善(17.4 vs. 10.8个月,HR 0.69)以及随机分组的所有患者的OS改善(12.4 vs. 9.8个月,HR 0.73)。在腺癌患者亚组中,应用帕博丽珠单抗治疗患者的OS更长,尽管效果不太明显(11.6 vs. 9.9个月,HR 0.73)。尽管经过了获批及广泛认可,NCCN指南还是强烈建议应用帕博丽珠单抗的PD-L1 CPS≥10的食管癌患者,应优先选择基于顺铂的化疗方案(1类),而非基于奥沙利铂的化疗方案(2a类)。
鉴于不同的地域有不同的肿瘤生物学特性,在亚洲国家进行的研究并不直接适用于所有患者,但为了严谨,将在此简要回顾。ATTRACTION-4是一项在日本、韩国和台湾进行的随机、多中心的Ⅱ/Ⅲ期研究,该研究探讨了724例初治胃癌和GEJ腺癌患者在化疗中联合纳武单抗的获益。该研究达到了PFS改善的主要终点(10.45 vs. 8.34个月,HR 0.68),但OS无差异,可能是由于后续治疗原因或未经生物标志物筛选(17.45 vs. 17.15个月,HR 0.90)。值得注意的是,这一患者群体的OS远高于其他全球研究,这反映了不同的肿瘤生物学特性。相比之下,一项在中国进行的Ⅲ期试验中(ORIENT-16,ClinicalTrials.gov标识符:NCT03745170),信迪利单抗(人源化抗程序性细胞死亡蛋白-1[PD-1]单克隆抗体)联合化疗显著改善了初治的晚期胃癌和GEJ腺癌患者的OS(15.2 vs. 12.3个月,HR 0.76)。在PD-L1 CPS≥5的肿瘤患者和随机分组的所有患者中都观察到了这种获益。
总的来说,部分HER2阴性的EGA患者可从一线化疗中联合IO获益(表2)。尽管IO疗法经过了FDA的广泛批准,但对HER2阴性患者应用IO时也应该仔细斟酌。越来越多的证据表明,只有PD-L1 CPS阳性肿瘤患者才能从IO中获益,而且获益程度与PD-L1阳性程度相关,正如KEYNOTE 590、KEYNOTE 062和ChecekMate 649的亚组分析中所见。KEYNOTE 590(CPS 1-9)、KEYNOTE 062(CPS 1-9)和CheckMate 649(CPS 1-4)的低PD-L1亚组的联合亚组分析进一步支持了这一观点,HER2阴性患者联合IO不会获益。因此,在一线治疗中,对于PD-L1 CPS≥5的EGA患者,应将纳武单抗加入化疗中;而对于PD-L1 CPS≥10的食管腺癌患者,应将帕博丽珠单抗加入化疗中。即使在经过生物标志物筛选的患者群体中,也不建议一线治疗中不进行化疗。目前尚不清楚辅助纳武单抗的食管癌和GEJ癌复发患者能否从新加入的IO中获益。复发的时间(在接受纳武单抗治疗完成6个月后)可能起到一定作用,但这个问题需要在前瞻性研究中进行探索。此外,肿瘤的空间与时间异质性仍然是处理临床患者和最佳治疗决策的混杂因素。
一线治疗:HER2-阳性
约20%的EGA患者过表达HER2或携带HER2基因扩增。十多年来,曲妥珠单抗联合化疗一直是这些肿瘤的标准一线疗法。最近在两项Ⅱ期临床试验中,标准治疗中加入帕博丽珠单抗显示出了可观的总缓解率(ORR)、PFS和OS。基于这些结果,一个正在进行的Ⅲ期研究KEYNOTE-811评估在标准治疗中加入帕博丽珠单抗的疗效。在对260例患者进行了至少8.5个月的随访后,预先计划的中期分析显示与安慰剂相比,帕博丽珠单抗显著提高了ORR(74.4% vs. 51.9%),并且没有新发安全问题。无论肿瘤PD-L1状态如何,在其标准治疗中加入帕博丽珠单抗已经得到了FDA的批准以及NCCN指南的认可。
二线及多线治疗
已经有许多研究评估了IO在EGA的二线或多线治疗的疗效。从这些数据中可以得出一些关键点。首先,这些研究纳入的是未经IO治疗过的患者,当抗PD-1抗体经过FDA批准用于一线和辅助治疗时,这些研究结果在很大程度上已变得无关紧要。其次,这些药物的临床疗效在多线治疗研究中相当有限,而且与一线治疗研究类似,仅限于经生物标志物筛选的患者群体。在此简要回顾一下这些研究的完成情况。KEYNOTE-181是一项全球Ⅲ期研究,纳入了在早期治疗中出现进展的食管腺癌和鳞癌患者。与医生选择的化疗方案相比,该研究达到了改善PD-L1 CPS≥10肿瘤患者OS的主要终点。然而,即使是在经过生物标志物选择的患者群体中,该趋势也主要见于ESCC患者,腺癌患者的HR为0.93。KEYNOTE-061是一项Ⅲ期研究,其研究对象是标准治疗后发生进展的胃癌和GEJ癌患者,比较帕博丽珠单抗联合紫杉醇治疗这些患者的疗效。该研究未能达到PD-L1 CPS≥1肿瘤患者OS和PFS的主要终点。尽管缺乏随机数据支持,但FDA暂时批准帕博丽珠单抗用于PD-L1 CPS≥1肿瘤的三线治疗。然而,由于没有更多数据的支持,该批准已被撤回。基于Ⅲ期ATTRACTION-2试验结果,纳武单抗相较于安慰剂的OS有所改善(5.25 vs. 4.14个月,HR 0.62),其在亚洲获批用于三线治疗。
总之,目前美国尚无FDA批准的二线或多线治疗晚期EGA的IO药物。未来的研究应考虑最近获批的用于早期治疗的IO。目前改善PD-L1阴性肿瘤患者在不同治疗阶段的预后仍任重道远。
【IO治疗晚期ESCC】
一线治疗
对于晚期(不可切除或转移)ESCC,IO在早期治疗中显示出了最好的疗效。根据之前讨论的KEYNOTE 590试验的结果,化疗联合帕博丽珠单抗目前已被FDA批准用于一线治疗。CheckMate 648是一项将纳武单抗加入化疗(氟尿嘧啶和顺铂)治疗ESCC的全球Ⅲ期试验。该研究将970例患者随机分配至化疗组、化疗联合纳武单抗组,或纳武单抗和伊匹木单抗组。在PD-L1 TPS≥1%的患者中(占入组患者的49%),化疗联合纳武单抗组OS最长,为15.2个月,而纳武单抗联合伊匹木单抗组OS为13.7个月,单独化疗组OS为9.1个月(P<0.0001)。再对所有患者进行分析,这种生存获益优势有所减弱,但仍有显著意义(P=0.0021)。在不久的将来,纳武单抗联合化疗可能会被FDA批准用于ESCC一线治疗。尽管CheckMate 648研究表明对于一些特别是那些不适合化疗的患者,纳武单抗联合伊匹木单抗的无化疗方案可以替代治疗,但在IO队列中治疗早期死亡人数较多,反映了化疗在这些患者的治疗中仍起着关键作用。此外从研究设计来看,伊匹木单抗的作用并不明确,因为没有设置单用纳武单抗的对照组。总的来说,理想情况下,适合全身治疗的患者应接受化疗联合IO方案,考虑到预期的耐受性问题可以对其方案进行改良。对于不适合细胞毒疗法的患者,如果其病灶小且相关症状较轻,仅用IO也是可行的。
除了CheckMate 648和KEYNOTE 590全球研究外,最近在中国进行的三项针对ESCC患者的Ⅲ期研究评估了IO加入一线化疗中的作用(ORIENT-15,ESCORT-1和JUPITER-06)。这些试验有相似的设计,但它们的化疗方案是紫杉醇和顺铂。这三项研究都表明,无论PD-L1状态如何,化疗联合IO均能改善OS。与类似患者群体的全球试验(KEYNOTE-590和CheckMate 648)相比,OS改善的程度似乎更大,而且对照组有更好的结果。这可能反映了西方和亚洲ESCC患者之间的生物学差异,也可能是不同化疗药物的疗效差异。这些试验的结果并不直接适用于国外患者,但它们确实提出了关于治疗ESCC最适合的化疗方案的问题。
二线及多线治疗
一线未接受IO的患者可以考虑在后续治疗中加入IO,尽管疗效预计会减弱。KEYNOTE 181肯定了帕博丽珠单抗对未经IO治疗过的PD-L1 CPS≥10肿瘤患者的疗效。与研究者选择的标准化疗方案相比,替雷利珠二线治疗(RATIONALE 302)生存率也有所提高,且与PD-L1状态无关。在ATTRACTION-3试验中,纳武单抗也显示出类似疗效(与PD-L1无关),OS得到了改善,基于这些结果FDA批准了纳武单抗。
总之,将单药IO应用于二线和多线治疗得到了高质量的Ⅲ期数据的支持。然而,与晚期EGA类似,在ESCC多线治疗中IO的疗效会降低,这与早期治疗中应用IO的程度呈负相关。
【IO治疗错配修复缺陷和微卫星不稳定(MSI-H)上消化道癌症】
约4%-22%的胃食管肿瘤为错配修复缺陷(dMMR)/MSI-H,这与改善临床预后相关。与MSS肿瘤相比,这些肿瘤对IO的反应有所不同,应采取不同的治疗方法。无论肿瘤分期如何,所有患者都应评估微卫星状态或MMR蛋白的表达。
在帕博丽珠单抗试验的事后分析中总结了IO在转移性dMMR/MSI-H EGA中的作用。KEYNOTE-059首次报告了IO的活性信号,特别是在MSI-H胃癌和GEJ癌中,帕博丽珠单抗在MSI-H肿瘤的晚期治疗中达到了57.1%的ORR(n=7)。此外早期应用抗PD-1疗法也具有显著疗效。在KEYNOTE-061中,与化疗组8.1个月的OS相比,帕博丽珠单抗组未达到dMMR/MSI-H的中位OS(n=27;5.3%)。帕博丽珠单抗组ORR为47%,而紫杉醇组为17%。在KEYNOTE-062一线试验中,接受帕博丽珠单抗单药治疗或帕博丽珠单抗联合化疗的dMMR/MSI-H癌症患者均未达到OS,而单纯化疗患者的OS为8.5个月(n=50;7.3%)。同样,在CheckMate 649中,接受纳武单抗联合化疗的MSI-H肿瘤患者未达到OS,而单纯化疗患者的OS则为12.3个月,HR为0.37(n=44;3%)。这些结果表明应尽早应用IO。在一线治疗中,化疗对IO的作用尚不清楚。由于这些肿瘤的罕见性,很难进行一项随机试验来回答这个问题,单用IO可能就足以作为MSI-H肿瘤患者的一线疗法。然而,无论MSI状态如何,有症状的患者可能应该开始接受化疗联合IO,以确保病情可以迅速缓解。患者可以逐步撤去化疗,继而单用IO。然而,这种方法并没有得到前瞻性随机数据的支持。
【IO毒性】
在化疗中加入免疫检查点*制剂抑**与毒性增加有关。许多试验表明≥3级与治疗相关的AEs发生率较高(表1)。例如,在CheckMate 649中,59%加入纳武单抗的患者出现了3级AEs,而单纯化疗的患者只有44%出现了3级AEs。尽管多达三分之一的患者出现了免疫相关毒性,但大多数是轻微的,在≤5%的患者中观察到了≥3级AEs。在所有的研究中,与治疗相关的死亡很罕见。鉴于IO最常与其他药物联合使用,在实践中可能很难确定IO的毒性作用。建议参考ASCO的免疫相关毒性管理指南,以了解如何实行最佳个体化治疗。
【总结与未来方向】
上消化道肿瘤是有复杂生物学性质的异质性肿瘤。如今免疫检查点*制剂抑**是早期和晚期EGA和ESCC的标准治疗方案的一部分。未来IO试验设计必须考虑这些变化,其中一些试验应侧重于研究克服IO继发性耐药的机制和方法。此外,相当大比例免疫冷肿瘤的患者并不能从IO中获益。改善现有药物活性,寻找新的药物联合方案以及更好的筛选最有可能获益于当前治疗的患者非常重要。新兴的免疫靶点,如TIGIT和DKK1,在早期研究中显示出了良好的活性,目前正在进行试验评估(ClinicalTrials.gov标识符:NCT04363801,NCT04047862)。将IO与小分子*制剂抑**和抗血管生成剂联合使用,如卡博替尼和仑伐替尼,是其他试验正在积极探索的方法(ClinicalTrials.gov标识符:NCT03321630,NCT03539822)。最后,随着新的生物标志物不断定义上消化道癌症的亚群,例如claudin-18.2和FGFR2b,如何优先考虑可用疗法或针对这些靶点联合药物以优化患者的预后将是至关重要的。
【文献来源】
Patel MA, Kratz JD, Lubner SJ, et al. Esophagogastric Cancers: Integrating Immunotherapy Therapy Into Current Practice.J Clin Oncol. 2022 Jul 15;JCO2102500. doi:10.1200/JCO.21.02500