干燥综合征是一种以炎症细胞浸润外分泌腺为特征的慢性系统性自身免疫性疾病,除累及唇腺、泪腺外,还可以累及肺、肾、肝、皮肤、神经或血液系统等。通常根据是否合并如系统性红斑狼疮、皮肌炎、类风湿性关节炎等其他自身免疫病,分为原发性和继发性。
其典型临床表现除外分泌腺受累所引起的口干、眼干外,还可有关节痛、皮疹、肾功能受损、间质性肺炎等脏器受累的表现。干燥综合征起病隐匿,临床表现不典型,部分患者起病多年后才明确诊断,临床上常出现误诊和漏诊。
原发性干燥综合征(pSS)的肾脏损害表现包括:以肾小管酸中毒、低钾血症、低钾性周期麻痹、泌尿系结石等为主要表现的小管间质损害,肾淀粉样变、混合性冷球蛋白血症相关的肾小球肾炎等。
由于肾脏损害的定义标准不同,其发病率在各文献中报道差异较大,约在 2%-67%之间。本文就原发性干燥综合征继发肾损害的发病机制、肾脏病理特点、临床表现、诊断标准、治疗进行叙述。
一、发病机制
干燥综合征的发病机制尚未明确,但已证实外分泌腺及腺上皮细胞中有大量增殖的B淋巴细胞。
慢性肾小管间质性肾炎是最常见的肾脏病理表现,主要引起三种形式的肾小管酸中毒:I 型 RTA、IV 型 RTA 和近端肾小管酸中毒(II 型 RTA),以 I 型 RTA 最常见。
与外分泌腺相比,在同样具有导管上皮细胞结构的肾脏中发现较多淋巴细胞、浆细胞的浸润,提示肾脏损害可能与淋巴细胞浸润,从而引起的机体体液免疫及细胞免疫有关。
最近的研究表明,干燥综合征的发病可能与涎腺异位生发中心(EGC)形成有关,IL-17、IL-23 等细胞因子参与EGC的形成并介导炎症反应。关于 EGC 在包括肾脏在内的其他器官损伤的作用,还需要进一步证实。
干燥综合征也可引起肾小球的损伤,较肾小管损伤少见。目前发病机制不明,可能为 B 淋巴细胞及浆细胞过度活化,产生大量自身抗体与暴露的抗原形成免疫复合物,沉积于肾小球毛细血管袢内,激活补体途径引起炎症细胞的浸润,从而导致内皮和系膜的损伤。
或是长时间的肾小管及间质损害引起肾小管萎缩、间质纤维化,进而导致肾小球硬化的发生。
二、肾脏病理
1、肾小管间质性肾炎
肾小管间质性肾炎是最常见的病理改变。在接受肾脏病理活检的患者中,TIN的发生率约为75%。主要表现为肾间质及肾小管淋巴细胞、浆细胞、单核细胞等炎症细胞的浸润,可引起肾小管萎缩和间质纤维化,病变严重处可见肾小球硬化。
与涎腺组织类似,浸润的淋巴细胞主要是 CD4+淋巴细胞。免疫荧光染色多为阴性,部分有少量免疫复合物的沉积,个别病例可见 IgG 在肾间质内沉积。

2、肾小球肾炎
国外文献报道与冷球蛋白血症相关的膜增生性肾小球肾炎是最常见的pSS 继发肾小球肾炎类型。我国北京协和医院较常见的病理类型为膜性肾病及系膜增生性肾小球肾炎。
其他可见的病理类型有局灶节段性肾小球硬化、微小病变肾病、IgA 肾病、硬化性肾小球肾炎等。这些肾小球改变可能是由于干燥综合征所继发,也有可能是在原发肾小球肾炎的基础上合并干燥综合征。
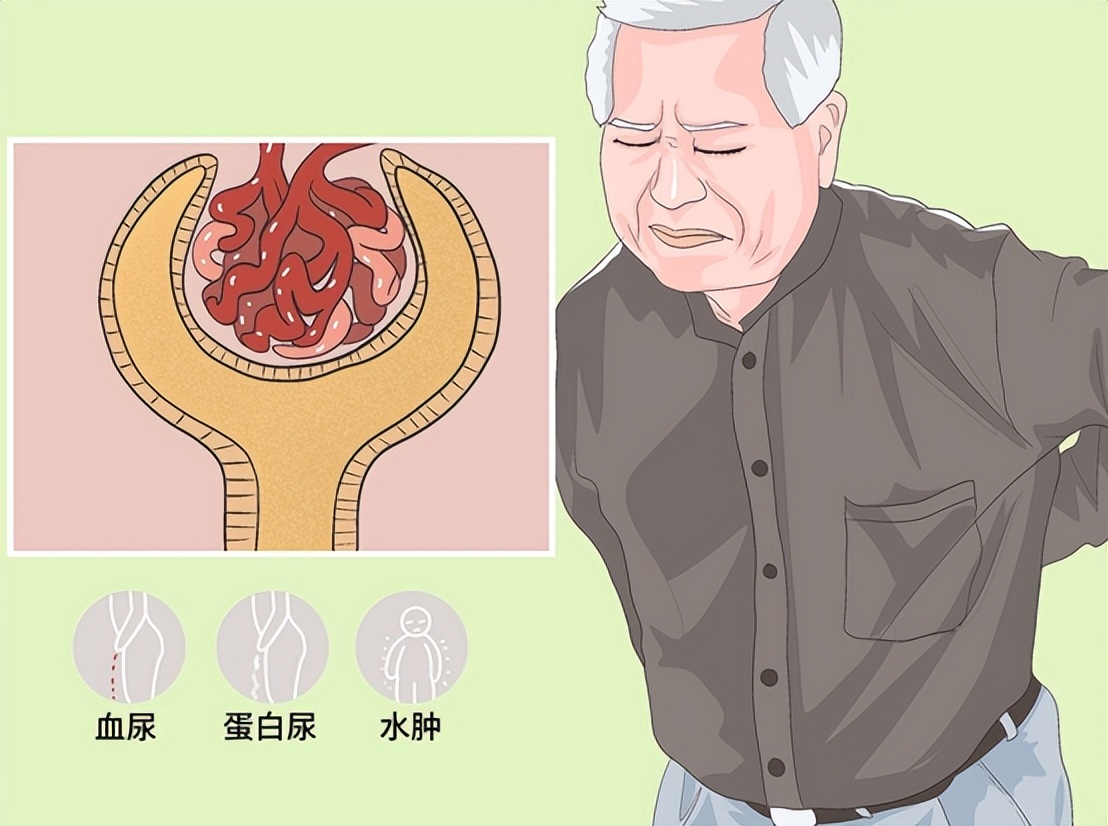
三、肾损害的临床表现
1、肾小管间质损害
(1)远端肾小管酸中毒
远端肾小管酸中毒也称 I 型肾小管酸中毒,是 pSS 最常见的肾损害类型。其发病机制尚未明确,推测可能是体内包括抗 SSA、抗 SSB 抗体在内的多种自身抗体。
与肾小管存在交叉免疫反应,从而使局部发生免疫反应,局部损伤造成集合管氢离子反流、肾小管泌氢功能障碍。由于氢离子无法排出体外,引起反常性碱性尿及代谢性酸中毒。
代谢性酸中毒使钙离子从骨骼中游离出来,与酸性产物结合从尿液中排泄增多,造成低钙血症,继发性甲状旁腺功能亢进,出现肾钙化、肾结石及骨软化病。
肾小管钾排泄过多导致低钾血症,轻者出现乏力、食欲下降、腹胀等不适,或仅在化验时发现血钾降低。严重的低钾血症可出现周期性瘫痪,四肢肌力下降,甚至产生呼吸肌麻痹、心脏骤停等不良后果。
(2)近端肾小管功能障碍
近端肾小管酸功能障碍在干燥综合征继发肾损害中的发生率较低。Fanconi 综合征是一种原发性或继发性的近端肾小管复合性功能障碍,主要临床表现为肾小管转运功能受损所引起的氨基酸尿、糖尿、磷酸盐尿、高氯性酸中毒、低钾血症等。
其干燥综合征继发近端肾小管受损的机制尚未明确,近期研究推测 pSS 患者肾间质树突细胞和异位生发中心的形成,与严重的肾间质炎症相关,可介导刷状缘破坏,导致近端肾小管上皮细胞重吸收功能障碍和 Fanconi 综合征。
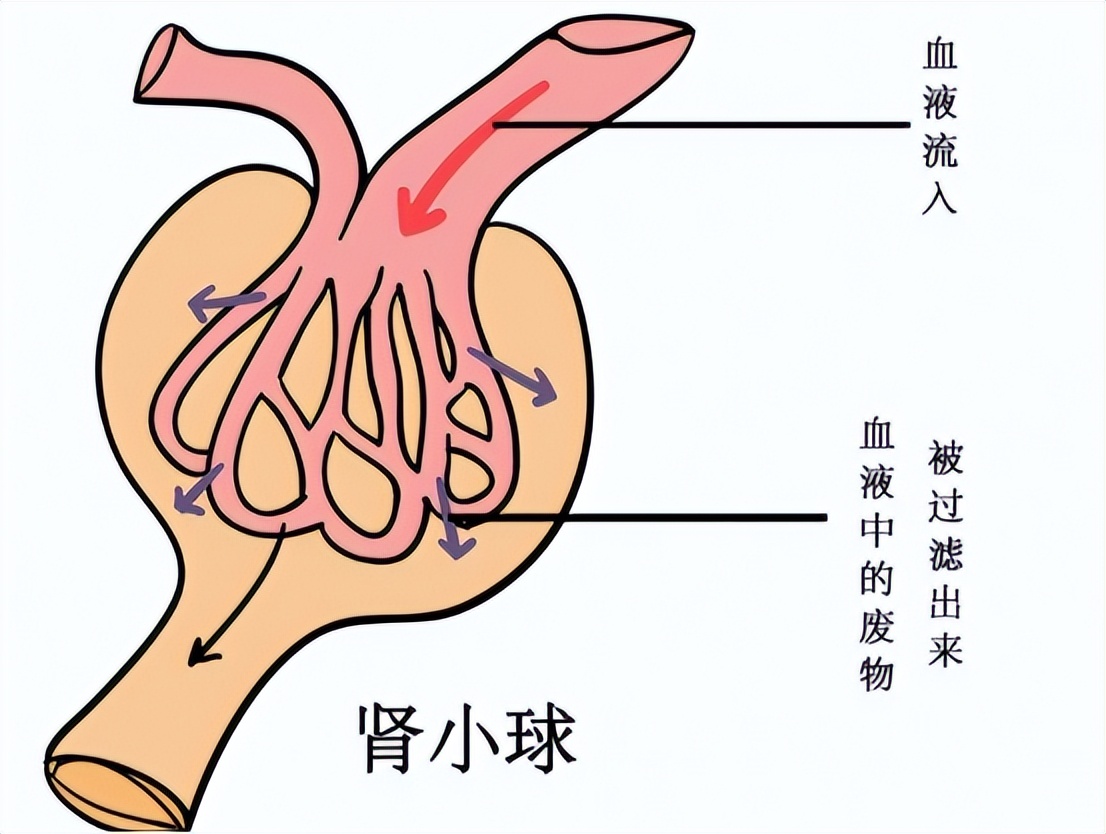
(3)肾性尿崩症
患者远端肾小管及集合管浓缩功能受损,可出现低比重尿、多饮多尿、夜尿增多甚至肾性尿崩症。原发性干燥综合征合并肾性尿崩症并不少见,发生率在 16%~82%,且可表现在疾病的早期,甚至早于口干、眼干等症状。
(4)获得性Gitelman综合征
Gitelman 综合征是一种主要累及远曲小管的常染色体隐形遗传疾病,其病因与负责编码远曲小管钠氯共同转运体蛋白的基因 SLC12A 突变发生功能缺失有关。
干燥综合征患者中也见有获得性 Gitelman 综合征的报道,患者可出现四肢痉挛、肌无力、低钾、低镁等症状。
(5)获得性Bartter综合征
Bartter 综合征通常被认为是一种罕见的遗传性疾病,但它在自身免疫性疾病中也可出现,现有 5 例病历报道原发性干燥综合征合并 Bartter 综合征,患者可出现低钾血症、高钾尿、高钙尿、代谢性酸中毒、高氯血症等。
2、肾小球损害
关于 pSS 继发肾小球损害并不少见,既往认为最典型的病变是与冷球蛋白血症相关的膜增生性肾小球肾炎,与淋巴瘤的发生密切相关。也可表现为其他的病理类型如IgA肾病、膜性肾病、局灶节段性肾小球硬化、微小病变型肾病等。

目前继发肾小球损害的发病机制未明,由于我国 IgA 肾病和膜性肾病占原发性肾小球疾病的比例较高,由干燥综合征继发还是合并原发肾脏病还需要进一步探究。
患者可表现出蛋白尿、镜下血尿、高血压等,或表现为肾病综合征,长期的肾小球损害可导致慢性肾衰竭。
四、肾脏损害的治疗
1、对症治疗
针对肾小管酸中毒,主要以维持水电解质、酸碱平衡为主。可使用碳酸氢钠纠正酸中毒、枸橼酸钾或氯化钾补钾,定期复查血气分析及电解质,调整碳酸氢钠及含钾药物的用法和用量。
部分患者因低血钙、高尿钙出现骨质疏松、骨软化症时,可以使用碳酸钙、骨化三醇补钙对症治疗。有研究表明免疫功能异常与骨病严重程度存在一定的相关性,使用小剂量泼尼松治疗可以通过多种途径抑制免疫反应。
在对严重骨病患者随访过程中,规律使用激素及骨化三醇治疗,患者的骨密度较治疗前增加,肾小管功能改善。

2、激素及免疫*制剂抑**治疗
由于 pSS 是一种免疫调节异常在发病机制中起重要作用的疾病,可选择糖皮质激素及免疫*制剂抑**作为治疗方案。
pSS合并关节、皮肤病变时,经典治疗方案通常以羟氯喹或甲氨蝶呤为基础,当患者出现耐药或其他腺外器官受累时,可使用糖皮质激素、抗增殖药物、钙调磷酸酶*制剂抑**、环磷酰胺或B细胞耗竭治疗。

对于TIN,轻度间质浸润、肾功能损害不明显时可对症治疗。但存在间质浸润明显、急性肾功能不全时可以使用大剂量激素联合细胞毒药物,两个包括 TIN 和 MPGN 在内的队列研究中发现激素及免疫*制剂抑**治疗可以改善患者肾功能。
但也有研究表示在 TIN 患者中,与单独使用激素相比,联合使用免疫*制剂抑**对肾脏预后并没有太明显的益处。国外有研究显示吗替麦考酚酯联合激素也可用于治疗 pSS 合并 TIN,可降低血肌酐及提高患者肾小球滤过率。
对于肾小球损害,应该根据病理类型及肾功能损害程度决定是否使用激素治疗及用量。
3、生物制剂治疗
利妥昔单抗是一种针对 CD20 分子的单克隆抗体,能与 B 细胞上的CD20 抗原特异性结合通过细胞毒反应、细胞凋亡等多种途径消耗 B 细胞。
现关于利妥昔单抗在 pSS 中的治疗疗效尚不确切,一项前瞻性研究表明 B细胞靶向治疗对伴或不伴淋巴瘤的 pSS 患者均可改善干燥症状。
目前研究证实对利妥昔单抗治疗有效的肾小球疾病包括:ANCA 相关小血管炎肾损害、原发性膜性肾病、难治性或对激素抵抗的肾病综合征、I 型系膜毛细血管增生性肾小球肾炎等。推测干燥综合征合并肾小球损害使用利妥昔单抗也可取得一定的疗效,但仍需被证实。

总结
pSS 合并肾脏损害的发生率并不低,但由于起病隐匿、病程进展较慢、临床表现不典型等常导致漏诊、误诊。其病理表现多种多样,主要以间质性肾炎为主,肾小球肾炎、血管炎肾损害等也可发生。
患者可表现为肾小管酸中毒,出现乏力、血钾偏低、代谢性酸中毒,也可表现为蛋白尿、血尿、高血压、肌酐或尿素氮升高等肾小球损害表现。
当患者出现上述累及肾脏损害的症状时,及时进行肾脏穿刺活检,定期监测肾功能及进行 ESSDAI 评分,为选择治疗方式提供依据,有利于患者的预后。
在治疗方面,仍缺少大样本、多中心的随机对照试验来证实激素、免疫*制剂抑**及生物制剂对pSS合并肾损害的疗效及不良反应。