
撰文 | 英成
责编 | 翊竑
基于PD-1/PD-L1的免疫治疗是目前最有潜力使肿瘤患者获得根治机会的疗法之一,NCCN指南已将联合免疫治疗 (Pembrolizumab联合Axitinib)列为晚期肾癌一线治疗的推荐治疗 【1】 。转移性肾癌临床试验初步表明,联用免疫治疗与靶向血管生成药物的总体有效率可达51% 【2】 ,显示出令人鼓舞的应用前景。但是,一部分患者仍对免疫治疗不产生应答,亟需探索其背后的机制,以设计更高效的免疫治疗策略。
近期,来自纽约纪念斯隆凯特琳癌症中心 (MSKCC) 的A. Ari Hakimi课题组、Timothy A. Chan课题组和Christina S. Leslie课题组联合在 Cancer Cell 上发表题为 Single-cell sequencing links multiregional immune landscapes and tissue-resident T cells in ccRCC to tumor topology and therapy efficacy 的研究论文, 系统揭示了肾透明细胞癌免疫治疗的微环境图谱。研究人员通过采集2名未治疗和4名免疫治疗后的肿瘤多点病灶、淋巴结、正常肾脏组织、外周血样本,利用单细胞转录组测序、单细胞TCR测序等高通量组学手段对167,283个细胞进行深度测序,发现组织驻留T细胞和肿瘤相关巨噬细胞与免疫治疗疗效显著相关。
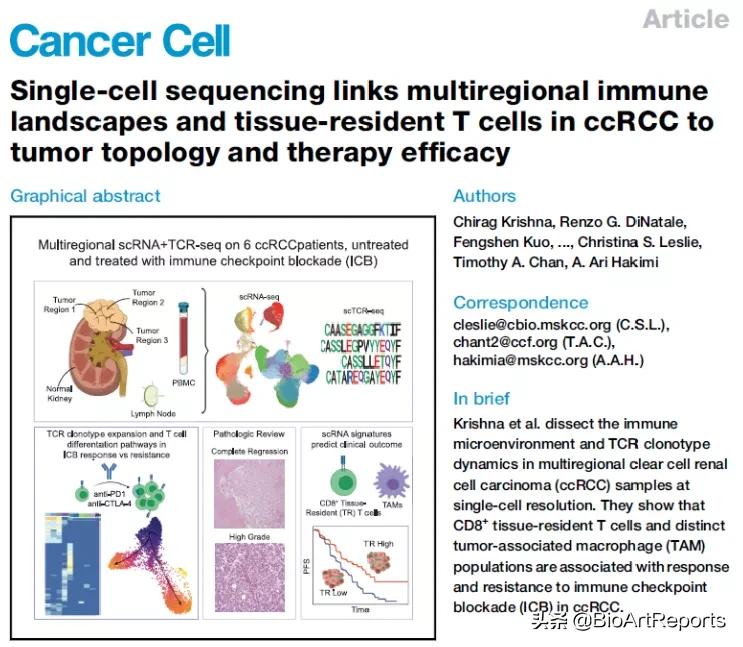
在这项工作中,共纳入了6名患者的多个组织样本,其中4名接受治疗的患者信息分别为:接受Nivolumab单药治疗、Ipilimumab+Nivolumab耐药、Ipilimumab+Nivolumab混合反应、Ipilimumab+Nivolumab完全缓解。在Ipilimumab+Nivolumab耐药的患者肿瘤组织中,研究者发现呈“免疫荒漠”的特征——即微环境无T细胞浸润。有趣的是,大量肿瘤相关巨噬细胞也浸润在了耐药肿瘤微环境中。相反,在免疫治疗完全缓解的肾癌微环境中,单细胞转录组测序与病理图像均捕获到了CD8+ T细胞的大量富集。
为了追踪微环境内T细胞的分化谱系,研究者利用单细胞TCR测序追踪了Clonotype。在Ipilimumab+Nivolumab耐药和Ipilimumab+Nivolumab完全缓解的微环境内,最广泛的Clonotype均来自CD8+组织驻留T细胞。免疫治疗给药后,发生扩增的亦有可能是CD8+组织驻留T细胞,表明这一群细胞可能对肾癌患者的免疫治疗获益扮演着重要作用。最后,作者在多个免疫治疗队列中验证了CD8+组织驻留T细胞的预后价值,能够一定程度上预测免疫治疗的疗效。
同期另一篇研究论文来自波士顿Dana-Farber Cancer Institute的 Eliezer M. Van Allen 课题组,题为 Tumor and immune reprogramming during immunotherapy in advanced renal cell carcinoma 。该研究比较了晚期肾癌免疫治疗前后组织活检样本的单细胞转录组变化,追踪了肿瘤微环境(尤其是衰竭CD8+ T细胞、肿瘤相关巨噬细胞、肿瘤细胞)随着免疫治疗的给药前后的动态变化,并揭示了免疫疗法耐药的潜在原因。
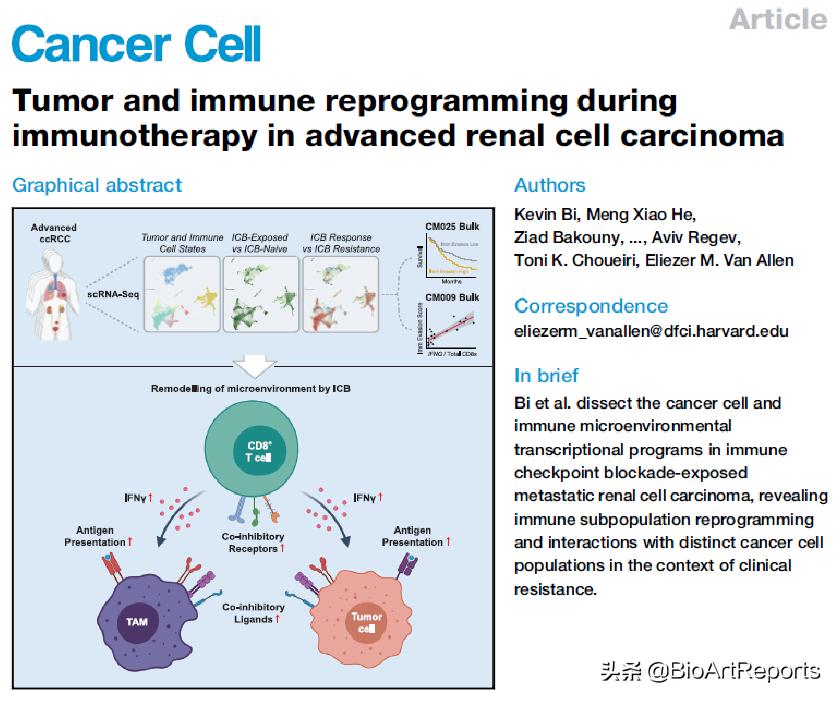
与上一篇研究论文不同的是,这项研究更多聚焦于免疫治疗后肿瘤细胞的状态变化。研究者发现,肿瘤细胞可分为TP1和TP2两种主要亚群。在功能上,TP1 群主要高表达血管生成特征;而TP2 细胞居然同时高表达糖酵解和氧化磷酸化特征,暗示TP2细胞癌变的特殊代谢重编程。这两群细胞对于免疫治疗的反应也大相径庭:TP1细胞在治疗后大幅上升nectin-2,而TP2细胞在一定程度上上调免疫检查点相关分子的表达水平。研究者进一步比较了肿瘤细胞转录组与疗效的关系。重要的是,在有效组和无效组之间TP2细胞展现出了巨大的差异,如有效组T细胞免疫检查点的广泛上调。相反,TP1细胞与患者生存呈正相关。最后,作者系统表征了微环境内的细胞相互作用,发现TP2细胞潜在更多的和T细胞发生交互,如高表达LGALS9和NECTIN2以潜在地抑制CD8 T细胞活性。
第三项工作来自波士顿Dana-Farber Cancer Institute的 Catherine J. Wu 课题组,题为 Progressive immune dysfunction with advancing disease stage in renal cell carcinoma 。该研究 比较了不同分期的透明细胞癌免疫治疗的单细胞图谱,发现衰竭CD8+ T细胞和M2样巨噬细胞在晚期肾癌样本中进行性富集,并形成了潜在的相互作用“环路”,与肾癌患者的不良预后结局显著相关。
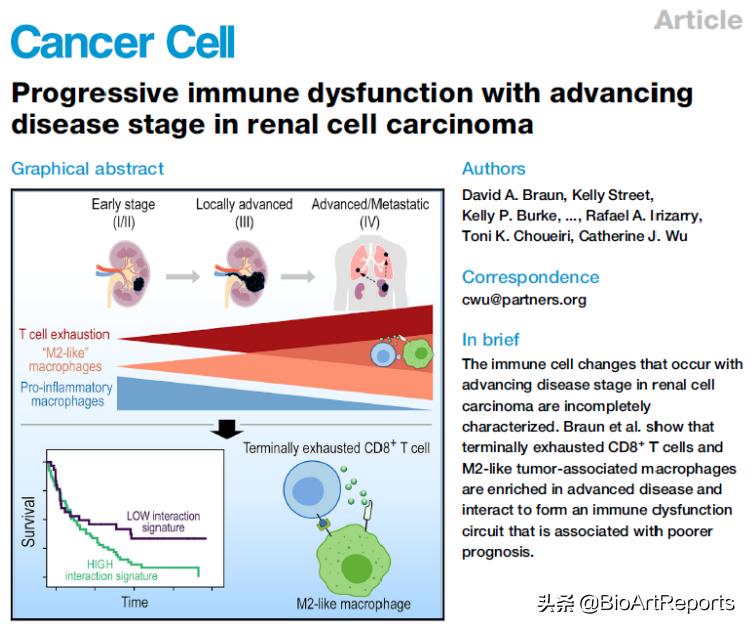
在这项研究中,作者收集了13名肾癌患者的肿瘤/癌旁样本 (I/II期,n = 4;III期,n = 4;IV期,n = 5),并利用5’端单细胞转录组测序、全外显子组测序,获取了164,722个细胞的转录组数据。有趣的是,肿瘤浸润的T细胞展现出了巨大的异质性。其中,衰竭CD8+ T细胞的变化与疾病进展的关联显著。为了探索这一重要亚群的状态变化,研究者利用了Slingshot算法来推测T细胞的分化轨迹。结果显示,晚期肾癌微环境内的CD8+ T细胞基本处于终末分化状态。决定T细胞衰竭命运的诸多重要转录因子(如TOX和EOMES等)亦与肾癌分级密切相关。
另一群免疫抑制性细胞——M2样巨噬细胞,也呈现出了与晚期肾癌的密切联系。在晚期肾癌微环境内,巨噬细胞显著高表达HLA分子 (如HLA-A、HLA-DRB1)、干扰素分子(如IFI27)、半胱氨酸组织蛋白酶(如CTSL、CTSS)、补体相关基因(如 C1QA、C1QB、SERPING1)和脂质转运相关基因(如APOE、PLTP)。伪时分析亦表明晚期巨噬细胞呈终末分化状态。最后,作者利用CellPhoneDB算法推断细胞间相互作用,并发现上述衰竭CD8+ T细胞和肿瘤相关巨噬细胞密集互作,并与不良患者结局显著相关。
总之, 上述三篇研究均利用高通量单细胞转录组测序,分别从不同角度阐述了肾癌进展和免疫治疗的微环境图谱。尽管这三项研究的患者队列样本量相对较小,但得出了相对一致的结论:抑制性免疫细胞如(衰竭CD8 T细胞、肿瘤相关巨噬细胞)的数量和状态对于免疫治疗的有效反应及肾癌的疾病进展至关重要。未来的更大规模、更多维的高通量测序将为攻克免疫治疗耐药、设计更高效的免疫治疗药物提供更多思路。
原文链接:
doi.org/10.1016/j.ccell.2021.03.007
doi.org/10.1016/j.ccell.2021.02.015
doi.org/10.1016/j.ccell.2021.02.013
制版人:十一
转载须知
【原创文章】BioArtMED原创文章,欢迎个人转发分享,未经允许禁止转载,所刊登的所有作品的著作权均为BioArtMED所拥有。BioArtMED保留所有法定权利,违者必究。