编者按: 自身免疫性肝炎(AIH)是一种由免疫介导的肝细胞炎症性损伤,近年来AIH患病率呈上升趋势。目前皮质类固醇激素和硫唑嘌呤是治疗AIH的首选药物,部分患者可能疗效欠佳,甚至出现对药物的不耐受,需要替换为二线药物治疗。临床上,治疗后获得持续生化缓解的患者可予以停药,但大多数患者停药后可出现复发,甚至需要终身维持治疗,一些患者可能还需要考虑肝脏移植。如何选择适当治疗时机,使用适量的一线药物,针对AIH患者治疗应答情况应该如何制订个体化的维持治疗方案,并对停药后复发的风险作出预测?以上问题都是决定患者预后的关键因素,本文将尝试进行解答。
1 药物治疗
国际上各大肝病学会均发表了AIH诊疗指南[1,2],指出AIH治疗的目标是同时达到生化学应答(血清氨基转移酶和IgG水平复常)和组织学缓解。表1总结了治疗方案。鉴于有关AIH的随机对照研究相对较少,多数推荐意见来源于专家意见和病例报道。
表1. AIH的治疗药物
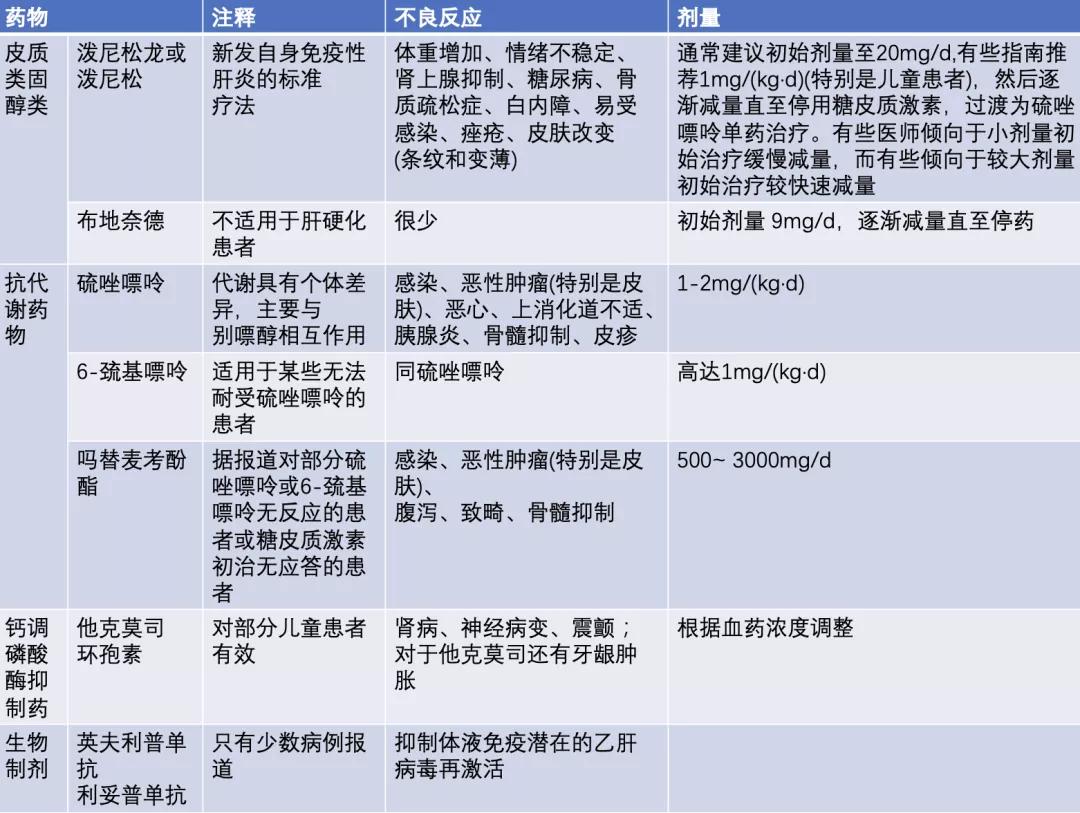
早期研究表明,糖皮质激素在急性起病的AIH患者中疗效显著,现已成为本病治疗的基石[3]。大多数中心使用泼尼松或其代谢产物泼尼松龙作为主要疗法,给药方法不尽相同,通常剂量范围为20 mg/d~1 mg/kg;在儿科病例中,宜采用根据体重计算的较高剂量[1,2]。在暴发性病例中,一些人主张静脉注射甲泼尼龙。大多病例生化指标应答迅速,而组织学应答较慢[4]。用于初始治疗泼尼松(龙)的主要替代品是布地奈德。这种合成的糖皮质激素经口服给药后具有肝脏首过效应。该药对AIH的诱导缓解治疗效果与泼尼松(龙)相似,但不良反应更少,故更适用于需减少糖皮质激素不良反应的非暴发性、非肝硬化的患者[5]。
从长远来看,为减少糖皮质激素长期治疗的累积不良反应,联合用药可减少激素用量的药物,其中最主要的是嘌呤类似物抗代谢物硫唑嘌呤。硫唑嘌呤单药在AIH的初始治疗中效果不及糖皮质激素,因此推荐糖皮质激素诱导治疗[6]。一部分患者可能需要联合低剂量的糖皮质激素治疗才能持续缓解,但在大多数患者采用硫唑嘌呤单药治疗即可维持缓解。
在晚期或暴发性疾病中,在胆红素小于≤100 μmolL()≤5.8mg/dl)前,通常不建议使用硫唑嘌呤或6-硫基嘌呤。这2种药物的严重但不常见的不良反应是骨髓抑制。硫唑嘌呤和6-硫基嘌呤的代谢部分取决于硫基嘌呤甲基转移酶( TPMT)的活性。TPMT活性有明显的个体差异,但不是嘌呤类似物毒性的唯一决定因素。因此,关于在开始治疗前是否检测TPMT水平,尚存在争议,但是治疗后一定要密切监测血常规、及时调整药物剂量和及时停药[1,2,7]。治疗中检测血清嘌呤类似物代谢物的水平,对于调整剂量和了解患者依从性有帮助。
表1总结了硫唑嘌呤和其他主要药物在AIH治疗中的不良反应。在一项大型系列研究中,大约10%的患者不耐受硫唑嘌呤[8]。部分不耐受硫唑嘌呤的人或许可以耐受6-硫基嘌呤。对于无法耐受硫唑嘌呤的患者,麦考酚酸或可以成为一种有效的替代疗法。有学者建议把麦考酚酸作为一线治疗药物,但在临床上并没有推广[9]。
此外,钙调磷酸酶抑制药他克莫司和环孢素在硫唑嘌呤耐药患者和儿童患者中被证实有效。有报道显示,采用抗B细胞药物利妥昔单抗和抗肿瘤坏死因子α药物昔改西单抗治疗AIH可成功达到缓解[10]。因此,有学者认为肝活检显示有一定程度的炎症活动的患者可考虑进行免疫抑制治疗。
重要的是,成功治疗AIH不仅可以预防疾病进展并降低死亡率,还可以在某些情况下减轻纤维化和肝硬化(见图1)[11]。
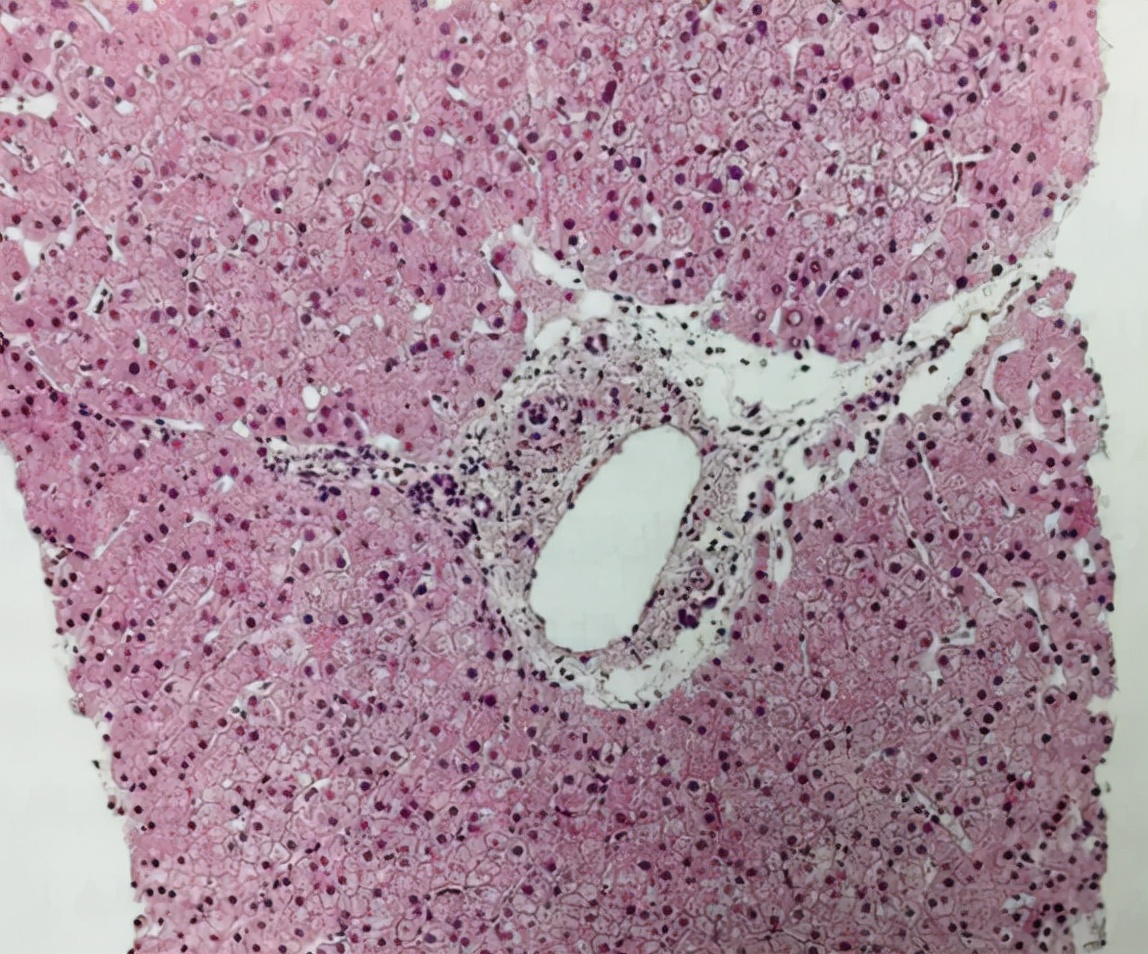
图1. 免疫性肝炎患者经过3年免疫抑制治疗后获得了临床缓解,肝穿刺提示肝组织活检未见异常。
2 肝脏移植
失代偿规肝病或暴发性肝衰竭患者需考虑肝脏移植。术前需要与肝移植团队进行讨论,对免疫抑制治疗与移植的风险-效益比进行个体化评估。一项来自英国的大型系列研究数据显示,约2%的AIH患者需要肝移植[8]。
AIH患者肝移植治疗预后良好,5年生存率超过80%[12]。移植后第1年感染发生率较高,需要密切监测。等待肝移植的患者应该减少免疫抑制药的剂量。值得注意的是,尽管急性排异的发生率相似,移植后免疫抑制药的剂量可能需高于其他病因患者。
肝移植后AIH可能会复发,文献报道的复发率差异很大,可高达50%。当供肝有活动性炎症及移植前受者免疫球蛋白升高时,易出现疾病复发[13]。术后复发的诊断需要基于生化指标和(或)免疫球蛋白异常,并结合肝旺组织学检查,自身抗体通常在移植后持续存在,因此对术后复发的诊断意义不大。
在其他病因行肝移植的患者中,移植术后可能会出现类似于AIH的综合征,称为“新发AIH”,有人认为它是一种免疫排异反应。
3 一般注意事项
AIH患者的长期管理包括维持最小有效剂量免疫抑制治疗、对可能出现的不良反应的治疗及对慢性肝病的治疗。
对于肝硬化患者,需像其他病因慢性肝病一样,对食管胃底静脉曲张和肝细胞癌进行定期监测。一项大型队列研究结果显示,AIH肝硬化患者肝细胞癌的年发生率约为1%[14]。肝硬化本身和糖皮质激素治疗均会增加骨质疏松症的风险,因此推荐定期监测骨密度,并建议长期服用糖皮质激素的患者同时加用钙剂、维生素D和(或)双膦酸盐等预防骨质疏松。
关于长期免疫抑制治疗是否会增加实体肿瘤的发生风险,尚存在争议。然而,皮肤恶性肿瘤发生率的增加是明确的,因此建议避免阳光照射、应用防晒霜和定期进行皮肤检查。
接受抗代谢物免疫抑制药如硫唑嘌呤、麦考酚酸等治疗的患者,对全身性病毒感染(如巨细胞病毒和水痘-带状疱疹病毒)的易感性增加,因此可考虑进行相关疫苗的预防接种。同样,需考虑进行病毒性肝炎疫苗的相关免疫接种。免疫抑制患者应该避免接种活疫苗如黄热病疫苗。
妊娠期间可能会新发AIH。然而,妊娠期间肝损伤的新表现通常代表另一种过程。更典型的是,10%~20%原本确诊并控制良好的AIH患者在产后免疫重建过程中可能会表现为肝脏炎症复发[15]。来自一项大规模病例研究数据显示AIH患者大多数可以成功度过妊娠期。值得注意的是,临床专家认为在受孕、妊娠和母乳喂养期间,使用硫唑嘌呤是安全的[15]。
4 预后
AIH通常预后良好,几项队列研究结果显示,包括代偿期肝硬化在内的AIH患者,其生存率与普通人群相似[16]。然而,一项英国队列研究显示,AIH患者的生存率略低于普通人群[8]。尽管具有肝硬化的临床表现并不影响对糖皮质激素治疗的应答,但会影响预后。据报道,2型AIH和SLA/LP阳性者预后较差。
对于经治疗后获得长期缓解的患者何时停药,一直是该病治疗中的一个临床问题。停药后复发较为常见,一项针对1型AIH的研究显示,停药后10年内复发率为80%[17]。对于生化指标或组织学未获得持续缓解的患者,停药后基本都会复发。而复发可能会使疾病进展。因此,建议仅对生化指标、组织学均复常且无肝硬化的患者,可以尝试停药[1]。
▼参考文献
[1] European Association for the Study of the Liver. EASL clinical practice guidelines: autoimmune hepatitis. J Hepatol 63:971-1004.
[2]Manns MP, Czaja AJ, Gorham JD, et al. Diagnosis and management of autoimmune hepatitis. Hepatology 51:2193- -213.
[3] Cook GC,Mulligan R, Sherlock S. Controlled prospective trial of corticosteroid therapy in active chronic hepatitis. Q J Med 40:159- - 85.
[4] Czaja AJ, Wolf AM, Baggenstoss AH. Laboratory assessment of severe chronic active liver disease during and after corticosteroid therapy: correlation of serum transaminase and gamma globulin levels with histologic features.Gastroenterology 80:687- -92.
[5]Manns MP, Woynarowski M, Kreisel W, et al. Budesonide induces remission more effectively than prednisone in a controlled trial of patients with autoimmune hepatitis.Gastroenterology 139:1198- 206.
[6] Murray- -Lyon IM, SternRB,Williams R. Controlled trial of prednisone and azathioprine in active chronic hepatitis. Lancet 1:735- -7.
[7] Heneghan MA, Allan ML, Bornstein JD, Muir AJ, Tendler DA. Utility of thiopurine methyltransferase genotyping and phenotyping, and measurement of azathioprine metabolites in the management of patients with autoimmune hepatitis. J Hepatol 45:584- -91.
[8] Hoeroldt B, McFarlane E, Dube A, et al. Long-term outcomes of patients with autoimmune hepatitis managed at a nontransplant center. Gastroenterology 140:1980- -9.
[9] Zachou K, Gatselis NK, Arvaniti P, et al. Areal. -world study focused on the long- -term efficacy of mycophenolate mofetil as first-line treatment of autoimmune hepatitis. Aliment Pharmacol Ther 43:1035- - 47.
[10] Trivedi PJ, Hirschfield GM. Review article: overlap syndromes and autoimmune liver disease. Aliment Pharmacol Ther 36:517- -33.
[11]Czaja AJ, Carpenter HA. Decreased fibrosis during corticosteroid therapy of autoimmune hepatitis. J Hepatol 40:646- -52.
[12]Schramm C, Bubenheim M, Adam R. Primary liver transplantation for autoimmune hepatitis: a comparative analysis of the European Liver Transplant Registry. Liver Transpl 2010;16(4):461-9.
[13] Montano- -Loza AJ,Mason AL,MaM, Bastiampillai RJ, Bain VG, Tandon P. Risk factors for recurrence of autoimmune hepatitis after liver transplantation. Liver Transpl 15:1254- -61.
[14] Yeoman AD, Al Chalabi T, Karani JB, Quaglia A. Evaluation of risk factors in the development of hepatocellular carcinoma in autoimmune hepatitis: Implications for follow-up and screening. Hepatology 48(3):863- -70.
[15] HeneghanMA, Norris SM, O'Grady JG, Harrison PM,McFarlane IG. Management and outcome of pregnancy in autoimmune hepatitis. Gut 48:97-102.
[16] Roberts SK, Therneau TM, Czaja AJ. Prognosis of histological cirrhosis in type 1 autoimmune hepatitis. Gastroenterology 110:848- 57.
[17] MontanoLoza AJ, Carpenter HA, Czaja AJ. Consequences of treatment withdrawal in type 1 autoimmune hepatitis. Liver Int 27:507-15.