9月2日,FDA批准度伐利尤单抗联合吉西他滨和顺铂用于成人局部晚期或转移性胆道癌的治疗。
度伐利尤单抗是一种PD-L1检查点*制剂抑**,在美国已被批准用于治疗化疗后疾病无进展的不可切除Ⅲ期小细胞肺癌患者的治疗,2019年7月其也被获批用于广泛期小细胞肺癌的治疗。
FDA批准度伐利尤单抗联合化疗治疗胆道癌的适应证是基于随机Ⅲ期TOPAZ-1试验的结果。
该研究为国际双盲试验,纳入685例先前未经治疗的不可切除局部晚期、复发或转移性胆道癌患者,患者中位年龄为64岁,50%为女性,37%为白人,2%为黑人,7%为西班牙裔或拉丁裔。近一半(47%)的患者年龄在65岁或以上,56%的患者有肝内胆管癌。
研究人员随机按1:1的比例将患者分为吉西他滨和顺铂联合1500 mg Q3W的度伐利尤单抗,或者联合安慰剂。吉西他滨和顺铂的方案为:每3周为一周期,在第1天、第8天接受吉西他滨1000 mg/m2,顺铂25 mg/m2,持续8个周期。之后度伐利尤单抗1500 mg或者安慰剂,每4周一次,直至疾病进展或发生不可接受的毒性。研究设计见图1。
主要终点为总生存(OS),次要终点包括PFS、客观缓解率和安全性。

图1. TOPAZ-1研究设计
(图片引自2022 ASCO GI)
TOPAZ-1试验的结果在2022年ASCO GI上公布,西安交通大学第一附属医院李恩孝教授对该研究进行了点评。
TOPAZ-1试验结果显示,度伐利尤单抗联合化疗组的OS和PFS均有显著改善:中位OS为12.8个月 vs. 11.5个月,HR=0.8,95%CI:0.66~0.97,详见图2;中位PFS为7.2个月 vs. 5.7个月,HR=0.75,95%CI:0.64~0.89,详见图2。
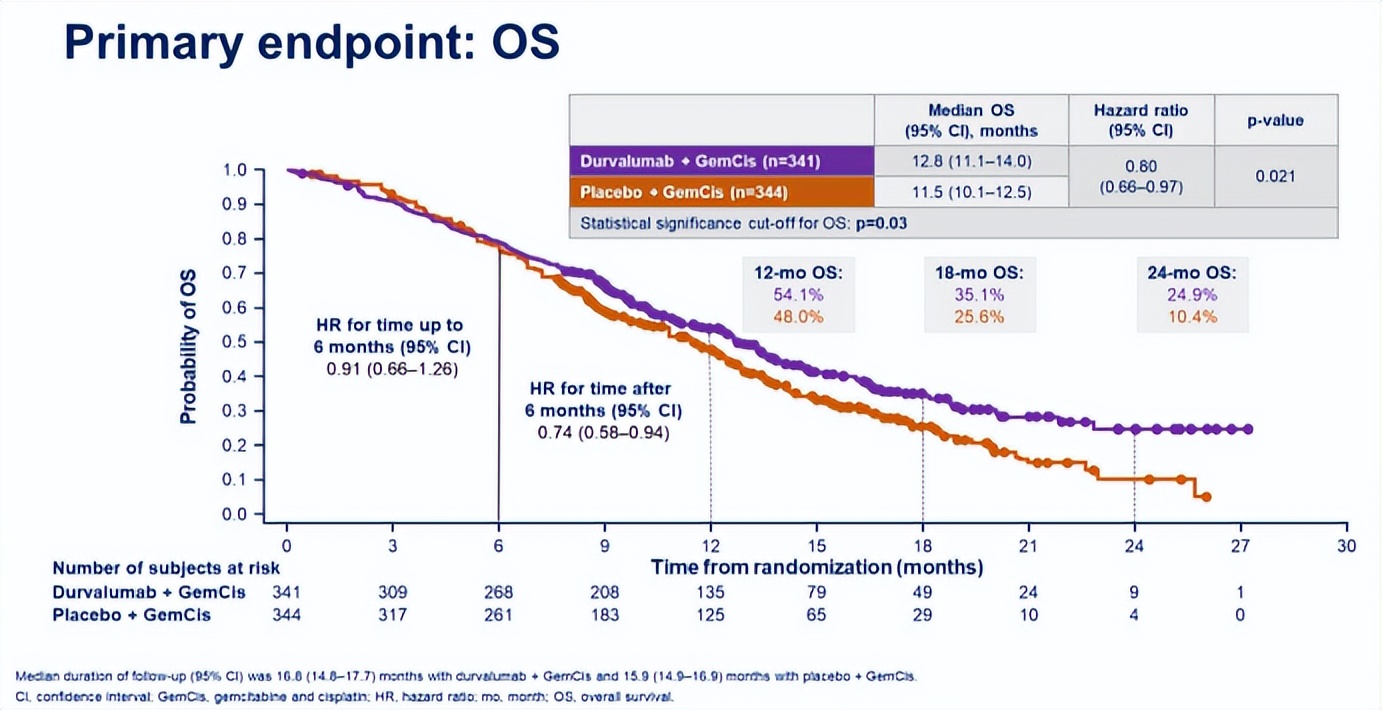
图2. 主要终点OS
(图片引自2022 ASCO GI)
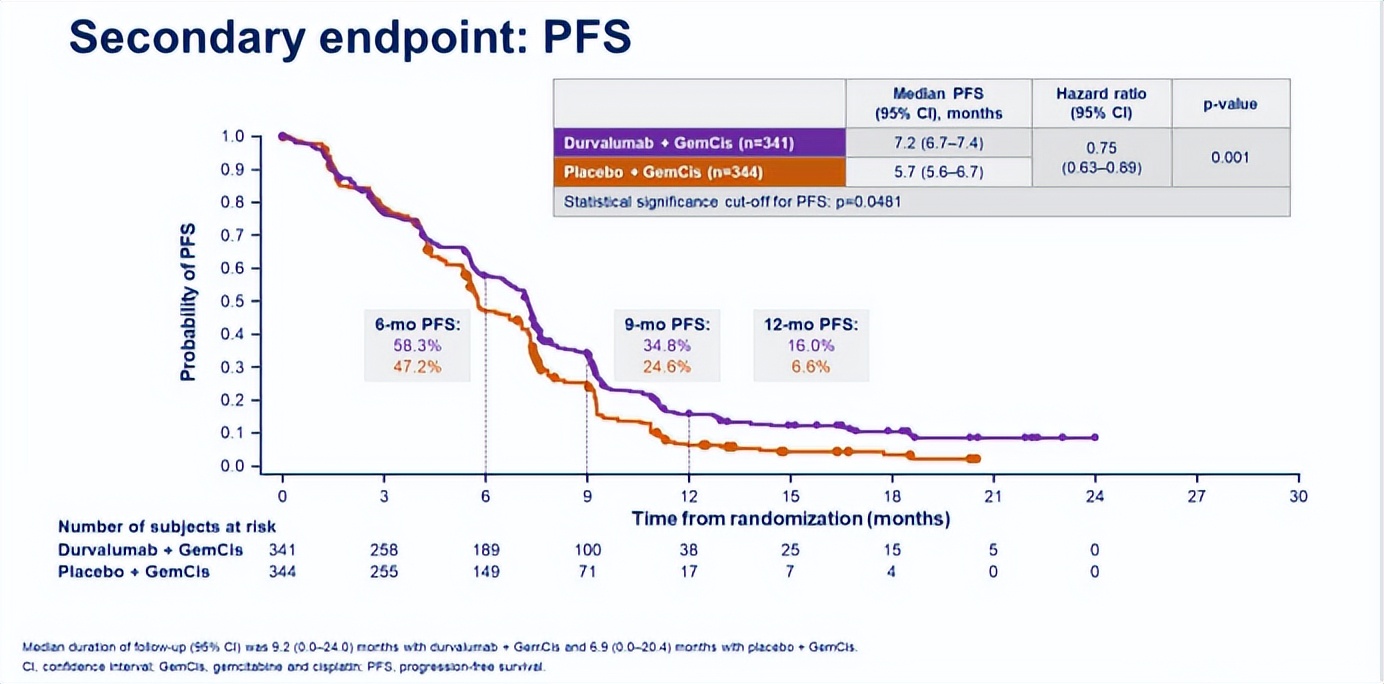
图3. 次要终点PFS
(图片引自2022 ASCO GI)
度伐利尤单抗联合化疗组的2年OS(24.9% vs. 10.4%)和ORR(26.7% vs. 18.7%)也更高,3~4级治疗相关不良事件(62.7% vs. 64.9%)和导致停用任何研究药物的不良事件(8.9% vs. 11.4%)的发生率更低。
最常见的不良事件包括疲劳、恶心、便秘、食欲下降、腹痛、皮疹和发热。
在2022年ASCO,以及欧洲肿瘤内科学会(ESMO)世界胃肠道肿瘤大会上,均有TOPAZ-1试验的相关结果更新。详情请点击:一线免疫治疗联合化疗可改善胆道系统肿瘤各原发肿瘤位置亚组预后。
需要说明的是,在Imfinzi的说明书中,对于体重≥30 kg的患者,当给予吉西他滨和顺铂时,推荐的度伐利尤单抗剂量为每3周1500 mg,随后每4周作为单药应用1500 mg,直到疾病进展或不可接受的毒性。而对于体重< 30 kg的患者,建议剂量为每3周20 mg/kg的度伐利尤单抗并联合吉西他滨和顺铂,随后每4周20 mg/kg,直到疾病进展或不可接受的毒性。
来源
FDA approves durvalumab for locally advanced or metastatic biliary tract cancer. www.fda.gov/