前两天中午听复旦肿瘤医院陈洁教授网上为患者举办的“内分泌肿瘤免费云会诊”,收获很多。同时,作为病理医生,听到她对病理报告提出的“批评”,也很不安。作为学习,也作为提醒自己和同行、患者,将陈教授建议的病理报告必须包含的内容总结如下。
1.一般情况下,神经内分泌肿瘤的分级及分类?
神经内分泌肿瘤起源于分布于全身的弥漫性神经内分泌系统的分泌细胞,因此可能出现在全身各处。此前,不同的部位神经内分泌肿瘤有不同的名称;但目前全身大部分系统的名称和分级均趋于一致,基本可以分为高分化神经内分泌肿瘤(NETs,分级为G1-G3)、低分化神经内分泌癌(NECs,包括大细胞癌和小细胞癌)和混合性神经内分泌-非神经内分泌肿瘤(MiNENs,两种成分均占总数的 30%以上的混合性肿瘤)。级别越高肿瘤的侵袭和转移潜能的风险也相应增加,预后相对较差,但一般小于1cm的肿瘤很少转移。
2.胃神经内分泌肿瘤分为哪些类型?
胃的神经内分泌肿瘤分为3种类型: I 型与自身免疫性萎缩性胃炎和胃酸过少、胃泌素升高有关,发病部位多位于胃底胃体, 胃镜检查时通常以多个小结节/息肉的形式出现 ;而 II 型可能和多发性神经内分泌瘤 (MEN) 1 型(综合征)患者有关,肿瘤常为 多灶性 ,胃可能并非原发,而是在其他部位,比如十二指肠或胰腺有更大的神经内分泌肿瘤存在,血清中胃泌素常常升高;III 型是散发性肿瘤,胃泌素不被认为参与其发病机制。
I 型和 II 型均与空腹 血清胃泌素浓度升高 有关,许多患者的病程相对缓慢,预后良好。高胃泌素血症对胃中的 肠嗜铬样内分泌细胞( ECL 细胞)有促进增殖作用,导致线性和微结节 神经内分泌细胞增生,最后发展成为肿瘤。
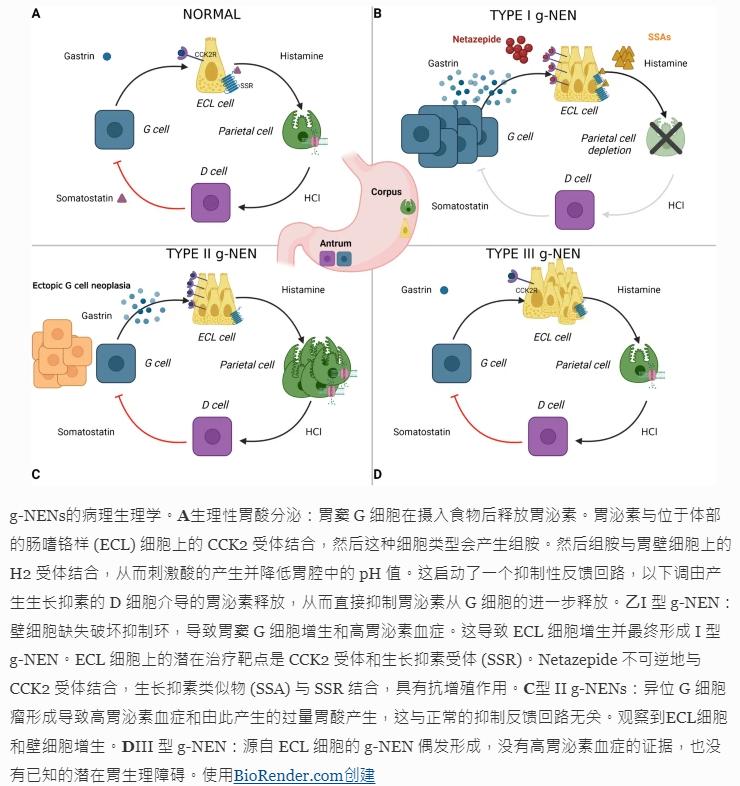
各型NEN形成示意图: New Developments in Gastric Neuroendocrine Neoplasms. Curr Oncol Rep 24, 77–88 (2022).
3.不同类型的内镜特点、临床需要的检查指标、预后及相应处理
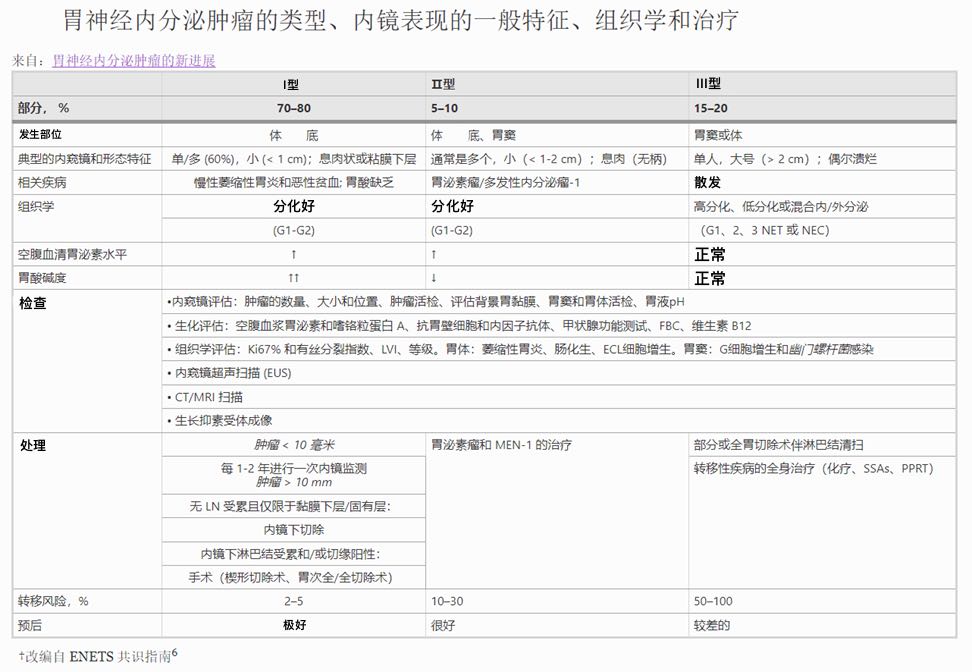
各型NEN特征及预后: New Developments in Gastric Neuroendocrine Neoplasms. Curr Oncol Rep 24, 77–88 (2022).
4.患者管理建议
I型: 欧洲神经内分泌肿瘤协会 (ENETS) 指南建议对大多数 I型肿瘤进行保守治疗,进行定期的内镜检查和组织学评估。指南建议每年或每 2 年对 I 型进行内镜监测,并对息肉进行活检,对于直径超过 10 毫米的病变,建议进行内镜切除。可能会有 50% 的患者出现多次复发。高 空腹血清胃泌素浓度 更可能与疾病进展有关。手术的方式包括内镜下剥除、内窥镜黏膜切除术 (EMR) 和内窥镜黏膜下剥离术 (ESD) 。Netazepide 是一种胃泌素/CCK2 受体拮抗剂,可作为治疗高胃泌素血症相关疾病的一种潜在的新型治疗方法;生长抑素类似物 (SSAs)可抑制胃泌素释放, 可对多发或经常复发的疾病而无法通过内镜随访或切除术安全管理的选定患者中进行应用。
III 型: 以部分或全胃切除及淋巴结切除的手术仍然是推荐的治疗方法。由于疾病发现的更早以及内镜手术的进步,目前手术楔形切除或内窥镜下的局部切除也是是一种合适的治疗选择:高分化、低级别(G1- 2 级)、 Ki67 指数 < 10%、肿瘤小于 10(或可能为 15)mm,浸润深度局限于黏膜下层,无 LVI 证据。
II型:主要是注意寻找胃外的原发灶并进行切除。
5.如果病理及临床检查时缺少相关内容,怎么办?
如果是病理是缺少对相关内容的评估(对照表2内容),这个比较好解决:请去手术医院的病理科,提出要求,希望完善相关检测,比如评估周围胃粘膜是否有萎缩的状态、壁细胞是否有增生、HP的检查。
临床中如果血清胃泌素术前并未检测,术后的胃泌素也可以进行;如果术后胃泌素都没有下降/仍然很高,要告诉怀疑II型内分泌肿瘤的可能;另外,需要注意的是PPI*制剂抑**会反馈性引起胃泌素水平升高,因此,也可能导致胃底多发息肉的形成。
其他,包括内镜超声、CT等的检查根据指南进行。
如果就医的医院,没有相关的检查就对您进行治疗或者都是建议大部胃切除,建议先不着急治疗,去比较规范的医院进行咨询就诊后再做决定。