诱导多能干细胞 (iPSC) 是成体细胞经过重编程进入多能状态的一种细胞,它可以分化出多种细胞和组织类型。近年来,以细胞医疗为代表的再生疗法, iPSC在组织器官损伤,神经退行性疾病以及多种难治性疾病的治疗中发挥了重要作用。
01
iPSC治疗神经遗传性疾病
ipscs可以通过暴露于生长因子和细胞培养条件下,诱导分化成神经元和胶质细胞,以及其他最终分化的细胞类型。因此研究人类中枢神经系统神经元谱系成为可能。
1.1 遗传性神经发育障碍
遗传性神经发育障碍包括一系列以发育过程中神经元功能障碍为特征的疾病。科学家们已经从神经发育性疾病的患者中培育出疾病特异性的ipscs,包括Rett综合征、脆性X染色体综合征、唐氏综合征、安杰尔曼综合征、普瑞德-威利综合征和蒂莫西综合征(表1)。基于ipsc的神经发育障碍模型概括了遗传背景下与特定疾病相关的神经发育的早期步骤, 并能有助于识别潜在的细胞和分子机制,建立新的治疗方法。
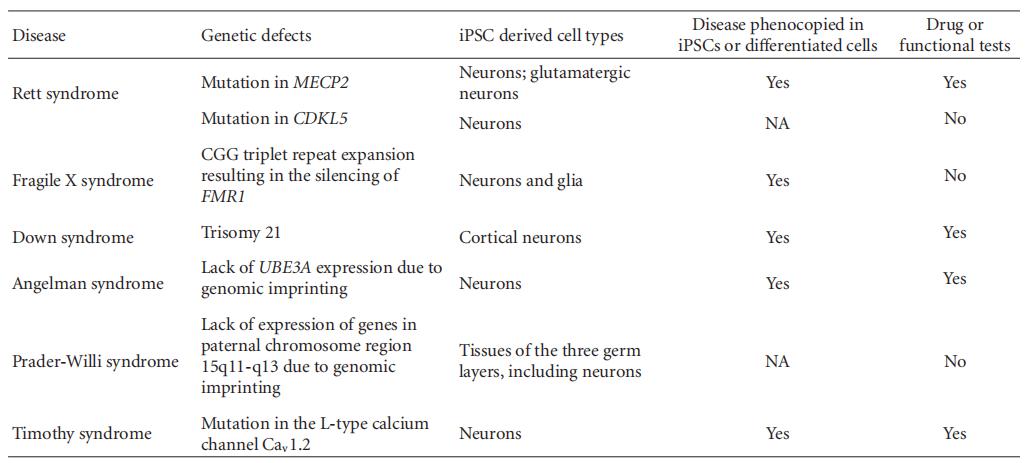
表1 遗传神经发育障碍的ipsc建模
1.2遗传性神经退行性疾病
遗传性神经退行性疾病包括各种涉及神经元结构和功能的慢性和进行性丧失的疾病。迄今为止, 科学家们已经从许多神经退行性疾病的患者中培育出ipscs, 包括脊髓肌肉萎缩、家族性自主神经功能异常、肌萎缩性侧索硬化症、亨廷顿病、弗里德里奇共济失调、马查多-约瑟夫病、x-连锁肾上腺脑白质营养不良、阿尔茨海默病和帕金森病(表2)。
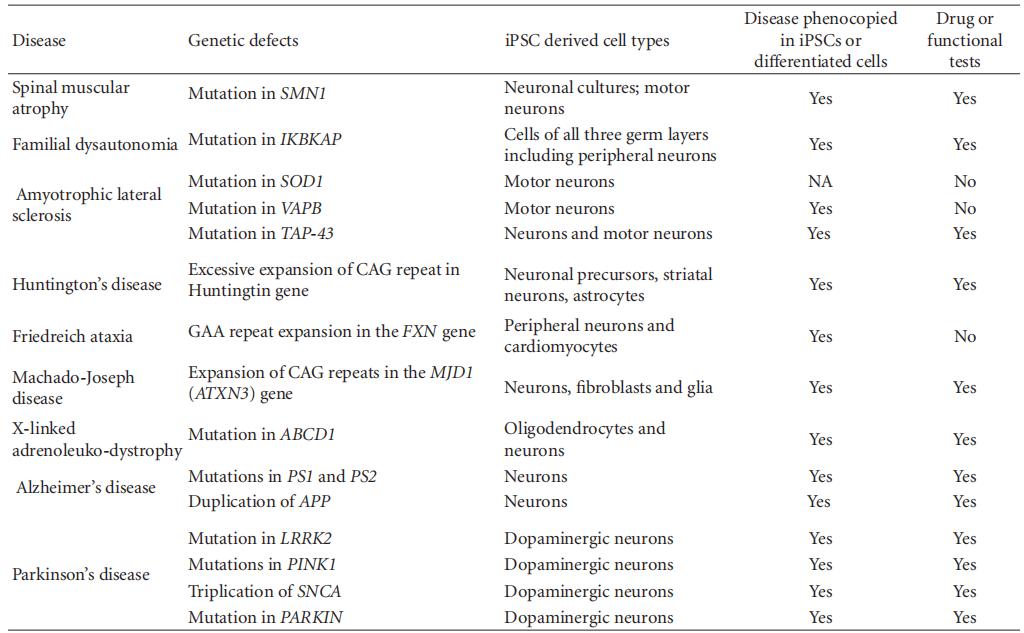
表2 遗传性神经退行性疾病的ipscs建模
02
iPSC治疗心脏类疾病
成人心脏无法修复缺血性损伤导致的心肌受损。近年来,ipsc和ipsc来源的心肌细胞使补充心脏的功能细胞成为了可能。ipsc来源细胞的治疗效果已进行了许多临床前研究,然而,ipsc来源的细胞治疗的潜在机制仍不是很清楚。一个可能的机制是移植细胞的旁分泌作用。 ipsc来源的心肌细胞分泌的外泌体等微囊泡通过转移内源性分子、调节细胞凋亡、炎症、纤维化和血管生成来挽救损伤的邻近细胞,从而发挥保护作用 (图3)。
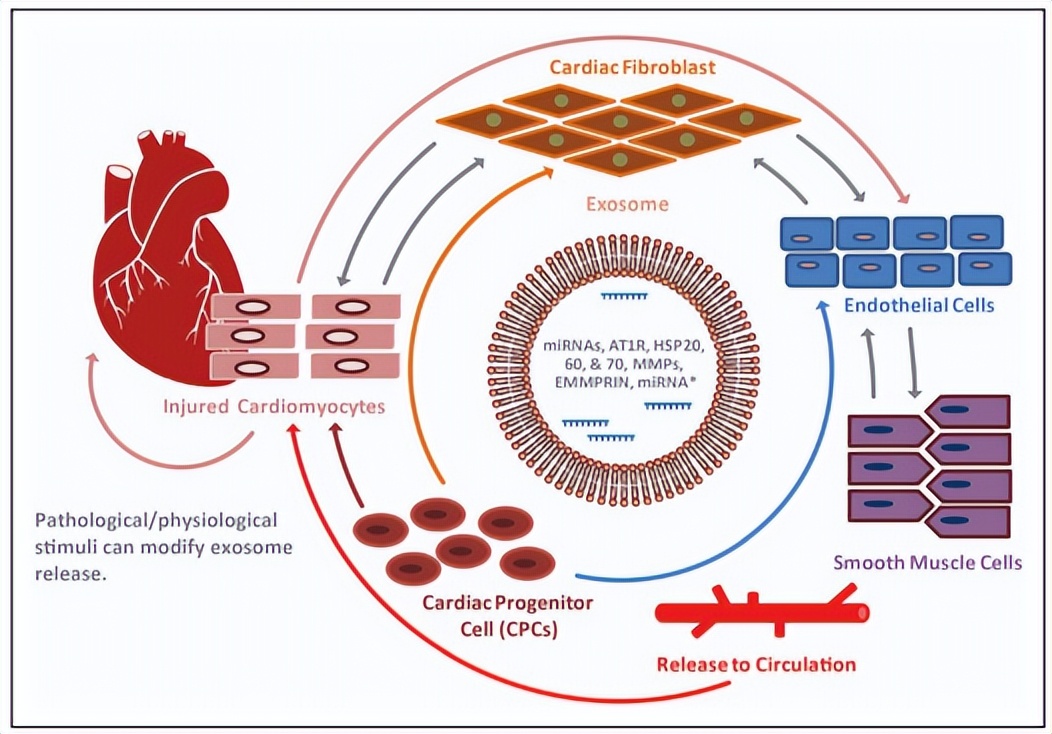
图3 外泌体介导的心脏细胞间通讯
2020年9月,日本卫生部批准了庆应义塾大学(Keio University)的一项临床研究项目,该项目将利用iPS细胞制备的心肌细胞移植到心脏病患者体内。由福田恵一(Keiichi Fukuda)教授领导的团队对3名年龄在20至74岁之间的扩张型心肌病患者进行移植手术。
2020年1月,大阪大学进行了由iPS细胞制成的心肌细胞移植。心肌细胞被制成薄片,粘贴在病人心脏的表面,这样它们释放的物质可以帮助心肌再生。然而,细胞本身消失得很快。与此同时,庆应大学在猴子身上进行的一项实验中证实 ,移植后的细胞在体内定植,心脏功能得到改善。
2020年5月,Nature杂志报道,两位终末期心衰患者在中国接受了世界首例基于“重编程”干细胞的心衰治疗,并在一年后康复出院。据悉,患者于2019年5月在南京鼓楼医院注射了从iPS细胞分化得到的心肌细胞,手术由该院心胸外科主任王东进教授完成。这是已知的全球首个用于治疗受损心脏的iPS技术的临床应用。
03
iPSC治疗血液类疾病
最初的血液疾病建模主要集中在两种主要疾病中,镰状细胞性贫血和白血病。表4总结了更多关于血液疾病ipsc疾病建模的报告。在造血系统疾病的诱导多能干细胞疾病建模的初步试验中,科学家们使用了血液干细胞,如骨髓(BM)、脐带血(CB)、骨髓来源的间充质干细胞来生成诱导多能干细胞。 相对于完全成熟的细胞,高度增殖的体细胞血干细胞是重新编程的更好来源。
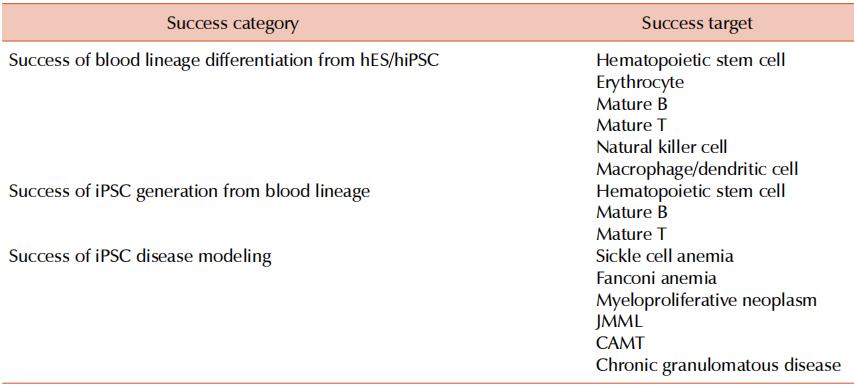
表4 非体细胞人多能干细胞在造血系统研究中的应用
Ye及其同事报道了一种来自骨髓增生性肿瘤(MPN)患者的含有诱导多能干细胞的JAK2α-V617F突变。他们使用CB和BM(CD34+)细胞产生ipscs,随后分化为血液祖细胞(CD34+CD45+)。Raya等还提供了来自范可尼贫血、血液疾病患者的ipsc疾病模型。
青少年骨髓单核细胞白血病(JMML)ipsc疾病建模显示了更先进的血液疾病建模的特征。
研究人员使用独立的含有PTPN11(E76K)错义突变的男性JMML患者血液样本,研究人员生成了诱导多能干细胞。利用诱导多能干细胞的造血谱系来测试概念药物筛选。从JMML患者来源的ipsc中,研究人员发现,激活的MEK和JAK1/2通路可能是未来治疗的一个靶点。
Hirata团队构建了先天性巨核细胞血小板减少症(CAMT)患者来源的ipsc,从而进行CAMT疾病建模。 Hirata团队发现,与正常ipsc相比,患者ipsc来源的造血分化最终占血小板数量的不到1%。逆转录病毒在缺陷的ipsc中引入正常的MPL基因(血小板生成素受体)导致了另一个关于血小板生物学的发现。与正常ipsc组相比,CAMT诱导多能干细胞来源的血液祖细胞中Fli1基因活性显著增加,这给科学家们寻找治疗CAMT可能的下游途径指明了方向。
04
iPSC治疗糖尿病
Yasushi Kondo团队以参与胰腺发育的关键转录因子的表达为指标,在体外模拟和复制胰腺的正常发育阶段, 从而诱导hESCs/ipscs分化为胰腺谱系细胞。 如图5所示,受精卵通过多个发育阶段,如最终内胚层、原始肠管、后前肠、胰腺内胚层和内分泌前体,分化为表达胰岛素的β-细胞。
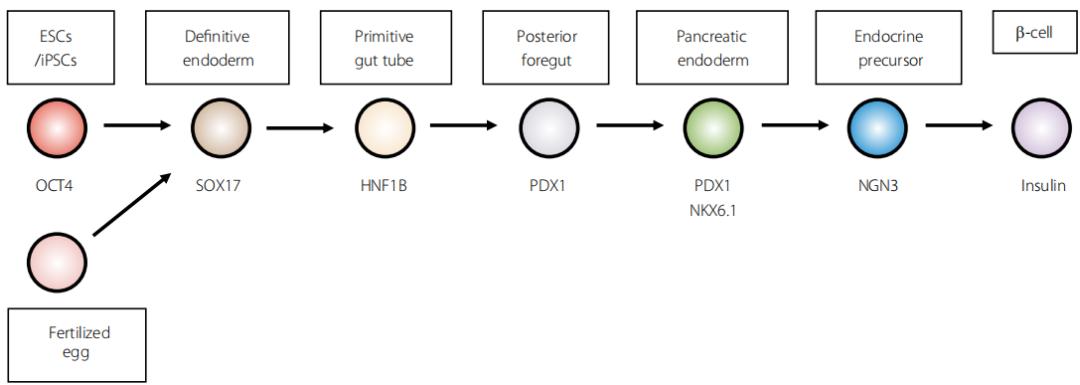
图5 通过模拟体内发育,从人类胚胎干细胞和诱导多能干细胞(hESCs/ipscs)中产生胰腺内分泌谱
05
iPSC治疗癌症
2020年10月22日,日本研究人员日前实施了一台移植免疫细胞治疗癌症的手术,用于移植的免疫细胞由ipsc培养而来。这是日本首次尝试利用ipsc治疗癌症。
千叶大学和理化学研究所的一个研究小组对一名头颈部恶性肿瘤患者实施了自然*伤杀**T细胞(NKT细胞)移植手术。手术采用注射形式,向患者癌组织附近血管一次注射约5000万个NKT细胞。首次注射后患者情况良好,患者还将接受两次注射。NKT细胞是一种可对癌细胞发动高效攻击的免疫细胞,但人体内仅有少量这种细胞。
研究人员从健康人的血液中采集NKT细胞并培育出ipsc,再使ipsc分化增殖出大量NKT细胞后注入患者体内。 ipsc是通过对成熟体细胞“重新编程”培育出的干细胞,拥有与胚胎干细胞相似的分化潜力。 研究小组计划2022年3月前对4至18名接受标准治疗后病情复发的头颈部恶性肿瘤患者进行同样的免疫细胞移植手术,以确认这种疗法的安全性和有效性。
06
iPSC构建肝癌模型
日本冈山大学研究生院的研究团队,利用分泌多种炎症性物质的人肝癌细胞株培养上清液,培养了小鼠的ipsc,并将ipsc诱导为癌症干细胞,然后将癌症干细胞移植到裸鼠的肝脏中,成功制作了肝癌模型。 本次研究无需实施基因突变和插入缺失等操作,即完成了认为形成特定肿瘤,这是世界首次成功制作出肝癌模型 (图6)。
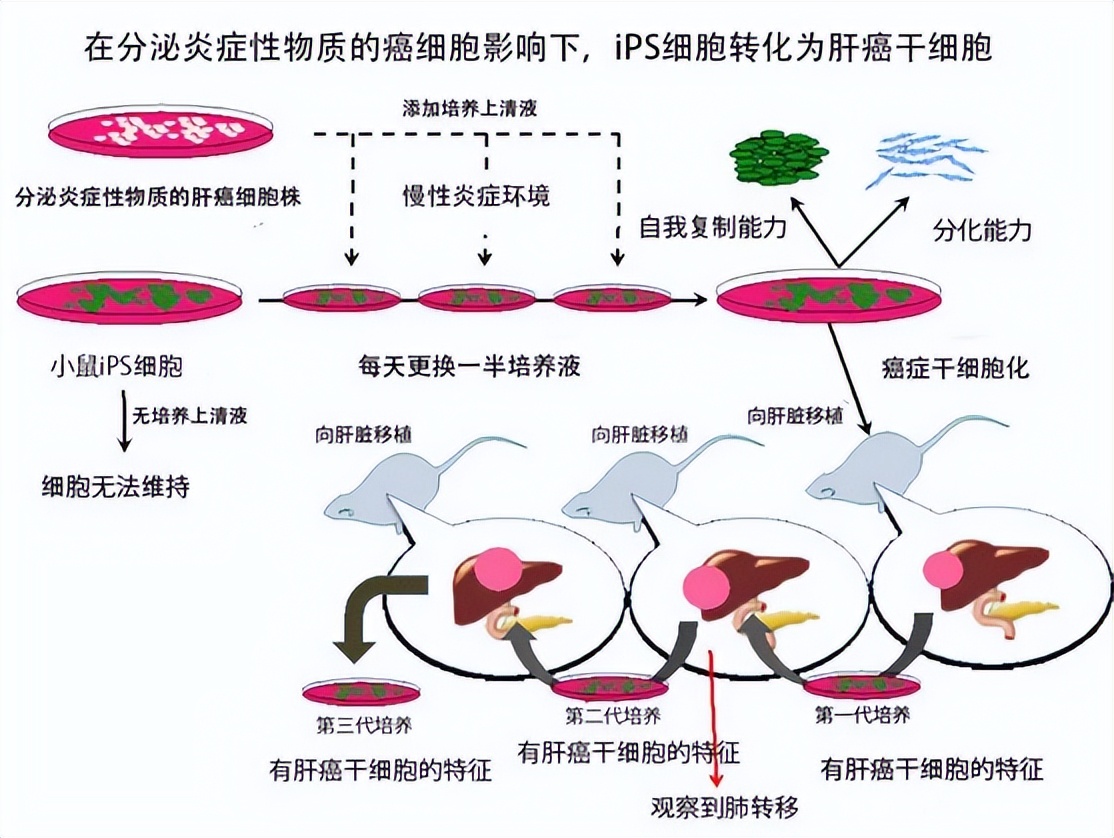
图6 在分泌炎症性物质的癌细胞影响下,ipsc转化为肝癌干细胞
07
iPSC在中风领域应用
有研究表面ipsc可以恢复中风大鼠的运动感觉能力,报道通过重新编程人类皮肤细胞成为神经细胞,再移植到大鼠的大脑里, 这种方法能够恢复运动能力和触觉。
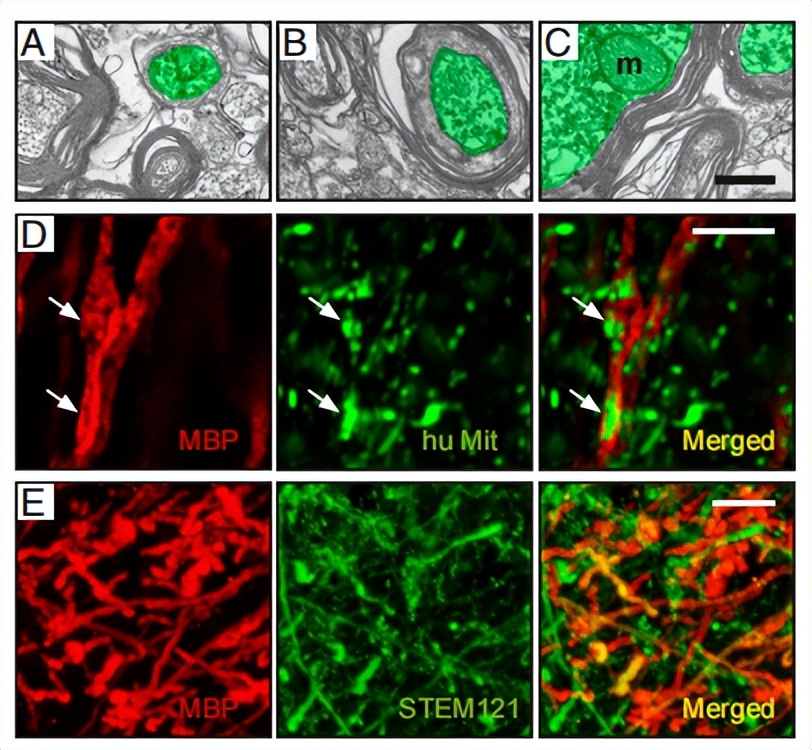
图7 移植六个月后的共聚焦显像
轴突髓鞘形成发生在不同阶段,髓鞘部分来源于人来源的少突胶质细胞。(A-C)对侧体感皮层的移植物衍生轴突。(A)初始和(B)髓鞘形成的中间阶段。(C)轴突,髓鞘致密。M:线粒体。(D)通过MBP(红色)和人类线粒体标记物(绿色)的共定位证明,移植物附近由人类髓鞘包裹的轴突的共聚焦图像。(E)表达人类细胞质标记STEM121(绿色)并与MBP(红色)共定位的移植物衍生纤维的共焦图像(图7)。
08
iPSC改造视网膜感光细胞
由CIRC Therapeutics公司视网膜创新中心眼科专家Sai Chavala博士领衔的科研团队,开发出一种技术,把皮肤细胞直接改造成视网膜的感光细胞——感受光的神经细胞。 将这种改造后的细胞移植到小鼠眼睛中,失明小鼠得以重见光明 (图8)。
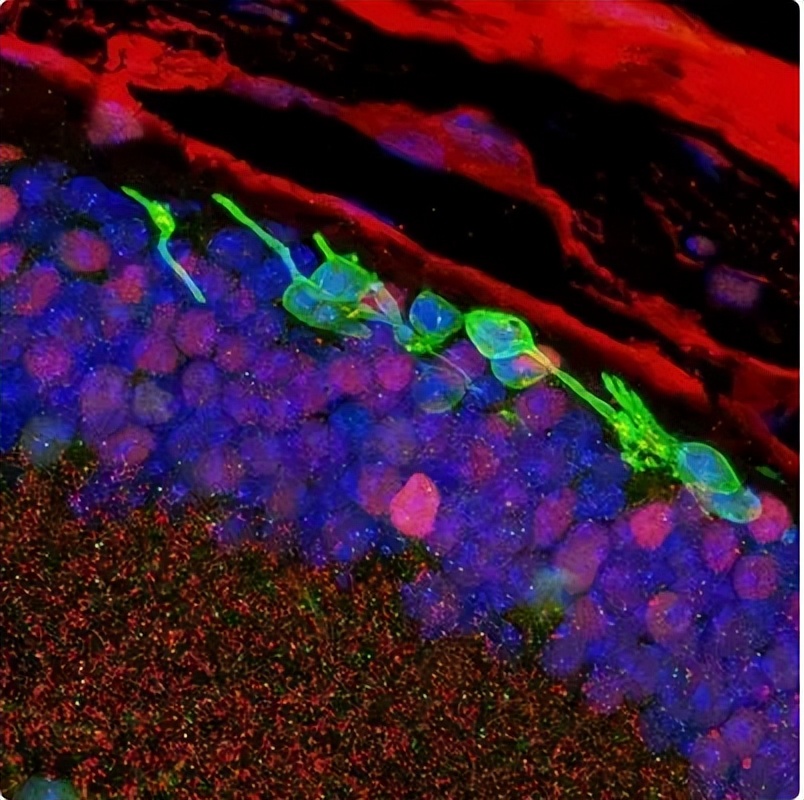
图8 移植3个月后,依然存活的CiPCs(绿色)整合进小鼠的视网膜
参考资料:
[1] FDA: Market access of cellular and gene therapy products in the US and EU
[2] Rowe R Grant,Daley George Q,Induced pluripotent stem cells in disease modelling and drug discovery.[J] .Nat. Rev. Genet., 2019, 20: 377-388.
[3] Liu Chun,Oikonomopoulos Angelos,Sayed Nazish et al. Modeling human diseases with induced pluripotent stem cells: from 2D to 3D and beyond.[J] .Development, 2018, 145: undefined.
[4] Wang, H.; Doering, L.C.; Induced Pluripotent Stem Cells to Model and Treat Neurogenetic Disorders. Neural Plast. 2012, Jul(19).
[5]Kim, C. Disease modeling and cell based therapy with ipsc: future
therapeutic option with fast and safe application. Blood Research 2014, 49, 7-14.
[6]http://xw.qq.com/cmsid/20210301A07EK200
[7]Kondo, Y.; Toyoda, T.; Inagaki, N. ipsc technology-based regenerative therapy for diabetes. J Diabetes Investig 2018, 9, 234-243.
[8]Afify, S. M.; Calle, A. S.; Hassan, G. A novel model of liver cancer stem cells developed from induced pluripotent stem cells. Br J Cancer 2020, 122(9), 1378-1390.
[9]Tortosaa, S. P.; Tornero, D.; Hansena, M. G.; et al. Activity in grafted human iPS cell–derived cortical neurons integrated in stroke-injured rat brain regulates motor behavior. PNAS 2020, 117(16), 9094-9100.
[10]Mahato, B.; Kaya, K. D.; Fan, Y.; et al. Pharmacologic fibroblast reprogramming into photoreceptors restores vision. Nature 2020, 581, 83–88.
[11]https://zhuanlan.zhihu.com/p/153146713
[12] Dashtban M , Panchalingam K M , Shafa M , et al. Addressing Manufacturing Challenges for Commercialization of ipsc-Based Therapies[J]. Methods in molecular biology (Clifton, N.J.), 2020.
[13]曹佳妮, 李晓燕, Lu X , et al. Cells Derived from ipsc Can Be Immunogenic - Yes or No?[J]. 2014.
[14] Huang C Y , Liu C L , Ting C Y , et al. Human ipsc banking: barriers and opportunities[J]. Journal of Biomedical Science, 2019, 26(1).