同时发现了多个高危肺部病灶后如何处理,将来会怎样,这是不是个很令人焦虑的问题呢,本文将聚焦这些问题进行解答。
流行病学调查显示,肺癌在各种肿瘤中的发生率及死亡率均占据首位。随着时代发展,肺癌的流行病学也有新的特点。
多原发肺癌(multiple primary lung cancer, MPLC)是指同一患者肺部同时或异时发生≧2个原发肺癌。1924年已有学者提出MPLC的概念,随着近年胸部CT检查技术的发展和人群癌症筛查意识的增强,MPLC患者数量快速增加。而且,以非小细胞肺癌为主的肺癌的临床特征及诊疗方式也发生了巨大的变化,表现为从“中心型“病变向“周围型“病变的转变、鳞癌向腺癌的转变、单发病灶向多发病灶的转变。
目前,广为使用的临床鉴别依据是Martini-Melamed诊断标准。
同时性肺内多原发性癌(synchronous MPLC, sMPLC) 的诊断标准是:1.双肺同时发生或在间隔6个月以内发生病变;2.经病理诊断证实是恶性肿瘤,其组织学类型不同,组织学类型相同时:位于不同肺段、肺叶,不同侧肺,由不同的原位癌起源,肺癌共同的淋巴引流部位无癌肿,确立诊断时无肺外转移;3.除外复发和转移。
异时性多原发肺癌(metachronous MPLC, mMPLC) :1.组织学类型不同;2.组织学类型相同时:无瘤间期至少2年,或均由不同的原位癌起源,或第二原发癌位于不同肺叶或不同侧肺时,肺癌共同的淋巴引流部位无癌肿,确立诊断时无肺外转移。这一基于临床指标的判断标准有很强的实用价值,但其较为粗略。
现阶段,胸外科处理最多的是同时性多原发肺癌。
sMPLC领域仍有诸多尚未得到解答的问题。术前如何明确诊断并制定手术方案、如何进行个体化的随访和治疗,多原发肺癌分子特征有何特异性,是临床需要解决的问题。
一.sMPLC的术前诊断
肺既是容易发生原发癌,也容易发生转移的器官。在诊断sMPLC的过程中,先要排除肺转移的情况,而sMPLC大多为早期癌,术后5年生存率较高。鉴于MPLC以肺腺癌居多,2013年美国胸科医师联盟(American College of Chest Physicians, ACCP)推荐利用肺腺癌的组织学亚型鉴别MPLC与肺内多发转移,还提出使用分子遗传学分析进行辅助判断,即利用特异的分子标志物或基因突变位点加以鉴别[14]。研究者们开始试图利用不同的分子遗传学指标来协助MPLC的诊断,基因拷贝数[15]、杂合性丢失(loss of heterozygosity, LOH)[16]、EGFR/Kras突变状态、微卫星标记等位基因变异等,但是上述研究的样本量均较小,且实施具有一定的技术难度,尚得到广泛认可的方案。因此ACCP指南建议仍需综合考虑临床特点及影像学特征鉴别MPLC和肺内转移。目前尚无诊断MPLC的金标准,多灶性肺癌也无统一分期标准。第8版肺癌分期系统首次单独描述多灶性肺癌。按临床病理特点,多灶性肺癌可分成4种类型,分别是第二原发肺癌、多灶磨玻璃样/附壁样成分肺腺癌、伴有卫星结节的实体肺癌和炎性肺癌。前两者为MPLC,后两者为肺癌肺内转移。
对同时性多原发肺癌的病灶,术后的病理类型多为腺癌,螺旋CT具有很好的空间分辨力及密度分辨力,有利于观察结节内部及周围的细节征象,对鉴别诊断很有帮助。目前临床上术前对sMPLC的诊断及鉴别主要仍依赖于胸部CT,MPLC的各癌灶大多具有原发性肺癌的典型CT表现,多为孤立的,如密度混杂(如磨玻璃样或实性)、边缘毛刺、胸膜牵拉、分叶、血管集束征、增强窗可见强化等,而且肿瘤倍增时间较长,可以作为鉴别转移癌的影像学依据。
各个肿瘤具有独特的病理形态特征为诊断MPLC的要点。
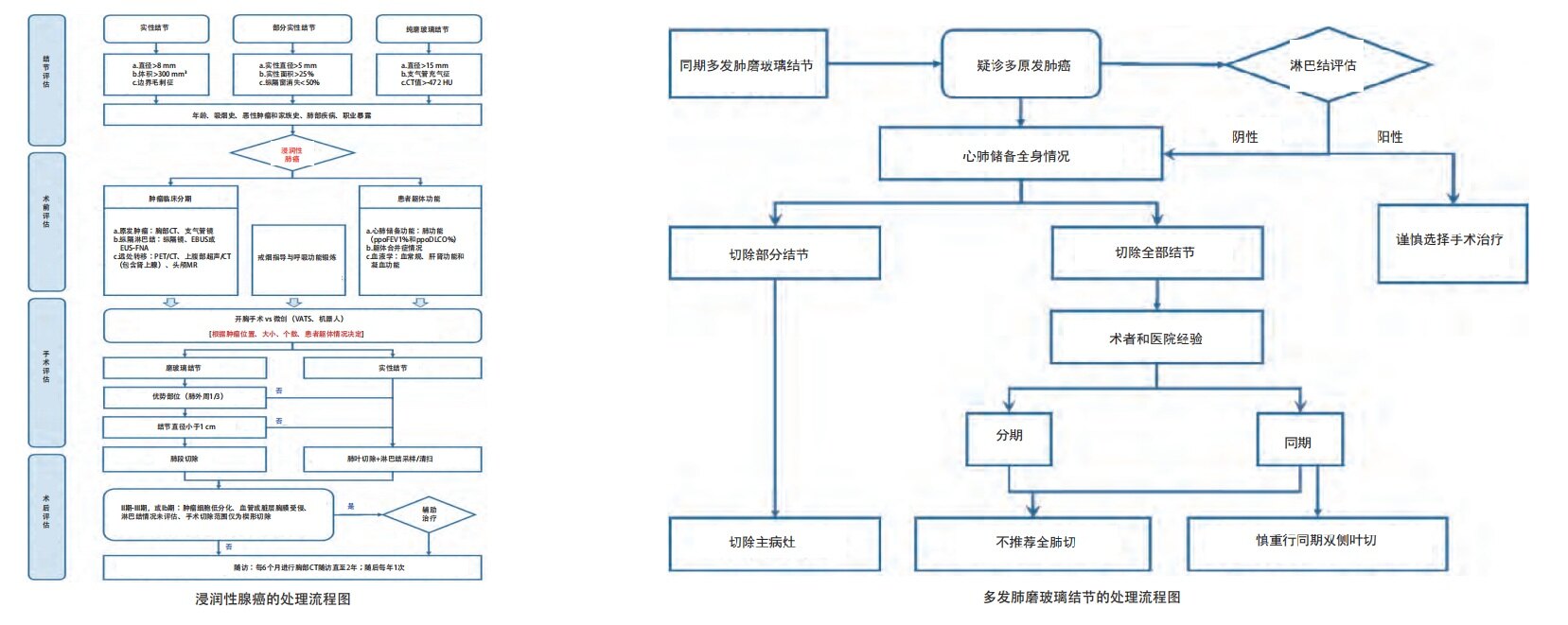
图片描述
二.sMPLC的治疗
目前,关于多原发肺癌的治疗还没有权威指南, 但大多数肺癌中心的报道认为积极的手术切除依然是治疗多原发肺癌最有效的方法,如Mun等报道I期sMPLC 5年生存率可高达75.8%,远高于晚期肺癌的生存率,故对肺多原发癌应尽量争取及时手术切除以求获得最佳疗效。目前的外科治疗原则:与单发肺癌一样,手术应遵循肿瘤外科治疗的两大基本原则,即最大限度地切除肿瘤组织,同时最大限度地保留正常肺组织。
同时性多原发肺腺癌因涉及多个病灶的治疗策略是 :1.在无手术禁忌证的情况下尽可能手术治疗;2.尽可能完整有效地切除肿瘤;3.尽可能多地保留健康肺组织;4.术后应采取多学科综合治疗,以提高生存率。
然而, 如何准确的识别主病灶,“同质性”的多发结节如何准确的处理,哪些结节需要手术处理,具体的手术方式,哪些结节可以保留、观察,淋巴结清扫术或淋巴结采样术对于不同类型的sMPLC是否必要,同期手术或分期手术的选择,现仍缺乏外科手术的标准 。
2013年一项Meta分析总结了影响MPLC根治术后的预后影响因素。该项研究共计纳入467例患者,大部分患者(67%)多病灶具有相同病理类型,有一半的肿瘤位于同侧。大多数患者有2个病灶,11%的患者有≧3个病灶。患者中位生存时间52个月,这一结果更接近早期肺癌而非转移性肺癌。不良预后分析中,N2是最主要的不良预后因素。尽管肺叶切除是肺癌根治的首选术式,楔形切除术或肺段切除术可能导致更高的局部复发率,但亚肺叶切除能更大程度保留患者肺功能,因此仍广泛应用于MPLC的外科治疗中。Guo等认为,病灶>2cm的sMPLC预后明显差于病灶<2cm者,所以建议对这部分患者的较大病灶施行肺叶切除及系统性淋巴结清除术,较小病灶行亚肺叶切除术,必要时辅以化学治疗或靶向治疗;对于<2cm的病灶或病灶≧3个的患者,尽可能行亚肺叶切除术;对于病灶位于双侧者,优先行分期手术,但目前分期手术间隔时间并无统一定论。sMPLC的手术原则应当遵循先切除分期较晚、对预后影响较大病变,再处理其他病变。同时,条件许可时行多病灶基因检测,以确定病灶间关系,并为日后可能的靶向治疗提供依据。
三. sMPLC的预后及基因组学研究
目前的肿瘤-淋巴结-转移(tumor-node- metastasis, TNM)分期系统并不能完全正确地的反映sMPLC的生存和预后。现在的处理方式是将多发病灶单独分期,分期较高者作为患者最终分期。回顾性研究发现,MPLC预后远好于肺内转移瘤。
然而,每个原发肿瘤都有其自身发展过程,虽是“同时“发现,但可能处于不同的发展阶段,其组织学类型也可能会有所不同。恶性肿瘤患者本身具有多发癌的倾向,在发病机制上多数学者支持“多中心性起源“的概念,有研究证明已发生恶性肿瘤的个体再次发生新的原发肿瘤的危险是正常人的1.29倍,两者之间的关系有待进一步的研究。
相比于同样分期的单发肺癌,sMPLC是否更容易出现新发肿瘤、肿瘤复发或转移的情况,现在缺乏数据,如何进行术后随访、哪些患者可能需要术后辅助治疗,现在仍没有标准。 需要进一步了解MPLC的分子特征,其病理标本做基因突变检测,为术后辅以靶向治疗提供应用指证。
随着二代测序的普及,近几年有研究通过全基因组或外显子测序方式从肿瘤异质性和基因进化角度对MPLC进行分析。有学者通过对MPLC的全外显子测序认为MPLC存在很大的肿瘤异质性。另外一些学者则通过研究证实MPLC多个病灶间扩展进化和趋同进化并存,分子靶向治疗可能在MPLC治疗中发挥重要作用。通过对早期多发磨玻璃样肺腺癌进行全外显子测序发现,磨玻璃样肺癌多病灶间存在相同的克隆,推测早期肺腺癌可能通过气腔播散形成肺内转移。
这些研究都说明,sMPLC的分子特征与单原发肺癌可能存在不同,导致肿瘤的生物学特征不同。
多原发肺癌进化及各克隆灶的形成是一个长期复杂的过程,理论上多原发肺癌的克隆性形成一般是基于癌基因或抑癌基因发生体细胞突变,如p53点突变、X染色体失活或杂合性丢失( LOH) 等。因此应该存在某一个或多个基因标志物,独立且突变率发生较高,出现较早且贯穿于整个过程,而在肺癌进化过程中各克隆产生了不同的体细胞突变。抑癌基因 p53的突变在肺癌中十分常见,且大多是点突变,在非小细胞肺癌中 ( NSCLC) 高达50%,可能符合多原发肺癌标志物的要求。另外,X染色体基因失活( X- inactivation) 也可用于检测克隆与肿瘤间的联系,不过这种技术仅用于女性患者。杂合性丢失( LOH) 为一个多态位点从种系杂合性到纯合性的转变,丧失一个等位基因标志。LOH分析方法是依靠单核苷酸多态性和微卫星基因型的比较或肿瘤 DNA 样本和病例匹配正常非瘤组织中获取 DNA 样本的比较。
2017 年在《新英格兰杂志》发表了一项大样本的非小细胞肺癌( 可切除的ⅠA至ⅡA 期 NSCLC患者) 的研究报道,通过对327个区域进行了全外显子组测序发现 EGFR、MET 和 BRAF突变大部分属于早期突变和克隆性突变,而参与 DNA 损伤修复等维持基因组完整性的基因,如PIK3CA、NF1、TP53和Notch在75%以上的肿瘤发生突变,并且时间轴上发生较晚,另外 CDK4、FOXA1和BCL11A的扩增,基因拷贝数的异常导致染色体不稳定性,这与肿瘤复发有着重要的相关性。 可能提示多克隆灶在肺癌早期在相同的致癌环境,产生了某一个或多个基因的高频点突变 。因此通过全外显子测序,对肺癌克隆的进化机制的阐明,起着关键作用,而通过多原发肺癌各配对癌症进行二代测序研究,将对肺癌的发生的异质性、演变、治疗及耐药等方面的研究具有重要意义。现阶段无大样本的后续研究,可能成为今后研究热点之一。
随着CT肺癌筛查项目的普及和对多原发肺癌认识的提高,多灶肺癌的检出率逐渐上升。通过分子遗传学检测将有助于多原发肺癌与肺内转移的鉴别,从而为多灶肺癌的诊断和分期及治疗做出贡献。目前,大多数肺癌中心的报道认为积极的手术切除依然是治疗多原发肺癌最有效的方法,可以预期,随着MPLC研究的广泛展开和不断深入,将会有更加合理规范的指南以引导临床实践。