病例优赏丨一例Ⅲ期鼻咽癌患者接受同步放化疗联合斯鲁利单抗治疗的经验分享
▌ 病例报告:王丽君 江苏省肿瘤医院
▌ 病例点评:王飞江 江苏省肿瘤医院
摘要
● 鼻咽癌(nasopharyngeal carcinoma,NPC)是指发生于鼻咽腔顶部和侧壁的恶性肿瘤,发病率居耳鼻咽喉恶性肿瘤之首。与其他类型恶性肿瘤相比,鼻咽癌并不常见,但是其发病率具有明显的地域特色。根据2018年国际癌症研究机构(IARC)的一份报告显示,全球新增鼻咽癌病例129079例,其中47.7%的病例发生在中国南方[1],随着诊治技术的推广及改进,鼻咽癌患者的生存率得到了很大提高,但局部复发及远处转移仍然是目前鼻咽癌治疗失败的主要原因。在传统的放化疗基础上,如何能够进一步提高鼻咽癌患者的生存率、减少不良反应、提高生活质量,是目前存在的主要挑战。
NPC的病理学特征主要表现为肿瘤病变周围及瘤内免疫细胞高度浸润,从机制来看,免疫治疗通过激活患者自身抗肿瘤免疫发挥疗效,而鼻咽癌的肿瘤组织和间质中浸润了大量的淋巴细胞。且既往多项研究已证实NPC发病与EB病毒(epstein-barrvirus,EBV)感染密切相关,90%以上的高发区NPC患者血浆 EBV DNA呈阳性,尤其是局部晚期 NPC 患者因肿瘤负荷大,外周血中 EBV DNA 检出率和拷贝数往往较高[2]。EB病毒感染会导致鼻咽癌肿瘤细胞PD-L1表达阳性率高,因此免疫治疗在鼻咽癌领域具有充分的理论基础。
肿瘤免疫治疗作为一种新的治疗方法已经应用于多种恶性肿瘤的研究,并在一些恶性肿瘤中取得较好疗效。在以单药免疫检查点*制剂抑**作为复发/转移性NPC挽救治疗的KEYNOTE-028[3]、NCI-9742[4]、POLARIS-02[5]、SHR1210[6]及 CAPTAIN[7]研究中,有效率达 20%~30%,显示出了较好的抗肿瘤效应。在此基础上,免疫治疗联合化疗进一步提高了复发/转移性 NPC 的疗效。CAPTAIN-1st[8]也证实了卡瑞利珠单抗联合GP方案在鼻咽癌一线治疗中的疗效,PFS获得显著的延长。本文通过一例鼻咽癌的患者使用靶免联合同步放化疗治疗后获得CR的疗效,探讨鼻咽癌患者的治疗选择。
病例作者

王丽君
江苏省肿瘤医院放疗科副主任医师,南京医科大学副教授,肿瘤学博士,南京医科大学硕士生导师
中国肿瘤放射治疗联盟放射免疫青委会委员
江苏省医师协会放射肿瘤专业委员会委员
江苏省抗癌协会大肠癌专业委员会委员
主持多项省厅级科研项目,发表sci论文
及中华杂志论文多篇
江苏省科教*卫强**工程青年医学人才
获江苏省新技术引进奖二等奖一项
《肿瘤放射治疗学》(人卫版)编者
《亨迪放射物理学》译者
病例介绍
▌基本情况
患者: 何**,男,77岁。
主诉:回吸性血涕伴左侧面麻2月余。
既往史:
平素健康状况:一般;疾病史:不稳定型心绞痛;传染病史:无,预防接种史:无;手术外伤史:手术:无;外伤:无;输血史:无;药物过敏史:无。
家族史、个人史、吸烟史、饮酒史: 无特殊。
▌检查情况
实验室检查:血常规、甲功、肾功能基本正常;肝功能示AST 140U/L,白蛋白 36g/L;EBV DNA拷贝数 3100。
PET-CT:1.鼻咽顶后壁黏膜明显增厚,FDG代谢明显增高,考虑鼻咽癌可能;右侧口咽旁问隙、右侧颈部多枚肿大淋巴结,PDC代谢明显增高,考虑多发转移灶可能;双侧颌下、左侧颈部多枚小淋巴结,部分FDG代谢轻度增高,考虑良性淋巴结可能。2.纵隔及双肺门、腹膜后、右侧盆壁、双侧腹股沟多枚小淋巴结,部分PDG代谢轻度增高,考虑炎性淋巴结可能。3. 前列腺FDG代谢分布不均。
2022-04-25病理学检查:(鼻咽部活检病理)形态考虑为低分化鳞状细胞癌,非角化型。免疫组化:BGFR (3+),BBER (部分+),P40 (局灶+),PD-L1(Dako22C3):肿瘤细胞大约10%表达阳性,CPS评分=15分。
2022-05-05鼻咽部增强CT示:鼻咽CA并左侧翼腭弓、海绵窦受侵,伴邻近蝶窦、左侧筛窦、枕骨斜坡、左侧框下裂骨质破坏;右侧颈部多发肿大淋巴结(最大2.4×1.4cm),考虑转移;2.双侧梨状窝闭塞。
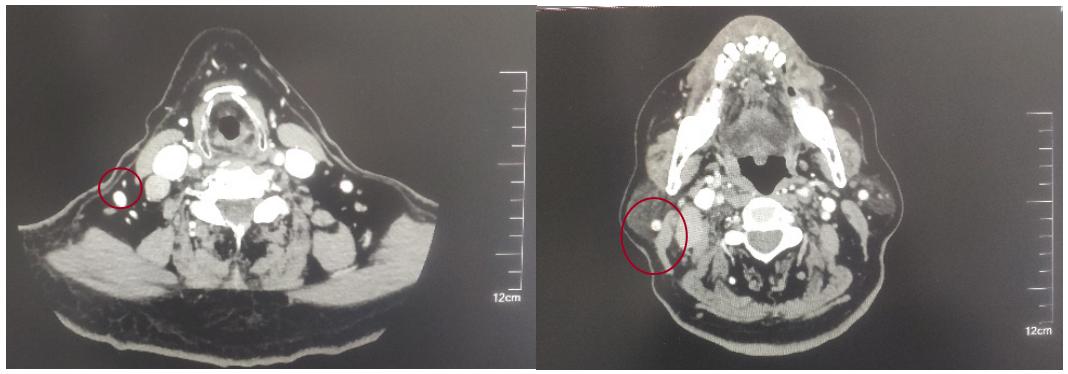
▌治疗情况
2022-05-09行“斯鲁利单抗300mg d1+紫杉醇脂质体150mg d1,120mg d8+奈达铂150mg d2+尼妥珠单抗400mg d2”治疗1周期。
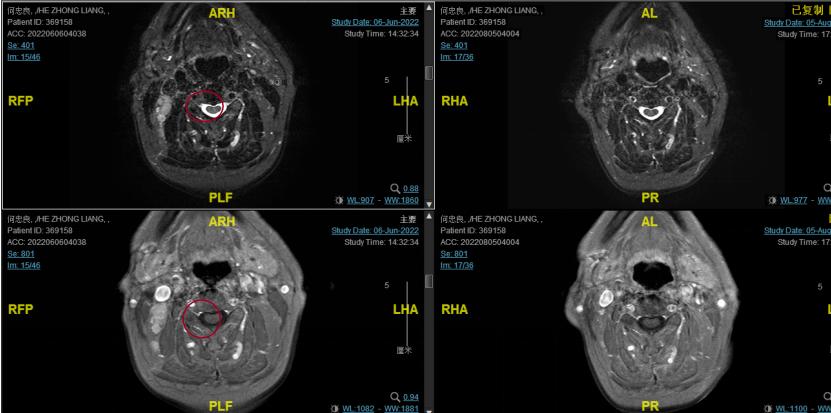
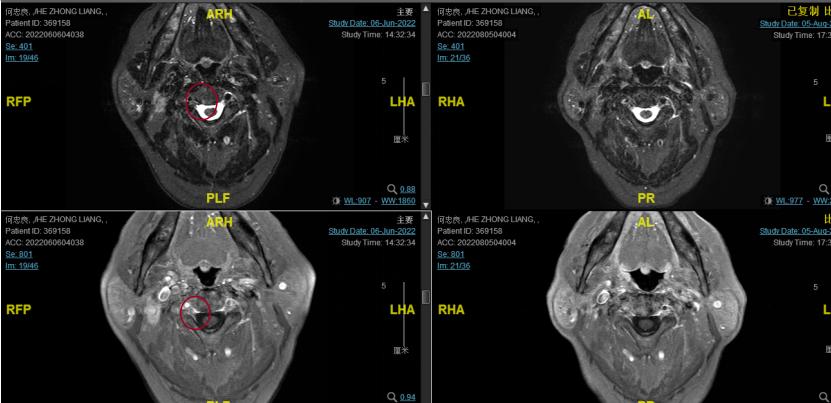
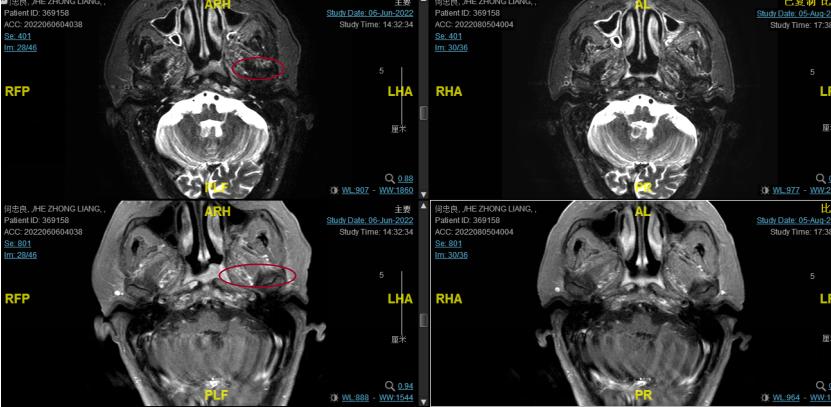
后患者至江苏省肿瘤医院放疗科就诊,2022-06-06完善头颅MR检查:
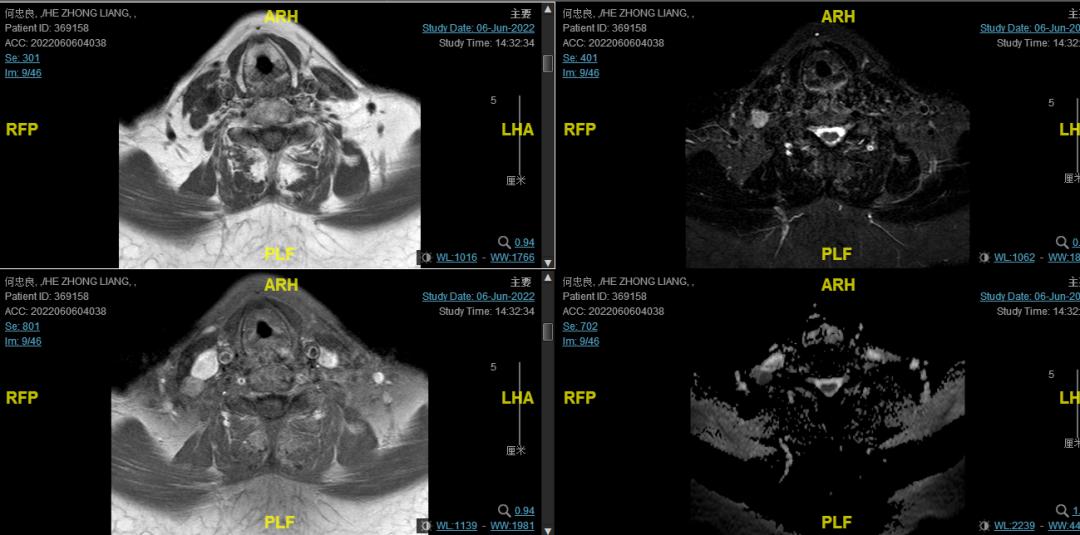

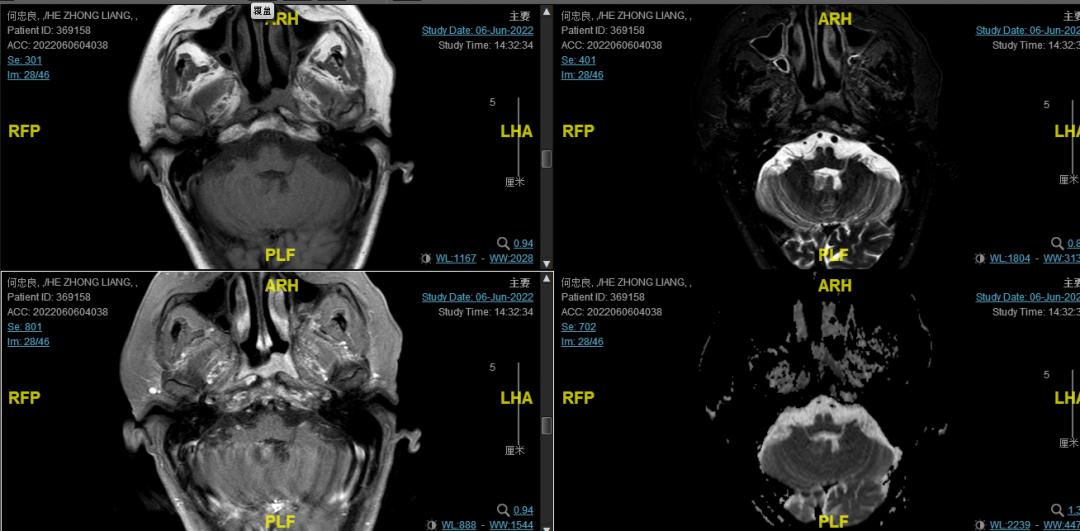

修正诊断: 鼻咽癌T3N1M0,Ⅲ期。
2022-06-08再次行“斯鲁利单抗300mg d1+紫杉醇脂质体150mg d1,120mg d8+奈达铂150mg d2+尼妥珠单抗400mg d2”治疗1周期。
2022-06-29行鼻咽IGRT放疗:GTV1 68Gy/32f 、GTV2 68Gy/32f、CTV1 60Gy/32f、CTV2 50.4Gy/28f。期间同步斯鲁利单抗+尼妥珠单抗+恩度治疗。
▌疗效评估
2022-08-05(放疗近结束)复查MR, 疗效评价:CR。鼻咽部肿物及咽后转移淋巴结颈部转移淋巴结均达到CR。
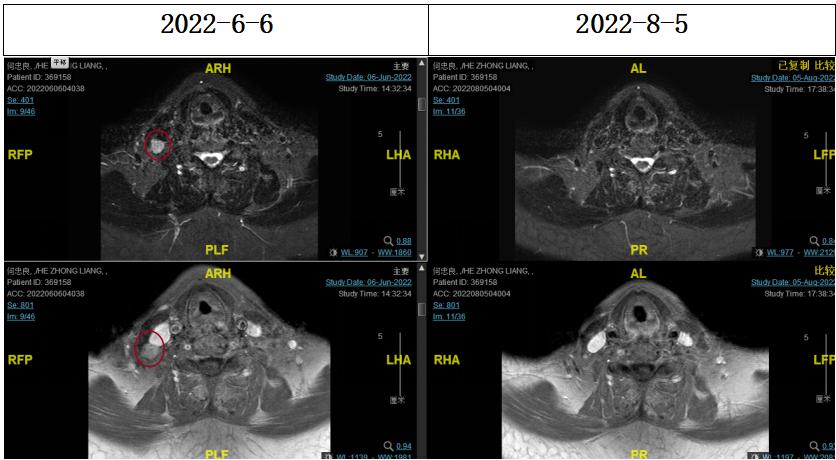
▌安全性
治疗期间患者耐受良好,未出现免疫相关不良反应。
▌病例小结
该患者为77岁老年男性,既往心脏疾病病史,初诊伴颈部淋巴结转移。对于高龄患者,因合并基础疾病,往往因体质较差,不能耐受标准剂量的放化疗。具有里程碑意义的Interproup0099随机试验发现同期放化疗和辅助化疗的生存终点优于单纯放疗,从而确立了同期放化疗作为局部晚期(Ⅲ-ⅣA期)鼻咽癌的标准治疗地位。该患者初诊时原发病灶已破坏枕骨斜坡及眶下裂,原发病灶较大,考虑仅联合同期化疗,疗效有限。近年来,多个PD-1单抗在晚期的鼻咽癌中显示出了疗效,多个PD-1产品在鼻咽癌的二线及三线治疗中获批。今年获批上市的斯鲁利单抗在同类免疫检查点*制剂抑**中显示出了良好的安全性,因此该患者使用了尼妥珠单抗+化疗联合斯鲁利单抗治疗,取得了PR的疗效,且患者未出现免疫相关不良反应。该病例显出出了斯鲁利单抗在鼻咽癌患者诱导治疗中的疗效及安全性,为后续鼻咽癌的诊疗提供新的思路。
点评专家

王飞江
主任医师
从事肿瘤放疗临床及带教工作三十余年
擅长鼻咽癌,直肠癌,前列腺癌等常见恶性肿瘤的诊治,对处理肿瘤相关疑难病症及后遗症并发症方面有丰富的临床经验
江苏省肿瘤防治联盟大肠癌专家委员会常务委员
江苏省抗癌协会泌尿男生殖系肿瘤专业委员会委员
病例点评
按照传统鼻咽癌治疗模式,约80%的患者可以获得很好的长期生存,但是还有20%的鼻咽癌高危人群会出现复发转移,而这部分患者主要包括T3、T4及N2、N3局部晚期及EB病毒拷贝数非常高或治疗后EB病毒拷贝数不能恢复到0的患者。该患者初诊时为T4N3Mx,局部分期较晚,诱导治疗期使用了斯鲁利单抗联合尼妥珠单抗、化疗治疗2周期,病灶较前缩小。后予放疗同步斯鲁利单抗、尼妥珠单抗、恩度治疗,所有病灶均达到了CR,避免了手术带来的损伤。
患者来我们医院修正诊断为T3N1M0 Ⅲ期,我们Ⅲ期病人临床指南推荐放化同步,但因该患者年龄偏大,恐怕不能耐受同步放化疗,所以选用放疗+靶免治疗。实践证明,我们多例老年患者使用此方案,疗效较好,能耐受相关毒副作用,治疗从未出现中断情况,所以临床工作中,对于>75岁老年肿瘤患者,我们经常在现有的治疗指南指导下,对方案进行改良,使之更符合老年肿瘤患者的需要,能完成治疗任务,并且获得较好的疗效。现在对于晚期头颈肿瘤的治疗,包括晚期鼻咽癌,有趋势将免疫治疗前移,用于新辅助/同步放化疗,真实世界取得了较好疗效,为局晚期头颈肿瘤(包括鼻咽癌)治疗提供了一个很好的方案选择。
从该病例中我们看到斯鲁利单抗联合化疗及靶向治疗模式获得的CR的近期疗效,且安全性良好,但是对于这部分患者的长期生存还需要更长的随访,和更多的病例去跟踪疗效。鼻咽癌目前的治疗包括化疗、抗EGFR单抗、VEGF单抗、PD-1/PD-L1单抗的全身治疗模式,如何将PD-1单抗与其他药物联合,免疫治疗在鼻咽癌中是否需要维持、维持多久,仍有很多值得探讨的地方。此外,放疗与抗PD-1单抗的联合治疗模式,是先使用PD-1单抗,还是同步进行,还是放疗后使用抗PD-1单抗维持也需要通过不断尝试和临床试验来告诉我们答案。但是我认为,免疫治疗在局晚期鼻咽癌中肯定会有一席之地。
▌参考文献
[1] JIN YN,TANG QN,YAO JJ,et al. The effect of adding concurrent chemotherapy to radiotherapy for stage II nasopharyngeal carcinoma with undetectable pretreatment Epstein-Barr virus DNA: Retrospective analysis with a large institutional-based cohort.[J].Transl Oncol, 2021,14(2):100990.
[2] BOSSI P,CHAN A T,LICITRA L,et al. Nasopharyngeal carcinoma:ESMO-EURACAN Clinical Practice Guidelines for diagnosis,treatment and follow-up(dagger)[J].Ann Oncol,2021,32(4):452-465.
[3] OTT P A,BANG Y J,PIHA-PAUL S A,et al.T-Cell-Inflamed GeneExpression Profile,Programmed Death Ligand 1 Expression,and Tumor Mutational Burden Predict Efficacy in Patients Treated With Pembrolizumab Across 20 Cancers:KEYNOTE-028[J].J Clin Oncol,2019,37(4):318-327.
[4] MABBY,LIM WT,GOHBC,et al.Antitumor Activity of Nivolumab in Recurrent and Metastatic Nasopharyngeal Carcinoma:An International,Multicenter Study of the Mayo Clinic Phase 2 Consortium(NCI-9742)[J].J Clin Oncol,2018,36(14):1412-141
[5] WANG FH,WEI X L,FENG J,et al.Efficacy,Safety,and Correlative Biomarkers of Toripalimab in Previously Treated Recurrent or Metastatic Nasopharyngeal Carcinoma:A Phase Ⅱ Clinical Trial (POLARIS-02)[J].J Clin Oncol,2021,39(7):704-712.
[6] FANG W,YANG Y,MA Y,et al. Camrelizumab (SHR - 1210) alone or in combination with gemcitabine plus cisplatin for nasopharyngeal carcinoma:results from two single -arm,phase 1 trials[J]. Lancet Oncol,2018,19(10):1338-1350.
[7] YANG Y,ZHOU T,CHEN X,et al.Efficacy,safety,and biomarker analysis of Camrelizumab in Previously Treated Recurrent or Metastatic Nasopharyngeal Carcinoma(CAPTAIN study)[J].J Immunother Cancer,2021,9(12):e003790
[8] YANG Y,QU S,LI J,et al.Camrelizumab versus placebo in combination with gemcitabine and cisplatin as first-line treatment for recurrent or metastatic nasopharyngeal carcinoma(CAPTAIN-1st):a multicentre,randomised,double-blind,phase 3 trial[J].Lancet Oncol, 2021,22(8):1162-1174