摘要
病毒本身和机体免疫应答是影响HBV感染病情进展和临床转归的重要因素。目前免疫学研究及临床观察结果表明,单纯的抗病毒治疗无法重建慢性乙型肝炎患者的抗病毒免疫功能,因而无法彻底治愈HBV 感染。联合新的免疫治疗策略,根据疾病的不同阶段采取针对性的治疗方案,可能是实现HBV 感染治愈的有效方法。本文综述慢性乙型肝炎治疗的现状与进展。
由乙肝病毒(hepatitisB virus,HBV)感染引起的乙型肝炎是一种传染性强、病死率高的传染病,以肝脏病变为主要表现,可引起多器官功能损害,已成为严重威胁人类健康的全球性公共卫生问题。目前,中国HBV感染者约7800万,其中慢性乙肝患者约2000多万,每年有近30万患者因肝癌而死亡,占世界肝癌患者数量的51%。按疾病进展可将HBV 感染分为急性感染、慢性感染、肝硬化、肝癌,患者自然转归或治疗干预后的转归各不相同,其中慢性乙肝处在疾病进展的关键环节,临床上有效的治疗可延缓疾病进展或实现功能性治愈。本文就慢性乙肝的发病机理、临床治疗的现状与进展作一综述。
HBV 感染的免疫发病机理
成人感染HBV后约90%以上能够控制病毒,表现为急性感染或急性自限性乙型肝炎,5%~10%进入慢性感染阶段。围产期及1~5岁儿童感染HBV后极易发展为持续性感染,慢性化率分别高达90%和30%。虽然导致HBV感染不同临床结局的因素不是完全清楚,但大量临床免疫学研究证明病毒本身和机体免疫应答是影响疾病进展和临床转归的重要因素。
1)急性HBV 感染
HBV复制、肝脏损伤、天然免疫及适应性免疫在急性HBV感染的不同阶段组成*态网动**络:HBV感染后即潜伏期,天然免疫活化与病毒复制高峰同时出现;急性肝炎期,适应性免疫应答出现并持续增强,HBV载量开始下降,该阶段病毒清除的同时伴随着肝脏损伤;感染恢复期,病毒彻底清除和ALT 恢复正常后,HBsAb 和HBV 特异性记忆性T细胞出现,保护机体免受二次感染或复发。
天然免疫系统作为机体抗病毒感染的第一道防线,在HBV感染的早期阶段,可通过Toll样受体识别HBV 感染,释放I型IFN-α/ß,激活NK或NKT细胞发挥早期的抗病毒作用。随后DC等抗原提呈细胞摄入病毒抗原,经加工处理后以MHC 1类、MHC II类分子的形式分别呈递给CD8+T细胞和CD4+T细胞,从而启动特异性细胞免疫和体液免疫。HBV特异性T细胞免疫应答,尤其是HBV 特异性CD8+T 细胞应答在HBV 感染的清除中起关键作用。强烈、持久、多表位的HBV特异性CD8+T细胞应答利于HBV的控制,在急性自限性HBV感染时,机体免疫系统可从HBV生命周期的各个环节(侵入、病毒DNA 复制、cccDNA 的生成、乙肝表面抗原的合成、病毒释放和感染肝脏细胞等)发挥作用,从而控制或清除病毒。当免疫功能受损时,则无法彻底清除病毒,导致感染的慢性化。
2)慢性HBV 感染
机体抗病毒免疫应答功能缺陷是慢性乙肝最重要的特征之一,具体表现为:1)固有免疫的损伤;2)特异性免疫的损伤;3)增强的肝脏免疫耐受。大量研究已经证实,HBV特异性CD8+T细胞是清除HBV的最主要的免疫成分[3]。然而持续的HBV复制、天然免疫紊乱、病毒特异性CD4+T细胞功能耗竭、树突状细胞(dendritic cell,DC)功能缺陷、调节性T 细胞(regulatoryTcell,Treg)增多、免疫抑制性途径异常活跃等严重损伤了病毒特异性CD8+T细胞功能(包括增殖和分泌细胞因子IL-2、IFN-γ和肿瘤坏死因子-α 的能力),使之处于耗竭状态。同时肝组织中Th17、NK、DC等大量非特异性淋巴细胞浸润,导致肝脏组织炎症和肝细胞坏死,甚至发生肝纤维化等病理变化,驱动着“慢性肝炎→肝硬化→肝癌”的进展。
慢性HBV感染的自然史可人为地划分为4个期,即免疫耐受期、免疫清除期、非活动或低(非)复制期和再活动期。新生儿时期感染HBV,仅少数(约5%)可自发清除HBV,而多数有较长的免疫耐受期,然后进入免疫清除期;但青少年和成年时期感染HBV,多无免疫耐受期,而直接进入免疫清除期。不同时期的免疫特点、体内的病毒水平、肝损伤的程度及肝内浸润淋巴细胞均不相同,这些对于抗病毒治疗时机的选择具有重要价值。
Sprengers 等对不同临床阶段的HBV感染者肝内淋巴细胞的比例进行观察,结果发现免疫耐受期患者肝内NK细胞比例较免疫清除期和非活动期患者明显升高,CD4+和CD8+T细胞比例在3者之间无明显差异。但在免疫清除阶段,ALT水平相似的情况下,按照病毒载量分为高、低2组,CD8+T细胞比例在高病毒载量组明显升高,而CD4+T淋巴细胞主要在免疫清除期低病毒载量的患者中存在。这些差异在外周血中并未发现。HBV 特异性的CD8+T淋巴细胞主要在免疫清除期低病毒载量的患者中存在。本研究组发现:1)免疫清除期患者外周血和肝内的单核/巨噬细胞及其促炎症CD16亚群比免疫耐受期患者明显升高,但外周血内中性粒细胞的数量降低,肝内中性粒细胞浸润增加。将免疫清除期患者按照肝脏病理炎症活动度分为高、低2 组,单核/巨噬细胞及其促炎症CD16亚群和中性粒细胞数量在肝脏炎症活动度高的患者肝内明显升高。2)免疫清除期患者肝内浸润的NK 细胞数量比免疫耐受期患者明显升高,而且免疫清除期患者肝内浸润的NK 细胞上调表达相关活化受体,并选择性地上调其*伤杀**活性。进一步分析发现,NK细胞升高的*伤杀**活性与患者ALT 水平、肝脏的炎症程度呈显著正相关。此外,在免疫清除期患者肝脏炎症微环境内细胞因子IL-12、IL-15和IL-18显著升高,而IL-10显著降低,这种炎症微环境下细胞因子的不平衡造成NK 细胞*伤杀**能力的激活。此研究结果拓展了当前对NK 细胞在慢性乙肝中作用的认识,更进一步指出,免疫清除期患者肝脏炎症微环境内细胞因子的不平衡可以选择性调节NK细胞的功能。
慢性HBV 感染治疗现状
目前慢性乙型肝炎的抗病毒治疗药物主要有核苷(酸)类似物(如拉米夫定、阿德福韦酯等)和干扰素α,虽然有利于抑制HBV复制,减轻肝损伤和延缓疾病进展,但这2类药物均无法根除HBV感染。而且不同患者对抗病毒药物的反应不同,分为完全应答、部分应答和不应答3种。理想的抗病毒治疗经历完全病毒抑制(病毒载量低于检测下限)伴随ALT正常、HBeAg血清学转换和HBsAg血清学转换3个阶段,其中HBsAg血清学转换被认为是慢性乙肝的基本治愈阶段(即功能性治愈阶段),但现有抗病毒治疗手段很难实现。
HBV DNA聚合酶和模板是病毒复制的2个重要因素,缺乏则无法复制。其中前者的作用是“催化”HBV基因的复制,核苷(酸)类似物的作用靶点均是HBV DNA聚合酶,它能够较强地抑制HBV DNA的复制,但不直接作用于蛋白质翻译过程,仅仅是通过减少合成病毒抗原的模板——mRNA 来降低抗原表达,所以临床表现为HBV DNA 降低比较迅速,且HBV DNA 阴转率很高,但HBeAg 和HBsAg 阴转率不明显,患者须长期治疗。IFN虽有直接抗病毒作用和部分免疫调节作用,HBeAg 和HBsAg血清学转化率较核苷(酸)类似物稍高,但经Peg IFN-α治疗3~4年后HBsAg 血清学转换率仅为8%~11%。同时,其不良反应发生率高且较严重,常导致药物减量和治疗暂停,适应症和禁忌症较严格,而且不能对病毒生活周期的每个环节发挥抑制作用。综合分析以上抗病毒药物存在的种种不足,可以认为目前的抗病毒治疗只是一个“狭义”的抗病毒治疗,仅仅能抑制病毒的复制,而无法清除病毒抗原和HBV共价闭合环状DNA(covalently closed circular DNA,cccDNA)。
研究证实抗HBV感染的关键在于重建患者HBV特异性细胞免疫功能,现有抗病毒药物无法彻底治愈HBV感染的原因在于未能建立有效的抗病毒免疫应答。如拉米夫定治疗早期CD4+T细胞反应性增高,但6个月后又恢复到治疗前水平,HBV特异性CD8+T细胞反应也不能长期维持,因而患者很难维持长期、持续的病毒学应答。阿德福韦酯虽然可以更好地抑制HBV复制,提高慢性乙肝患者的mDC数量和功能,但也不能使CD4+T细胞功能完全恢复,抗病毒治疗仍不能产生长期、持续的病毒学反应。IFN 具有直接抑制病毒和免疫调节的双重作用机制,其中免疫调节所获得的持久免疫控制是IFN 疗效维持的关键因素,但临床经IFN治疗达到持久免疫控制的患者过少。临床抗病毒治疗过程中,无论是血清HBeAg 阳性、还是HBeAg 阴性的慢性乙肝患者,只要伴随高ALT水平往往预示着发生HBeAg血清学转换的可能性较大,这是因为ALT水平高时,机体也相对具有较强的抗HBV免疫应答能力。此外,能够出现HBsAg 血清学转换的患者通常免疫功能恢复很好。可见乙肝的抗病毒药物可以通过抑制病毒的复制而发挥始动牵引作用,肝功能和损伤恢复是治疗的根本,但有效的抗病毒治疗始终离不开机体免疫系统自身功能的恢复和对病毒及其抗原成分有效的清除。
“爬坡假说”和新的抗病毒治疗策略
1 )“爬坡假说”
慢性HBV 感染过程中,机体免疫状态、HBV及肝脏三大因素相互作用,共同影响着疾病的进展和转归,其中机体的免疫应答不仅能够控制病毒复制和清除,而且还参与慢性乙肝的致病过程,是决定慢性乙肝临床转归和疗效的重要因素。无论是核苷(酸)类似物长期抗病毒治疗,还是固定疗程的长效IFN治疗,都难以达到彻底清除病毒的目的。如何提高现有药物的治疗效果、彻底清除或抑制体内的HBV复制、恢复机体的特异性抗病毒免疫功能成为临床最为关注的问题。
根据目前的研究和临床观察结果,我们提出“爬坡假说”(图1)。慢性乙肝的抗病毒治疗须要跨越3座“大山”(持续的病毒复制、肝脏的病理学改变和机体抗HBV免疫应答水平低下)才有可能使患者恢复到健康状态。应根据这3座“大山”的特点,有针对性地开展3个方面的治疗,即抗病毒治疗(最好包括抑制HBV复制和抗原合成多个方面)、保护肝脏治疗(阻断肝脏炎症反应和纤维化的进程等)和免疫调节治疗。我们初步认为:慢性乙肝患者应首先进行最基本的抗病毒治疗,有效抑制HBV DNA复制和部分抗原合成,为机体免疫功能的恢复“减压”,同时进行保肝治疗,阻断肝脏炎症反应和纤维化进程;然后在抗病毒和保肝治疗基础上联合有效的免疫调节治疗,帮助患者完成HBeAg 和HBsAg 血清学转换,充分恢复患者抗病毒免疫应答,最终达到持久清除病毒、恢复机体保护性免疫的目的。
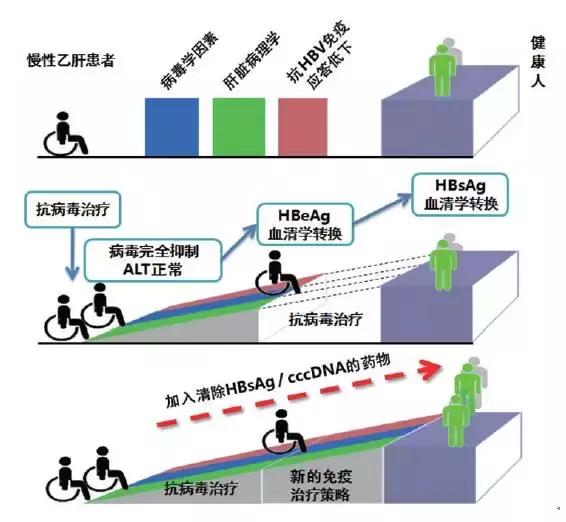
图1 慢性乙肝患者抗病毒治疗策略:“爬坡假说”
2)新的抗病毒治疗策略
(1)针对病毒复制靶点的药物
HBV 从感染宿主开始,其生命周期包括:进入(受体),病毒DNA复制,cccDNA的生成,乙肝表面抗原的合成,病毒释放和感染肝脏细胞等环节。现有的治疗方案仅针对病毒复制这一特定环节,并不能有效和彻底清除cccDNA,一旦停药,相当多的患者会出现反弹,病情可能发生反复。此外,长期用药还可能导致耐药变异的发生。近年来,一些针对HBV生命周期中多环节、更安全有效的药物被相继开发,虽尚未应用临床,但为实现慢性乙肝的治愈提供了可能。
破坏HBV cccDNA 的药物。HBV cccDNA 的持续存在是现有抗病毒药物无法彻底治愈HBV 感染的关键,新的药物开发着眼于清除cccDNA或者沉默cccDNA 转录。人工核酸内切酶介导的三大基因编码技术ZFNs、TALENs 和CRISPR/Cas 被用于破坏HBV cccDNA。通过阻断cccDNA 转录,ZFNs 可抑制病毒的转录和复制。TALENs靶定S或C区的ORF,可导致35%cccDNA发生突变,通过靶定保守区可降低HBeAg、HBsAg、HBcAg和前基因组RNA 产生,从而降低cccDNA的水平。在Huh-7细胞模型中,CRISPR/Cas 可降低HBsAg 和HBcAg,破坏HBV 表达模板。另外,2 个二代磺胺类药物CCC-0975、CCC-0346 最近被发现具有抑制HBV cccDNA的功能。
抑制病毒核酸组装的药物。包括苯基丙烯酰胺衍生物(AT- 61、AT130)、异芳基-二氢嘧啶(Bay 41-4109)等药物可抑制病毒衣壳的形成或阻止病毒前基因组RNA进入核衣壳。由于这类药物抑制病毒复制,优先于病毒合成,因此对核苷(酸)类药物耐药株同样有效。
靶定HBV RNA 的药物。基于RNA干扰技术的治疗策略可特异性敲除病毒蛋白(包括HBsAg)和病毒复制。ARC-520 能够有效拆解HBV RNA、病毒蛋白和DNA,显示强烈的抑制HBV复制功能。
阻断HBV 入侵的药物。最近钠离子-牛磺胆酸共转运多肽(sodium taurocholatecotransporting polypeptide,NTCP)被发现可作为HBV大包膜蛋白pre-S1 区的特异性结合受体,介导HBV 侵入宿主细胞。这一机制的阐释,为开发HBV 侵入*制剂抑**提供了基础。Volz 等利用人源化小鼠证实了来自HBV pre- S1 蛋白的肽段Myrcludex-B通过结合NTCP,不仅能有效阻止HBV在感染肝脏内肝细胞间的扩散,而且能抑制最初感染的肝细胞内病毒cccDNA储存库的扩增。
(2)恢复机体免疫应答的生物治疗策略
抗病毒免疫在HBV清除中发挥着重要作用,研发出能够恢复患者特异性抗病毒免疫功能的药物对HBV感染的治愈具有重要意义。多种免疫活性细胞如CIK、DC、CAR-T 等,治疗性疫苗及免疫调节因子等相继出现,并取得不错的前期实验结果,部分亦进入临床试验阶段。
恢复天然免疫功能的制剂。Lucifora 等报道β-淋巴毒素受体激动剂可上调HBV感染细胞中APOBEC3A和APOBEC3B 的表达,以非溶细胞途径清除cccDNA,降低cccDNA、HBV DNA和HBsAg的水平。将其与抗病毒药物联合可能在治愈HBV感染方面具有较大前景。GS-9620,选择性的TLR7激动剂,可延长抑制慢性HBV感染黑猩猩血清和肝脏的HBV DNA。且血清中HBsAg、HBeAg水平,HBV阳性肝细胞数量明显下降。最近一项1b期临床试验结果显示,GS-9620用于治疗慢性乙型肝炎安全性好,且可诱导外周血中ISG 15的产生。
恢复特异性免疫功能的策略。随着基因编码技术的应用,通过HBV特异性嵌合抗原受体(CARs)和HBV特异性T细胞受体(TCR)修饰的T细胞被用于重建CHB患者的病毒特异性细胞免疫应答。另外,PD-1、CTLA-4、TIM-3等抑制性受体与HBV特异性T细胞功能耗竭密切相关,阻断这些抑制性信号可在一定程度上恢复T细胞增殖和分泌IFN-γ能力。PD-1*制剂抑**的上市,使其用于治疗CHB成为可能。
治疗性疫苗一直是重建患者特异性免疫应答研究的热点,陆续有多种疫苗被开发用于临床试验,但未取得满意疗效。新型Nasvac疫苗是当前中国正在引进的乙肝治疗性疫苗。已在古巴完成Ⅲ期临床试验,结果表明,该疫苗可提高CHB患者特异性免疫功能,在减少HBVDNA 的同时降低HBsAg 水平。同时Nasvac 疫苗与现有疫苗相比,有以下优势:1)针对乙肝核心抗原和表面抗原进行综合性治疗,其核心抗原能诱导特异性免疫应答,发挥很强的抗病毒作用;2)皮下注射给药与鼻黏膜给药相配合,利用黏膜免疫的特性,可能激发特异性免疫;3)药物剂量较足,疗程短;4)药物安全性系数高。目前,为进一步扩大临床试验规模,Nasvac 疫苗正在中国台湾、中国香港、新加坡、新西兰等地区及国家进行III期临床试验。
结论
2016 年的欧洲肝病大会上,亚太肝病研究学会(APASL)、欧洲肝病研究学会(EASL)、美国肝病研究学会(AASLD)及拉丁美洲肝病学会(ALEH)共同提出了“清除乙肝病毒”倡议,签署了《消除肝病宣言》,旨在加强乙肝治愈药物研发与临床研究。同时,临床药物的不断创新和治疗理念的转变也为治愈慢性乙肝奠定了基础。在中国,多家科研单位和企业正在集中力量进行乙肝药物研究,并取得了较好的研究结果。我们相信,通过对乙肝免疫机制的深入研究,采用有效的抗病毒药物抑制病毒复制、cccDNA*制剂抑**减少或控制病毒储存库、HBV抗原*制剂抑**降低或清除表面抗原和HBeAg“三箭齐发”,联合新的生物治疗策略恢复特异性免疫功能(图2),乙肝治疗将会取得重大突破,乙肝终将转变为能够治愈的疾病。
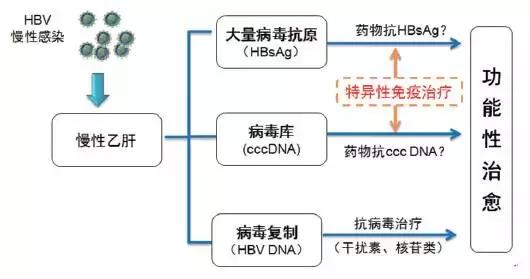
图2 慢性乙肝治愈的关键问题和机遇
(责任编辑 王媛媛)
本文作者:史继静,常文仙,李元元,王福生 。
作者简介:史继静,北京大学解放军302医院教学医院感染性疾病诊疗与研究中心,博士,研究方向为慢性病毒性肝病的免疫发病机理及细胞治疗;王福生(通信作者),中国科学院院士,研究方向为病毒性肝炎、艾滋病和疑难危重肝病的临床诊治、免疫发病机理及细胞治疗。