研究背景
肺动脉高压(PAH)是一种罕见的疾病,其特点是肺血管重塑,最终导致右心衰竭和死亡。迄今为止,尽管已有三种治疗方法针对前列环素、一氧化氮/环磷酸鸟苷和内皮素途径,但PAH仍然是一种严重疾病。因此,需要寻找新的靶点和治疗药物。线粒体代谢功能障碍是PAH发病机制之一,部分原因是通过诱导Warburg代谢状态,增强糖酵解,并通过上调谷氨酰胺酯酶作用、三羧酸循环和电子传递链功能紊乱、脂肪酸氧化调控失衡或线粒体动力学改变等途径参与。本综述的目的是探讨PAH中涉及的主要线粒体代谢途径,并提供有趣的潜在治疗前景的最新进展。
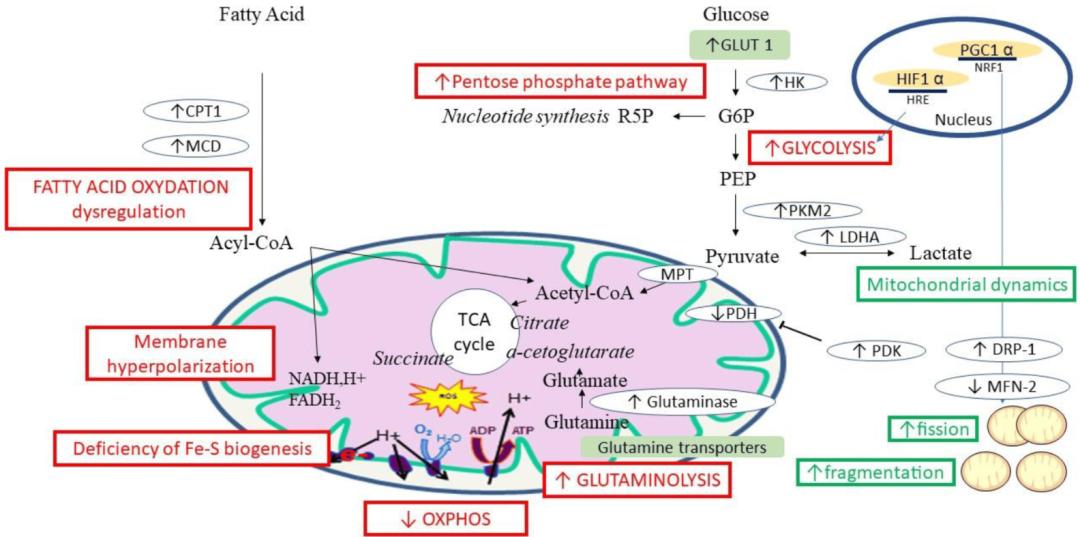
线粒体代谢功能障碍与PAH
尽管在PAH的发病机制理解方面取得了显著进展,但该疾病常在晚期诊断,从而无法实施早期治疗以减缓其进展。在过去的15年中,已经确定了三种基于血管舒张剂靶向肺血管内皮功能调节因子(前列环素、一氧化氮[NO]/环磷酸鸟苷[GMP]和内皮素途径)的治疗方法,导致了约10种药物的上市。PAH治疗的最新进展显示了根据疾病的严重程度采用这些治疗方法的组合策略的价值。因此,在最严重的患者中将启动三重疗法。然而,尽管有这些治疗创新,PAH仍然是一种严重疾病,5年生存率为60%。因此,需要寻找新的靶点和治疗药物。
根据许多已发表的论文,线粒体功能障碍是PAH中越来越受关注的治疗靶点。线粒体是所有真核细胞的能量中心,通过氧化磷酸化(OXPHOS)提供能量。它具有自己的去氧核糖核酸(DNA),在细胞内和细胞间通信、调节细胞凋亡、钙平衡和各种代谢途径中起着重要作用。因此,线粒体的缺陷或调控失衡导致不成比例的炎症反应、免疫调节紊乱和异常组织重塑。在PAH中,线粒体在肺血管重塑中发挥着重要作用,氧化磷酸化能量产生向糖酵解的代谢转变以及在所有肺血管细胞和右心室中的发生似乎是该疾病的主要机制之一。此外,在肺血管中,线粒体是产生活性氧化物(ROS)的生理来源,并作为参与肺部低氧性血管收缩的氧感受器。基于这些数据,目前正在对许多有趣的潜在治疗途径进行研究。
1. 瓦尔堡效应(The Warburg Effect)
瓦尔堡效应是指在PAH患者中,肺血管细胞呈现出类似癌细胞的代谢特征,即即使在有氧条件下,细胞也会利用糖酵解产生能量。正常情况下,糖酵解和葡萄糖氧化是耦合的,产生ATP和*酮丙**酸。然而,在PAH中,由于*酮丙**酸脱氢酶(PDH)的抑制,*酮丙**酸被转化为乳酸,导致ATP产量减少。这种代谢途径的改变被称为瓦尔堡效应,促使肺动脉血管细胞表现出癌症样的增殖和细胞损伤。瓦尔堡效应的发生机制尚不完全清楚,但缺氧诱导因子(HIF-1α)的活化被认为是一个重要因素。HIF-1α的上调和稳定会导致糖酵解相关蛋白的表达增加,从而进一步促进瓦尔堡效应。另外,研究还发现其他代谢调节因子如核糖核蛋白(PTBP1)和Micro-RNA-124(Mir124)也参与了瓦尔堡效应的调控。
有趣的是,瓦尔堡效应在PAH患者的肺血管系统中可以通过FDG-PET扫描来检测,并且与疾病的严重程度相关。此外,瓦尔堡效应对心肌细胞也产生影响,导致右心室肥大、收缩力降低和细胞凋亡。然而,与癌细胞不同,PAH患者的肺血管细胞仅在肺血管中增殖,并且在肺移植后没有复发的报道。因此,瓦尔堡效应在PAH中的存在可以被视为肺血管细胞的一种假瘤表型。总的来说,瓦尔堡效应在PAH的发病机制中起着重要的作用,但具体的调控机制和治疗方法仍需要进一步研究。
2. 谷氨酰胺分解上调和 TCA 循环功能障碍
谷氨酰胺分解的上调和TCA循环功能障碍也可能促进瓦尔堡效应。研究表明,在肺动脉高压(PAH)患者的血浆中发现了酰基肉碱、谷氨酸和TCA循环中间产物的积累,表明存在TCA循环功能障碍或无法满足PAH肺血管细胞增殖的需求。此外,PAH患者肺组织中柠檬酸盐、琥珀酸盐和脂肪酸代谢物水平升高,进一步强调能量代谢功能紊乱的假设。谷氨酰胺分解的增加似乎是PAH中肺血管细胞增殖的另一种机制。
谷氨酰胺是血液和肌肉中最丰富的循环氨基酸,对于维持线粒体代谢和细胞信号传导激活非常重要。谷氨酰胺分解是补充TCA循环碳中间产物的途径之一,并有助于补充反应。谷氨酰胺分解的增加涉及谷氨酰胺酶1(GLS1)的上调,GLS1参与将谷氨酰胺脱氨为谷氨酸,并且PAH患者的血管系统对谷氨酰胺的摄取增加。研究还发现,BMPR2基因突变的PAH患者内皮细胞中谷氨酸摄取增加。动物模型的研究也证明,在青蛙心脏素诱导的右心室肥大模型中,谷氨酰胺分解也得到上调。因此,针对异常的谷氨酰胺代谢可能是治疗PAH的一种有前途的方法。
3. 脂肪酸氧化失调 (FAO)
脂肪酸氧化失调(FAO)是一个重要的因素,在PAH中引起异常的脂肪酸代谢。脂肪酸代谢包括细胞摄取和储存脂肪酸、脂肪酸合成、线粒体中的脂肪酸转运和FAO。在心肌细胞中,FAO产生的ATP占总产量的60%至90%,剩下的10%至40%能量由糖酵解和葡萄糖氧化产生。这两个过程之间的平衡被称为兰德尔循环。脂肪酸进入线粒体后经历β-氧化反应,转化为乙酰辅酶A并进入TCA循环,最终转化为柠檬酸。柠檬酸的产生会抑制磷酸果糖激酶,增加葡萄糖-6-磷酸水平并抑制己糖激酶,从而减少*酮丙**酸的产生。此外,FAO产生的乙酰辅酶A会抑制PDH酶,从而减少葡萄糖的氧化。
同样地,抑制FAO会导致代谢转向糖酵解过程。在PAH中,脂肪酸代谢异常存在于血液、右心室(RV)和肺血管细胞中。在PAH患者的RV中观察到三酰甘油、二酰甘油和神经酰胺的积累。在BMPR2基因突变患者和动物模型中,PAH心肌细胞中的CD36转运蛋白介导的脂质摄取增加。然而,使用放射性示踪剂123I-β-碘苯基十五烷酸的单光子发射计算机断层扫描(SPECT)显示,严重PAH患者的RV似乎存在脂肪酸摄取受损。一种假设是受损的RV对脂肪酸的摄取受到限制。有趣的是,脂肪酸摄取增加与FAO的上调无关。PAH患者血浆中肉碱和酰基肉碱等脂质代谢产物的增加表明存在不完全线粒体FAO。
参与FAO的两个关键酶在PAH中表达上调。第一个酶是肉*碱毒**棕榈酰转移酶1(CPT1),在野百合碱大鼠的肺部和PAH患者的肺动脉中表达上调。过度表达的CPT1允许脂肪酸转运到线粒体中,促进平滑肌细胞的增殖和ATP产生。第二个酶是丙二酰辅酶A脱羧酶(MCD),它催化丙二酰辅酶A转化为乙酰辅酶A。抑制MCD会导致丙二酰辅酶A水平增加,减少脂肪酸的氧化,解除对PDH酶的抑制,从而促进糖酵解。因此,MCD是治疗PAH代谢功能障碍的一个潜在目标。此外,在实验性右心室肥大中,通过抑制FAO靶向兰德尔循环,可以增加右心室的葡萄糖氧化和功能。
4. 电子传输链 (ETC)
PAH中存在电子传输链(ETC)异常,ETC位于线粒体内膜,由复合物I、II、III、IV和V(ATP合酶)组成。研究表明,在PAH患者的肺动脉内皮细胞、心肌细胞和骨骼肌中,ETC复合物的表达和/或活性发生改变。
具体观察和发现包括:
1. PH动物模型中心肌呼吸耦合减少,提示ETC功能异常。
2. 抗霉素A长期抑制大鼠复合物III可诱导肺血管收缩,并降低参与脂肪酸氧化、三羧酸循环、ETC和蛋白质代谢的关键蛋白表达。
3. PAH患者肺血管内皮细胞的线粒体呼吸(状态3和4)降低,复合物IV活性降低,线粒体数量减少。
4. PAH动物模型中心肌细胞中,复合物II表达和活性增加与产生的活性氧物质(ROS)增加相关。
5. PAH患者的骨骼肌中复合物I和III减少。PAH患者的血小板呼*储吸**备能力增加,与脂肪酸氧化和复合物II活性增加有关。PAH患者的外周血单核细胞(PBMC)线粒体呼吸与疾病严重程度呈负相关。
这些观察结果表明,PAH中存在ETC异常,可能导致ROS产生紊乱和能量代谢紊乱。因此,靶向ETC复合物可能是治疗PAH的一个有趣选择。然而,进一步的研究需要确认这些初步发现,并探索具体的治疗策略。
5. 线粒体膜超极化
线粒体膜的超极化是细胞存活和增殖的重要机制之一。线粒体膜的超极化依赖于质子梯度,对线粒体呼吸至关重要。一些因素参与了线粒体膜超极化的调控,其中包括STAT3通路、活化T细胞核仁因子(NFAT)和Pim-1。通过调节线粒体内离子浓度和活化相关蛋白质,可以实现线粒体膜的超极化,并对细胞功能和代谢产生影响,进而调节HIF-1的活性。
6. 线粒体动力学
在肺动脉高压(PAH)中,线粒体动力学的改变对于细胞的增殖和抗凋亡表型起到重要作用。具体来说,线粒体裂变的增加和融合的减少促进了肺动脉细胞的增殖。这种失衡的线粒体动力学导致了代谢的重塑,而在这个过程中,肺动脉平滑肌细胞中的一些蛋白质起到了重要作用,如细胞质GTP酶动力相关蛋白1(DRP1)、PPAR-γ共激活剂1(PGC1α)和HIF-1。抑制DRP1的活性可以逆转PAH,并且调节DRP1活性来影响线粒体裂变是治疗PAH的一种策略。另一方面,增加线粒体融合可以减少肺动脉平滑肌细胞的增殖和增加凋亡。视神经萎缩1(OPA1)和GTPases mitofusin-1和2(MFN1/2)是参与线粒体融合的主要蛋白质。最后,线粒体自噬也在PAH的治疗中扮演着重要角色,通过去除受损线粒体来维持线粒体质量控制。调节线粒体动力学成为治疗PAH的一个有趣的潜在靶点。
7. 线粒体外的其他代谢途径:戊糖磷酸途径 (PPP)
在肺动脉高压(PAH)中,除了Warburg效应外,还观察到戊糖磷酸途径(PPP)的增加,并认为它与疾病的发展有关。PPP是细胞质中与糖酵解平行的代谢途径。它的两个主要产物是核糖5-磷酸(R5P,核苷酸合成的前体)和烟酰胺腺嘌呤二核苷酸磷酸(NADPH,用于细胞内的氧化还原稳态)。在PAH中,肺微血管内皮细胞(EC)和平滑肌细胞(SMC)中存在NADPH的过量产生。此外,葡萄糖-6-磷酸脱氢酶(G6PD)是PPP的主要限速酶,在PAH动物模型中的肺组织或体外实验中显示其活性增强与高增殖状态相关。这些数据表明,G6PD的减少或缺乏可能预防PAH的发生。然而,G6PD的作用是多方面的,它参与新陈代谢、氧化应激和红细胞脆性。G6PD缺乏会通过减少NADPH的产生来降低一氧化氮(NO)的合成,或者诱导p38途径的激活,从而导致PAH的恶化。因此,针对PPP途径的治疗潜力尚不确定。
8. 铁硫 (Fe-S) 生物发生不足
PPP增加:在PH患者和动物模型中观察到戊糖磷酸途径(PPP)的增加,该途径在细胞质中发生,并产生核糖5-磷酸(R5P)和烟酰胺腺嘌呤二核苷酸磷酸(NADPH)。PPP增加导致肺微血管内皮细胞和平滑肌细胞中NADPH过量产生,可能与PH的发展有关。
Fe-S生物发生不足:Fe-S簇是线粒体复合物I、II和III的重要辅助因子,当Fe-S簇发生改变时,会导致电子传递链(ETC)功能障碍。突变影响Fe-S簇生物发生和插入ETC的基因可能导致PH的发展。此外,缺乏一些与Fe-S生物合成相关的蛋白质也与PH相关。
这些因素的变化可能导致细胞代谢异常和线粒体功能障碍,进而促进PH的发展。进一步的研究有助于深入了解这些代谢异常与PH之间的内在机制,并为PH的治疗提供新的治疗策略。
PAH线粒体功能障碍的当前治疗靶点
针对线粒体代谢异常的治疗方法在肺动脉高压(PAH)中显示出潜在的前景。以下是一些可能的治疗靶点和策略:
1. 促进线粒体氧化磷酸化(OXPHOS):通过增加线粒体的氧化磷酸化代谢,可以改善PAH。例如,使用二氯乙酸(DCA)作为*酮丙**酸脱氢酶(PDK)*制剂抑**,可以逆转肺血管平滑肌细胞和右心室心肌细胞中的Warburg效应,从而改善PAH。类似地,雷帕霉素或依维莫司等哺乳动物雷帕霉素靶点(mTOR)*制剂抑**可以促进线粒体氧化磷酸化并对PAH产生积极影响。
2. 恢复线粒体平衡:通过抑制线粒体裂变和促进线粒体融合,可以恢复线粒体的功能和平衡。针对线粒体分裂蛋白1(DRP1)的*制剂抑**,如Mdivi或SiDRP-1,以及针对线粒体融合蛋白MFN2的上调等策略显示出治疗潜力。
3. 减少糖酵解:研究发现,减少糖酵解并恢复葡萄糖氧化是一种有效的治疗策略。通过针对糖酵解酶、糖酵解调节剂、谷氨酰胺分解*制剂抑**等靶点进行干预,可以改善PAH。例如,谷氨酰胺拮抗剂6-Diazo-5-oxo-L-正亮氨酸和谷氨酰胺酶*制剂抑**CB-839显示出对PAH动物模型的益处。
4. 线粒体移植:线粒体移植作为一种治疗选择,可以挽救线粒体功能障碍。实验模型显示,线粒体移植可以改善右心室功能、肺动脉重塑和血管收缩。然而,对于这种治疗方法的长期效果仍需进一步确定。
需要指出的是,虽然在动物模型中已经观察到上述治疗策略的积极影响,但在人类研究中尚未充分证实其疗效。进一步的临床研究和试验将有助于确定这些治疗方法在PAH患者中的可行性和有效性。

研究临床意义
线粒体代谢异常是 PAH 病理生理学的机制之一。线粒体代谢异常在PAH的发展中起着重要的作用,包括糖酵解的变化、谷氨酰胺分解的增加以及脂肪酸氧化(FAO)等代谢途径的改变。针对线粒体代谢异常的治疗策略被认为具有潜在的前景,并可能为PAH的治疗带来未来的进展。
由于PAH涉及的机制多样化,针对线粒体代谢异常的治疗可能与目前用于PAH的其他治疗方法相互补充。此外,针对转化生长因子β超家族的药物sotatercept在PAH的三期临床试验中取得了积极的结果,这也为PAH治疗提供了希望。
然而,目前针对线粒体代谢功能障碍的治疗方法在不同的PAH患者中表现出异质性反应。因此,推广精准医疗对于选择最有可能从这些治疗方法中受益的患者至关重要。通过对患者进行个体化的评估和分析,可以更好地确定哪些患者适合接受针对线粒体代谢异常的治疗,并优化治疗效果。
参考文献
Riou M, Enache I, Sauer F, Charles AL, Geny B. Targeting Mitochondrial Metabolic Dysfunction in Pulmonary Hypertension: Toward New Therapeutic Approaches? Int J Mol Sci. 2023 May 31;24(11):9572. doi: 10.3390/ijms24119572. PMID: 37298522; PMCID: PMC10253387.