根据2020美国AACR年会的研究结果,宫颈癌免疫治疗疫苗BVAC-C在HPV 16或HPV 18阳性复发性宫颈癌患者中显示出持久的抗肿瘤活性。
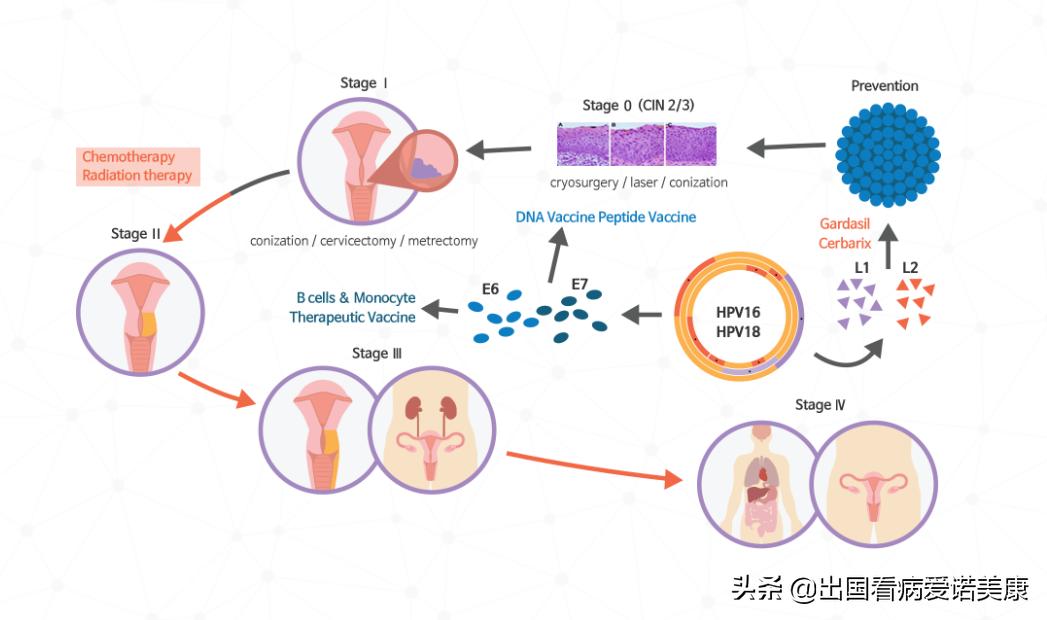
BVAC-C是一种基于B细胞和单核细胞的免疫治疗疫苗,转染了重组人乳头瘤病毒(HPV)16/18 E6 / E7基因,并装有自然*伤杀**性T细胞配体α-半乳糖苷神经酰胺。CeliVax免疫治疗疫苗是使用患者自身细胞(自体免疫细胞)的个性化药物,它可以帮助患者的免疫系统找出并消除癌细胞。CeliVax由三部分组成:抗原呈递细胞(APC),肿瘤相关抗原基因和佐剂。
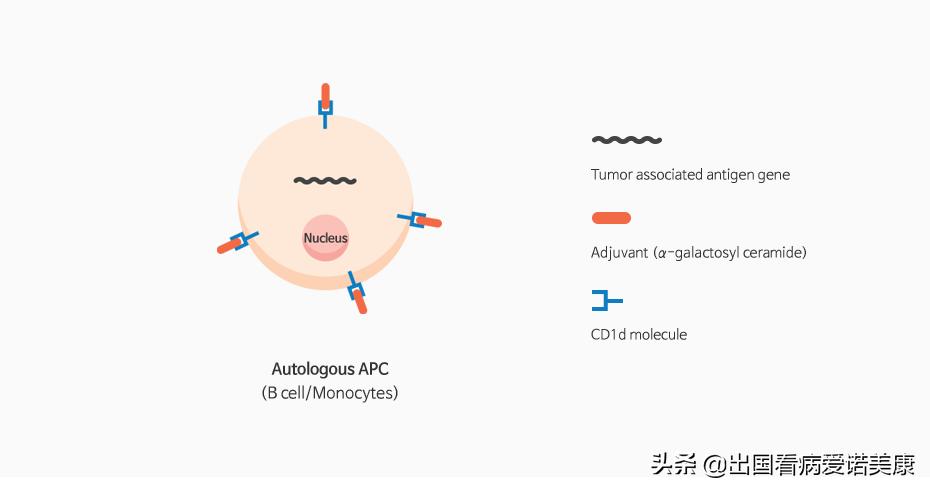
免疫治疗疫苗的结构
它使用自体淋巴细胞(患者的B细胞和单核细胞)作为APC。APC将外来抗原和/或受损细胞加工成肽片段,并将其呈递给免疫细胞。CeliVax的APC具有肿瘤特异性抗原基因。它们将肿瘤抗原呈递给免疫细胞并激活它们以消除特定的肿瘤细胞。α-半乳糖基神经酰胺是佐剂,可增强CeliVax的抗肿瘤活性。
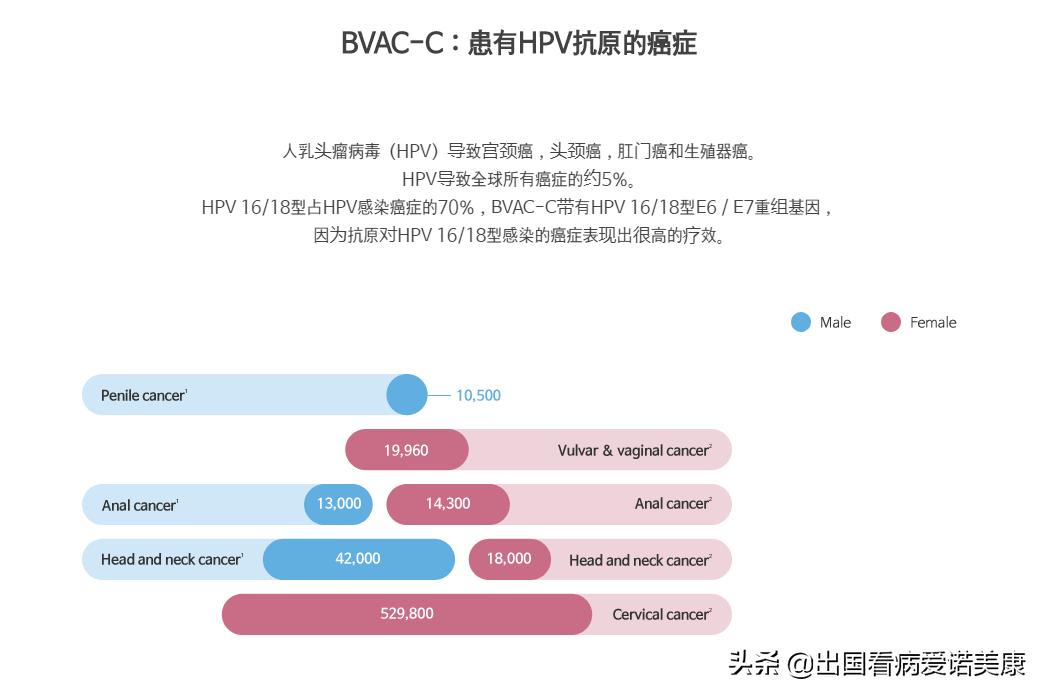
这种疫苗可以潜在地针对任何HPV 16阳性或18阳性的癌症,包括宫颈癌。癌细胞通过逐渐丧失表面抗原和/或MHC分子来抵抗细胞毒性T细胞的攻击。BVAC-C可以通过激活先天性效应细胞(例如自然*伤杀**T(NKT)细胞和自然*伤杀**(NK)细胞)消除那些免疫逃逸的癌细胞。此外,癌细胞通过在肿瘤微环境中诱导那些效应细胞的衰竭来抵抗T细胞和自然*伤杀**细胞的作用。这可以通过BVAC-C疫苗接种来抵消,该疫苗可以激活肿瘤微环境中的NKT细胞释放细胞因子,例如IL-21,IL-2和IFN-γ。总共有11名患者参加了该试验。在标准治疗失败后,患者患有多发性转移性进行性或复发性HPV 16或HPV 18阳性子宫颈癌。所有患者入选该试验前均已接受至少1种铂类化学疗法联合治疗。六名(55%)患者在入组前已接受2线或更多行铂类化学疗法。
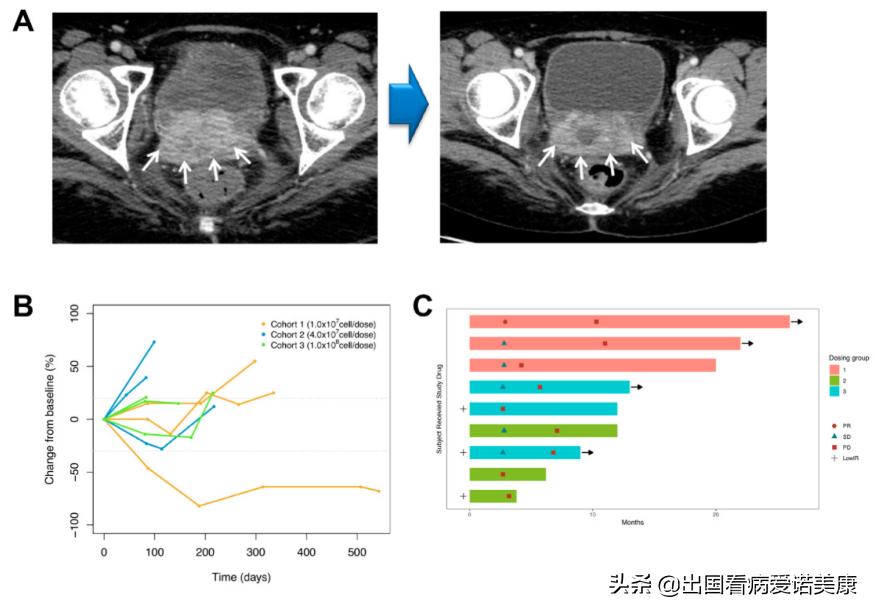
A白色箭头表示复发的肿瘤, 肿块直径稳定, 但注射疫苗后肿瘤中心坏死。
在开放标签,剂量递增,多剂量研究中,患者每四周接受3次BVAC-C注射。在3位患者的队列设计中以1×10* 7,4 ×10 *7或1×10*8的剂量实施剂量递增 细胞/剂量。主要结局指标为剂量限制性毒性,浆液性不良事件和临床实验室检查。客观反应率是探索性的次要终点。
在部分缓解的患者中,缓解时间为10个月。在9例可评估患者中,有5例疾病稳定,疾病稳定率为56%。这些患者稳定疾病的持续时间范围为4.2个月至11个月。总体中位无进展生存期为6.8个月。6个月时的中位总体生存率为89%,而12个月时的中位OS率为65%。大多数不良事件为轻度至中度。没有剂量限制性毒性。这项研究表明,对于HPV 16或HPV 18阳性复发性宫颈癌患者,BVAC-C具有良好的耐受性和持久的抗肿瘤活性。基于这一令人鼓舞的结果,现在正在进行一项多中心2期临床试验,目前该研究仍在招募中。将BVAC-C和BVAC-C与二线化疗对复发性宫颈癌的女性进行比较。此外,目前正在研究BVAC-C与PD-1或PD-L1*制剂抑**的组合。
入选标准:
- 多发性转移性进行性或复发性HPV 16或18型阳性子宫颈癌患者
- 患者已接受1种或多种铂类双线化疗作为进展性或复发性肿瘤病变的既往治疗方法(先前的治疗方法不包括铂类化学疗法在进展或复发之前接受放射线疗法作为一线治疗)
- 根据RECIST至少有1个可测量病变的患者
- 20至70岁之间的女性患者
- ECOG表现状态介于0到2之间的患者
- 患者在筛查测试中符合血液测试标准ANC≥1500/微升LLN≤ALC≤ULN血小板≥100,000/μL血红蛋白> 9g / dL
- 患者在筛查测试中符合血液化学测试标准血清肌酐≤2.0 mg / dL计算的肌酐清除率≥50 mL / min血清胆红素≤1.5×正常值上限ALT和AST≤2.5×ULN(肝转移患者≤5 x ULN)
- 在此临床试验中同意医学上可接受的避孕措施的患者
- 可以预期至少三个月或更长时间的患者
- 患者决定参加此临床试验并签署书面知情同意书
【出国看病爱诺美康】