不论是支持与理解,还是不同见解,请先关注后一起参与评论探讨,感谢支持!

文丨江玉珘
编辑丨江玉珘
前言
假单胞菌属细菌与肠杆菌类细菌在优先碳底物的消耗顺序上几乎相反,并且这一过程受RNA结合翻译抑制子和调节性非编码RNA拮抗子的控制。
它们在微生物与植物相互作用中的作用以及潜在的机制仍不确定,展示了根际固氮假单胞菌,其次是较不利的底物柠檬酸,最后是葡萄糖。
并且有助于最佳的氮酶活性和高效的根部定殖,Hfq在这个调控网络中有着核心作用,通过不同的作用机制,包括抑制底物特异性分解基因的翻译。
促进氮酶基因nifH的转录后调控,以及对外源多糖基因簇的转录产生积极影响,结果展示了一个Hfq介导的机制,将碳代谢与固氮和根部定殖联系在一起,这可能赋予根际细菌在根际环境中的竞争优势。
绿脓杆菌A1501中碳分解抑制机制与根际固氮及植物互作的调节关系探析
碳分解抑制控制了优选碳底物的顺序分解,从而增强了细菌在其自然栖息地中的竞争能力,绿脓杆菌属细菌被认为是广义菌。
因为它们可以从各种生态位中分离出来,并具有广泛代谢化合物作为碳源和能源的显著特性。
绿脓杆菌在代谢上多样化,并且表现出智能的取食者特性,优先分解有机酸,特别是三羧酸循环中间产物,而不是碳水化合物。
绿脓杆菌使用了与肠杆菌相比的“反向”碳分解抑制,这可能反映了在不同生态位中发生的不同进化,以更好地适应特定环境。

细菌的碳分解抑制的分子机制在微生物中有显著差异,特别是,大肠杆菌和枯草杆菌在转录水平上介导碳分解抑制,而在绿脓杆菌中,碳分解抑制在翻译水平上发挥作用。
在优选碳源存在的情况下,Hfq通过在特定目标mRNA上与Crc形成抑制复合物来抑制参与利用非优选碳源的靶基因的翻译,新兴证据进一步揭示。
Crc没有固有的RNA结合活性,但增加了Hfq/Crc/mRNA三部复合物的稳定性,类似于CA基序的序列存在于绿脓杆菌的oprB1、gtsABC、benR、benA、alkS和alkB基因,假单胞菌的amiE、antR、estA、bkdR和aroP2基因,荧光绿假单胞菌的xutR和xutA基因。
溶菌草杆菌的oprB基因,以及沃兰杆菌的gluP基因中,这些基因参与了非优选碳源的利用,几个调节性非编码RNA。
如绿脓杆菌的CrcZ、假单胞菌或荧光绿假单胞菌的CrcZ/CrcY,以及溶菌草杆菌的CrcZ/CrcX,已被确认为碳分解抑制的对抗因子。
这些ncRNA的合成受两组分系统CbrAB和替代sigma因子RpoN的控制,唯一的例外是CrcY,其中激活被认为涉及假单胞菌中的不同转录调节因子。
尽管细菌的碳分解抑制是研究最充分的代谢策略之一,但远未理解这种调节系统的复杂性,碳分解抑制操作的机制似乎不仅控制了参与特定分解途径的基因的表达,还控制了参与微生物-植物相互作用的基因的表达。
发现碳分解抑制的控制对于绿脓杆菌DC3000在感染过程中的生长和存活是必要的,绿脓杆菌的矿物质甘氨酸产生能力。

已报道碳分解抑制控制在与细菌-植物相互作用相关的功能中的参与,如肺炎克雷伯菌和根瘤菌,这表明这种机制在根际细菌中是普遍存在的。
根际是一个氮限制环境,有利于根瘤菌的增殖;维持与根部相关的固氮所需的能量来自于根际中可用的富含碳的分泌物的氧化,另一个有趣的新兴方面是碳分解抑制与根际固氮细菌的氮固定之间的关联。

属于绿脓杆菌属的细菌对于植物根际的高效定殖,得益于多种功能的共存,如趋化运动性、表面附着、生物膜形成、应激响应和固氮。
其中最具代表性的菌株之一是绿脓杆菌A1501,这是一个模型固氮菌,最早是从水稻根际中分离出来的,由于其固氮能力。
A1501能够击败其他土壤细菌,在碳丰富但氮限制的根际环境中增殖,以定殖于根表面或内皮层,并有益于寄主植物的生长。
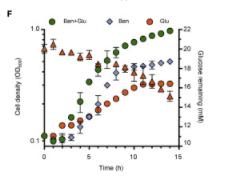
之前在P. stutzeri A1501中鉴定了几个与碳分解抑制有关的基因,随后对P. stutzeri A1501基因组进行的转录分析结果。

鉴定出53个非编码RNA,包括crcZ和crcY,发现伴侣基因Hfq在固氮控制中发挥了作用,因为hfq突变株显示出降低的氮酶活性,尽管这种调控的实际机制尚待证实。
专注于对参与碳分解抑制控制的遗传决定因素进行详细分析,以及参与这一机制的一些靶基因。
绿脓杆菌A1501中碳代谢调控机制及其在根际固氮与植物相互作用中的功能研究
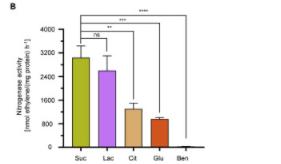
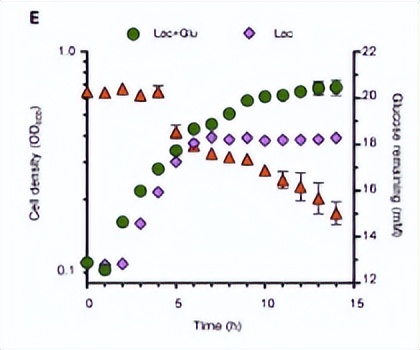
通过测量A1501菌株在单一或双重碳源上的呼吸活性和生长能力,确定了碳底物利用的层次,首先使用Biolog GENIII MicroPlates测量了不同碳源上的呼吸活性。
这些数据与事实一致,即有机酸在假单胞菌属中优先于糖类和芳香化合物使用,与葡萄糖或苯甲酸相比,P. stutzeri A1501在乳酸、琥珀酸或柠檬酸上显示出更好的生长能力。
之前已经报道过A1501菌株在4mM苯甲酸上生长良好,但很少在8mM苯甲酸上生长,因为其有毒效应。
观察到在存在4mM苯甲酸加琥珀酸或乳酸的情况下,A1501菌株能够很好地生长,但没有显示出双相生长。
苯甲酸混合物上,A1501菌株的生长非常差,而且在苯甲酸上生长更慢,这意味着苯甲酸对柠檬酸利用产生了强烈的抑制作用。
构建了单突变和双突变体以深入了解其生物学功能,在任何突变株中,生长在首选的碳源乳酸或琥珀酸上的生长没有受到损害,但在柠檬酸上没有观察到类似的结果。
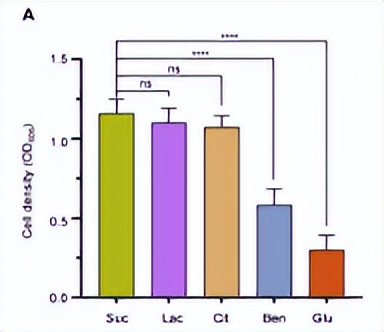
在hfq突变株的表型分析有助于确定P. stutzeri A1501中与非首选碳源利用有关的可能靶基因,在假单胞菌属中,葡萄糖通过Entner-Doudoroff途径代谢。
51gltR基因编码一个转录调节因子,与不同的启动子相互作用,以调节A1501基因组中不同簇中的oprB、glk和edd基因的表达。
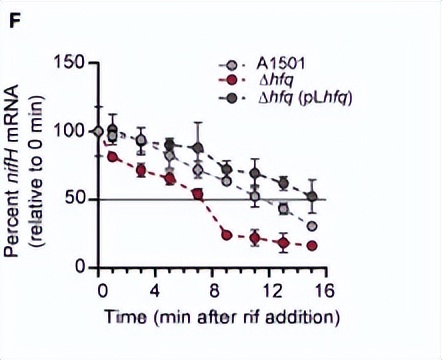
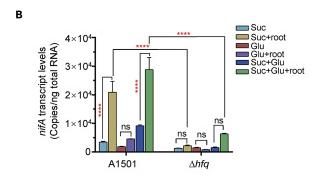
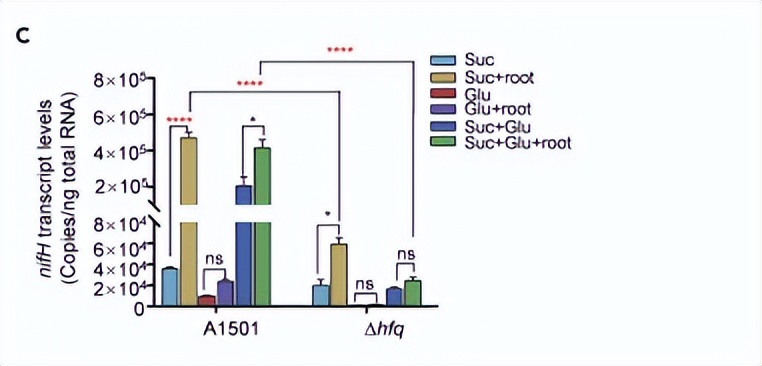
hfq突变株显示出氮酶活性降低,在氮酶Fe蛋白编码基因nifH的编码区域中也识别出了一个CA基序,可能是Hfq的一个潜在靶标,这表明Hfq介导的控制不仅限于碳源利用。
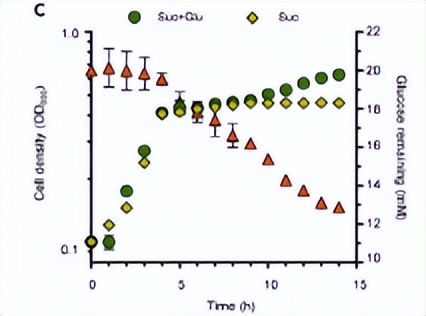
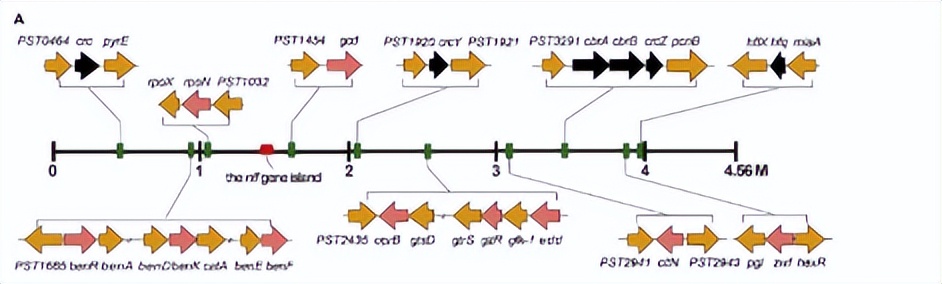
为了进一步评估hfq和crc基因对碳代谢抑制的贡献,首先使用液滴数字PCR在产生强碳代谢抑制条件下测量它们的绝对转录水平,在采用同时含有琥珀酸和葡萄糖的培养基进行双相生长的过程中。

hfq mRNA水平在第一生长阶段迅速上调,然后在第二生长阶段明显下调,crc mRNA水平非常低,并且在两个生长阶段都保持不变。
在第一个指数生长阶段中,hfq mRNA的丰度较高,培养基中的葡萄糖浓度几乎没有变化,这表明Hfq对葡萄糖利用的碳代谢抑制是必需的。

而Δhfq或ΔhfqΔcrc突变体则没有显示出双相生长,这表明碳代谢抑制并没有通过删除Crc而被废除,Hfq的存在可能是碳代谢抑制的必要和充分条件,正如首次在P. aeruginosa中报道的那样。
假单胞菌中Hfq和Crc在碳代谢调控中的协同作用及其植物相互作用机制研究
在P. aeruginosa中,与Hfq不同,Crc并没有发现结合CA基序,而是在Hfq介导的抑制中具有辅助功能。

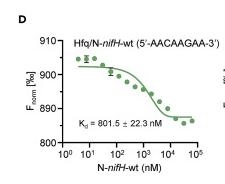
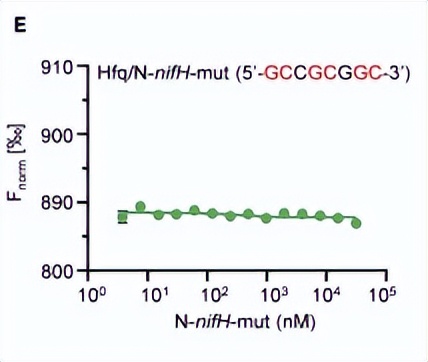
使用微尺度热测池来分析Hfq和Crc蛋白是否能够识别靶基因5'非翻译区域中的预测CA基序,包括gluR、oprB、edd和zwf基因负责葡萄糖利用,编码苯甲酸降解途径的转录激活子的benR基因,以及编码柠檬酸转运体的citN基因。
Hfq直接结合了每个野生型mRNA,使用不含CA基序的突变mRNA重复进行了相同的实验来支持这些数据,且丧失了与Hfq的结合能力。
在Crc存在的情况下,Hfq与靶mRNA的结合显著增强,在没有Hfq的情况下,没有观察到Crc与野生型mRNA的结合。
用于MST分析的包含靶mRNA 5'UTR和完整编码区域的寡核苷酸以及WT或突变的CA基序的序列总结在图3O中。
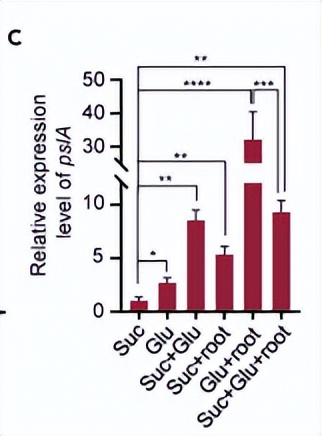
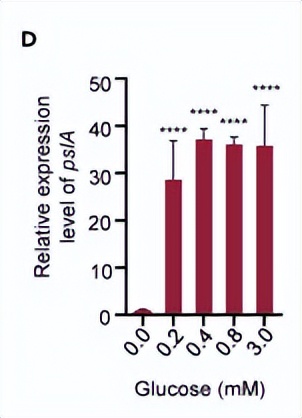
还使用携带了gltR和edd基因的翻译lacZ融合子的菌株进行了其他实验,在同时含有琥珀酸和葡萄糖的培养基中测量体内β-半乳糖苷酶活性时,当融合子引入Δhfq和Δcrc突变体中时,活性增加。
但通过携带野生型hfq和crc基因的质粒进行基因互补后,这种增加被消除,这些体内实验进一步支持了Hfq和Crc协调作用来在翻译水平上介导对葡萄糖利用所需基因的抑制的假设,
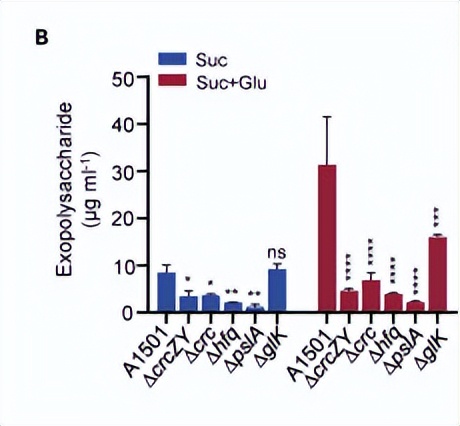
crcZ的水平在引起强烈分解抑制的条件下很低,但在葡萄糖或苯甲酸作为唯一碳源存在的情况下显著增加,值得注意的是,在以柠檬酸为唯一碳源生长时。
在存在琥珀酸和葡萄糖的二相生长中,CrcZ的水平在从第一指数生长阶段过渡到第二指数生长阶段时急剧增加,这表明这种非编码RNA可能对解除Hfq介导的翻译抑制至关重要。

crcY的水平非常低,而且在所有测试条件下,不管使用的碳源如何,几乎不发生变化,这意味着CrcY似乎不在调整分解抑制的强度方面发挥作用。
缺少crcZ的菌株中crcY的水平增加了3.0倍以上,与野生型菌株相比,这个结果可能解释了为什么单独删除crcZ或crcY对分解抑制没有影响。

CrcY的水平在高温或存在盐胁迫条件下上调了约13.4倍和4.5倍,与CrcZ相反,在固氮条件下,其表达上调了约2.2倍,这表明CrcZY在环境胁迫和碳/氮代谢之间存在调节联系。
总结
这表明在根部存在或更精确地说是某些根分泌物存在下,固氮酶活性显著增加,使用相同的条件对突变菌株进行了乙炔还原试验。
而携带Δcrc、Δhfq或ΔcrcZY突变体的接种导致根相关的固氮酶活性显著降低,尤其是在存在混合碳源的情况下。