代谢相关脂肪性肝病(MAFLD)是一系列肝脏疾病的总称,病程复杂,由单纯性脂肪变性(NAFL)进展为非酒精性脂肪性肝炎(NASH),严重者甚至导致肝硬化和肝细胞癌(HCC)。MAFLD与多种代谢紊乱密切相关,包括肥胖、2型糖尿病、高血压、血脂异常和代谢综合征[1]。其发病机制涉及脂质代谢异常、线粒体功能障碍、氧化应激、肠道菌群紊乱和肠-肝轴相关信号转导等[2]。
中医学理论对MAFLD病名无相关记载,按照其症状表现可归属为“痞证”“胁痛”“肝癖”“积聚”“肥气”等范畴,中医药理论和现代临床发现肝气虚弱是其始动病机和重要病因[3]。中医认为“邪之所凑,其气必虚”。肝为刚脏,以气为“用”,肝气属阳,主温煦、升发、推动等功能,肝的疏泄作用需肝气推动。肝气虚,推动无力,则气血雍滞,诸病丛生。肝气虚,三焦不通,脾失健运,胆失疏泄,则脂浊内聚于肝,形成MAFLD[4]。
近年来,多项研究证明肠道微生态失调与MAFLD的发生发展存在密切的联系[5-7]。1项研究已经确定了20种常用于治疗MAFLD的中药,如黄连、人参、大黄、姜黄等[8]。中药发挥作用需要肠道菌群,许多治疗MAFLD的中药成分多以糖苷的形式存在,口服后难吸收、生物利用度低,难以发挥应有的药理作用。但经肠道菌群代谢后,可转变为更易吸收的苷元形式,发挥治疗作用[9]。本文基于肠道菌群和MAFLD的相互作用以及口服难吸收中药对肠道菌群的调节作用在MAFLD治疗中的研究进展进行综述。
1 MAFLD与肠道微生态
1.1 “肠-肝轴”与MAFLD
肠道菌群是寄居在人体肠道内并与宿主共生的微生物群,其数量超过100万亿,1个健康成年人肠道中菌种超过500种,其中99%以上的细菌来源于厚壁菌门(Firmicutes)、拟杆菌门(Bacteroidetes)、变形菌门(Proteobacteria)、放线菌门(Actinobacteria)、疣微菌门(Verrucomicrobia)5个菌门[10]。肠道菌群的数量和结构组成因机体和环境因素而有所不同,但在一定范围内保持动态平衡。当宿主患病时,该动态平衡就会被打破,导致菌群失调、肠道屏障削弱,致病菌增多,正常菌和有益菌的定植能力下降,免疫功能降低,进一步引发或加重疾病。
“肠-肝轴”学说是在1998年时由Marshall[11]提出,该轴是1个复杂的结构,其2个组成部分(肠屏障和肠道微生物群)的改变在肝损伤中起关键作用[12]。在肝脏功能异常或者受损而导致肠道屏障损伤后,肠道内的细菌及其产生的内毒素经过门静脉系统进入肝脏,激活Kupffer细胞释放炎症因子,并通过刺激toll样受体(TLR)促进肝脏炎症。由于肠-肝轴的双向性,肝脏在体循环和胆道释放的胆汁酸可能对肠道内引起细胞膜或DNA损伤的细菌有直接影响[13]。肠-肝轴学说的提出和研究说明了肠道菌群对肝脏疾病发生、进展的作用,以及疾病导致的肠道内环境的改变。肝脏产生的胆汁酸、免疫细胞释放的炎症因子、肠道菌群的代谢物如胆碱、乙醇、短链脂肪酸等共同影响MAFLD的发展。
1.2 MAFLD病理状态下的肠道菌群变化
1.2.1 肠道菌群结构组成的变化
许多研究表明MAFLD患者与健康人群的肠道菌群在组成和数量上存在显著差异[14-26],具体变化见表1,↑代表升高、↓代表降低。与健康人相比,高脂饮食或者肥胖导致的MAFLD患者肠道菌群均呈现厚壁菌门/拟杆菌门(F/B)值增加,或者厚壁菌门相对丰度升高、拟杆菌门相对丰度下降。产特定化合物的细菌也发生了菌群微生态失调,如产乙醇的细菌,尤其是克雷伯菌属和埃希氏菌属的含量在MAFLD患者中更丰富[14]。
此外,对动物的研究发现MAFLD组的厚壁菌门、放线菌门相对丰度上升,拟杆菌门、梭杆菌门、钩端杆菌门、栖热菌门、疣微菌门相对丰度下降[15]。梅璐[16]比较了高脂饲料喂养和正常饲料喂养大鼠的肠道菌群成分,发现高脂饲料组大鼠的颤螺菌属丰度升高,拟杆菌属、乳酸杆菌属丰度下降。Kang等[17]发现MAFLD小鼠丹毒梭菌属、戈氏杆菌属和链球菌属丰度增加,双歧杆菌属丰度减少。

1.2.2 肠道屏障受损
大量研究证明了肠道菌群与MAFLD的发展密切相关,相关机制是菌群失调导致肠道屏障受损,引起肠道通透性增加,以及肠道菌群代谢物和免疫炎症的作用(图1)[27]。
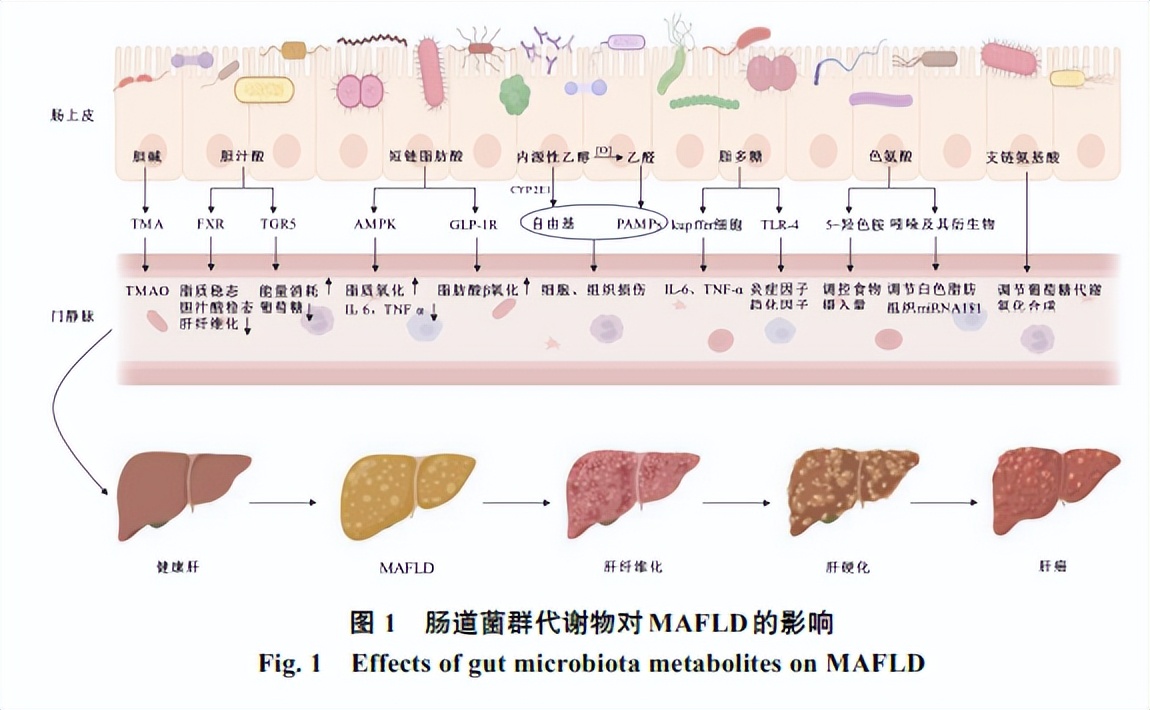
肠道屏障主要是由黏膜上皮、紧密连接蛋白(TJP)和免疫细胞屏障组成[28]。肠道紧密连接蛋白包括occludin、claudin家族、黏附分子(JAMs)、紧密连接相关MARVEL蛋白(TAMPs)以及闭锁小带蛋白-1(ZO-1)、闭锁小带蛋白-2(ZO-2)、闭锁小带蛋白-3(ZO-3)等连接子蛋白[29-30]。Rahman等[31]通过研究缺失编码JAMs基因小鼠的肠上皮屏障,发现高脂饮食诱导的MAFLD小鼠结肠黏膜上的occludin和claudin-4蛋白表达减少。
在对人体研究中发现与健康组相比MAFLD患者肠道黏膜中JAM-A蛋白含量减少、转录功能减退,并且JAM-A蛋白含量减少与黏膜炎症增加相关。研究表明肠道通透性增加与MAFLD进展之间存在线性关系,而且随着疾病严重程度的增加,相关性增强。具体而言,39.1% MAFLD患者表现出肠道通透性增加[32]。肠道通透性增加会促使内源性乙醇、脂多糖(LPS)等菌群代谢物通过肠腔易位至血液,再由门静脉进入肝脏,激活肝脏内Kupffer细胞、肝星状细胞上的TLR,诱导释放白细胞介素-1(IL-1)、白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α),促进肝脏炎症和纤维化,最终导致MAFLD的发生[33]。
1.2.3 肠道菌群代谢物对宿主的影响
胆碱作为人体必需的营养素,影响肝脏的脂质代谢和胆固醇代谢。机体主要从食物中获取胆碱,肠道细菌的特定亚群(大肠埃希氏菌、奇异变形杆菌、彭氏变形杆菌等)可将胆碱转化为三甲胺(TMA)和二甲胺(DMA)[34]。TMA通过门静脉进入肝脏,在肝脏进一步代谢为三甲胺- N -氧化物(TMAO)。Barrea等[35]发现TMAO水平与MAFLD的严重程度呈正相关。Chen等[28]检测了MAFLD患者和健康人群血浆TMAO水平,发现MAFLD患者的TMAO水平是健康组的4.17倍。TMAO除了与MAFLD直接相关外,其介导的其他代谢紊乱(如血脂异常)也可能间接促进MAFLD的发展[36]。此外,微生物群的胆碱转化降低了胆碱在肝脏中的生物利用度,从而导致极低密度脂蛋白(VLDL)低效输出、脂质积累和肝脏炎症[37]。
胆汁酸是肝肠循环中的重要物质,同时也是重要的信号分子,能够通过法尼酯X受体(FXR)与胆汁酸G蛋白耦联受体(TGR5)调节糖脂代谢[38]。在小肠中激活FXR可以抑制胆汁酸合成、调节脂肪生成和减少肝脏纤维化;激活TGR5会增加肠道胰高血糖素样肽-1(GLP-1)的释放,从而提高机体耐糖量[39]。研究表明,MAFLD患者肠道和血浆中出现高水平胆汁酸代谢物。肠道中高水平的胆汁酸不仅对肠道微生物群有害,而且会导致慢性代谢紊乱的发展[40]。Janssen等[41]通过瓜尔胶刺激肠道菌群诱导的肝脏炎症和纤维化模型来研究胆汁酸在MAFLD中的作用,结果表明脂肪肝炎患者的胆汁酸水平显著升高,并且脱氧胆酸参与促进肝损伤和MAFLD。
短链脂肪酸(SCFAs)是难以消化的碳水化合物经肠道菌群发酵而来的代谢物,是少于6个碳的脂肪酸,其中乙酸盐、丙酸盐、丁酸盐是胃肠道中含量最高的SCFAs。SCFAs有调节肠道激素、免疫功能、维持肠道完整性、能量稳态的作用[42]。SCFAs能增加GLP-1的分泌,使肝脏中肠道胰高血糖素样肽-1受体(GLP-1R)激活,增加脂肪酸的β氧化,从而缓解MAFLD[38]。此外,补充SCFAs能激活腺苷酸活化蛋白激酶(AMPK)信号通路,增加脂质氧化以及抑制肝脏炎性细胞因子IL-6和TNF-α的表达,减少肝脏脂肪沉积和减轻炎症,进而改善MAFLD[43]。然而,由于乙酸盐、丁酸盐参与脂质的合成,因此SCFAs进入肝脏会促进MAFLD的发生[44]。
肠道菌群代谢碳水化合物的产物除了SCFAs之外还有内源性乙醇,这也是MAFLD的病因之一。Ivana等[45]的研究结果显示NASH患者的血清内源性乙醇浓度显著高于健康对照组。在肠道中,乙醇及其氧化代谢物乙醛通过促进炎症细胞因子表达、减少单磷酸腺苷(AMP)产生、破坏肠道紧密连接、增加肠道通透性,促使病原体相关分子模式(PAMPs)转运至肝脏,增加炎症细胞因子TNF生成、升高脂肪生成相关因子脂肪酸合成酶水平、上调核转录因子-κB(NF-κB)信号通路,从而加快MAFLD进程[34]。过量乙醇能增加乙醇氧化酶——细胞色素P450 2E1(CYP2E1)的活性,促进自由基的生成,进一步损伤肝脏[35]。
MAFLD导致肠道屏障失调和肠道菌群中革兰阴性菌过度生长,其细胞壁成分脂多糖(LPS)通过肝肠循环到达肝脏。LPS到达肝脏后,能够激活Kupffer细胞,释放IL-6、TNF-α等炎性因子,促进肝脏细胞脂质化[46]。同时,LPS也可以与TLR-4结合,激活NF-κB信号通路,诱导炎症因子和趋化因子产生,导致肝脏损伤和NASH[47]。有研究证明由LPS诱导的NOD样受体蛋白3(NLRP3)炎症小体激活与NASH的进展有关[48-49]。NLRP3炎症小体可增加促炎细胞因子的分泌,介导无菌炎症、导致组织损伤。
在MAFLD晚期尤其NASH和肝硬化期间,由梭状芽孢杆菌、肠杆菌等代谢氨基酸产生的氨若无法通过鸟氨酸循环生成尿素则会导致高氨血症,严重时甚至发展为肝性脑病,加重肝脏疾病。因此高氨血症可以作为衡量肝脏疾病严重程度的标志物[39]。此外,肠道菌群的其他代谢物(如吲哚类、色氨酸类等)也能从不同方面调节宿主的脂质代谢、免疫功能,进而影响MAFLD的发展[28]。
综上所述,肠道菌群对MAFLD的影响主要来自其代谢物的作用、肠道屏障的改变以及对免疫系统的调节。其中肠道通透性的增加是MAFLD发生、发展中的重要环节。肠道菌群的代谢物能通过调节细胞因子、刺激免疫细胞、激活炎症信号等不同方面加剧MAFLD。
2 口服难吸收中药治疗MAFLD
越来越多的研究证明,中药单体或化合物可以通过肠-肝轴调节肠道菌群及其代谢产物的组成,从而在调节免疫炎症、减轻炎症损伤、促进肝脏再生等方面发挥重要作用,延缓MAFLD的进程。一方面中药发挥扶正祛邪作用,调节人体气血阴阳偏盛,增强机体免疫功能;促进有益菌生长繁殖,抑制致病菌生长繁殖,直接或间接调节肠道微生物群的组成并维持其动态平衡,调节肠道屏障[50]。另一方面,中药治疗MAFLD也离不开肠道菌群的调节,口服中药具有使用方便、安全性高、毒副作用小等特点,但有效成分常存在难吸收、生物利用度低的问题。肠道菌群可通过氧化、还原、羟基化、乙酰化代谢药物,促进中药成分吸收,提高生物利用度[51]。
许多中药成分具有很强的生物效应,却存在生物利用度极低的问题,如皂苷、黄酮、生物碱类等成分。临床应用较多的为口服给药,但在口服过程中中药成分的溶解性和渗透性对药物在体内的生物利用度有很大影响。
影响口服药物吸收速度和程度的3个主要因素是溶出度、溶解性和肠道渗透性,生物药剂学分类系统(BCS)根据溶出度和渗透性原理将药物分为4类:Ⅰ类药物(高溶解性、高渗透性),Ⅱ类药物(低溶解性、高渗透性),Ⅲ类药物(高溶解性、低渗透性),Ⅳ类药物(低溶解性、低渗透性)[52]。除Ⅰ类药物外,其他3类药物均存在生物利用度低的问题,多数治疗MAFLD的中药有效成分均属于这3类。例如姜黄素、白藜芦醇属于Ⅱ类药物;人参皂苷Rb1属于Ⅲ类药物;小檗碱为Ⅳ类药物。这些化学成分可以恢复肠道菌群多样性,促进有益菌生长,抑制致病菌的生长,改善肠通透性,提高机体免疫功能(图2)。
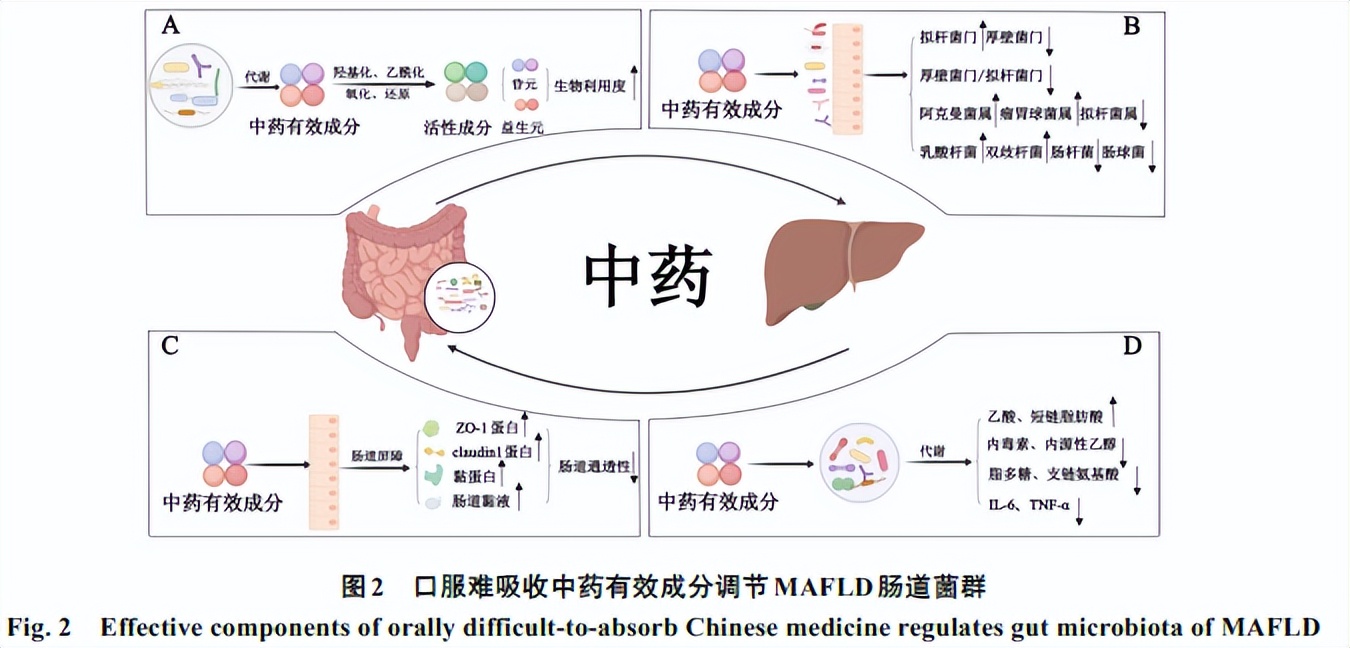
2.1 黄酮类成分
槲皮素(3,5,7,3',4'-五羟基黄酮)是存在于槐米、桑叶等多种中药的黄酮类化合物。口服槲皮素后游离型槲皮素、结合型槲皮素(包括槲皮素的硫酸酯和葡糖醛酸苷)和总槲皮素的生物利用度分别为5.3%、47.8%、59.1%[53]。槲皮素口服后被唾液淀粉酶部分分解为酚酸,以酚酸(原儿茶酚)的形式被吸收[54]。在小肠中槲皮素经肠道微生物作用发生葡萄糖酸化、硫酸化、甲基化等反应,生成II相代谢产物被吸收利用,发挥相应的药理作用[53]。
槲皮素能调节高脂饮食诱导的肥胖大鼠的肠道菌群,抑制与肥胖相关的韦荣球菌、芽孢杆菌、圆柱状真杆菌生长,降低F/B值,减少变形菌门细菌的数量,从而恢复大鼠肠道菌群平衡[55]。Yang等[56]研究发现,槲皮素可以显著降低血清转氨酶水平,恢复肝脏过氧化氢酶和谷胱甘肽的含量。此外,槲皮素能显著抑制IL-1β、IL-6和TNF的生成,升高血清总胆汁酸水平和降低肝脏总胆汁酸水平。Porras等[57]的实验发现与高脂饲料组相比,饲料中加入槲皮素喂养的MAFLD小鼠阿克曼菌属丰度升高,阿克曼菌属丰度与MAFLD的活动程度呈负相关,并且阿克曼菌属的细菌能减少内源性乙醇、内毒素的产生。
姜黄素是从姜科植物姜黄等中药提取的天然活性成分,口服生物利用度低(4.13%),难以被机体吸收利用而发挥作用[58]。但经肠道微生物作用后,姜黄素发生还原、羟基化、脱甲氧基化、脱甲基化等生物转化,生成二氢姜黄素、四氢姜黄素、单葡萄糖醛酸聚合物等,生物利用度提高、水溶稳定性提高,更易被胃肠道吸收[59]。研究发现姜黄素能调节高脂饲料喂养大鼠紊乱的肠道菌群,升高具有抗炎作用的乳酸杆菌和双歧杆菌的丰度,降低大肠杆菌的丰度[60]。乳酸杆菌能恢复肠道屏障,双歧杆菌能改善机体代谢,改善糖耐量[61]。姜黄素能恢复肠道紧密连接蛋白ZO-1和claudin-1的表达,提高肠道碱性磷酸酶活性,改善肠道屏障,从而改善MAFLD[62]。
2.2 生物碱类成分
黄连生物碱治疗MAFLD以及与肠道菌群的相互作用已有大量研究,黄连生物碱的主要成分为小檗碱,属于异喹啉类生物碱,不易被肠上皮吸收,口服生物利用度仅为0.68%[63]。肠道菌群能生物转化小檗碱,保证吸收和分解。在宿主肠道中,小檗碱在肠道菌群分泌的硝基还原酶的催化作用下转化为更易吸收、但无活性的代谢物二氢小檗碱(dhBBR),二氢小檗碱被肠壁组织吸收后,立即被氧化为小檗碱,在血液循环中发挥作用[64]。
小檗碱主要通过肠-肝轴改善MAFLD,相关机制是升高肠道紧密连接蛋白occludin的水平,改善肠道屏障功能[65];调节肠道菌群,减少代谢产生的肠源性内毒素,降低肝*毒脏**性作用[66]。张园园等[67]研究发现小檗碱能降低血清和肝脏中LPS、IL-6水平,抑制炎症损伤。此外,小檗碱对肠道菌群也有调节作用,能降低厚壁菌门丰度,升高变形菌门和疣微菌门丰度。疣微菌门中的阿克曼菌对MAFLD治疗有重要作用,阿克曼菌能降解黏蛋白、刺激黏液产生、增加黏液厚度,从而增强肠道屏障功能[68]。
荷叶生物碱是从荷叶中提取的生物碱类活性物质,口服后主要在肝脏和肾脏通过氧化、脱甲基化、葡糖糖醛酸化及硫酸化反应生成I相、II相代谢产物被机体吸收利用[69]。研究表明荷叶生物碱能调节高脂饲料诱导肥胖小鼠的肠道菌群,主要表现为降低罗斯伯里氏菌属、考拉杆菌属等产生SCFAs菌属的相对丰度,降低脱硫弧菌属的丰度[70]。脱硫弧菌属的代谢产物硫酸盐会诱发炎症反应,破坏肠道黏膜屏障,扰乱肠道微生态。荷叶生物碱能调节肝脏中脂质的β-氧化控制脂质代谢紊乱,缓解MAFLD[71]。此外,荷叶生物碱在人体肠壁形成的1层脂肪隔离膜能阻止脂肪的吸收和堆积,发挥调脂作用[72]。
2.3 皂苷类成分
人参皂苷是人参的主要活性成分,具有抗炎、抗肿瘤、预防糖尿病和MAFLD等作用。由于人参皂苷在肠道内难吸收、滞留时间长,因此难以直接进入血液发挥药理作用。肠道微生物分泌的糖苷酶使人参皂苷去糖基化,生成次级糖苷或糖苷配体,与原皂苷相比更容易被肠道吸收,具有更高的生物利用度[73]。在该过程中,皂苷本身被肠道菌群代谢,同时调节肠道菌群结构。人参皂苷能升高MAFLD大鼠厚壁菌门和拟杆菌门丰度,而降低厚壁菌门/拟杆菌门的F/B值,同时升高乳酸杆菌的丰度[74]。研究发现人参皂苷Rg3能通过抑制Th1细胞分化,调节肠道内Th1/Th2平衡,抑制NF-κB信号通路激活,调节肠道免疫,促进肠道黏膜的修复等途径改善MAFLD[75]。
绞股蓝皂苷是从中药绞股蓝中提取到的,对肝脏有一定的保护作用。研究表明绞股蓝皂苷可以减轻MAFLD小鼠的脂肪型炎症,降低血清谷氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、总胆固醇水平并能显著改善肠道菌群结构。绞股蓝皂苷干预后,MAFLD小鼠肠道菌群F/B值降低,阿克曼菌和Fissicatena的丰度升高[76]。实验发现绞股蓝组大鼠与MAFLD组相比对照组大鼠肠道微绒毛更规则,紧密连接和桥粒得到改善,间隙更小。这些现象均表明绞股蓝总皂苷能改善MAFLD大鼠肠道屏障[77]。
甘草皂苷是甘草的主要提取物,生物活性高。实验发现甘草皂苷能升高MAFLD小鼠肠道菌群丰度,具体表现为升高瘤胃球菌科、毛螺菌科细菌丰度,促进SCFAs生成,降低F/B值、降低内毒素产生菌——脱硫弧菌丰度。此外,甘草皂苷能促进肠道紧密连接蛋白、黏蛋白表达,增强肠道屏障功能[78]。
2.4 萜类成分
白藜芦醇是来自虎杖等中药的蒽醌萜类化合物,其与肠道菌群密切相关。缪萍等[79]发现白藜芦醇能重塑代谢综合征大鼠肠道菌群,减少大肠杆菌、链球菌等致病菌含量,增加益生菌乳酸杆菌、双歧杆菌含量。此外,白藜芦醇能抑制IL-6、TNF-α等炎症因子表达,减轻炎症因子对肠黏膜的损伤,维持肠道屏障完整。肠道菌群在白藜芦醇的生物代谢中也发挥重要作用。白藜芦醇口服后被葡萄糖醛酸化和硫酸酯化,导致血液中游离白藜芦醇的含量非常低,生物利用度降低,不足1%[80]。经肠道菌群作用后可以将白藜芦醇代谢为白藜芦醇衍生物(如二氢白藜芦醇),提高生物利用度[81]。
研究发现从泽泻根茎中提取的泽泻醇对改善MAFLD有一定的疗效,主要通过降低乳酸杆菌、都灵菌属、粪棒状杆菌属、Muribaculaceae丰度,升高 Ileibacterium 丰度,进而改善紊乱的肠道菌群,调节肠道菌群多样。此外,泽泻醇能减少支链氨基酸、脂多糖等肠道菌群代谢物的产生[82]。
2.5 酚类成分
丹参总酚酸是来自中药丹参中的多酚化合物,其中丹酚酸A、B是水溶性成分中重要的活性单体。研究表明丹酚酸A给药可以减轻高脂饲料和高碳水化合物饲料喂养小鼠的肝脏损伤,抑制肝脏脂肪变性,减少过氧化氢和氧自由基的产生以及TNF-α、IL-6的分泌,从而抑制MAFLD小鼠的氧化应激[83]。丹酚酸B上调Sirt1抑制高脂饲料诱导小鼠的肝脏脂肪变性,减轻肝脏炎症,降低拟杆菌属、臭杆菌属、螺杆菌属、黏螺菌属等有害菌的丰度,减轻肝脏损伤[84]。
但丹酚酸A、B的生物膜透过性差、口服生物利用度低、胃肠道稳定性差,临床应用受到限制[85-86]。实验研究发现丹参总酚酸能调节2型糖尿病模型小鼠肠道菌紊乱,升高瘤胃球菌科未分类菌属、瘤胃梭菌属_5等乙酸产生菌、脱硫弧菌属等丙酸产生菌和瘤胃梭菌属_UCG-004、罗氏菌属等丁酸产生菌的丰度,从而增加肠道内短链脂肪酸的产生,为机体供能[87]。
2.6 多糖类成分
多糖溶解度较好,但因不稳定、相对分子质量大的特点导致生物利用度较差。研究发现肠道无法吸收的多糖可以作为益生元对肠道菌群发挥作用[88]。
玉屏风多糖是由黄芪、白术、防风水煮醇沉干燥后得到的提取物。李东琦[89]发现玉屏风多糖能调节肠道微生态,增加拟杆菌属、 Muribaculum 属细菌含量,且不同剂量的玉屏风多糖对MAFLD小鼠肠道菌群的调节作用不同。低剂量组的拟杆菌属细菌数量显著高于MAFLD组,高剂量组能显著减少粪杆菌 Faecalibaculum 属细菌含量,增加拟杆菌属、肠鼠杆菌 Muribaculum 属细菌含量。甘露[90]研究发现玉屏风多糖能抑制结肠上皮细胞死亡,促进外周血中性粒细胞凋亡,抑制中性粒细胞向结肠聚集的趋化作用,减轻肠道局部炎症反应,维持肠道屏障完整。
研究发现黄芪多糖抗MAFLD作用显著。黄芪多糖能重塑肠道微生态,增加高脂饲料小鼠肠道菌群的丰富度和均匀度。显著降低厚壁菌门丰度,升高拟杆菌门丰度,降低厚壁菌门/拟杆菌门的比值,增加脱硫弧菌属细菌的相对丰度,其中寻常脱硫弧菌丰度最高且与代谢紊乱呈负相关。此外,寻常脱硫弧菌还能高效产生乙酸,缓解MAFLD[91]。
枸杞多糖是从枸杞中提取的蛋白多糖,结构复杂,主要由葡萄糖、阿拉伯糖、鼠李糖等单糖组成,难以被吸收消化入体,肠道细菌可以通过消化其单糖、降低分子量、降低多糖总含量等方式进行代谢利用[92]。枸杞多糖能升高高脂饲料小鼠肠道内一些潜在益生菌的相对丰度,如双歧杆菌、乳酸杆菌,抑制肠球菌、肠杆菌的生长,发挥益生元作用[93]。
五味子多糖能促进肠道双歧杆菌、乳酸杆菌等有益菌生长,抑制肠球菌、大肠杆菌等致病菌生长,改善肠道菌群紊乱。进一步研究发现肠道菌群能将五味子多糖代谢为乙酸、乳酸等短链脂肪酸,降低肠道pH值,进而抑制肠球菌、肠杆菌生长繁殖[94]。口服难吸收中药有效成分调节MAFLD肠道菌群的作用总结为表2。
2.7 中药复方
除中药单体成分外,含口服难吸收成分组成的中药复方也能有效防治MAFLD。
王晶等[95]研究发现茵陈蒿汤可以调节NASH模型鼠脂质平衡,降低血糖水平。茵陈蒿汤也能改善甘油磷脂、嘌呤和谷胱苷肽代谢进而抑制肝脏脂肪变性和肝损伤;降低肠道厚壁菌门、变形菌门、放线菌门的丰度,升高拟杆菌门的丰度[96]。葛根芩连汤主要成分是葛根素、大豆苷、小檗碱等。研究发现,葛根芩连汤能增加ZO-1、claudin-1、趋化因子C-X3-C-基元受体1(CX3CR1)等肠道紧密连接蛋白的表达,保护肠道屏障并能升高拟杆菌门、拟杆菌属细菌丰度,降低厚壁菌门、脱硫弧菌属、颤杆菌属细菌丰度,调节肠道菌群紊乱,从而干预MAFLD的进程[97]。
护肝清脂片主要组成为泽泻、蒲黄、山楂、荷叶、三七,含大量黄酮、生物碱类成分。护肝清脂片可以显著改善MAFLD大鼠肝脏的脂质沉积,促进肠道紧密连接蛋白claudin-1和ZO-1的表达[98]。肠道菌群方面,能降低F/B值,调节瘤胃杆菌、Bacteroidales_S24-7_group、双歧杆菌、Alistipes和厌氧菌丰度[99];促进有益菌norank_f_Bacteroidales_S24-7_group、Alistipe生长,抑制有害菌Blautia生长[98]。
3 结语
MAFLD是除过量饮酒及其他已知致病因素导致的慢性肝病,能通过肠-肝轴影响肠道菌群的结构组成及其代谢,进而破坏肠道屏障,导致机体免疫功能降低,严重威胁人们的身体健康。现代社会高脂饮食、高糖饮食及久坐不动的生活方式导致MAFLD的发病率越来越高,但目前尚无有效的治疗药物。中医以整体观念为核心,通过多环节、多靶点、多途径治疗MAFLD,为治疗MAFLD提供新的思路和方向。从本文所述的临床及实验研究中发现中药活性成分及其复方能通过调节紊乱的肠道菌群、改善肠道菌群多样性、调节肠道菌群代谢物、修复受损肠道屏障、调脂、抗炎、抗纤维化等多种途径缓解MAFLD,这表明中医药具有治疗MAFLD的潜在优势与光明的发展前景,同时也说明中药是治疗MAFLD的理想候选药物,有独特的优势。
但目前仍存在一些不足,限制了中药的临床应用。
首先,MAFLD的临床病理表现主要为肝脏脂质积累、纤维化、炎症反应、氧化应激,但发病机制尚未完全阐明,需选用适宜的动物模型模拟MAFLD的发病机制,进而深入研究中药与肠道菌群的相互作用,促进中药活性成分的发现。
其次,现阶段所使用的治疗MAFLD的部分单味中药及复方口服吸收率低、代谢速率快,中药有效成分尚未完全发挥疗效便被机体代谢排出。所以寻找合适的药物递送系统、提高中药有效成分的生物利用度或寻找肠道益生菌代谢中药促使更多的中药有效成分进入血液增强疗效成为未来的研究趋势。
再次,肠道菌群及其代谢物复杂多样,在中药调节肠道菌群的基础上深入研究中药对特异性菌群的调控及阐明微生物途径的靶向作用尤为重要,这将进一步明确中药的药效作用机制并促进微生物导向的中药研发。
最后,在进一步明确中药对肠道菌群的调节作用后进行系统研究,制定一套适宜、完整的中药调节肠道菌群治疗MAFLD的方案是现阶段亟待解决的问题。
在今后的研究中,针对上述问题进一步探讨,制定更好的解决方案,才能充分发挥中医药治疗MAFLD的优势。同时,中药、肠道菌群、MAFLD三者相互作用、密切联系,找出中药与肠道菌群、MAFLD间以及肠道菌群与MAFLD间的作用靶点并开展深入研究,将为中药治疗MAFLD提供新的方向。
利益冲突 所有作者均声明不存在利益冲突
参考文献(略)
来 源:卢倩,胡静雯,陈洁,贾国香,董亚倩,杨珅珅,李遇伯.口服难吸收中药重塑肠道微生态干预代谢相关脂肪性肝病的研究进展 [J]. 药物评价研究, 2022, 45(10): 2113-2126 .