人胚胎肾293细胞,也常被称为HEK 293、HEK-293、293细胞,或不太精确地称为HEK细胞,是一种从自然流产或流产的胎儿或1973年从女性胎儿组织培养中培养的人胚胎肾细胞中提取的特异性永生化细胞系。
HEK 293细胞因其生长可靠且易于转染而被广泛应用于细胞生物学研究多年。它们还被生物技术行业用于生产用于基因治疗的治疗性蛋白质和病毒,以及对大量化学品进行安全性测试。
293T(或HEK 293T)是一种衍生的人类细胞系,表达SV40大T抗原的突变版本。它在生物研究中非常常用,用于制造蛋白质和生产重组逆转录病毒。
历史
HEK 293细胞是1973年在荷兰莱顿的Alex van der Eb实验室用剪切腺病毒5 DNA转染正常人类胚胎肾细胞培养物而产生的。这些细胞来自一个流产或流产的胎儿,其确切来源尚不清楚。采用van der Eb法培养;腺病毒的转导是由范德埃布实验室的博士后弗兰克·格雷厄姆完成的。1977年,格雷厄姆离开莱顿去了麦克马斯特大学(McMaster University)它们被称为HEK,因为它们起源于人类胚胎肾脏培养物,而293这个数字来自格雷厄姆给他的实验编号的习惯;最初的HEK 293细胞克隆来自他的第293次实验。Graham总共进行了8次转染,只获得了一个培养了几个月的细胞克隆。在可能适应组织培养后,来自该克隆的细胞发育成相对稳定的HEK 293系。
随后的分析表明,这种转化是通过从病毒基因组的左臂插入约4.5K碱基而实现的,这些碱基被整合到人类的19b染色体中
多年来,人们一直认为HEK 293细胞是由成纤维细胞、内皮细胞或上皮细胞转化产生的,这些细胞在肾脏中都很丰富。然而,最初的腺病毒转化是低效的,这表明最终产生HEK 293系的细胞可能在某种程度上是不寻常的。Graham和同事提供的证据表明,由腺病毒转化人胚胎肾细胞产生的HEK 293细胞和其他人类细胞系具有许多未成熟神经元的特性,这表明腺病毒在原始肾脏培养中优先转化神经谱系细胞。
我们对HEK 293及其5个衍生细胞系的基因组和转录组进行了综合研究,并将其转录组与人肾、肾上腺、垂体和中枢神经组织的转录组进行了比较,HEK 293的模式与肾上腺细胞最相似,肾上腺细胞具有许多神经元特性。考虑到肾上腺的位置(肾上腺的意思是“紧邻肾脏”),一些肾上腺细胞可能出现在胚胎肾源培养物中,并可能被腺病毒优先转化。腺病毒转化神经系细胞的效率远高于典型的人肾上皮细胞。因此,胚胎肾上腺前体细胞似乎是HEK 293细胞系最有可能的起源细胞。因此,HEK 293细胞不应用作典型肾细胞的体外模型。
HEK 293细胞具有复杂的核型,每条染色体有两个或更多的拷贝,模态染色体数为64。它们被描述为低三倍体,包含的染色体数量不到人类单倍体配子的三倍。染色体异常包括X染色体的3个拷贝和17号染色体和22号染色体的4个拷贝。多个X染色体的存在和没有任何Y染色体衍生序列的痕迹表明来源胎儿是女性。
293T细胞系是在斯坦福大学的Michele Calos实验室通过用编码SV40大T抗原温度敏感突变的质粒稳定转染HEK 293细胞系而创建的;它最初被称为293/tsA1609neo.该细胞系第一次被称为“293T”可能是用于制造用于生产逆转录病毒颗粒的BOSC23包装细胞系
变体
HEK 293的多种变体已被报道。
- HEK 293F
- HEK 293FT
- HEK 293T
- HEK 293S
- HEK 293FTM
- HEK 293SG
- HEK 293SGGD
- HEK 293H
- HEK 293E
- HEK EBNA1-6E[11]
- HEK 293MSR
- HEK 293A
- HEK 293T
用于创建293T的转染(涉及质粒pRSV-1609)赋予了新霉素/G418抗性和SV40大T抗原tsA1609等位基因的表达;该等位基因在33°C(其允许温度)时完全活跃,在37°C时具有基本功能,在40°C时不活跃。293T是非常有效的DNA转染(像它的亲本HEK 293)。由于SV40大T抗原的表达,携带SV40起源复制的转染质粒DNA可以在293T中复制,并会暂时保持较高的拷贝数;这可以大大增加从细胞中产生的重组蛋白或逆转录病毒的数量。
已经确定了三个不同的293T分离株的全基因组序列。它们彼此非常相似,但与亲本HEK 293细胞系表现出可检测的差异。
应用
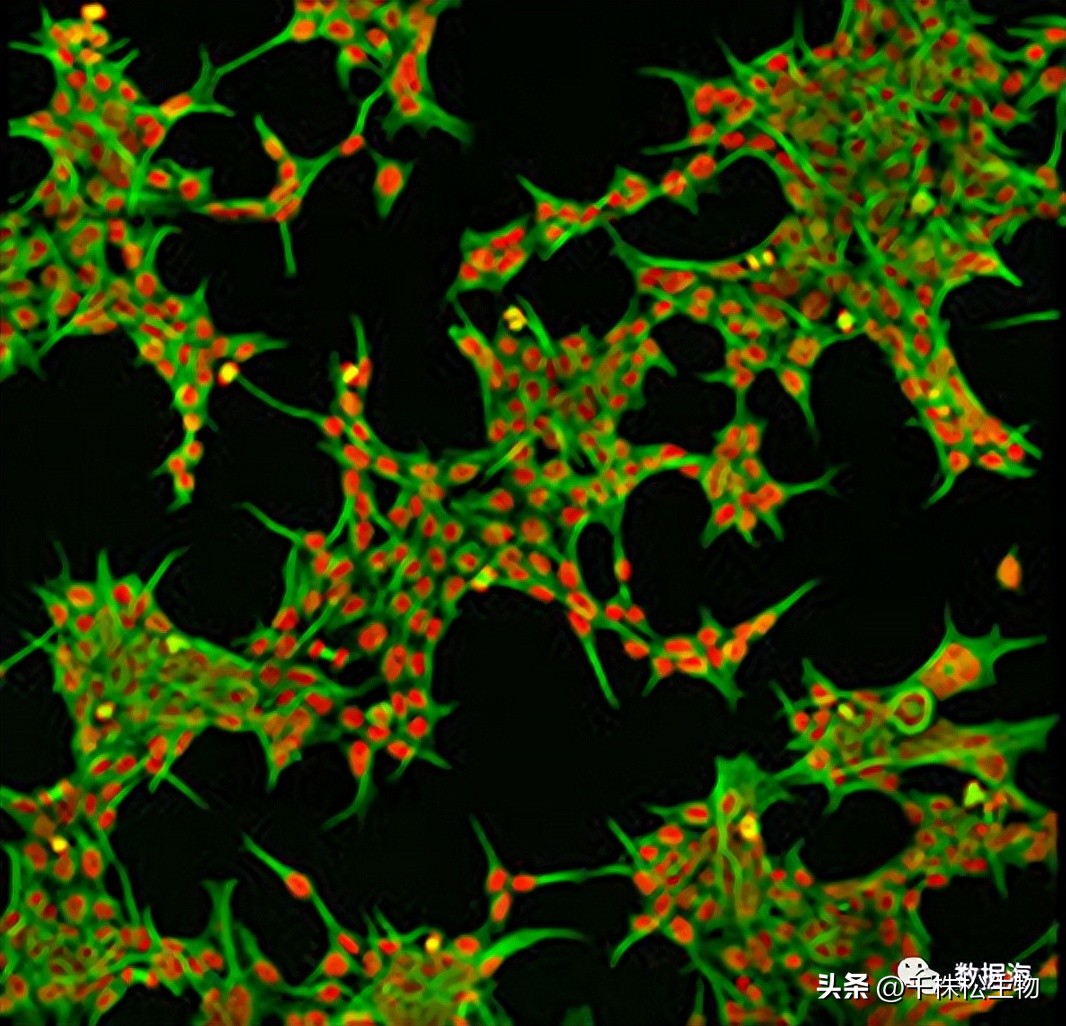
HEK 293细胞的培养和转染都很简单。它们被用作基因表达的宿主。通常,这些实验包括转染感兴趣的基因(或基因组合),然后分析表达的蛋白质。该细胞系的广泛应用是由于其可通过各种技术(包括磷酸钙法)转染,其效率接近100%。
这类实验的例子包括:
- 药物对钠通道的影响
- 诱导型RNA干扰系统
- 异构体选择性蛋白激酶C激动剂
- 两种蛋白之间的相互作用
- 蛋白质中的核输出信号
1985年,HEK 293细胞被用于悬浮培养而不是在塑料板上增殖。这使得大量重组腺病毒载体得以生长。
HEK 293细胞更具体的用途是用于腺病毒载体的增殖。腺病毒提供了一种将基因传递到细胞中的有效手段,这是它们进化的结果,因此作为实验工具非常有用。然而,作为病原体,它们也给实验者带来了风险。这种危险可以通过使用缺乏关键基因的病毒来避免,这些病毒在进入细胞后无法复制。为了繁殖这种病毒载体,需要一种表达缺失基因的细胞系。由于HEK 293细胞表达许多腺病毒基因,它们可以用来繁殖这些基因(通常是E1和E3)缺失的腺病毒载体,如AdEasy.然而,插入的细胞Ad5序列与载体序列之间的同源重组虽然罕见,但可以恢复载体的复制能力。
该细胞系的一个重要变种是293T细胞系。它含有SV40大t抗原,允许含有SV40复制起源的转染质粒的体外复制。这允许扩增转染质粒和延长所需基因产物的时间表达。HEK 293,特别是HEK 293T细胞通常用于生产各种逆转录病毒载体各种逆转录病毒包装细胞系也以这些细胞为基础。
感兴趣的天然蛋白质
根据不同的表达条件,HEK 293细胞的基因表达产物可能不同。以下是在未处理的HEK 293细胞中常见的蛋白:
- 促肾上腺皮质激素释放因子1型受体
- 鞘氨醇-1-磷酸受体EDG1、EDG3和EDG5
- 毒蕈碱乙酰胆碱受体M3
- 瞬时受体电位TRPC1、TRPC3、TRPC4、TRPC6
生物伦理学
Alvin Wong认为,尽管获得细胞系的胎儿来源尚不明确,但有间接证据强烈表明,胎儿来自自愿堕胎。对于一些天主教徒和东正教基督徒来说,这为使用HEK 293及其衍生产品(如疫苗和许多药物)带来了伦理困境。
2020年12月21日,经教皇批准,罗马天主教信仰教义会表示,“在研究和生产过程中使用流产胎儿细胞系的COVID-19疫苗在道德上是可以接受的”,但只有在不存在其他替代方案(或目前无法获得)或存在更严重危险的风险时才可接受。
在COVID-19大流行期间,反疫苗活动人士指出,HEK 293细胞被用于生产牛津-阿斯利康COVID-19疫苗(AKA AZD1222)。最终产物中细胞被过滤掉。
再生元制药(Regeneron Pharmaceuticals)等制药公司表示,现代细胞系已远离其起源,不再被认为是胎儿组织。