目前,已有疫苗来降低乙肝的新发感染率,以及核苷(酸)类似物已延缓慢乙肝患者的肝病进展。但学界仍不满于此,仍坚持探索乙型肝炎病毒(HBV)的感染机制和新的药物靶点,以治愈乙肝为目的,开发新的抗病毒药物和免疫干预措施。
为此, The Lancet Gastroenterology & Hepatology与Nature Reviews Drug Discovery分别发表了一篇综述,详细阐述了HBV的生命周期,并回顾了目前不同的药物研发策略。以下是这两篇综述的主要内容。
HBV病毒学和生命周期
了解HBV的生命周期非常重要,因为每一步都是药物开发的潜在靶点。
乙型肝炎病毒(HBV)是嗜肝DNA病毒科(Hepadnaviridae)家族的成员。HBV感染肝细胞后,开始建立自己的复制周期,并在细胞核中持续存在。
HBV病毒粒子是以脂质为基础的球形结构,直径约为42-47 nm,三种不同的表面抗原(HBsAg)暴露于其外侧,分别为小(S)、中(M)、大(L)病毒包膜蛋白(viral envelope proteins)(图1)。
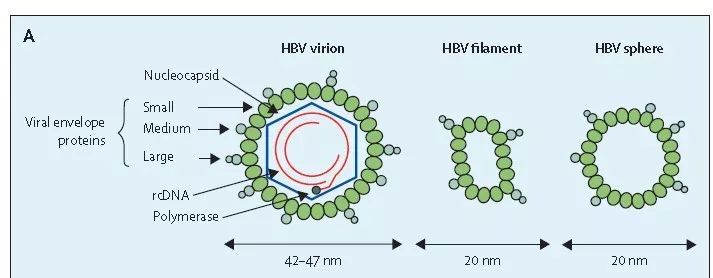
图1 HBV病毒粒子结构(来源:参考文献1)
HBV生命周期如图2所示。
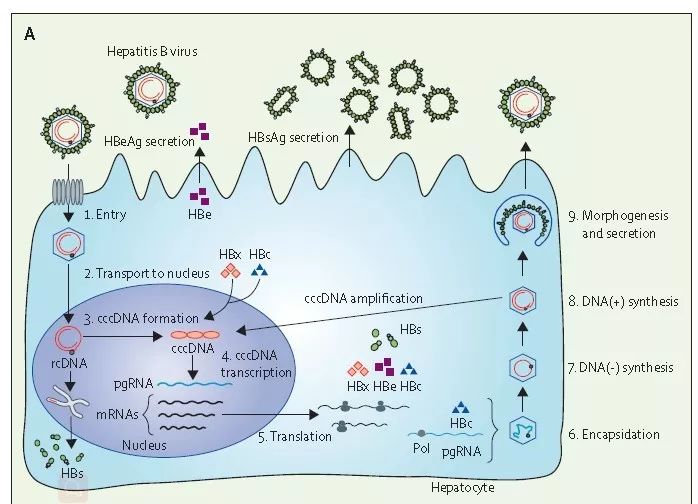
HBV的生命周期:(1)HBV与NTCP受体结合后感染肝细胞;(2)HBV核衣壳运至细胞核,rcDNA进入细胞核,并整合到人类基因组中;(3)rcDNA经宿主因子转化为cccDNA,形成稳定的cccDNA;(4)以cccDNA为模板转录生成病毒RNA;(5)病毒RNA被翻译成HBV蛋白;(6)连接HBV聚合酶的pgRNA被包装成衣壳颗粒;(7)以pgRNA为模板逆转录生成DNA负链;(8)随后生成DNA正链;(9)HBV病毒颗粒和非感染性亚病毒颗粒的形成和分泌。
图2 HBV的生命周期(来源:参考文献1)
大包膜蛋白包含参与病毒进入(viral entry)的受体结合域,在感染时,该受体结合域与人牛磺胆酸钠共转运多肽受体(hNTCP或SLC10A1)相互作用——后者在肝细胞上表达。这种相互作用使病毒通过内吞作用进入肝细胞,并将HBV核衣壳(nucleocapsid)释放到肝细胞质中。所以,可通过阻断病毒与NTCP受体的相互作用,阻止HBV进入肝细胞来预防感染。
HBV的核衣壳由HBV核心蛋白二聚体(HBc)组成,包含部分双链DNA基因组,后者呈松弛环状构象(松弛双连环状DNA,rcDNA)。这个rcDNA长度约为3.2kb,与HBV聚合酶共价连接。在DNA链的5ʹ末端有一个来自前基因组RNA(pgRNA)的RNA引物,对病毒的逆转录来说十分重要。
在感染细胞的胞质中,病毒核衣壳运输至核膜,并释放rcDNA进入细胞核。
rcDNA可以整合到宿主基因组中,通过基因组改变导致癌症的发生。这种整合在HBV复制周期中没有直接作用,但可以作为HBsAg分泌的模板。rcDNA被宿主DNA修复转化为共价闭合环状DNA(cccDNA)。cccDNA与宿主组蛋白结合,形成一个稳定的小染色体,作为所有病毒转录的转录模板。
当翻译出病毒蛋白后,HBV聚合酶与pgRNA相互作用,同时,核心蛋白(HBc)与pgRNA相互作用,启动新核衣壳的组装。
被衣壳包裹的pgRNA逆转录成rcDNA,作为病毒合成的DNA负链模板(正链稍后合成)。最后生成新的核衣壳(nucleocapsid),其可以返回细胞核,并被循环利用以扩充cccDNA池。
另外,核衣壳可与与内质网结合,HBsAg在内质网聚集,并通过分泌途径排出细胞。HBsAg的过量产生导致非感染性亚病毒颗粒的分泌,后者在免疫逃避中起重要作用。
直接抗病毒治疗策略
HBV生命周期的所有步骤都有可能成为抗病毒治疗的靶点(图3)。
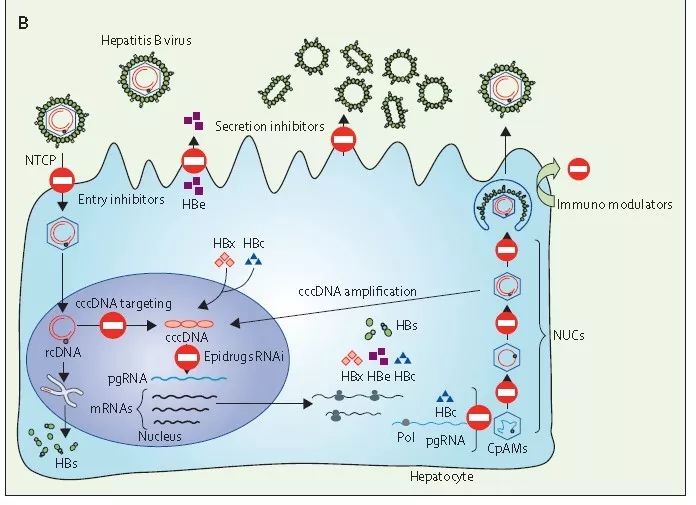
注:RNAi=RNA干扰;Pol=HBV聚合酶;NUCs=核苷(酸)类似物;CpAMs=衣壳组装*制剂抑**。
图3 HBV治疗策略的示意图(来源:参考文献1)
1. 防止HBV进入细胞(Preventing HBV entry)
病毒不断地复制和释放可导致新的肝细胞被感染,从而维持慢性感染状态并扩充cccDNA池。在大多数患者中,核苷(酸)类似物(NUC)治疗不能完全抑制病毒产生。因此,联用病毒进入*制剂抑**和复制*制剂抑**,是阻止新细胞受到感染,并减少cccDNA池的潜在手段。
防止病毒进入的策略包括开发HBsAg衍生的多肽,如Myrcludex B,其可通过与NTCP受体竞争性地结合,阻碍HBV病毒进入细胞。
除了多肽以外,小分子药物如ezetimibe和环孢素衍生物也在研究中被用于阻断HBV进入细胞。另外,HBV的病毒进入也受到靶向HBsAg的单克隆抗体影响,这些抗体还可能具有额外的抗病毒活性,其可以干扰血清HBsAg和感染性病毒的分泌。
丁肝病毒(HDV)利用HBV包膜,因此使用的是相同的病毒进入受体。HBV病毒进入*制剂抑**对同时感染HBV和HDV的患者有很大的益处。
2. 直接靶向cccDNA(Directly targeting cccDNA)
抑制cccDNA的形成是一有力的直接抗病毒策略。然而,在开发相关药物之前,需要对cccDNA的形成过程有更全面的了解。
cccDNA形成的许多关键步骤需要宿主细胞核中的酶(包括TDP2、FEN1和POLK),而病毒微型染色体(minichromosome)的形成需要宿主染色质的组蛋白和其他成分。因此,若要抑制cccDNA的形成可能需要靶向宿主蛋白,由此会造成更多不良反应。
cccDNA形成后,就可以被锌指核酸酶(zinc-finger nucleases)或转录激活因子样效应核酸酶(transcription activator- like effector nucleases)靶向,这些酶已在细胞培养模型中成功用于编辑HBV cccDNA。
基于CRISPR–Cas9的基因编辑策略——在cccDNA中加入突变或者敲除某一基因,可能导致cccDNA失活。临床前实验表明,超过90%的HBV DNA可被Cas9裂解。然而,大约7%的cccDNA基因组在经过CRISPR-Cas9介导的切割之后,能够被修复成不影响cccDNA功能的状态。因此,这一策略需要引入靶向cccDNA中不同位点的多个指导RNA(gRNA),确保cccDNA的失活。在这些基因编辑方法应用于临床之前,还需要解决潜在的问题,包括肝细胞递送、脱靶效应、由于染色体整合HBV DNA的裂解和染色体DNA重组而导致不可预测的后果。尽管存在这些问题,但目前这是唯一一种在组织中让cccDNA永久性失活的方法。
3. 靶向病毒基因表达(Targeting viral gene expression)
高病毒抗原负荷被认为在形成和维持慢性感染中起到重要作用,因此,通过沉默cccDNA转录或者降解病毒RNA直接降低病毒抗原和调节蛋白的表达也具有意义。
(1)转录前的调控:对cccDNA的转录前调控可以通过靶向HBx或HBc来实现,这两种蛋白都与cccDNA的稳定性和表达有关。
(2)转录后的调控:可使用RNA干扰(RNAi)、反义寡核苷酸(ASOs)来降解HBV mRNA。普遍的观点是,靶向HBV mRNA是治疗的一个重要缓解,因为这将限制cccDNA产生HBsAg,从而有助于恢复患者特异性免疫。
4. 抑制衣壳组装(Capsid assembly)
与NUCs单独治疗相比,衣壳组装*制剂抑**与NUCs联合使用可能会进一步降低病毒水平,并有更利于患者HBV特异性免疫重建。目前抑制衣壳组装的小分子化合物可以分为两类:(1)核蛋白异构调节剂(CpAMs),如GLS4和RO7049389,可以导致非衣壳核蛋白多聚体的组装错误;(2)衣壳组装调节剂,如AT-130、NVR-3778、JNJ6379等,可以形成形态正常的衣壳,但病毒核酸缺失。
5. 靶向HBsAg的释放(HBsAg release)
核酸聚合物(nucleic acid polymers, NAPs)具有抗病毒作用并可抑制受感染肝细胞释放HBsAg,不过其具体的抗病毒作用机制尚未被阐明。
免疫调节疗法
通过适当地激活抗病毒免疫,可以实现HBV的功能性治愈。若患者HBV得到控制,其特征便是抗HBV特异性体液和细胞免疫的协调激活。激活宿主免疫机制使HBV感染自发性清除,也是一种慢乙肝治疗手段。
1. 靶向先天性免疫力的策略
靶向先天性免疫力主要是利用细胞因子(TNF、IFNα、IFNγ、IL-1β)的直接抗病毒效应,从而诱导适应性免疫。IFNα疗法就是基于这个原理,该疗法对少数CHB患者(约5%-10%)有效,在这些患者中可实现真正的功能性治愈。此外,IFNα还提高NK细胞的免疫应答能力,接受IFNα治疗后达到HBsAg阴性的患者恢复了HBV特异性T细胞反应。
抗病毒细胞因子不仅可以减少HBV的复制,还可以消除cccDNA——这是治愈CHB最直接有效的策略。
2. 靶向适应性免疫力的策略
HBV特异性免疫在CHB患者中存在缺陷,理论上可以通过免疫检测点*制剂抑**(如抗PD1或抗CTLA-4疗法)或治疗性疫苗来恢复。阻断PD1-PDL1相互作用的抗体可部分恢复缺陷的HBV特异性T/B细胞应答。抗PD1治疗对CHB患者的抗病毒活性有限,但仍需根据其病毒学和临床特征选择合适的患者,抗PD1抗体的最佳剂量也有待确定。
结语
综上所述,新的乙肝治疗策略旨在实现功能性治愈,持续的治疗后达到HBsAg的消失。
参考文献:
[1] Tarik Asselah, Dimitri Loureiro, Nathalie Boyer, Abdellah Mansouri. Targets and future direct-acting antiviral approaches to achieve hepatitis B virus cure. Lancet Gastroenterol Hepatol (2019); 4: 883–892.
[2] Gregory C. Fanning, Fabien Zoulim, Jinlin Hou, Antonio Bertoletti. Nature Reviews Drug Discovery (2019). DOI:
https://doi.org/10.1038/s41573-019-0037-0