
慢性肾脏病(chronic kidney disease,CKD)已成为全球范围内威胁健康的重要公共卫生问题。我国18岁以上成人CKD患病率接近10.8%,患病人数约有1.19亿,而人群知晓率却只有12.5%[1]。65岁以上老年人已成为终末期肾病患者中增长最快、人数最多的人群[2-3]。且随着我国人口老龄化程度加剧,高血压、糖尿病及超重/肥胖等一系列慢性病高发导致CKD发病率呈逐年上升趋势。因此,早发现和早干预CKD潜在危险因素对预防及延缓老年人CKD进展及减少其并发症发生至关重要。
血尿酸(SUA)是嘌呤核苷酸代谢的产物,约2/3的SUA经肾脏排泄[4]。SUA水平升高导致的高尿酸血症(HUA)已被证实是CKD发生发展的独立危险因素[5-7]。有研究显示,SUA水平每升高1 mg/dL,CKD发病风险增加19%[8]。也有证据表明,降尿酸治疗在延缓CKD进展中已获得一定的临床益处[9]。然而,仍有研究显示SUA水平升高与CKD风险关联不明显[10-11]。
以往研究都是基于成年人资料分析SUA水平与CKD风险关联,目前国内关于老年人SUA水平与CKD发生发展相关的队列研究较少。因此,本研究基于中国老年健康影响因素跟踪调查(CLHLS)子队列——老年健康生物标志物队列研究(HABCS),分析中国长寿地区老年人基线不同SUA水平及其变化与CKD发病风险及估算的肾小球滤过率(estimated glomerular filtration rate,eGFR)变化情况的关联,以期为我国老年人CKD防控管理提供科学依据。
1 对象与方法
1.1 研究对象 2021年12月—2022年5月,选取HABCS中接受健康体检并采集生物医学指标的老年人为研究对象。此队列分别在2009、2012、2014年对8个健康长寿地区(包括山东省烟台市莱州市、河南省商丘市夏邑县、湖北省荆门市钟祥市、湖南省怀化市麻阳县、广东省佛山市三水区、广西壮族自治区桂林市永福县、海南省澄迈县和江苏省南通市如东县)的≥65岁老年人进行健康体检,采集及提取血常规、尿常规及血浆生化等生物医学指标。由于2009年典型调查中并未采集老年人尿微量白蛋白(Ualb)及尿肌酐(Ucr),未能计算尿微量白蛋白肌酐比值(ACR),因此本研究将基线调查定为2012年的典型调查。纳入标准:(1)基线SUA值完整;(2)基线血肌酐(Scr)值完整;(3)基线Ualb及Ucr值完整。排除标准:(1)基线eGFR<60 mL·min-1·(1.73 m2)-1;(2)基线ACR≥30 mg/g;(3)有慢性肾炎病史;(4)失访。最终981名老年人纳入队列研究。本研究已获得天津医科大学总医院伦理委员会伦理审批(审批号:IRB2022-WZ-118)。
1.2 数据收集 (1)一般资料:通过HABCS数据库收集老年人的人口学特征(年龄、性别)、健康状况和患病状况(包括高血压、糖尿病、肾脏疾病及HUA病史)。(2)体格检查数据:包括BMI、腰围、小腿围、收缩压(SBP)及舒张压(DBP)。(3)生物医学指标:收集包括空腹血糖(FBG)、糖化血清蛋白(GSP)、总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、超敏C反应蛋白(hs-CRP)、超氧化物歧化酶(SOD)、维生素D3(VD3)、白细胞计数(WBC)、红细胞计数(RBC)、血小板计数(PLT)、血尿素氮(BUN)、Scr、UAlb、Ucr、ACR、SUA、尿蛋白。
1.3 定义和诊断 SUA水平分类标准:(1)根据基线SUA水平进行四分位数分组,Q1为<223 μmol/L,Q2为223~270 μmol/L,Q3为271~325 μmol/L,Q4为≥326 μmol/L。(2)将基线SUA水平男性>420 μmol/L或女性>360 μmol/L,或有HUA病史定义为HUA[12]。参照2017年《慢性肾脏病筛查、诊断及防治指南》和美国肾脏病基金会“肾脏病预后质量倡议”,CKD的诊断标准为eGFR<60 mL·min-1·(1.73 m2)-1或ACR≥30 mg/g或基于医学记录新发诊断为CKD者[13-14]。采用适于中国人群的CKD-EPI(chronic kidney disease epidemiology collaboration)公式计算eGFR[15]。本研究终点事件为CKD的发生。
1.4 统计学方法 应用Stata 13.0软件进行统计分析。非正态分布的计量资料以中位数(下四分位数,上四分位数)〔M(P25,P75)〕表示,多组间比较采用Kruskal-Wallis H检验;分类变量以频数和构成比表示,组间比较采用χ2检验。分别以SUA四分位数分组、SUA水平(连续变量)及是否患HUA为自变量,以CKD发病为因变量,采用Cox比例风险回归模型分析老年人基线SUA水平与CKD发病风险关联;以SUA四分位数组中值进行趋势性检验。采用Spearman秩相关分别分析老年人基线SUA水平与基线eGFR的相关性及老年人SUA水平变化(ΔSUA=基线SUA-随访期SUA)与eGFR变化(ΔeGFR=基线eGFR-随访期eGFR)的相关性;采用广义线性模型分别分析老年人基线SUA与基线eGFR的关联及ΔSUA与ΔeGFR的关联。所有检验均为双侧检验,以P<0.05为差异有统计学意义。
2 结果
2.1 研究对象基线特征 共纳入研究对象981名,其中男548名(55.9%),中位年龄79(70,88)岁。HUA患病率为6.8%(67/981);其中男性HUA患病率为7.8%(43/548),女性HUA患病率为5.5%(24/433),两者比较,差异无统计学意义(χ2=2.018,P=0.155)。累积随访2 029人年,中位随访2.05年(范围1.0~4.0年),CKD新发病例共179例,随访期间CKD累积发病率为18.2%〔95%CI(15.9%,20.8%)〕,发病密度为88.22/1 000人年〔95%CI(76.24/1 000人年,101.41/1 000人年)〕。基线时不同SUA水平老年人的性别、BMI、腰围、小腿围、SBP、GSP、TG、hs-CRP、VD3、WBC、PLT、Scr、Ucr、ΔSUA、ΔeGFR及新发CKD患者占比比较,差异有统计学意义(P<0.05),见表1。
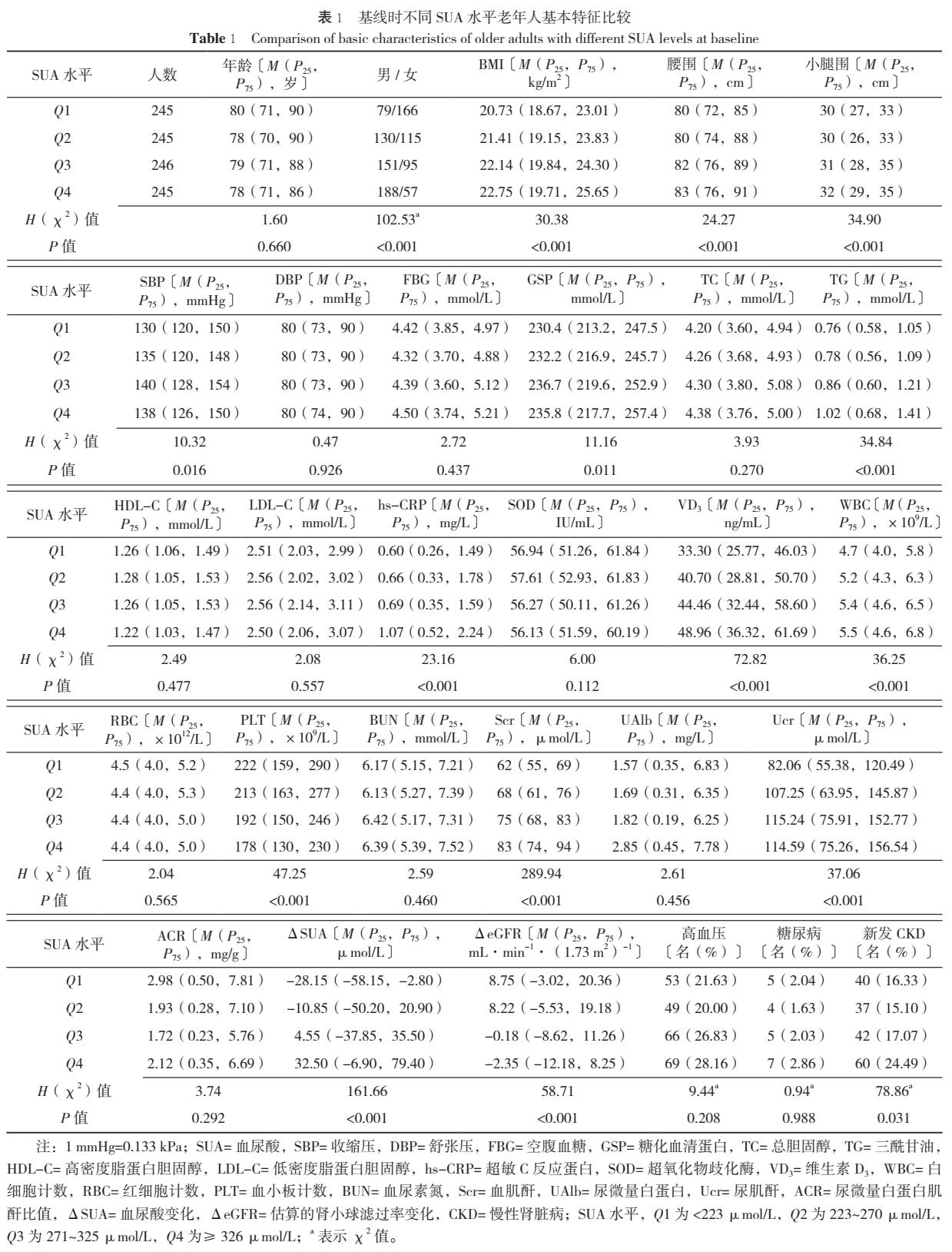
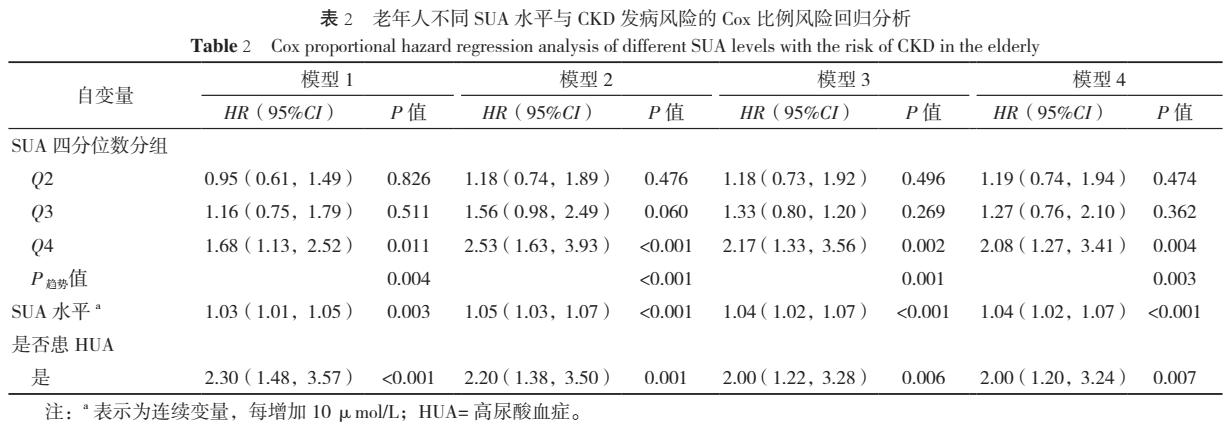
2.2 老年人不同SUA水平与CKD发病风险的Cox比例风险回归模型分析 模型1以是否患CKD为因变量(赋值:否=0,是=1),分别以SUA四分位数分组(赋值:Q1=1,Q2=2,Q3=3,Q4=4)、SUA水平(赋值:原值纳入)及是否患HUA(赋值:否=0,是=1)为自变量,进行Cox比例风险回归模型分析;模型2在各模型1基础上调整年龄(赋值:连续变量)、性别(赋值:男=1,女=2)、BMI(赋值:原值纳入)、腰围(赋值:原值纳入)、小腿围(赋值:原值纳入);模型3在各模型2基础上调整SBP(赋值:原值纳入)、DBP(赋值:原值纳入)、FBG(赋值:原值纳入)、GSP(赋值:原值纳入)、TC(赋值:原值纳入)、TG(赋值:原值纳入)、HDL-C(赋值:原值纳入)、LDL-C(赋值:原值纳入)、hs-CRP(赋值:原值纳入)、SOD(赋值:原值纳入)、VD3(赋值:原值纳入)、WBC(赋值:原值纳入)、RBC(赋值:原值纳入)、PLT(赋值:原值纳入)及BUN(赋值:原值纳入);模型4在各模型3基础上调整高血压病史(赋值:无=0,有=1)及糖尿病病史(赋值:无=0,有=1)。以SUA四分位数分组为自变量的Cox比例风险回归模型分析结果显示,与基线SUA最低四分位数组(Q1)相比,最高分位数组(Q4)老年人CKD发病风险的HR值为2.08〔95%CI(1.27,3.41),P=0.004〕;且呈趋势性增加(P趋势=0.003)。以SUA水平为自变量的Cox比例风险回归分析模型结果显示,基线SUA水平每升高10 μmol/L,老年人CKD发病风险增加4%,P<0.001。以是否患HUA为自变量的Cox比例风险回归模型分析结果显示,与基线未患HUA老年人相比,患HUA老年人CKD发病风险增加,HR值为2.00〔95%CI(1.20,3.24),P=0.007〕,见表2。
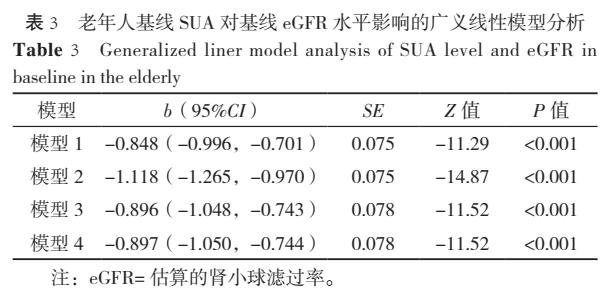
2.3 老年人基线SUA与基线eGFR关联分析 老年人基线SUA中位数为270.60(223.10,325.90) μmol/L,基线eGFR中位数为84.07(73.08,98.38)mL·min-1·(1.73 m2)-1,Spearman秩相关分析结果显示,二者呈负相关(rs=-0.363,P<0.001)。以老年人基线eGFR(赋值:原值纳入)为因变量,基线SUA为自变量(赋值:原值纳入),多因素(模型1~模型4的变量调整及其赋值同2.2)广义线性模型分析结果显示,老年人基线SUA水平每升高10 μmol/L,基线eGFR下降0.897 mL·min-1·(1.73 m2)-1(P<0.001),见表3。
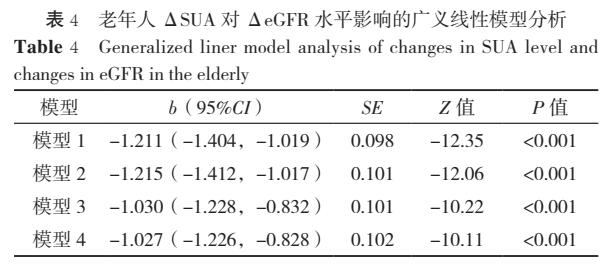
2.4 老年人SUA水平变化与eGFR变化关联分析 本研究随访期间老年人ΔSUA中位数为-3.55(-40.60,31.90) μmol/L,ΔeGFR中位数为3.49(-8.13,15.89) mL·min-1·(1.73 m2)-1,Spearman秩相关分析结果显示,二者呈负相关(rs=-0.355,P<0.001)。以老年人ΔeGFR为因变量(赋值:原值纳入),ΔSUA为自变量(赋值:原值纳入),经多因素(模型1~模型4的变量调整及其赋值同2.2)的广义线性模型分析结果显示,随访期间老年人SUA水平每升高10 μmol/L,伴随老年人eGFR下降1.027 mL·min-1·(1.73 m2)-1(P<0.001),见表4。
3 讨论
本研究基于CLHLS子队列——HABCS,探讨中国长寿地区老年人基线SUA水平及其变化与CKD发病风险及eGFR变化的关联,结果发现老年人基线SUA水平升高及患HUA时,CKD发病风险增加,且eGFR随SUA的升高而降低。
本研究结果显示,老年人基线SUA水平最高四分位数组(≥326 μmol/L)CKD发病风险是最低四分位数组的2.08倍〔95%CI(1.27,3.41)〕,且基线SUA水平每升高10 μmol/L,老年人CKD发病风险增加4%,研究结果与以往研究发现相一致[16-18]。LAI等[16]通过随访追踪425名70岁以上老年人CKD及肾功能变化情况发现,基线老年人SUA水平最高四分位数组(≥6.5 mg/dL)发生CKD的风险是最低四分位数组的6.79倍〔95%CI(3.45,13.75)〕。WU等[17]4年随访4 546名志愿者,结果发现SUA水平最高四分位数组(>5.1 mg/dL)发生CKD的风险是最低四分位数组的2.73倍〔95%CI(1.65,4.50)〕。STORHAUG等[18]基于Tromsø队列评估总人群血尿酸与GFR的变化关联,随访13年发现,基线SUA水平每升高1 mg/dL,肾功能不全风险增加16%〔95%CI(4%,29%)〕。
本研究结果发现,老年人基线SUA水平与老年人基线eGFR水平呈负相关,且随访4年期间老年人SUA水平每升高10 μmol/L,eGFR下降1.027 mL·min-1·(1.73 m2)-1〔95%CI(-1.23 mL·min-1·(1.73 m2)-1,-0.83 mL·min-1·(1.73 m2)-1〕。LAI等[16]发现随访3年期间老年人基线SUA水平每升高1 mg/dL,eGFR降低1.25 mL·min-1·(1.73 m2)-1〔95%CI(-1.83 mL·min-1·(1.73 m2)-1,-0.67mL·min-1·(1.73 m2)-1〕。TSAI等[19]研究结果显示,较高的SUA水平与eGFR明显快速下降和较高的肾衰竭风险有关,基线SUA水平每升高1 mg/dL,进展到肾功能衰竭的风险增加7%。YE等[20]也发现SUA水平升高与eGFR降低及新发CKD风险增加独立相关。均与本研究结果相一致。
SUA水平升高与CKD风险增加有关的潜在病理学机制包括:(1)肾脏是SUA最主要的排泄器官,尿酸晶体可通过在肾脏沉积引起直接的肾*毒脏**性,从而导致肾功能降低[21];(2)SUA被内皮细胞吸收,通过抑制一氧化氮(NO)的产生和加速其降解来降低NO的水平,胞质和血浆黄嘌呤氧化酶又通过产生超氧化物来降低NO水平,因此,SUA水平升高会诱导肾内氧化应激和线粒体功能障碍,导致内皮细胞、平滑肌细胞、肾小管细胞受损,从而激活肾素-血管紧张素系统[22-23];(3)HUA可诱导肾小球前血管的小动脉病变,从而损害传入小动脉的自身调节反应。同时,血小板粘附性增加,沉积后导致血管壁增厚,血流变紊乱,可引起管腔闭塞缺血。肾灌注不足是一种有效的血管活性和炎症递质刺激,可导致小管间质炎症和纤维化[21,24],最终肾功能下降。
本研究仍有一些局限性:首先,本研究纳入老年人群样本量较少,可能会减弱SUA水平与CKD风险之间的因果关系;其次,本研究仅采用一次Scr和蛋白尿指标的测量值进行分析,对老年人中CKD真实发病状况评估存在一定偏倚;最后,本研究中位随访时间为2.05年,相对较短,未能观测到研究人群终末期肾病等事件,研究结果的外推性受限。因此,未来研究将拓宽观测的终点事件,延长随访时间继续关注老年人群中CKD的发病状况。
综上所述,本研究发现中国长寿地区老年人基线SUA水平升高及患HUA时会增加CKD发病风险,且老年人eGFR会随SUA水平的升高而降低。因此,定期监测老年人SUA水平,及早采取干预措施控制SUA水平以减缓未来eGFR下降的趋势,对控制老年人CKD的发生发展有重要意义。
本文无利益冲突。
参考文献略
本文来源:张鹏,高鹰,杨洪喜,等. 中国长寿地区老年人血尿酸水平与慢性肾脏病发病风险研究[J].中国全科医学,2023,26(31):3884-3889,3907. DOI:10.12114/j.issn.1007-9572.2023.0001.