在临床试验发展的岁月长河中,曾发生过无数大大小小的事件,你可知在上个世纪中叶,曾经发生过这三个震惊世界以至于影响了临床试验立法进程的事件,正是这些事件用生命和血泪换来了切实有效地推动临床试验迈向正轨,让我们先从20世纪最严重的群体中毒之一磺胺酏(yǐ)剂事件说起吧。
磺胺酏剂事件
致命的液体:1937年,美国田纳西州布里斯托尔市的S.E. Massengill 公司开始销售 Elixir Sulfanilamide 磺胺酏剂,这是一种在当时流行的抗菌药物的液体口服制剂。但在服用该制剂后,出现了超过100人例的死亡病例,美国食品药品监督管理局 (FDA) 的调查人员确定该药物的溶剂二甘醇是导致人们死亡的杀手。

酏(yǐ)剂是一种由药物、甜料和芳香性物质配制而成的水醇溶液,乙醇含量一般在25%以下,供口服。
磺胺,是一种抗菌药物,可以安全地用于治疗链球菌感染。
1935年,药学家们经过研究发现磺胺具有抗菌作用,于是各类磺胺片剂或胶囊纷纷问世。1937年,美国一家制药S.E. Massengill公司的主任药师发现,使用二甘醇(DEG)和水把磺胺溶解,再加入覆盆子提取物和糖精等调味成分,可以制备出含有覆盆子香甜口感的新液体制剂Elixir Sulfanilamide(磺胺酏剂)。这种新剂型相比当时磺胺主要的剂型片剂和胶囊来说,带有香甜口感的液体制剂无疑要好得多,尤其方便儿童的口服。据称这种药物可以治疗流感和链球菌感染等各种疾病,号称"万灵药"。
可在当时的美国,新制剂投入市场之前没有明确的规定必须进行毒性研究(动物试验和相关安全性试验)。在磺胺酏剂上市之前,没有人意识到二甘醇(DEG)可能是致命的,在未做动物试验的前提下,不知不觉该公司已在全美各地分销磺胺酏剂,更糟的是购买这种药不需要处方,消费者在各地的药店都能买到。
该药上市后一个月,美国医学会就关注到了由磺胺酏剂引起的致死性病例,尽管立即尝试召回这种药物,但仍有105例服用该药物的患者死亡,其中有71名成年人和34名儿童在服用了Elixir Sulfanilamide之后因为肾功能衰竭而死亡。
这起事件对社会造成了恶劣影响,它夺走的不止是34名儿童的生命,还有家庭的希望。后来,经动物试验证明磺胺本身并无毒性,造成中毒死亡的正是二甘醇,它会损伤肾脏,导致肾衰竭。
从"磺胺肔剂事件"中,FDA没有严格的监管措施为世人所诟病。直接在市场上公开销售没有进行过动物试验和未知安全性的新药,无异于在把一个*弹炸**埋在闹市区,而周围的人们却压根不知道*弹炸**的存在,一旦引爆,*伤杀**力极大。
于是,为了弥补过错和对国民的安全负责,在1938年,美国国会顺利通过《食品、药品和化妆品法案》,由FDA强制实施,并在其中做出明确的要求:药品上市前必须进行动物安全性测试,且提交给FDA审批合格后才允许上市销售。

纽伦堡审判
二战时期出现了很多难以想象的违反伦理的人体实验,比如有一对双胞胎姐妹斯特凡妮和安妮塔,暴徒曾向往她们的眼睛里注射化学药剂,以观察她们的眼睛是否会变成和雅利安人一样的蓝色,这是暴徒所进行的所谓改良人种的实验,在现世看来,简直是荒唐至极。
数不清的无辜的人在战争的人体实验中死去,二战结束后在1945-1947年间在德国的纽伦堡法庭对进行医学人体实验的暴徒进行了审判。伦堡法庭还制定了人体实验的十条基本原则,即《纽伦堡法典》,作为国际上进行人体实验的行为规范,并于1948年公布于世。

该颁布法典对于人体进行临床试验的启示有:
1. 受试者的参加必须处于自愿。
2. 在参加任何临床试验前,必须完成充分的知情同意
3. 必须有实验研究提供科学的依据
4. 实验须力求避免对受试者造成肉体或精神上的伤害
5. 在试验进行期间受试者有权利退出
反应停事件
反应停事件的主角是药物沙利度胺,目前它已经是一种公认的人类致畸剂,它的右旋异构体具有镇静作用,而左旋异构体则是引发致畸性的罪魁祸首,可导致严重的危及生命的出生缺陷。在1957年至1962年期间,正是沙利度胺的存在,当时它被认为是一种可以缓解孕妇妊娠反应的药物,在全球范围内导致了超过1万名儿童出现严重的出生缺陷。
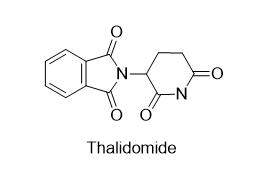
沙利度胺
1957年,用于缓解孕吐的药物沙利度胺在欧洲上市,它被称之为"反应停"。起初,由于"反应停"号称无任何副反应作用且能有效使用缓解孕吐,沙利度胺迅速风靡欧洲、非洲、大洋洲和拉丁美洲各国。可后来,全世界球陆续发现很多畸形儿都有一个共同点,就是四肢发育不全,手脚特别短小,形似海豹肢,这引起了很多人科学家和医生的关注。

形似海豹的畸形儿
经过调查发现,畸形儿的母亲在怀孕期间都无独有偶服用过"反应停"。从1961年11月起,"反应停"在世界各国陆续被强制撤回,这起事件被称为"20世纪最大的药物灾难"。在反应停事件中,受害人数达到上万人,这些孩子原本带着家庭的期盼可以四肢健全地落地,却因为沙利度胺从一生下来就成为畸形儿,家庭的期盼转眼就化成了悲剧和不幸。
"反应停"沙利度胺在上市前,并未进行严格的临床试验,而是以不严谨的实验室报告、动物试验等研究资料就通过了德国、英国等国家的上市批准。不过,由于在当时(1960年),FDA的一名新的医学官员凯尔西医生并不相信这种药物是安全的,她要求药厂提供更多的动物试验数据和完整的临床试验数据,以证明该药真正安全,所以沙利度胺未能通过FDA对其在美国上市的批准。凯尔西的犹豫得到了回报,这也使得,美国社会因此躲过了一场灾难。

FDA官员凯尔西医生
由于反应停事件对国际社会造成的严重影响,在1962年,美国国会通过了《科夫沃—哈里斯修正案》,明确要求药物上市前必须提供临床试验证明的安全性和有效性的信息,并且保留药物的不良反应记录。
沙利度胺的故事还没有结束。1964年,耶路撒冷哈达萨大学医院的一名麻风病患者服用了沙利度胺,而其他镇静剂和止痛药却帮不上忙。他的医生注意到这种药对病人的麻风病症状有影响,三天之内麻风病就消失了,皮损也愈合了,但当病人停止服用沙利度胺时,麻风又复发了。这种药似乎能抑制这种疾病,尽管它不能治愈。
因此,世界卫生组织(WHO)在1967年进行了一项关于沙利度胺治疗麻风病的临床试验。在取得更积极的结果后,沙利度胺在许多国家被用作麻风病的治疗。但由于沙利度胺过去的历史,其重新使用仍有争议。 科学知识的产生和新的疾病治疗方法使人类受益匪浅。但是,临床研究不应危及受试者的生命。临床研究必须在伦理上进行,以保护受试者的权利、安全和健康。过去曾对社会中的弱势群体,包括囚犯、奴隶和其他主体进行过许多不道德的研究,但没有得到他们的同意。为了应对这些广为人知的悲剧,全世界制定了各种监管指南,以符合伦理原则的方式组织临床试验的开展,确保受试者的利益至上。
如今新版《药物临床试验质量管理规范》发布之际,我们一同回首一个世纪以前的历史事件,是前车之鉴,也是后世之师。临床试验行业犹如清晨缓缓升起的朝阳,生机蓬勃,欣欣向荣,与此同时对生命的敬畏却不能有丝毫的缺位。
注:本文内容参考《药品安全监管——在重大安全事件中踯躅前进》、《揭秘二战时期德国的*行暴**:纳粹人体实验》,在此表示感谢。