随着肿瘤精准医疗的不断发展,基因检测的技术也不断升级。通过更加全面、精准的基因检测,可以使受检者有更高的临床获益,帮助医生分析耐药机制和制定耐药应对策略,更好的评估免疫治疗疗效并制定更加精准的个体化治疗方案。
NCCN指南推荐DNA+RNA联合检测,提高临床获益率

多项指南推荐,将DNA检测与RNA检测相结合,可以全面覆盖基因融合/重排,更大程度的提高临床获益率。并且已有多项研究证明,将DNA检测与RNA检测相结合,可以实现核心治疗靶点及罕见、有效的融合变异的同时测定,弥补常规检测方法可能的漏检、融合基因不明确等不足,有效提高融合基因检出率,更好的帮助医生进行临床诊断及治疗。
01.DNA+RNA同时测序,全面检测基因融合

在本项研究中,研究者们开发了一种平行扩增数字优化测序(PANO-Seq)的检测方法,能够同时检测DNA和RNA序列并对其进行整合分析。利用PANO-Seq,他们从66例新鲜的肺癌组织切片样本的预队列中检测到了36例常见突变(27例EGFR,4例KRAS,4例PIK3CA,1例BRAF和1例CDKN2),此外,还检测到3例融合变异(2例EML4-ALK融合和1例KIF5B-RET融合)。在后续的大样本量研究中,研究人员收集了1095例患者的FFPE样本,涵盖了肺癌已知的各种亚型,包括815例(74.4%)腺癌,183例(16.7%)鳞状细胞癌和97例(8.9%)其他类型病例。结果表明,在所有患者中有69例为融合阳性(主要为ALK、ROS1、RET三个基因的融合),另外还检测到6例MET 14外显子跳跃突变,1例HLA-DRB1-MET融合,以及BBS9-BRAF、AGK-BRAF、CD74-NRG1、MKL2-NRG1四例融合事件。由于这种检测方法在检测常见核心治疗靶标的同时,也能够准确、有效的检出较罕见的融合变异,有望为携带罕见变异的患者带来更多的临床获益。
02.DNA+RNA检测分析,解读肿瘤耐药机制

基于西妥昔单抗的化疗已经为结直肠癌(CRC)患者带来巨大的临床获益,但其治疗效果也同样受到耐药性的困扰。在本项研究中,研究者对前瞻性收集的25例接受西妥昔单抗治疗的CRC患者的肿瘤样本进行了DNA+RNA检测分析。在25例患者中,13例表现出对西妥昔单抗的内在耐药,12例表现为内在敏感,并且有11名在接受西妥昔单抗治疗后出现了获得性耐药。结果表明,在内在耐药的患者中发现了NCOA4-RET和LMNA-NTRK1融合以及NRG1和GNAS扩增,在内在敏感患者中,除了BRAF V600E、AKT1 E17K、PIK3CA E542K和FGFR1或ERBB2扩增外,还发现了KRAS K117N和A146T突变。
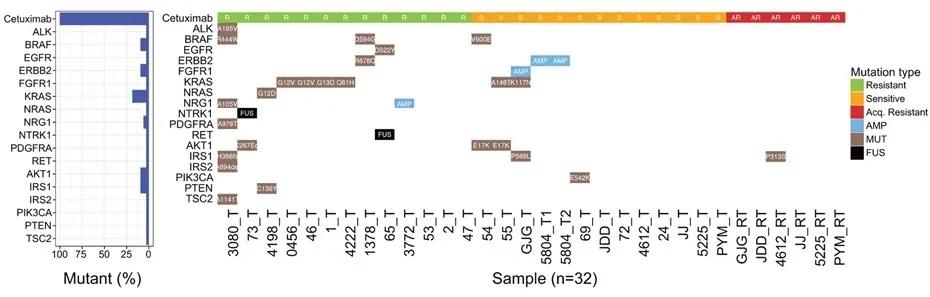
通过基线和获得性耐药患者之间的比较显示,体细胞变异体的变异等位基因频率发生了显著的变化,并且获得性耐药患者的上皮-间充质转化(EMT)也增加,免疫浸润减少。此外,对获得性耐药的患者来源细胞系的鉴定表明,抑制PI3K/mTOR通路可以改善西妥昔单抗的耐药性。本项研究发现了耐药患者新的基因组的改变,阐明了CRC患者抗EGFR治疗的敏感性和耐药性机制,并且也对其耐药性的应对提出了新的替代治疗方向。
03.WES+RNA联合,寻找临床治疗策略

当前,奥希替尼已被国内外多个权威临床指南作为EGFR突变晚期NSCLC一线治疗的首选推荐,但临床治疗中应用奥希替尼仍不可避免会出现耐药现象。发表在Cell Rep Med.的一项研究对EGFR突变肺癌中奥希替尼获得性耐药机制的克隆进化和异质性进行了探索。在本项研究中,研究团队利用WES+RNA测序对前瞻性收集的奥希替尼耐药前后的肿瘤组织进行检测,检测结果表明,在接受一线奥希替尼治疗的患者中,MET扩增是最常见的耐药机制,发生在66%的患者中。然而,获得的MET扩增是亚克隆且高度异质的,这可以解释在以前报道的一线奥希替尼治疗的患者中MET扩增的比例较低的原因。此外,通过对多区域、多时间的克隆进化分析发现,大多数患者具有两种或两种以上的耐药机制,这表明在奥希替尼治疗后发生疾病进展的患者可能需要靶向双重耐药治疗。
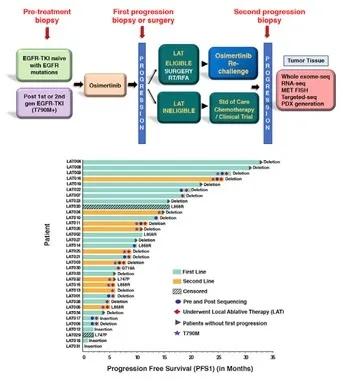
研究者称:“由于大多数接受奥希替尼治疗的患者具有两种或更多种耐药机制,我们的数据表明需要联合疗法来克服获得性耐药。MET*制剂抑**将是此类联合治疗的重要组成部分,特别是在发生早期进展的一线奥希替尼治疗患者中。”
04.补充RNA检测提高突变基因检出率,实现更高临床获益

越来越多的证据表明MET*制剂抑**在MET 14外显子跳跃突变的患者中取得了良好的抗肿瘤效果,提示MET 14外显子跳跃突变或可作为治疗NSCLC患者的新的重要靶点,因此可靠的突变检测方法对于指导临床治疗具有至关重要的意义。Kurtis等分别采用DNA-seq和RNA-seq方法对肿瘤组织进行检测,基于DNA-seq在856个NSCLC样品中的11个(1.3%)中检测到MET外显子14跳跃突变,而基于RNA-seq在404个样品中的17个(4.2%)中检测到MET外显子14跳跃突变,与基于DNA的分析相比,统计学上显著增加。
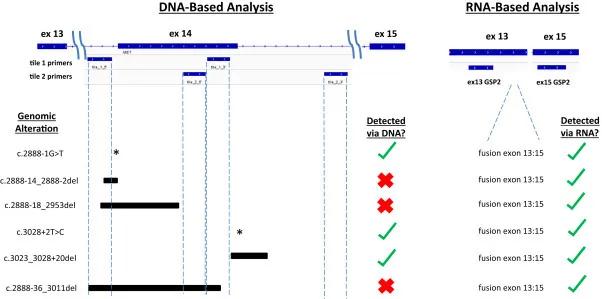
此外,Magdalena等也比较了基于DNA和RNA检测方法对MET 14外显子跳跃突变的检测结果,发现通过DNA检测仅检测出2.5%(16/644)MET 14外显子跳跃突变,但在驱动基因阴性的患者中通过RNA检测又检出了9例(共检出3.9%),因此对于此类跳跃突变基因的检测,尤其是检测FFPE样本时,RNA+DNA测序显然是更优选择。相信这一联合检测方式的发展,将进一步提高肿瘤基因检测的精准度,助力精准医疗的发展,为肿瘤患者的诊断和治疗带来更多福音。
参考文献:
1.Song Z. B., Xu C. W., He Y. W. et al. Simultaneous Detection of Gene Fusions and Base Mutations in Cancer Tissue Biopsies by Sequencing Dual Nucleic Acid Templates in Unified Reaction. Clin Chem. 2020;66(1):178-187. doi:10.1373/clinchem.2019.308833
2.Bray S. M., Lee J., Kim S. T. et al. Genomic characterization of intrinsic and acquired resistance to cetuximab in colorectal cancer patients. Sci Rep. 2019;9(1):15365. Published 2019 Oct 25. doi:10.1038/s41598-019-51981-5
3.Roper N., Brown A. L., Wei J. S., et al. Clonal Evolution and Heterogeneity of Osimertinib Acquired Resistance Mechanisms in EGFR Mutant Lung Cancer. Cell Rep Med. 2020;1(1):100007. doi:10.1016/j.xcrm.2020.100007
4.Davies K. D., Lomboy A., Lawrence C. A., et al. DNA-Based versus RNA-Based Detection of MET Exon 14 Skipping Events in Lung Cancer. J Thorac Oncol. 2019;14(4):737-741. doi:10.1016/j.jtho.2018.12.020
5. Jurkiewicz M., Saqi A., et al. Efficacy of DNA versus RNA NGS-based Methods in MET Exon 14 skipping mutation detection. J. Clin. Oncol. 2020 38:15_suppl, 9036-9036
