转自“肿瘤瞭望-消化时讯”

编者按:随着精准治疗的发展,针对BRAF、HER2、RAS、NTRK以及VEGF等靶点的靶向治疗研究陆续取得进展,结直肠癌治疗逐渐步入多样化的精准治疗阶段。5月29~31日以在线形式召开的2020年美国临床肿瘤学会(ASCO)年会上,公布了多项结直肠癌靶向治疗研究结果。我们选择几项重要的研究,特邀上海交通大学医学院附属瑞金医院刘静教授进行了点评。
1曲妥珠单抗-deruxtecan(T-DXd;DS-8201)治疗HER2表达的转移性结直肠癌(mCRC)的Ⅱ期、多中心、开放标签研究:DESTINY-CRC01(Abstract 4000)
1
背景:T-DXd是一种由抗HER2抗体、可裂解的四肽连接剂和拓扑异构酶I*制剂抑**组成的抗体偶联药物。早期研究表明该药物在晚期表达HER2的肿瘤中有较强的活性。DESTINY-CRC01(DS8201-A-J203;NCT03384940)是一项关于T-DXd治疗HER2表达的转移性结直肠癌(mCRC)的Ⅱ期开放性多中心研究。
方法:HER2表达的RAS野生型转移性结直肠癌患者,既往接受过≥2次治疗,依据HER2表达程度分为3个队列(A:HER2 IHC 3+或IHC 2+/ISH +;B:IHC 2 +/ISH-;C:IHC 1+),每组每3周接受一次T-DXd 6.4 mg/kg治疗,主要终点为通过队列A评估客观缓解率(ORR);次要终点包括B组和C组的疾病控制率(DCR;CR + PR + SD)、反应持续时间(DOR)、无进展生存期(PFS)、总生存期(OS)和B、C各队列的客观缓解率(ORR)。
结果:时间截止点为2019年8月9日,有78例患者(A队列53例;B队列7例;C队列18例)接受T-DXd治疗。中位年龄为58.5岁(范围为27~79岁),男性患者占52.6%,左半结肠癌或直肠癌占89.7%;既往接受不同治疗方案次数的中位数为4(范围2~11);所有患者既往均接受伊立替康治疗。中位治疗持续时间为3.5个月(95%CI:2.1~4.3个月;队列A为4.8个月,95%CI:3.9~5.8个月);38.5%的患者仍持续T-DXd治疗。队列A中的ORR为45.3%(24/53;95%CI:31.6%~59.6%),包括1例疾病完全缓解(CR)和23例疾病部分缓解(PR)。未达到中位DOR(95%CI,4.2个月-NE)。既往接受过抗HER2治疗的患者ORR为43.8%(7/16;95%CI:19.8%~70.1%)。DCR为83.0%(44/53;95%CI:70.2%~91.9%);中位PFS为6.9个月(95%CI:4.1个月-NE);未达到中位OS。在队列B或C中未见到治疗有效。61.5%患者发生3级以上的治疗相关不良事件(TEAE)(48/78);最常见的(≥10%)是中性粒细胞减少(21.8%)和贫血(14.1%)。有7例患者(9.0%)因不良事件导致停药。5例患者(6.4%)因T-DXd罹患间质性肺疾病(ILD)(2级2例;3级1例;5级2例[1例因药物相关不良反应而死亡])
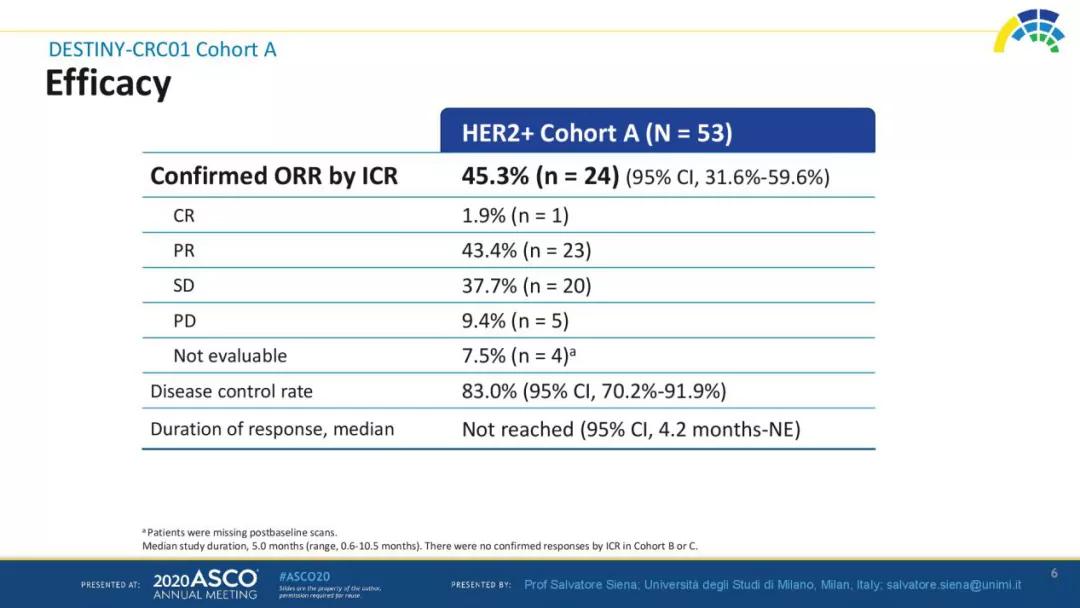
图1. HER2+队列A的有效性
结论:总体而言,T-DXd 6.4 mg/kg q3w的方案在HER2表达且对标准疗法耐受的mCRC患者中显示出较高的有效性,药物安全性与先前的结果一致。ILD是一个重要的危险因素,需要仔细识别和干预。临床试验信息:NCT03384940。
评论
该研究是又一项针对HER2表达mCRC的临床研究,与既往同类研究相比,该研究有以下几大亮点:第一,不仅入组了HER2过表达的队列A(HER2 IHC 3+或IHC 2+/ISH +),还纳入了HER2低度表达的队列B和C(IHC 2 +/ISH-;或IHC 1+)。结果提示,仅队列A取得了45.3%的反应率,而低表达的队列B和C未见疗效,证实了抗HER2治疗仅在HER2过表达mCRC患者中有效,低表达患者无法获益。而该研究45.3%的反应率,也在同类研究中位居前列,仅略逊于MOUNTAINEER研究(曲妥珠单抗+图卡替尼)的52.2%。第二,队列A入组了既往接受过抗HER2治疗的患者,且结果提示,这些患者的反应率与总体人群十分接近,提示T-DXd这一新型抗体偶联药物与其他抗HER2制剂可能不存在交叉耐药,具体既往抗HER2治疗情况尚待会议披露。此外,根据目前摘要披露的信息,对于HER2表达仅采用经典的IHC和ISH,并未提及是否同时应用NGS进行检测,其他生物标志物与疗效的关系有待后续分析。不良反应方面,T-DXd引起的ILD不容忽视,其他常见不良反应并未提及血小板减少,提示T-DXd与T-DM1的毒性谱似有不同,值得临床医生警示。
2随机、3臂、Ⅲ期研究BEACON CRC的更新最新生存期结果:Encorafenib联合西妥昔单抗±binimetinib对比研究者选择的伊立替康+西妥昔单抗(对照)或FOLFIRI+西妥昔单抗(对照)治疗BRAF V600E转移性结直肠癌(BEACON CRC).(Abstract 4001)
背景:BEACON CRC是一项Ⅲ期随机研究,评估了encorafenib(ENCO)+binimetinib(BINI)+西妥昔单抗(CETUX)的三联疗法和ENCO+CETUX的两联疗法与研究者选择伊立替康+西妥昔单抗或FOLFIRI + 西妥昔单抗在治疗BRAFV600E突变的、既往接受过1-2种方案治疗后进展的转移性结直肠癌(mCRC)的疗效差异。主要研究终点是对比三联疗法和对照组的总生存(OS)和疾病客观缓解率(ORR),在既往中期分析中显示三联和两联疗法可以明显提高OS和ORR,本次我们将汇报更新的疗效分析。
方法:更新所有分组患者中的后续6个月随访和疾病缓解率。研究仍在进行。
结果:接受三联疗法的患者为224例,两联疗法的为220例,对照组患者221例。中位OS在三联疗法组中为9.3个月(95%置信区间[CI]:8.2~10.8),对照组中为5.9个月(95%CI:5.1~7.1)(危险比[HR](95%CI):0.60(0.47~0.75))。双联疗法的中位OS为9.3个月(95%CI:8.0~11.3)(与对照组比较HR:0.61(0.48~0.77)。三联疗法的ORR为26.8%(95%CI:21.1%~33.1%),两联疗法为19.5%,对照组为1.8%。回顾性亚组分析显示相比于两联疗法,某些患者更能从三联疗法中获益,在所有亚组中,相比于对照组,无论是三联疗法还是两联疗法均可提高患者的OS,治疗不良相关反应的分析与既往研究一致,三联疗法、两联疗法和对照组的3级以上不良事件分别为65.8%、57.4%和64.2%。

图2. 三联疗法的最新OS数据

图3. 两联疗法的最新OS数据
结论:BEACON CRC研究的最新分析证实,与标准化疗相比,encorafenib+西妥昔单抗联合或不联合binimetinib均可改善BRAF V600E 转移性结直肠癌患者的总生存期和疾病客观缓解率。临床试验信息:NCT02928224。
评论
BEACON CRC研究是第一项在BRAF V600E突变晚期肠癌患者中开展的Ⅲ期随机对照研究,2019年ESMO年会首次公布了中位随访7.8个月的生存数据,显示了三药及两药联合靶向治疗相比标准治疗组的显著生存优势,研究结果同期发表在《新英格兰医学杂志》上。基于BEACON CRC研究的初步结果,美国FDA于2020年4月正式批准ENCO+ CETUX的两联疗法用于经一种或二种方案治疗失败的BRAF V600E突变mCRC,这也是FDA批准的首个针对BRAF V600E突变mCRC的靶向治疗药物。此次ASCO会议报告的更新生存数据,并没有太多惊喜,在继续随访6个月后,三药及两药组的中位OS均为9.3个月,显著优于标准治疗组的5.9个月。自2018年被FDA认定为“突破性疗法”以来,BEACON CRC研究相继斩获了JCO、NEJM两大权威杂志,并先后在ESMO及ASCO年会上做口头报告,最终一举拿下本领域的第一个适应症,可谓是真正的“人生赢家”。相信后续进行的生物标志物等探索分析,还会带来更多惊喜。
3FOLFOX+帕尼单抗对比5FU+帕尼单抗一线治疗RAS-BRAF野生型转移性老年结直肠癌患者:PANDA研究(Abstract 4002)
1
背景:关于老年结直肠癌患者的一线治疗疗效研究仍十分缺乏,许多分析采用65岁为临界值,且抗EGFRs的研究证据仍十分有限。FOLFOX-帕尼单抗(pan)疗法是RAS野生型(wt)未接受过治疗的转移性结直肠癌(mCRC)患者的一种选择。指南建议考虑将氟嘧啶单药治疗作为老年患者的选择之一,但尚无随机对照研究探讨联合EGFR抗体的疗效成果。
方法:这是一项前瞻开放的多中心Ⅱ期随机试验,年龄≥70岁的无法手术切除且先前未接受治疗的RAS-BRAF野生型mCRC患者被随机分配为两组,一组接受FOLFOX-pan(A组),另一组接受5FU / LV-pan(B组),两组各自接受长达12个周期化疗,然后用pan维持治疗至疾病进展(PD)。首要观察终点是PFS。分层标准为年龄(≤75 vs. >75岁),ECOG PS评分(0~1 vs. 2)和基于G8评分的老年评估(≤14 vs. >14)。在每个治疗组中,中位PFS的无效假设均设定为≤6个月,假设两种实验方案的预期中位PFS时间均≥9.5个月,则每组90例患者的样本量具有90%的效能,Ⅰ型错误率等于5%(单侧Brookmeyer-Crowley检验)以拒绝原假设。没有计划在两组之间进行正式比较。
结果:2016年7月至2019年4月共筛查394例患者,其中211例符合纳入条件,最终入组185例并随机分为A组(92例)和B组(93例)。患者主要基线特征(A/B组):男性66%/61%;中位年龄77/77岁;PS评分≥1 49%/55%;右结肠23%/21%;G8>14 31%/30%。中位随访时间为20.5个月,135例患者PD(A/B组:64/71)。A组中位PFS为9.6个月(95%CI:8.8~10.9),B组中位PFS为9.1个月(95%CI:7.7~9.9)。疾病缓解率(A/B组):65%/57%。3~4级毒性为(A/B组):中性粒细胞减少症9.8%/1.1%;腹泻16.3%/1.1%;口腔炎9.8%/4.4%;神经毒3.3%/0%;疲劳6.5%/4.4%;皮疹25%/24.2%,低镁血症3.3%/7.7%。

图4. FOLFOX-pan(A组)和5FU/LV-pan组的主要终点PFS
结论:在多中心协作下基于分子筛查的老年转移性结直肠癌的前瞻性随机研究是可行的。两个治疗组均达到主要观察终点。12个周期的5FU/LV加帕尼单抗治疗,随后维持帕尼单抗治疗直至疾病进展可作为RAS/BRAF野生型老年结直肠癌患者的合理治疗方案,需在Ⅲ期试验中进一步研究。临床试验信息:NCT02904031。
评论
老年患者作为一组特殊群体,其治疗应与年轻患者采用同样模式,还是应区别对待,一直缺乏有力证据。在NCCN指南中,针对不适合强烈治疗的mCRC患者,一直以来的推荐都是氟尿嘧啶单药±贝伐珠单抗(基于AVEX研究结果),而对于RAS/BRAF野生型肠癌,至今尚无研究评价氟尿嘧啶联合抗EGFR单抗的生存获益。千呼万唤始出来的PANDA研究,正是填补了这一领域的空白,不仅证实了对于70岁以上的老年患者,5FU/LV-pan疗效与FOLFOX-pan相当,从中位PFS时间来看,并不劣于其他大型Ⅲ期研究的PFS结果。此外,PANDA研究还尝试了在一线治疗12周期后,应用帕尼单抗维持治疗的模式,为今后开展Ⅲ期验证研究提供了重要的依据。值得提出的是,相比于AVEX研究,PANDA研究更具实用价值,因AVEX研究对比的是卡培他滨+贝伐珠单抗与卡培他滨的疗效,而PANDA研究证实了帕尼单抗联合单药氟尿嘧啶与联合标准双药化疗的疗效相当。该研究与去年ASCO会议报告的针对老年胃癌进行减量化疗的GO2研究异曲同工,为老年胃肠肿瘤患者的治疗提供了新的模式。
文献来源:
1. Salvatore Siena, Maria Di Bartolomeo, et al. A phase II, multicenter, open-label study of trastuzumab deruxtecan (T-DXd; DS-8201) in patients (pts) with HER2-expressing metastatic colorectal cancer (mCRC): DESTINY-CRC01. 2020 ASCO Virtual Scientific Program, Abstract 4000. May 29-31.
2. Scott Kopetz, Axel Grothey, et al. Encorafenib plus cetuximab with or without binimetinib for BRAF V600E metastatic colorectal cancer: Updated survival results from a randomized, three-arm, phase III study versus choice of either irinotecan or FOLFIRI plus cetuximab (BEACON CRC). 2020 ASCO Virtual Scientific Program, Abstract 4001. May 29-31.
3. Sara Lonardi, Marta Schirripa, et al. First-line FOLFOX plus panitumumab versus 5FU plus panitumumab in RAS-BRAF wild-type metastatic colorectal cancer elderly patients: The PANDA study. 2020 ASCO Virtual Scientific Program, Abstract 4002. May 29-31.
专家简介

刘静
医学博士,主任医师
上海交通大学医学院附属瑞金医院肿瘤科
上海交通大学医学院附属瑞金医院无锡分院肿瘤科执行主任
专业特长:常见实体瘤的靶向和免疫治疗为主的综合治疗
美国国立癌症研究所(NCI/NIH) 、华盛顿大学医学院访问学者
中华医学会肿瘤学分会结直肠肛肿瘤学组委员
中国抗癌协会肿瘤靶向治疗专业委员会委员
中国抗癌协会肿瘤支持治疗专委会青委会副主任委员
中国抗癌协会肿瘤营养专业委员会精准营养学组副组长
中国医师协会结直肠肿瘤专委会肝转移专委会副秘书长,内科治疗专委会秘书
CSCO青年专家委员会常委兼秘书
CSCO抗肿瘤药物安全管理专委会委员
CSCO肝癌专家委员会委员
参与《临床肿瘤学手册》第6版、《结直肠癌规范化诊疗》、《中国临床肿瘤学年度研究进展2016》等7部著作的编译工作,担任《胃癌腹膜转移防治中国专家共识》2017版专家组成员,《中国Ⅱ、Ⅲ期结直肠癌县域医师诊疗指南-内科部分(2019版草案)》执笔人。
#医师报超能团#
#超能健康团#
#健康科普排位赛#