
文|夜舒刀
编辑|夜舒刀
前言
近几十年来,水污染已成为人类面临的最重要的环境问题之一,无机污染物也被称为可溶性金属离子,它被认为是最重要的环境问题之一。
人们担忧有毒金属进入水体中的释放,进而会污染环境以及危害身体健康,例如,金属离子Pb(II)、Cr(III)、Hg(II)、Cd(II)、Zn(II)、Co(II)和Ni(II),这些金属离子在环境中排放超过人体健康风险的数量时,被认为是有毒的。
在重金属去除方面,我们已经使用和认可了许多方法,而这些方法包括光催化降解、电化学沉淀、离子交换、膜分离和吸附等。
然而这些传统方法仍然存在一些限制,如对操作环境的敏感性、低效率、高处理成本和污泥产生等。
我们这次研究准备通过一种新型Fe3O4/钠沸石纳米复合材料, 研究从水溶液中去除镉和铜离子的方法 ,并使用场发射扫描电子显微镜(FE-SEM)、傅里叶变换红外光谱(FT-IR)和X射线衍射对合成产物进行表征。
化学品
我们这次所需要的试验品包括硫酸亚铁七水合物(FeSO4·7H2O)、氢氧化钠(NaOH)、六水合氯化铁(FeCl3·6H2O)和烟雾二氧化硅(SiO2)等均来自Sigma Aldrich化学公司,并且这都是在无需纯化的情况下使用。
我们在准备实验材料之后,随即将1.50克的Fe3O4和7.50克的钠沸石,放在100毫升乙醇中搅拌回流反应24小时,然后使用磁铁将形成的纳米复合材料分离,最后用蒸馏水多次清洗产物,并在烘箱中干燥。
随后我们使用D8 Advance X射线衍射仪(铜靶,CuKα波长=1.5 Å)获得了化学合成粉末的X射线衍射图谱。合成粉末的傅里叶变换红外光谱,在4000至400 cm-1范围内使用Nicolet iS50分光光度计压片成钾溴化物后获得。
合成粉末的形貌通过JSM-IT800 Schottky型场发射扫描电子显微镜进行了研究,并使用Perkin Elmer-3300多元素原子吸收光谱仪,估计了铜离子和镉离子的浓度。
合成复合材料的磁性在室温(27 °C)下使用振动样品磁强计(VSM-Cryogenic Limited PPMS)测定,并使用热重分析仪(TGA-Shimadzu DT-60H)在氮气氛下,研究了合成复合材料的稳定性,加热速率为10 °C/min。
合成粉末的鉴定
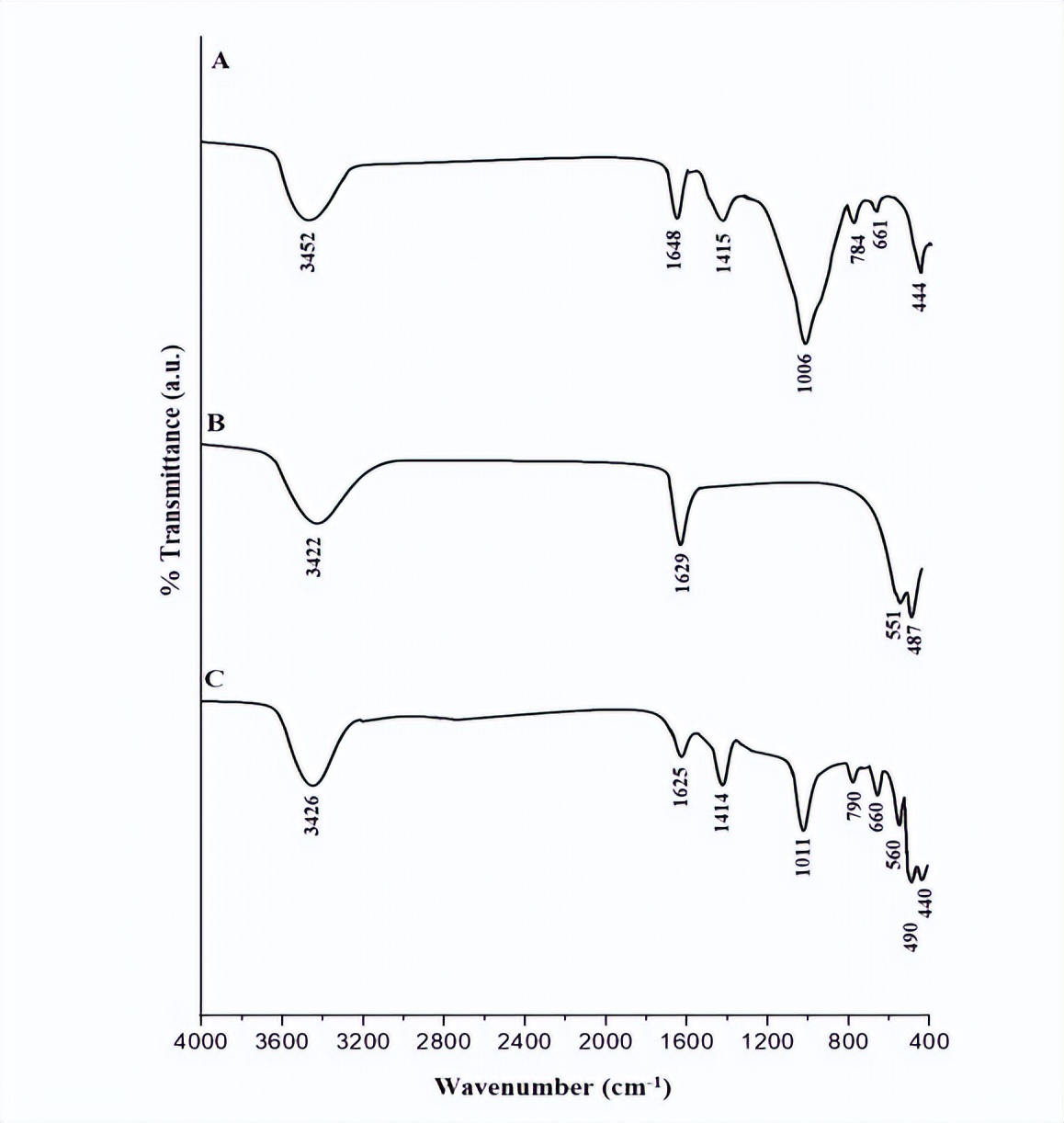
图1A-C显示了钠沸石、Fe3O4和Fe3O4/钠沸石纳米复合材料的FT-IR光谱,我们发现钠沸石的FT-IR带分别出现在444、661和784 cm-1,分别由于W–O–W(W=Si和/或Al)的弯曲振动、内部对称振动和外部对称振动。
钠沸石的FT-IR带分别出现在1006、1415、1648和3452 cm-1,由于W–O–W的内部非对称振动、外部非对称振动、H–O–H的弯曲振动和H–O–H的伸展振动,Fe3O4的FT-IR带出现在487和551 cm-1,由于Fe–O的伸展振动。
我们发现Fe3O4的FT-IR带出现在1629和3422 cm-1,这是因为H–O–H的弯曲和伸展发生了振动,在Fe3O4/钠沸石纳米复合材料中,钠沸石的FT-IR带出现在440、660、790、1011、1414、1625和3426 cm-1。
而Fe3O4/钠沸石纳米复合材料中Fe3O4的FT-IR带出现在490和560 cm-1,通过比较钠沸石、Fe3O4和Fe3O4/钠沸石的FT-IR光谱,结果显示几乎所有的钠沸石和Fe3O4,都可以在合成的Fe3O4/钠沸石纳米复合材料中观察到, 这表明成功合成了经过改性的Fe3O4/钠沸石。
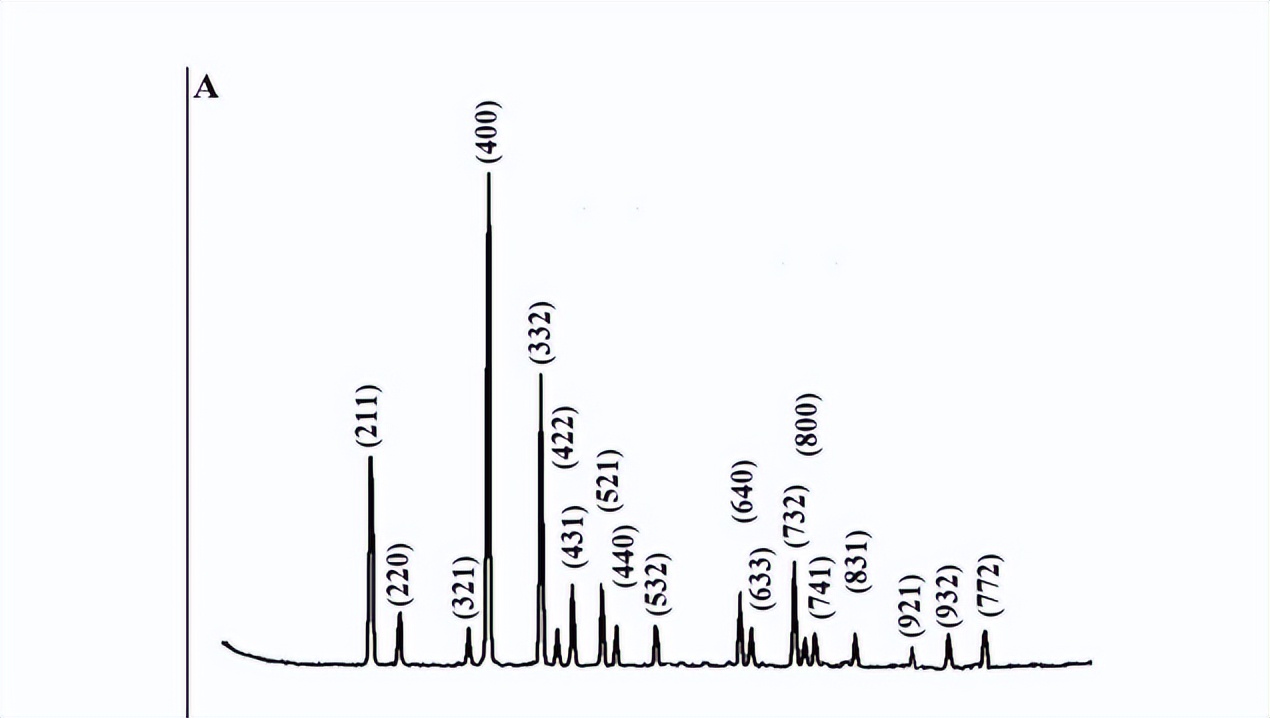
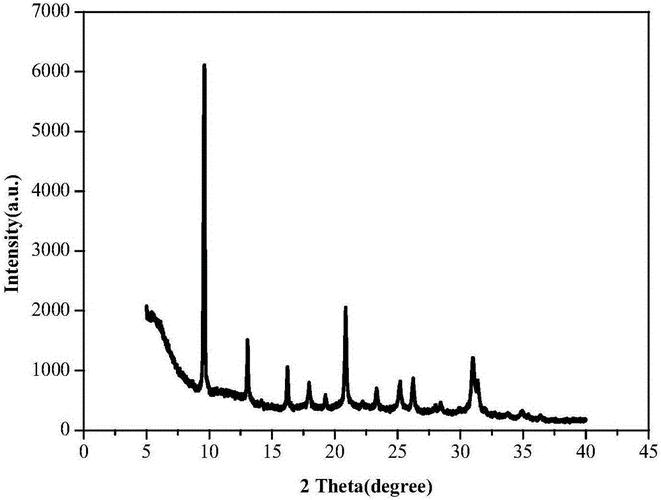
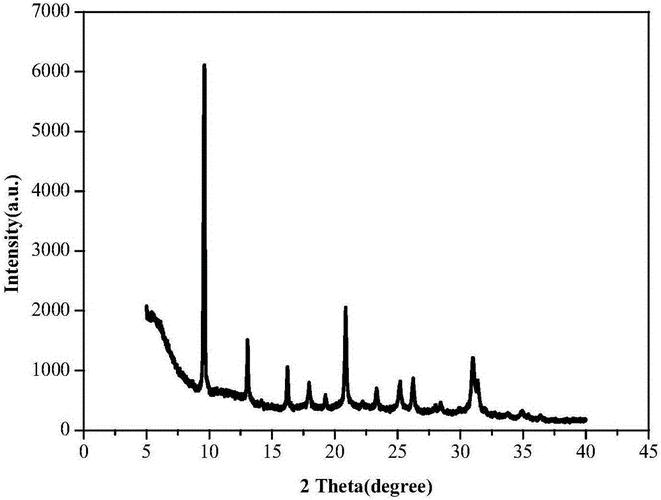
图A显示了钠沸石、Fe3O4和Fe3O4/钠沸石纳米复合材料的X射线衍射图谱。
我们发现在2Ɵ=15.83°、18.39°、24.33°、25.99°、30.64°、31.90°、33.25°、35.88°、37.03°、40.49°、47.84°、48.68°、52.46°、53.29°、54.25°、57.71°、62.75°、65.90°和69.04°位置的X射线衍射峰,是由于钠沸石的(211)、(220)、(321)、(400)、(332)、(422)、(431)、(521)、(440)、(532)、(640)、(633)、(732)、(800)、(741)、(831)、(921)、(932)和(772)米勒指数。
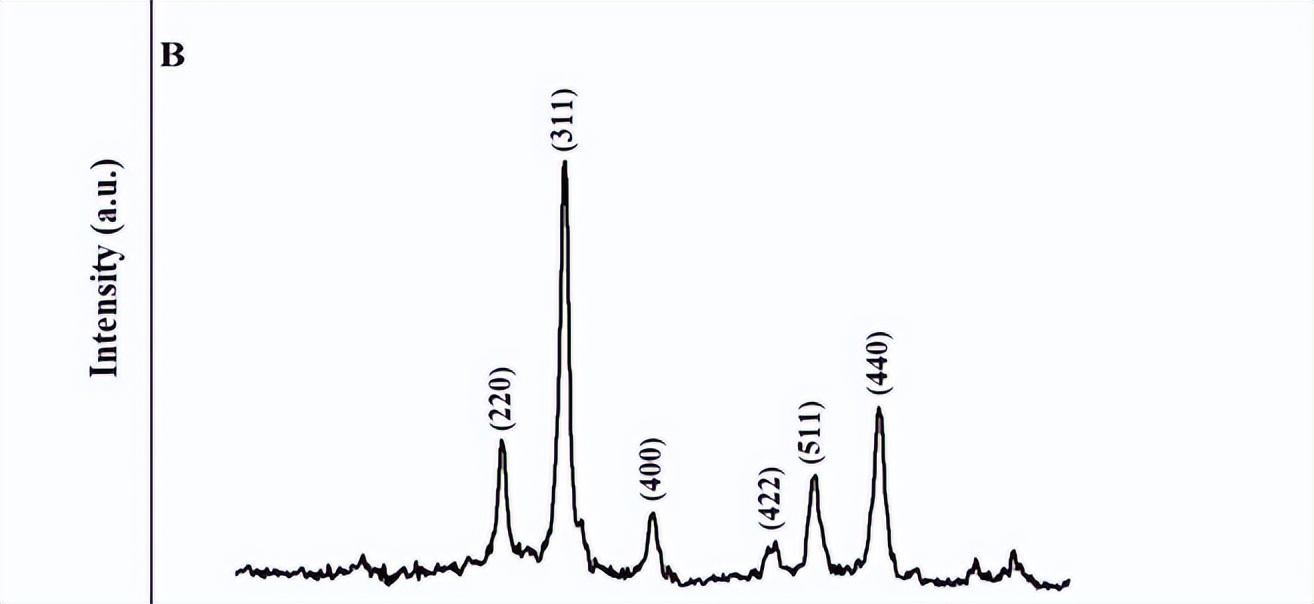
而出现在2Ɵ=30.22°、35.57°、43.23°、53.83°、57.29°和62.85°位置的X射线衍射峰是由于Fe3O4的(220)、(311)、(400)、(422)、(511)和(440)米勒指数,这从JCPDS No. 85-1436中可以得到证实。
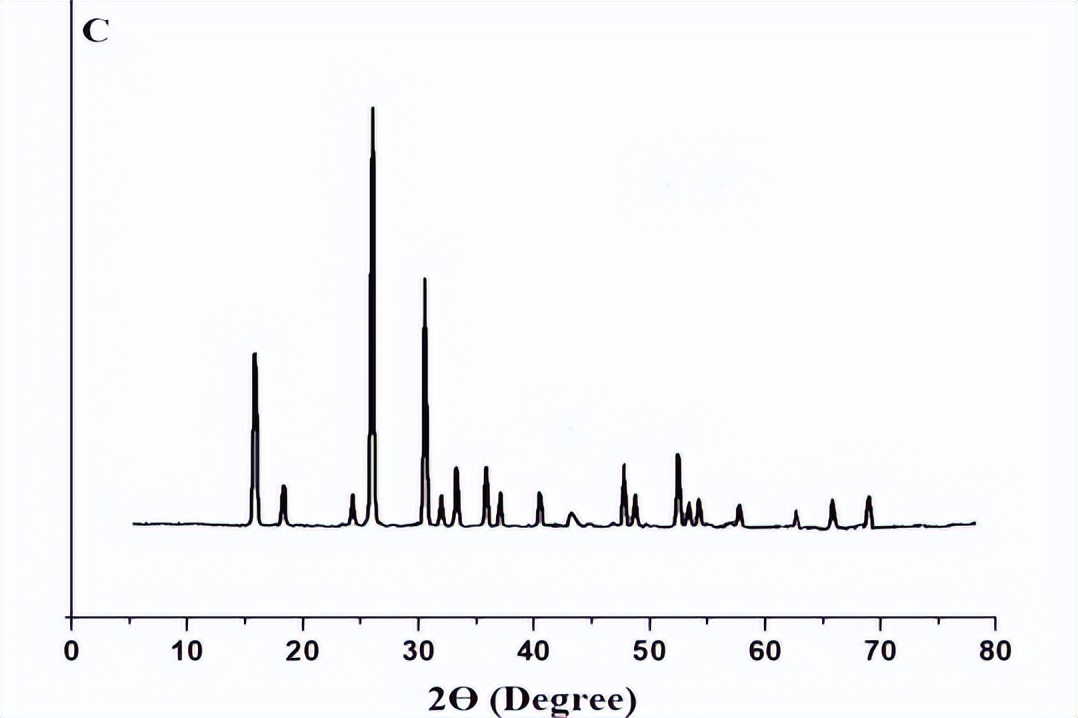
Fe3O4/钠沸石纳米复合材料的X射线衍射峰强度受到影响,这与钠沸石非常相似。在纳米复合材料的X射线衍射图案中,Fe3O4最强的峰位于2Ɵ=35.57°,由于与Fe3O4相比,钠沸石的峰位更强,我们通过Scherrer方程计算,钠沸石、Fe3O4和Fe3O4/钠沸石纳米复合材料的平均结

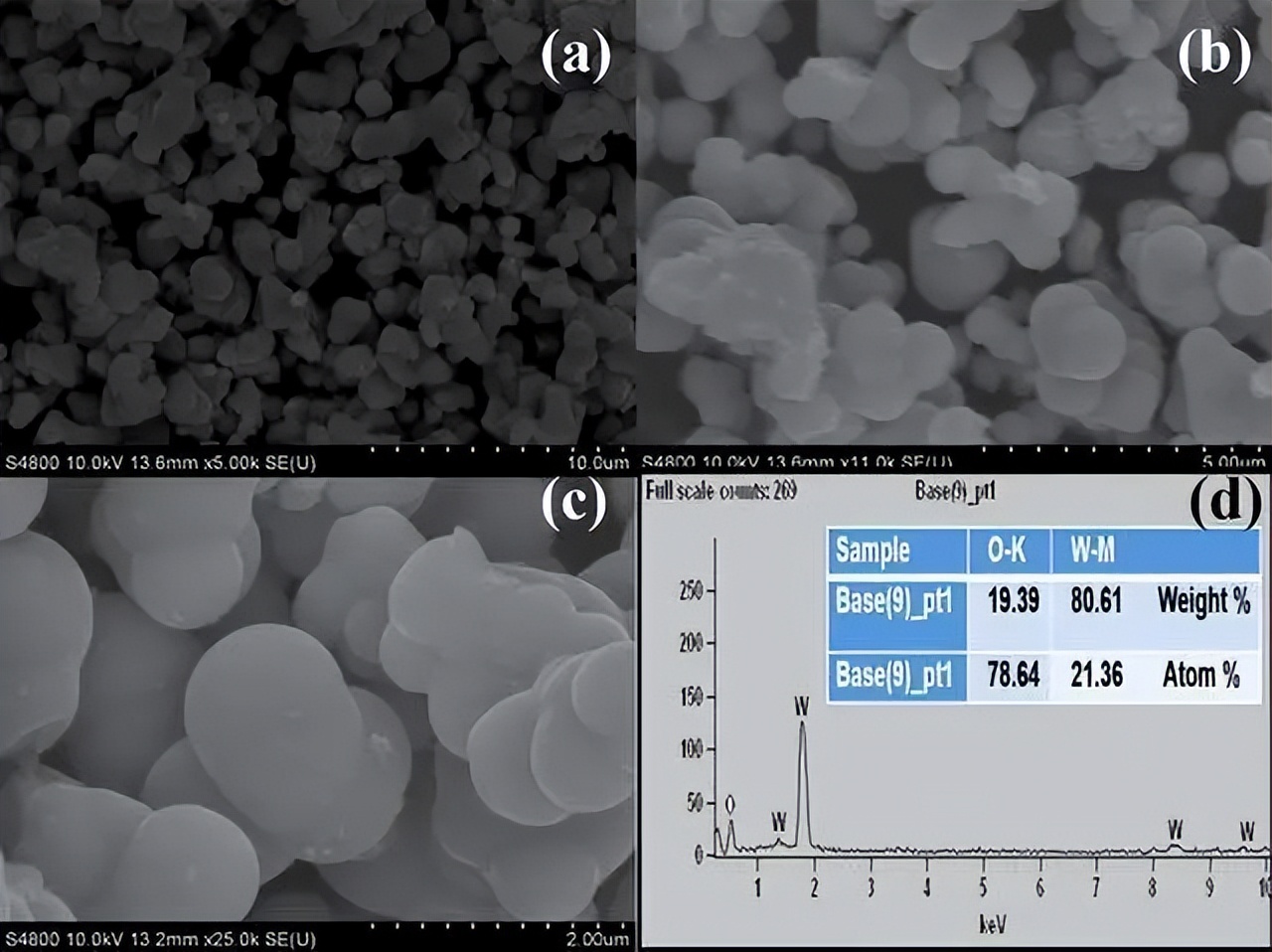
图3A-C展示了钠沸石、Fe3O4和Fe3O4/钠沸石纳米复合材料的FE-SEM形貌图像。结果显示钠沸石和Fe3O4样品具有多面体和准球形形状,平均直径分别为923.28和28.57 nm。
Fe3O4/钠沸石纳米复合材料具有多面体和准球形形状,平均直径为1100.00 nm,在Fe3O4纳米颗粒并入钠沸石框架后,观察到了钠沸石原始多面体结构的畸变。 这表明钠沸石和Fe3O4纳米颗粒之间存在结合相互作用,导致形态变化。

众所周知,SEM显示的是样品表面的形状,而不是颗粒的形状,颗粒可能是多个颗粒的组合,因此SEM不能用于确定样品是否是纳米尺寸,但XRD可以确定样品是否是纳米尺寸。
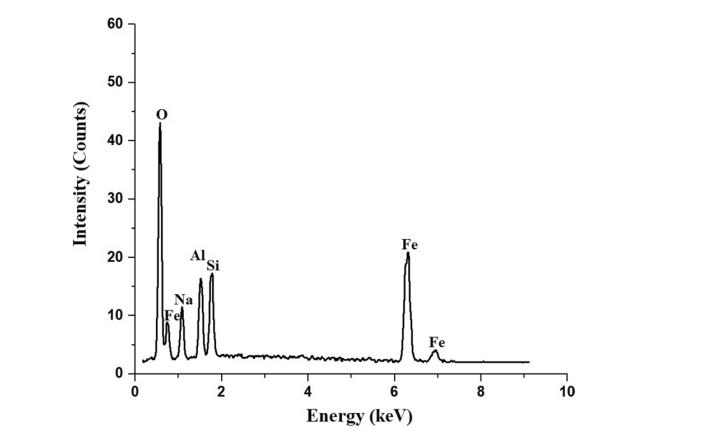
上图显示了Fe3O4/钠沸石纳米复合材料的EDX图谱。结果显示Fe3O4/钠沸石纳米复合材料由Fe、Si、Al、O和Na组成,其重量百分比分别为18.76、12.82、12.57、51.10和4.75%。因此这确认了钠沸石和Fe3O4纳米颗粒之间存在结合相互作用。
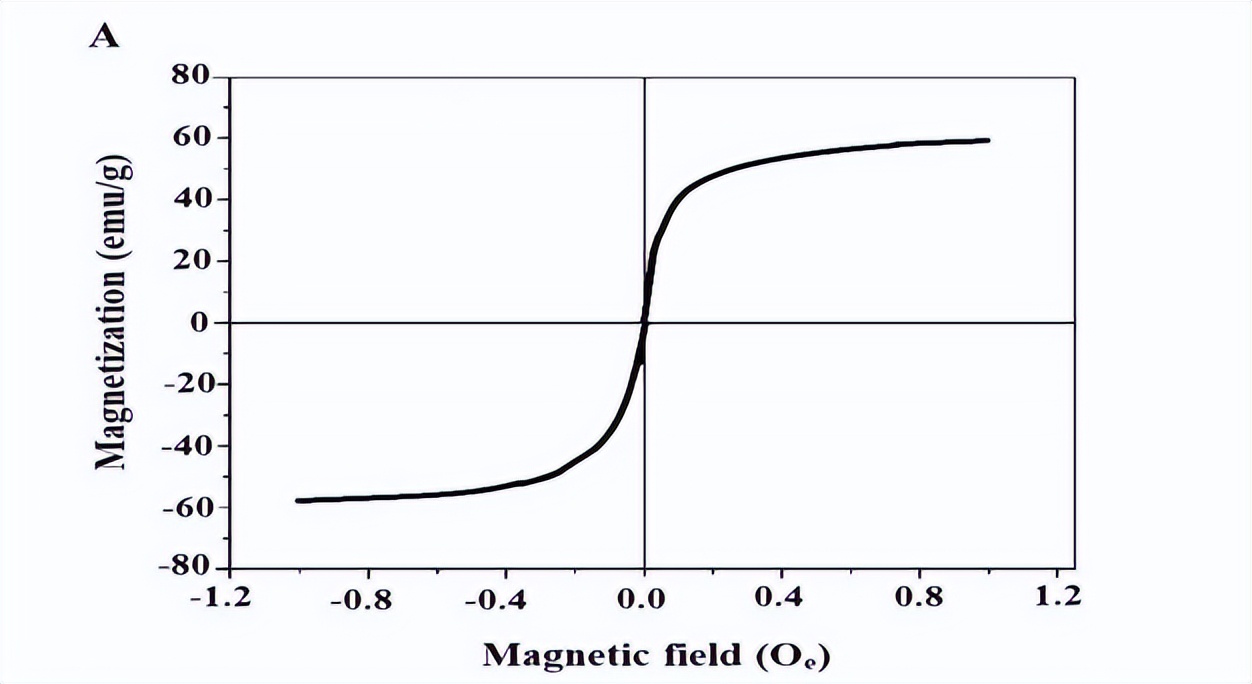
上图A显示了在27°C下合成纳米复合材料的磁化强度与磁场的关系图。图中显示合成纳米复合材料表现出超顺磁行为,具有零矫顽力和剩磁,饱和磁化强度(MS)约为59.50 emu/g。
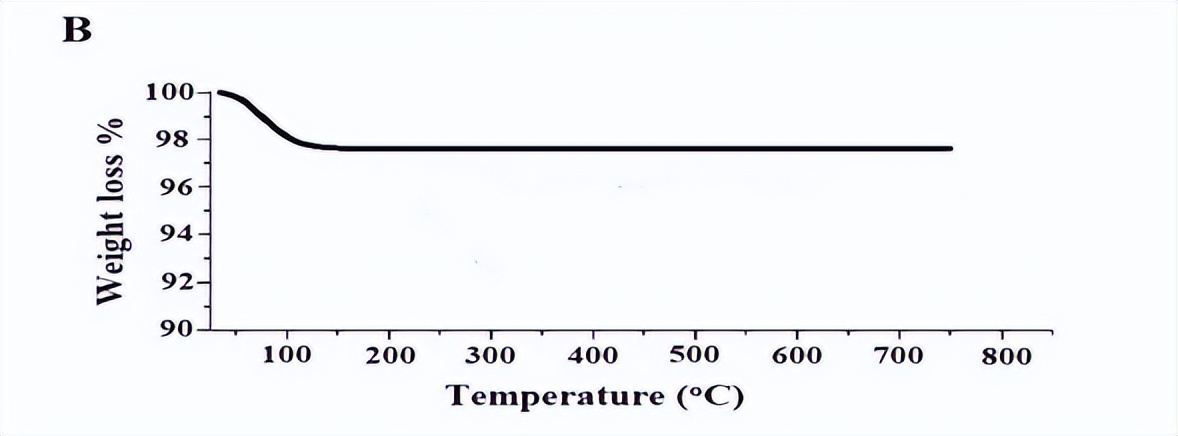
我们为了确定合成纳米复合材料的稳定性,进行了热重分析(TGA),如上图B所示。结果证实,由于去除了吸附水分子产生了约2.43%的重量损失, 因此这证实了合成纳米复合材料的稳定性。
水溶液中镉离子和铜离子的处理
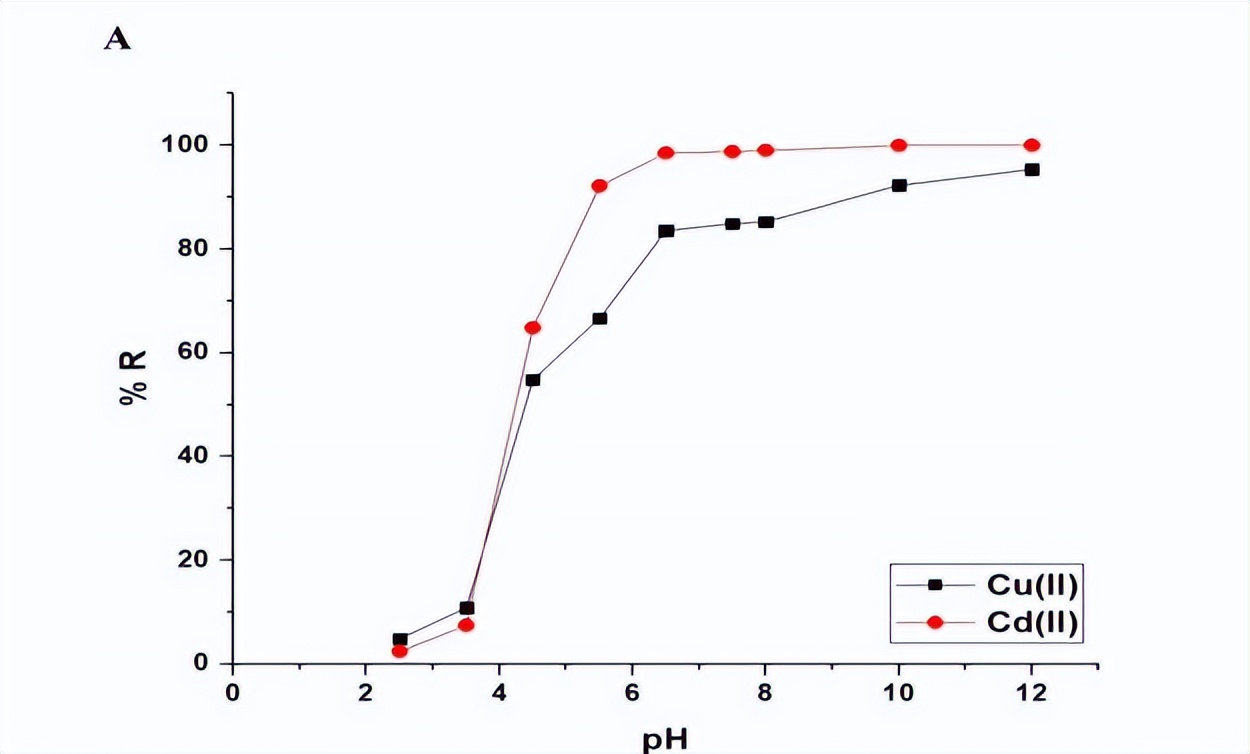
上图A展示了pH值对铜离子和镉离子的吸附百分比,以及Fe3O4/钠沸石纳米复合材料吸附能力的影响。结果显示随着pH值从2.50增加到6.50,吸附百分比和吸附能力均显著增加。
当pH值从6.50增加到8.00时,由于吸附剂的活性位点数量保持不变,增加非常微小。因此,pH值为6.50是实现最高铜离子和镉离子吸附率的理想值。在pH值为6.50时,使用Fe3O4/钠沸石纳米复合材料吸附铜离子和镉离子的吸附百分比分别为85.56%和98.50%。
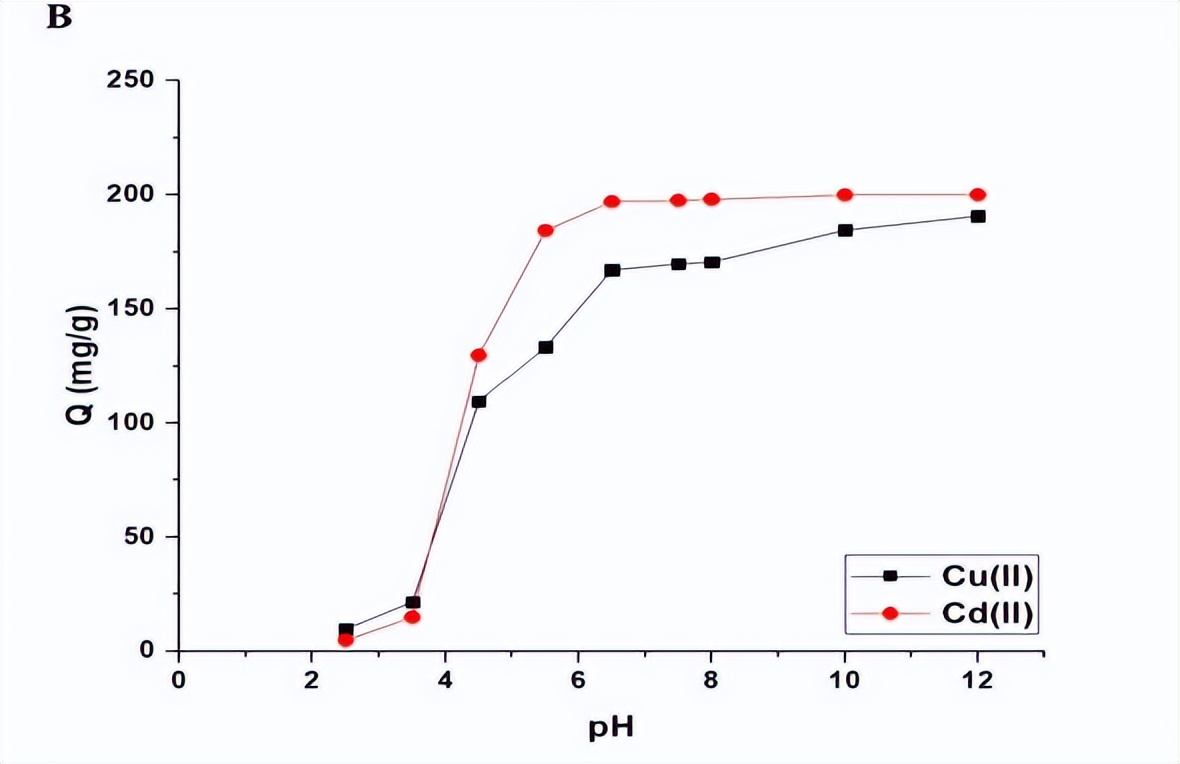
Fe3O4/钠沸石纳米复合材料对铜离子和镉离子的最大吸附能力,分别为167.11毫克/克和197.00毫克/克。我们为了理解pH值对镉离子和铜离子吸附过程的影响,确定了Fe3O4/钠沸石纳米复合材料的等电点(pHPZC),发现其为3.40。
在较低的pH值(即pH < pHPZC)下,Fe3O4/钠沸石纳米复合材料的正电位点数增加,这不利于正电荷的铜或镉离子的吸附,因为存在电荷斥力。
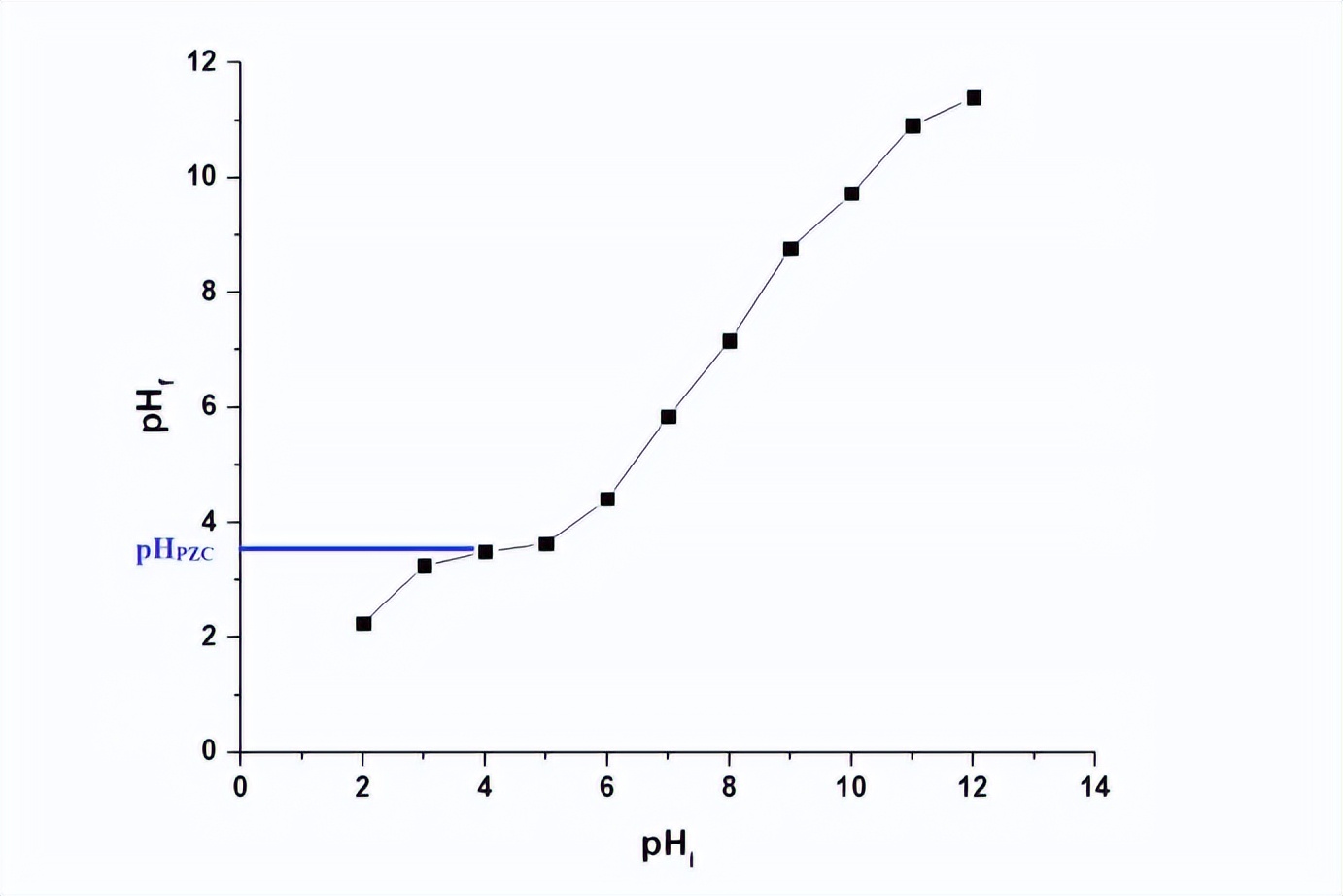
在较高的pH值(即pH > pHPZC)下,Fe3O4/钠沸石纳米复合材料的负电位点数增加,这有利于正电荷的铜或镉离子的吸附,因为存在电荷吸引,在较高pH值范围内(从10到12),氢氧化物与Cu(II)和Cd(II)离子的沉淀是高去除率的另一个原因。
时间效应
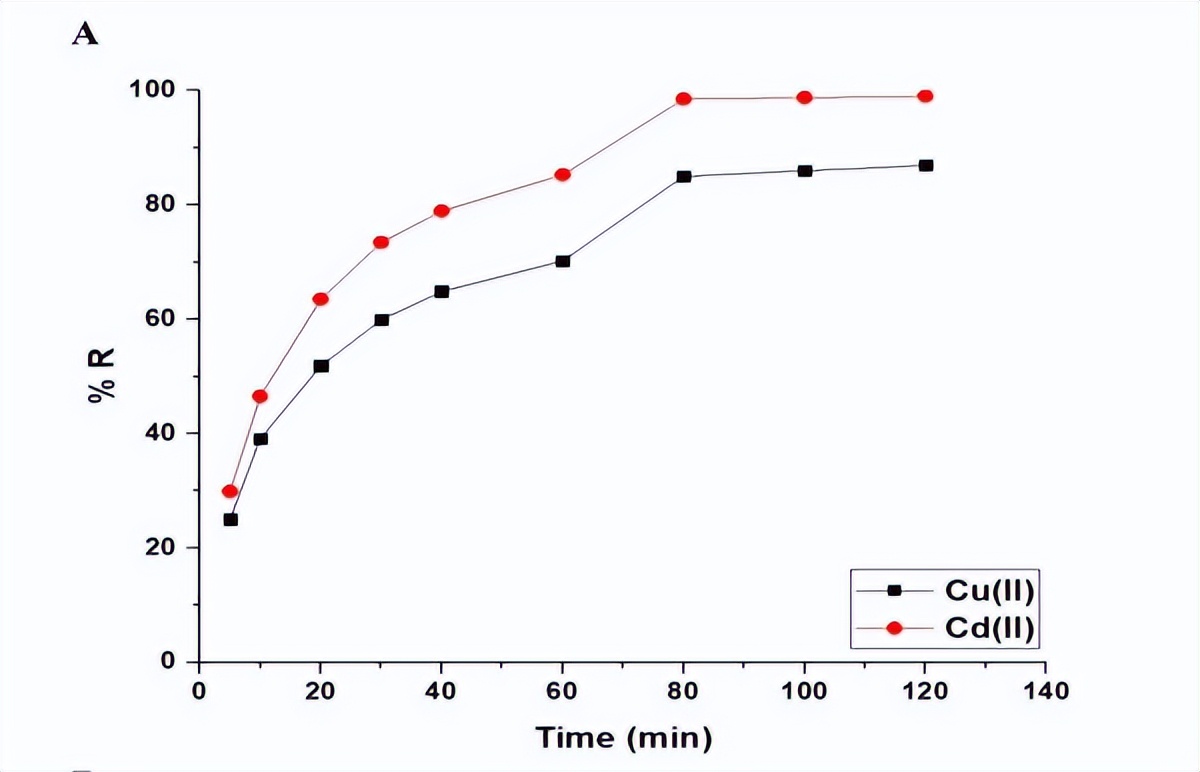
图8A展示了处理时间对铜离子和镉离子的吸附百分比,以及Fe3O4/钠沸石纳米复合材料吸附能力的影响。随着时间从5.00增加到80.00分钟,吸附百分比和吸附能力均显著增加。
当处理时间从80.00增加到120.00分钟时,由于吸附剂的活性位点饱和,增加非常微小,80.00分钟是实现最大铜离子和镉离子吸附率的理想值,在时间等于80.00分钟时,使用Fe3O4/钠沸石纳米复合材料吸附铜离子和镉离子的吸附百分比分别为85.00%和98.50%。
Fe3O4/钠沸石纳米复合材料对铜离子和镉离子的最大吸附能力分别为170.00毫克/克和197.00毫克/克。
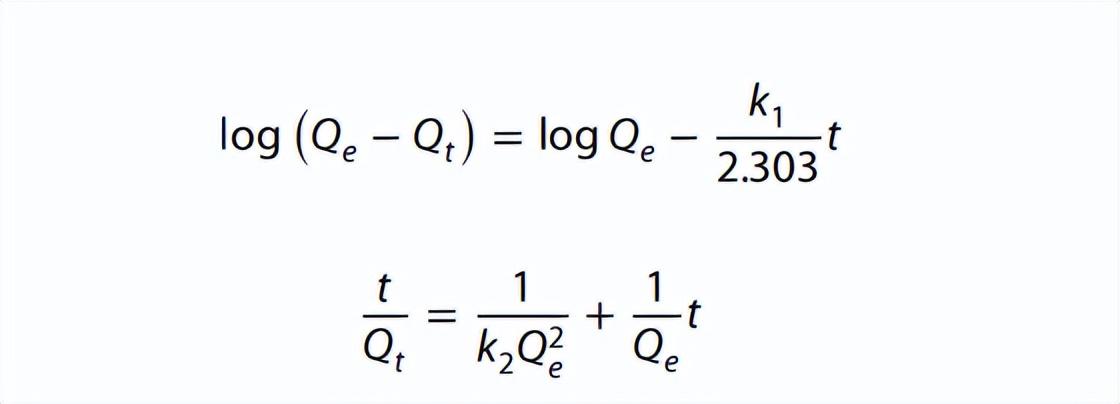
我们为了理解使用Fe3O4/钠沸石纳米复合材料吸附铜离子和镉离子的吸附过程,应用了两个动力学模型,伪一级(方程式3)和伪二级(方程式4)。
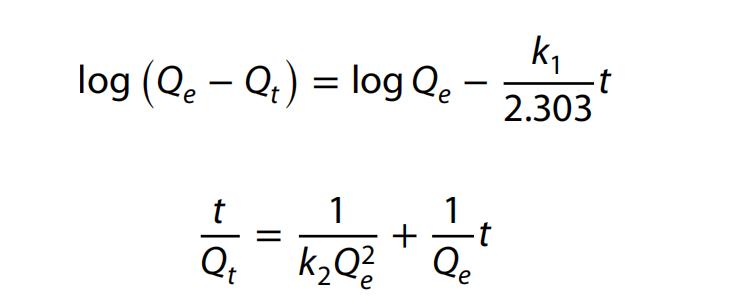
其中,Qt是时间t时吸附的铜离子或镉离子的量(毫克/克),Qe是平衡时吸附的铜离子或镉离子的量(毫克/克),k1是伪一级速率常数(1/分钟),k2是伪二级速率常数(克/毫克.分钟)。
与伪一级模型相比,伪一级模型拟合效果较差,相关系数值(R2)较低,因此伪二级模型可能更好地描述,使用Fe3O4/钠沸石纳米复合材料吸附铜离子或镉离子的过程。
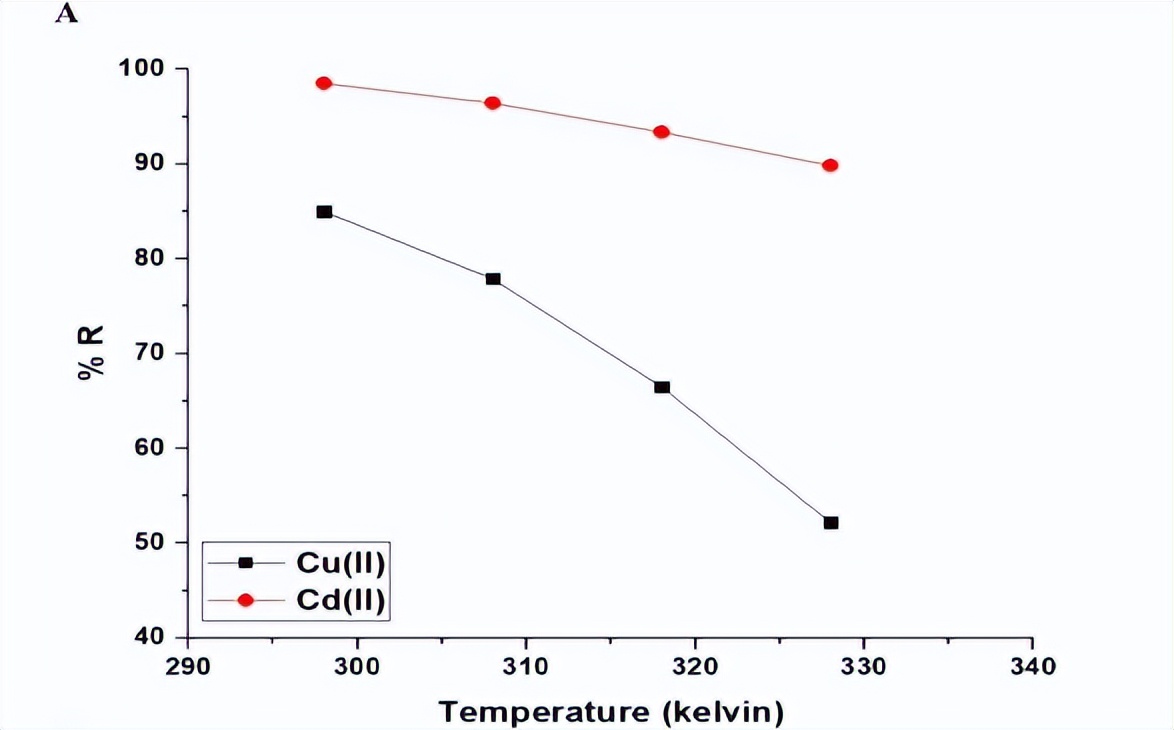
图10A展示了吸附温度对镉离子和铜离子的吸附百分比,以及Fe3O4/钠沸石纳米复合材料吸附能力的影响。结果显示,随着温度从298.00升高到328.00 K,吸附百分比和吸附能力均显著降低。
因此298.00 K是实现最大铜离子和镉离子吸附率的理想温度。我们利用方程式5、6和7,可以确定热力学参数,例如自由能变化(△Go,KJ/摩尔)、焓变化(△Ho,KJ/摩尔)和熵变化(△So,KJ/摩尔K)。
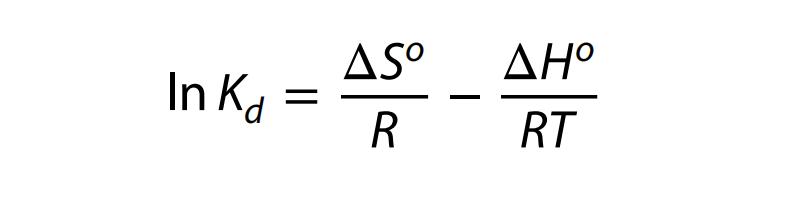
其中,Kd是分配常数(L/g),R是气体常数(KJ/摩尔开尔文),T是吸附温度(开尔文)。我们使用Fe3O4/钠沸石纳米复合材料吸附镉离子和铜离子是放热的,由△Ho的负值显示出来。
△Ho的值大于40 KJ/摩尔,表明吸附是化学性质的,熵是随机性的一种度量,当使用Fe3O4/钠沸石纳米复合材料处理铜离子和镉离子时,熵的正值意味着这些离子在溶液中随机运动,并从所有方向进入吸附剂,从而提高了分离效率。
浓度效应
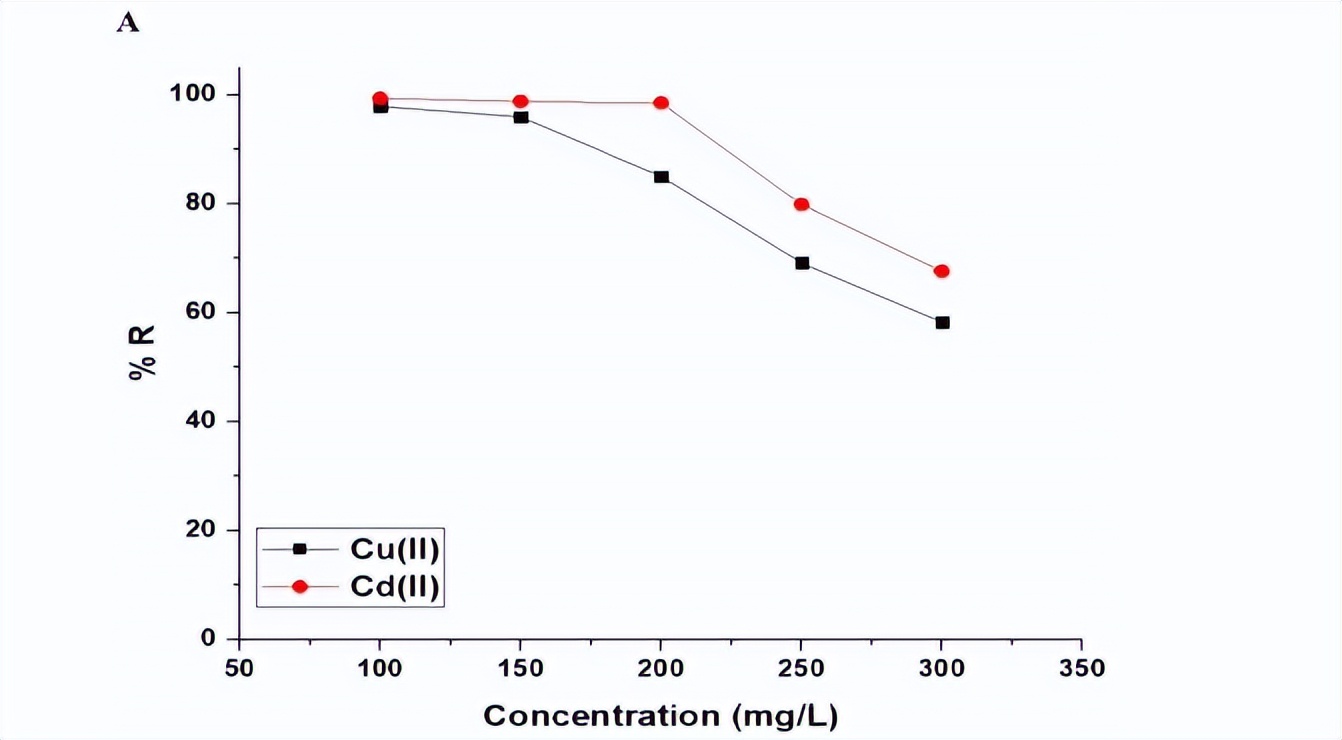
图12A和B展示了浓度对铜离子和镉离子的吸附百分比,以及Fe3O4/钠沸石纳米复合材料吸附能力的影响。结果显示,随着浓度从100.00升高到300.00 mg/L,吸附百分比显著降低,而吸附能力则显著增加。
我们为了理解使用Fe3O4/钠沸石纳米复合材料吸附铜离子和镉离子的吸附过程,应用了两种平衡等温线模型,Langmuir模型(方程式8)和Freundlich模型(方程式9)。
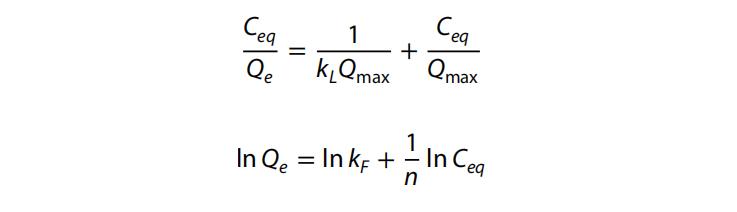
其中,1/n是异质性常数,kL是Langmuir等温线的平衡常数(L/mg)。kF是Freundlich等温线的平衡常数(mg/g)(L/mg)1/n,而Qmax是Langmuir等温线的最大吸附能力(mg/g)。
方程式10可以用于使用Freundlich等温线计算Qmax。
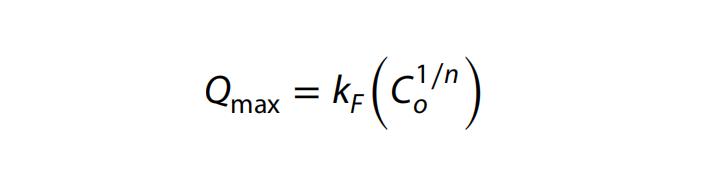
与Langmuir等温线相比,Freundlich等温线提供了拟合效果较差的结果,其相关系数值(R2)较低。
因此Langmuir等温线可能更好地描述使用Fe3O4/钠沸石纳米复合材料处理铜离子或镉离子的过程。Fe3O4/钠沸石纳米复合材料对铜离子和镉离子的最大吸附能力分别为176.68毫克/克和203.67毫克/克。
结论
在这次实验当中我们发现, Fe3O4/钠沸石纳米复合材料可以轻松地合成为一种新颖的纳米结构,被用于从水溶液中有效处理铜离子和镉离子。
我们通过场发射扫描电子显微镜(FE-SEM)、傅里叶变换红外光谱(FT-IR)和X射线衍射(XRD)对产物进行了表征,发现Fe3O4/钠沸石纳米复合材料对铜离子和镉离子的最大吸附能力,分别为176.68毫克/克和203.67毫克/克。