自发性蛛网膜下腔出血(SubarachnoidHemorrhage,SAH)是神经外科临床常见急症,大多数由颅内动脉瘤破裂导致,死亡率和致残率颇高。
开颅夹闭和介入治疗是当前主要的手术治疗方法, 即使在动脉瘤安全化后,患者在围手术期依然面临诸多并发症的风险,其中脑血管痉挛(CerebralVasospasm,CVS)发生率相对较高、后果严重。
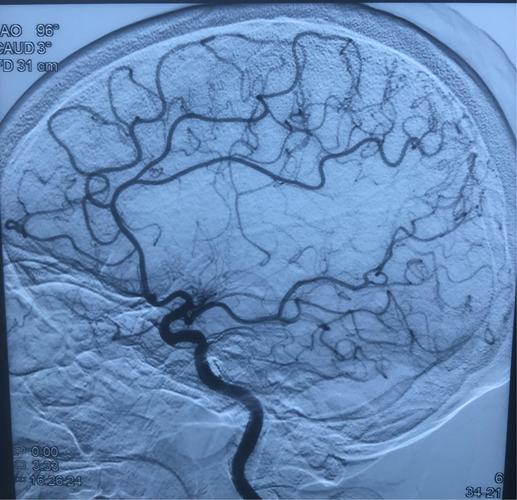
动脉瘤性蛛网膜下腔出血术后脑血管痉挛的危险因素分析
因缺乏有效的早期预测标志物和方法,目前临床上对CVS的诊断和治疗常较为被动,有关CVS的预测模型的研究亦鲜有报道, 针对动脉瘤性蛛网膜下腔出血 (AneurysmalSubarachnoidHemorrhage,aSAH)患者CVS并发症临床研究。
拟通过临床病例整理和分析,探究aSAH患者术后CVS的危险因素,尝试构建CVS早期预测模型并转化为临床可用的实用工具,并对 手术技术、相关研究现状 等加以讨论。
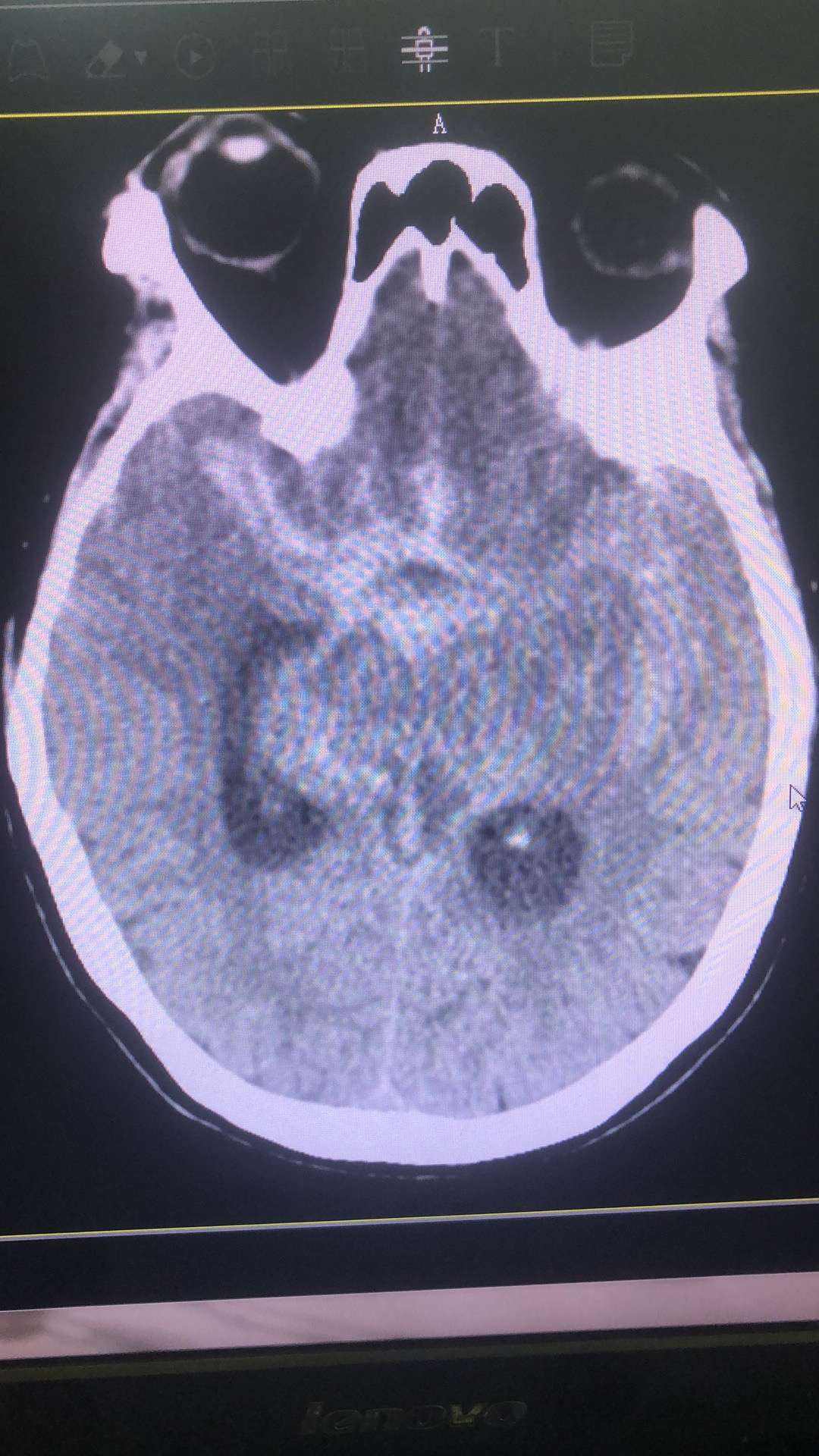
脑血管疾病是现代人类健康面临的重要威胁 ,自发性蛛网膜下腔出血,是其中尤为危险的一类,它发病突然,即便在如今医疗水平迅速发展的条件下,死亡率和致残率仍旧很高。
近乎80%的自发性SAH 是由颅内动脉瘤破裂引起的,一旦发病需立即接受治疗 ,随着诊疗技术的提升,近年来我们对动脉瘤性蛛网膜下腔出血的诊断、手术治疗都取得了一定进展。
通过血管成像,对动脉瘤的诊断已经很容易明确, 随着手术技术的成熟和手术材料的更迭,手术治疗方案也逐渐向科学化、个体化发展。然而,在很多情况下,aSAH带来的各种并发症可以对患者预后产生决定性的影响。
脑血管痉挛(CerebralVasospasm,CVS)是aSAH的常见并发症,通常会导致迟发脑缺血(DelayedCerebralIschemia,DCI),并产生相应临床症状。现在通常认为, 症状性CVS多发生于动脉瘤破裂后的一周内,发生率可达1/3 。
目前, 即便在非常成熟的脑血管病中心 ,多数情况下临床医生只能通过患者的临床恶化来判断CVS并采取更加激进的抗CVS治疗方案,对CVS的诊治处于相对被动的状态。
而CVS及DCI一旦发生,则有可能产生严重后果, 显著改变患者的预后和生存质量 ,因此临床上对CVS的早期预测具有重要意义。

对于aSAH患者来说,术后并发症特别是CVS的早期诊断极为重要,尤其是对发病时状态本就不好的患者来说,因此我们可以将P/C作为一个潜在的、简单的预测CVS易感性的标志物来使用。
CVS的病理生理机制较为复杂,尚不完全清楚 ,有研究发现P/C是aSAH患者术后CVS的独立危险因素,很可能是由于P/C反映了CVS复杂病理生理过程中一些微妙、暂时无法量化的改变,这些病理生理变化可能进一步影响患者的一般状态,使其呈现出不同的临床分级。

有文献报道,同样是常规的血液化验项目,来作为预测aSAH患者CVS/DCI的标志物,比较经典的有MPV(MeanPlateletVolume,平均血小板体积,中性粒细胞/白蛋白比值)。据我们所知,关于P/C对CVS可能的预测价值, 其中的具体机制,以及其究竟是危险因素还是保护因素 ,暂无相关报道。

血小板和血清钙离子都在凝血稳态及血管功能中具有重要作用 ,因此更高P/C比值相关的CVS风险或许能从中得到解释。
Morotti等报道对于颅内出血的患者,入院时更低的血Ca2+值与更多的出血量以及血肿扩大相关联,可能和血Ca2+对于血小板功能的作用,以及血Ca2+对凝血级联反应的作用有关。
尼莫地平是可以通过血脑屏障的钙通道阻滞剂,是我们 目前最常用,可能也是仅有的有效的抗CVS药物 ,它可以阻止细胞外Ca2+内流进入血管平滑肌,对于脑血管的选择性则可能来自于其平滑肌收缩对胞外Ca2+更强的依赖性。
在临床上,静脉应用的尼莫地平通常选用0.02%浓度(10mg:50ml),每日常规应用2-3剂,口服给药亦是可选方案。然而即使大剂量的预防性给药,有时也无法避免CVS的发生。

由于钙调节机制的复杂性,低钙血症同样也可能通过影响脑血管活动导致其收缩,进而血压升高及动脉瘤二次破裂的风险也相应升高。
目前我们知道, 血小板在内环境稳态、炎症反应、血管节律中均是关键媒介 。在发生aSAH时,血小板暴露于蛛网膜下腔,处激活状态,暂抛开其他因素,血小板直接释放的血管收缩物质即可以直接介导脑血管的收缩。

这些血管收缩物质中有两个,对于血小板介导的aSAH患者的CVS尤为重要,即TXA2(ThromboxaneA2,血栓素A2)和PDGF-β(Platelet-derivedGrowthFactor-β,血小板源性生长因子-β)。
有报道明确指出aSAH发病后的高PDGF-β水平和CVS/DCI的发生发展具有相关性。亦有基于动物模型的研究支持血小板对SAH后CVS起重要作用。
此外,多项研究认为,在SAH发生后的 极短时间内即可发生微血管收缩和血栓形成 ,同时在痉挛最为严重的微血管中能观察到血小板聚集,因此有理由认为血小板聚集/血栓形成与SAH后微血管的收缩有很强相关性。
总之,血小板对大血管和微血管的痉挛都起重要作用从而导致症状性CVS。通过自聚集 促进血栓形成、与内皮细胞及免疫细胞的交互作用、释放趋化因子和细胞因子参与炎症反应 等这些因素都使得血小板在CVS事件中起关键作用。

高凝状态
颅内动脉瘤破裂出血后另外一个重要的病理生理就是高凝状态, 高凝状态可以直接导致脑动脉中发生血小板聚集和微血栓形成 ,基础和临床研究都证实了动脉瘤破裂后早期的血小板聚集。并且,尽管凝血机制在动脉瘤破裂出血后即刻启动是为了止血,出血停止后高凝状态却并不结束。
即使在进行了手术治疗,动脉瘤被安全化后数天,aSAH患者依然保持高凝状态,尤其是在发生CVS的患者中, 血小板活动比那些没有发生明显CVS的患者更高 。在微血管中沉积的聚集血小板/微血栓进一步减少相应区域血流量,结果是形成恶性循环,导致明显的临床症状和预后改变。
在aSAH发病后,通过介导和促进炎症反应,血WBC同样可能对CVS产生影响,有趣并值得注意的是, WBC亦可以促进高凝状态 。
通常,动脉瘤破裂后,蛛网膜下腔内的积血激发一系列反应,其中自然包括对RBC的清除,血管内皮细胞表面快速表达特定的细胞黏附分子,以 使循环中的巨噬细胞和中性粒细胞进入蛛网膜下腔发挥吞噬作用 。
随后脑脊液中死亡的白细胞和被吞噬的红细胞体可释放大量有害物质包括内皮素、氧自由基、血红蛋白/亚铁血红素(及降解产物)等等, 这些物质的释放会促进炎症反应通路和内皮细胞介导的血栓形成 ,后者更是能够形成激活血小板、导致微血栓形成的正反馈通路。
血小板激活后,血小板致密体中会释放包括Ca2+的一些物质, 参与炎症反应和血栓形成的反馈通路,但其具体机制尚不明晰。
我们有理由相信,上述交互作用会增进aSAH患者术后CVS的发展。当然,P/C对CVS影响的具体机制没有定论需要我们进一步探索和更深入的研究。传统的“3H”疗法(高血容量,Hypervolemic;高血压,Hypertensive;血液稀释,Hemodilution)一度被认为是防治CVS的关键。
入院时血容量相关指标(HCT、RBC、Hb等)在组间未显现出差异,近年也有观点对3H疗法提出了挑战,2021版《中国脑卒中防治指导规范》则倾向于把重点放在平衡血容量,而 仅对动脉瘤已经安全化且高度怀疑CVS/DCI的患者实行诱导性高血压治疗 。
关于对血压和血容量的管理如何正确理解、其与CVS的关系,尚需进一步的研究来探讨。我们发现在动脉瘤开颅或介入手术治疗后, 年龄更大的患者发生术后CVS的风险更高 。目前年龄和aSAH后CVS的关系仍有争议,有相关研究得出相反的结论,认为相对年轻的患者更容易发生CVS的并发症。
在单因素分析中,发病到手术时间在是否发生CVS组间有显著差异,由于种种原因,我们无法将这一时间精确到小时甚至分钟。但 尽早手术对于减少术后CVS风险更有利 ,有超过8000例患者的大规模临床研究支持这一观点。
这不得不让我们提起aSAH治疗中的常见的一个矛盾,aSAH发病早期通常伴有颅内压的增高,会对手术形成障碍,尤其是开颅夹闭, 颅高压带来的暴露困难会使手术难度和危险性增加,即使是经验丰富的手术医师也无法规避这一问题。
在最初的分析中,腰大池引流成为了术后CVS的一个危险因素,但我们最终将其作为偏倚因素予以排除在logistic模型之外,仅5.7%(15/262)的患者进行了腰大池引流治疗。
实际上,另外有一些患者做了多次腰椎穿刺术,目的与腰大池引流基本一致,均是 加快脑脊液循环,促进血性脑脊液的排出。
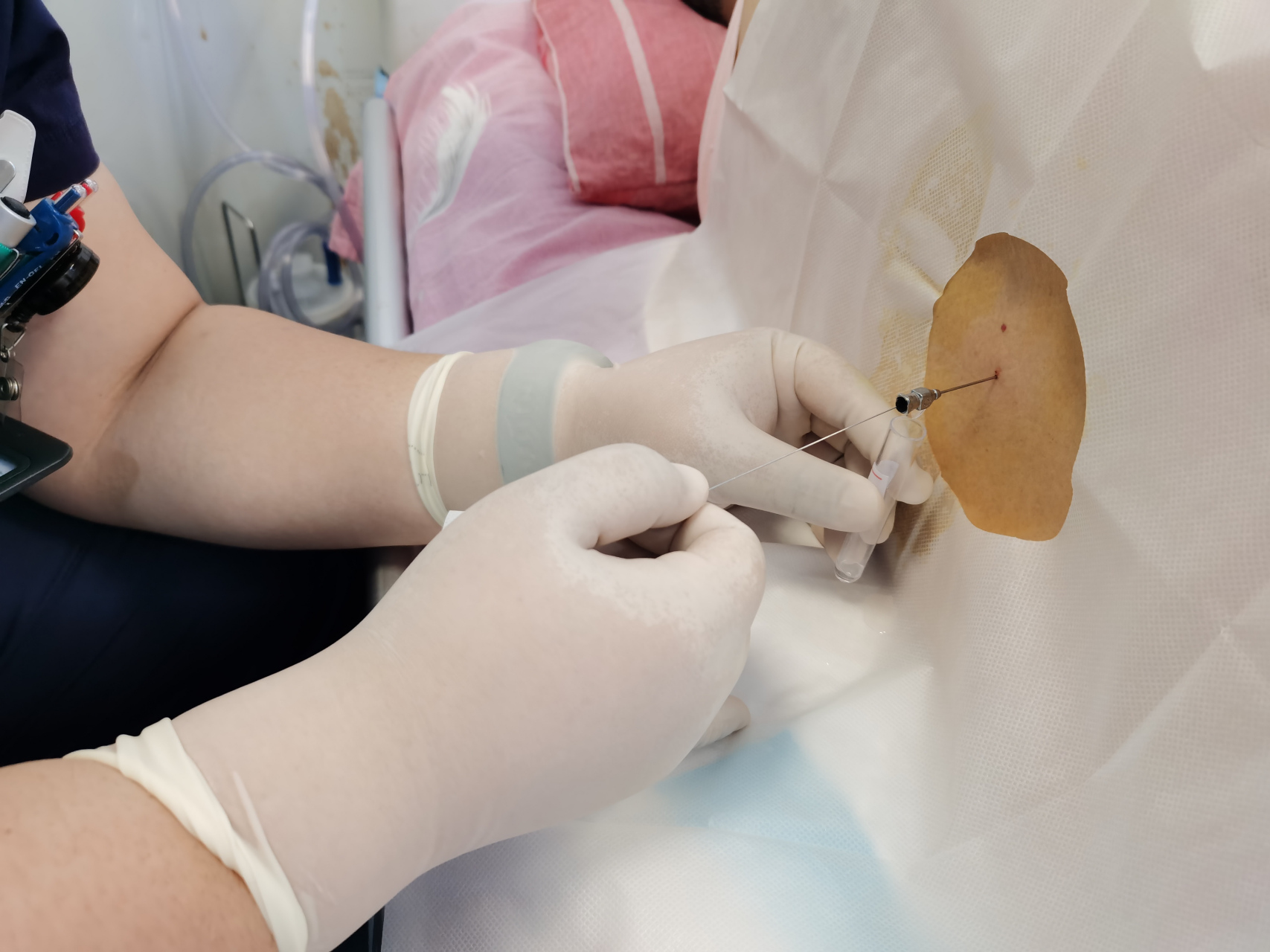
通常在腰椎穿刺时每次释放最多20-30ml脑脊液,其中3-5ml送检,其余为治疗性释放,而在腰大池引流的患者,每24h的引流量多控制在200-300ml。
在临床实际中,我们往往是根据经验, 对一般状态较差,出血量较多(可能伴有小血肿)的患者进行腰大池引流 ,换言之,这一部分患者同时即是入院高Hunt-Hess分级、高改良Fisher分级的患者。
也可以理解为CVS风险“已经”较高的患者。对一些有选择余地的患者,行多次腰椎穿刺术还是行腰大池引流,往往需要综合考虑, 除了患者的临床实际情况,比如还有经济原因(腰大池引流系统更为昂贵)、患者或家属的意愿,以及医师的倾向或习惯。

二者均为有创操作,目前我们通常认为它们均可以通过释放血性脑脊液来改善aSAH的相关并发症,但也存在 感染、引流过度等风险 ,不可忽视。似乎神经外科医生对aSAH患者管理过程中行腰大池引流更为积极,但更加激进的治疗与相应风险之间,如何寻找一个安全的平衡点,还需要更多大规模临床研究的支持。

动脉瘤性蛛网膜下腔出血术后脑血管痉挛的早期预测模型的构建和内部验证
作为神经外科临床常见疾病,aSAH的预后往往不尽如人意, 动脉瘤的二次破裂出血、严重的脑血管痉挛脑干缺血都是病程恶化的重要原因 ,致死率、致残率居高不下。
虽目前缺乏一些特异性血清标志物来预测CVS,但 常规的血实验室检查指标往往能够反应生理、病理生理状态,对CVS的发生产生潜在影响 ,所以我们希望通过构建aSAH患者术后CVS的早期预测模型,针对临床上CVS高风险的患者做出提示。
对原研究人群(262例)进行拆分, 通过科学的方法拆分、建模,并对模型加以检验 (内部验证),在下一部分我们还会通过前瞻性的病例入组,进一步对预测模型进行外部验证等工作。
值得注意的是,在70%人群的CVS预测因素分析中,我们经过单因素分析和多因素分析,在统计方法没有改变的情况下,得出的结论与第一部分并不完全一致,除了临床因素基本相同外,入院时化验结果则见到差异,尤其是对于P/C。
在第一部分的分析中,得出了P/C可能是aSAH患者术后CVS的危险因素,而在本次建模前的回归分析中,P/C对CVS有显著影响,但为保护因素,就此我们认为,很可能是 数据本身的特性导致这个差异,并且有其他化验指标进入了方程。

CVS是一个极为复杂的临床病理生理学过程, 单一的血清标志物很难做到“完全”准确的预测 ,这也是我们进行本项研究、构建CVS临床预测模型的初衷,尝试通过对CVS预测的探索,应用于临床并指导进一步研究。
如同多数作者认为高龄是aSAH患者术后CVS的危险因素,然而美国一项8000例以上的大规模研究却给出了相反意见,认为年轻的aSAH患者更易发生CVS。

以目前我们对CVS的认知尚不足的现状, 各种探索和争论在情理之中,都是有益的 。尽管在预测模型的性能上,我们构建的临床模型(CBM)以及联合预测模型(CPM)只达到中等水平。
但对于模型性能,以及化验指标对CVS的影响(尤其是P/C)这些问题上,真实的数据才会得出令人信服的结论,因此,笔者没有选择对数据进行随意的编篡和更改而获得“漂亮”的结果,只有这样,我们构建的预测模型才是有意义的。
在临床上, aSAH患者的病情进展经常让人措手不及 ,而CVS的机制、治疗方向都可能是未来进一步研究、探索的热点。
临床上可能以第二种稍多,偶有另外两种情况的出现。不过,作为神经外科医师,在向aSAH患者家属交代病情时,我们无例外的会强调病情变化的 突然性、凶险性、发生严重CVS的可能性 ,即使这些都是客观事实,也确实存在许多令人惋惜的局面,在面对家属“发生这一并发症的可能性多大”的问题时,往往难以给出准确的回答。
此时,预测模型转化的意义凸显出来,诚然,凭借寥寥几个血液标志物和临床状态的评估,不足以诠释aSAH和CVS的全部要素, 但这种有益的探索让我们能够将风险量化,为临床治疗提供科学的决策依据 ,尤其是对处在“非极端区”的患者。借此,还有很多aSAH的并发症值得我们研究,并可通过类似方法构建预测模型指导诊疗实际,比如对aSAH患者脑积水的预测、对aSAH患者重症肺炎的预测等等。
在对大人群(262例)拆分建模部分,模型B为最优模型,其中纳入的血液指标为血小板值(Plt), 并不是纳入的因素越多越好 ,有报道称,只有不到2/3的临床预测模型研究全面评估了模型的区分能力,可能不到1/3的临床预测模型研究报道了校准度。
对全身来说,血小板的生理功能都是非常繁杂的, 血小板出现病理性改变或反应的情况也绝不仅仅限于aSAH一种疾病 ,因此通过某一个血液学检查的结果,来推断CVS发生与否,一定是片面的,但回到我们进行研究的初衷,对于预测模型构建的探索来说,Plt在模型B(包括模型C、模型D)中的表现已经足够。

入院高Plt可能是CVS的一个危险因素,另一方面, 血小板具有内源性抑制机制,所以对于CVS来说,血小板的调节可能是潜在的治疗靶点 ,就此,有临床研究提示前列环素(Prostacyclin)和一氧化氮(NitricOxide,NO)具备一定前景,它们均是血小板*制剂抑**和血管扩张剂。这些研究甚至指出,对aSAH患者进行抗血小板治疗,其诱发再出血事件的风险和减少CVS以及DCI的获益相比,可以忽略不计。
在对先前构建的aSAH患者术后CVS早期预测模型进行了外部验证后,模型表现出了较好的稳定性和可靠性,并且模型得以转化,形成了方便易用、科学合理的可视化计算工具,可以直接对临床做出提示。
CPM对CBM的性能有提升,但紧急情况下,若不能及时获取相关化验结果,可以依靠CBM对CVS事件进行预测。
