多年以来,人们一直在努力寻找以更生理方式将HBV基因组传递到细胞的替代方法。例如,在昆虫细胞中产生的重组HBV杆状病毒系统的开发,使HBV基因组能够进入肝癌细胞,从而产生HBV复制,形成感染性病毒,并建立可以检测的细胞内cccDNA池。
乙肝干扰素研究领域,通过化学改性,延长其半衰期至40小时
经过多年的科学实践,全球前沿科学认为HBV进入细胞的机制是一个值得探索的HBV生命周期其一关键步骤。开发出HBV基因组的传递载体系统,全球已经用于多种体外研究,比如检测新型抗HBV药物的有效性和耐药性研究。另外一个潜在的HBV基因组传递系统是腺病毒载体。携带HBV基因组的腺病毒载体(Ad-HBV)已经被证明,可以感染广泛的肝细胞,而不受到物种屏障影响,可导致强大的HBV复制。
虽然,这种HBV基因组传递系统已经用于慢病毒载体的体外试验,尽管和传递的HepG2.2.15细胞系及其衍生物相比,它具有一定的优势,但是,这些传递载体系统依然存在明显的局限性。局限性主要表现在,通过病毒载体传递HBV基因组完全绕过了HBV的自然进入阶段,从而避开了关于HBV生命周期中的这一步骤的研究。另外,部分宿主对HBV感染的应答,可能很大程度上被用于HBV载体的非特异性应答所掩盖;

比如,目前还很难解释清楚对HBV感染的先天免疫应答的数据。而安全性问题,尤其是乙肝病毒携带慢病病毒载体的工作,是全球科研人员关注的领域,所以上述这些,都是广泛应用这种HBV基因组传递载体系统的阻力面。近期,小番健康介绍了乙肝病毒生命周期及其关键步骤,这是药物开发者关注的靶点研究方向,接下来,我们谈谈已经上市的抗HBV药物,它们的机制和开发初衷。
例如,免疫调节药物,这个方向研发出来的药物已经广泛地被使用在严重肺炎、免疫缺陷病和慢性乙肝领域。主要是基于许多乙肝病毒携带者,目前尚没有临床肝炎表现,但后来可能会出现肝损伤。因此,免疫调节药物的开发,主要是提高患者的免疫应答,尤其是针对HBV的特异性免疫。免疫调节因子,可以帮助免疫细胞识别和破坏HBV感染细胞,从而清除这些被破坏细胞中的HBV。
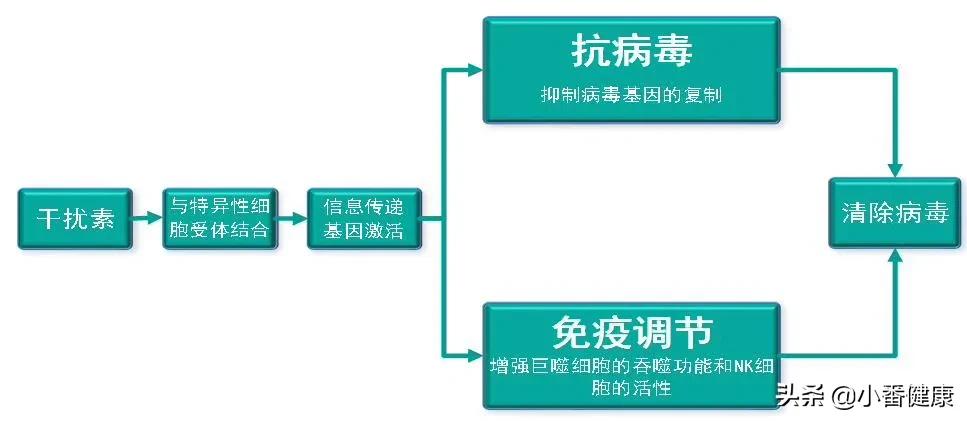
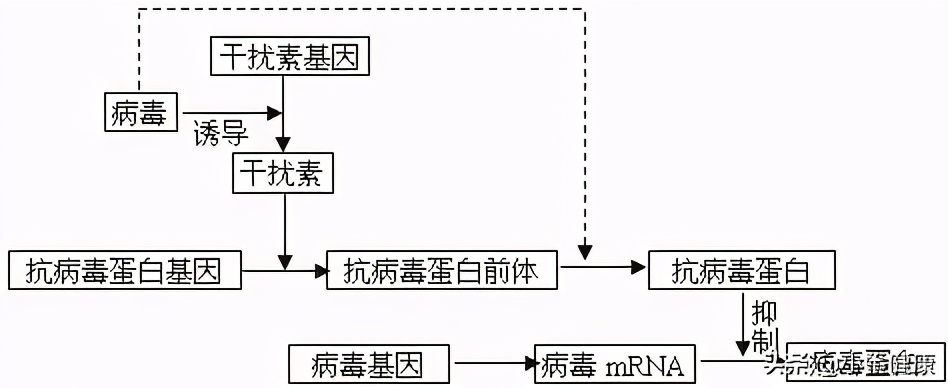
干扰素(IFN),它属于一种分泌性糖蛋白,具有抗病毒、抗增殖和免疫调节细胞因子功能作用。如果宿主细胞对各自刺激做出反应时,就会触发IFN的产生。IFN根据产生细胞分为α-(白细胞),β-(成纤维细胞)和γ-(淋巴细胞)。目前,被用于治疗慢性HBV感染的IFN主要类型与细胞表面的特定受体结合,触发一系列信号转导事件,从而产生抗病毒蛋白(抗病毒蛋白AVP),进而降解病毒的mRNA,抑制HBV复制。
此外,增强自然*伤杀**细胞、巨噬细胞和T淋巴细胞的活性,表明IFN除了直接抗病毒作用外,它还兼具有调节免疫应答作用。全球研究人员通过化学改性(chemical modification,通过化学反应改变聚合物的物理、化学性质的方法),可以延长IFN的半衰期。目前,使用较为广泛的该方向药物是聚乙二醇(PEG),它可以形成IFN分子的多副本,注射后,IFN分子降解较慢。
pegIFN具有较长的半衰期,可达40个小时,并能够有效抑制HBV复制168小时(相关科研文献可查询到)。所以,pegIFN只需要每周注射1次,对于患者而言使用更方便、更容易地遵从肝病临床医生的治疗方案,提高药物依从性。当然,在对pegIFN药物开发过程中,药物开发者也发现其缺陷,例如干扰素治疗昂贵,并且短期和长期干扰素的副作用都较为严重,主要包括发烧、脱发和白细胞减少。在一些有文献记录中,pegIFN对丙氨酸转氨酶(ALT)正常或轻度升高的患者,抗病毒效果较差等。