胃癌仍然是最致命的恶性肿瘤之一,尤其是在疾病晚期被诊断出来时;大多数在疾病进展后期诊断的患者会出现一定程度的腹膜污染,例如腹膜细胞学阳性或腹膜转移结节。 在这种情况下,大多数情况下会发展为腹膜癌并在 一年内 死于该疾病。
为了延长这类病人的生存期,临床医生提出了多种治疗策略,例如根治性手术和腹膜内加热化疗或直接腹膜内化疗,然后进行根治性手术。迄今为止,已广泛研究了切除时腹腔内加热化疗的益处;但该方法仍然与围手术期并发症发生率增加有关。因此需关注新辅助治疗后进行根治性手术等手术的益处上。本文着重对晚期胃癌最有效的治疗策略,如新辅助腹腔镜加热腹腔化疗、围手术期加热腹腔化疗以及新辅助全身和腹腔化疗进行文献论文介绍。
胃癌是影响全世界人民的最致命的消化系统恶性肿瘤之一,总体估计 5 年生存率为 25%,而在出现晚期病例中,5年生存率降低至 <5%。与许多其他恶性肿瘤一样,胃癌可通过多种途径扩散,例如导致远处内脏转移出现的血源性癌症、导致淋巴结转移发展的淋巴性癌症和导致腹膜癌病发展的腹膜性癌症。
腹膜性癌传播途径是由恶性细胞从胃浆膜脱落并进一步植入腹膜腔引起的。随着时间的推移,这些细胞会增殖并发展为腹膜癌结节;据估计,高达 45% 的患者在初诊时会同时出现腹膜结节,而即使在初诊时已进行根治性手术,也会有相似比例的患者在疾病的某个阶段出现此类病变诊断。
癌性腹膜结节一旦形成,可出现腹水、肠梗阻、肠穿孔或营养剥夺等多种并发症,导致顽固性并发症的出现,最终患者死于该病。因此,以前的研究认为腹膜癌病是一种局部区域疾病,而不是全身性疾病。 然而胃癌导致腹膜癌患者的估计生存率小于 6 个月,在接受全身化疗的病例中,该寿命的改善微乎其微 。
在这方面,已经提出了积极的外科手术,例如腹膜内化疗、术后早期腹膜内化疗、新辅助腹膜内和全身治疗以及细胞减灭术。腹腔热灌注化疗 (HIPEC) 已被证明在晚期胃癌的治疗中发挥重要作用,作为预防工具以及在选定的腹膜转移病例中发挥作用。 该方法似乎具有多个优点,例如在肿瘤水平直接递送大量细胞毒剂,使用加热剂可增加抗肿瘤作用并减少全身毒性;所有这些优势引起了人们的极大兴趣,尤其是在胃癌患者中,胃癌患者的疾病最常通过腹膜途径复发 。然而,该方法已被证明与围手术期发病率显着相关;因此,这些方法可以最大限度地发挥这些手术的效果,从而最大限度地降低围手术期发病率和死亡率的风险。
文献来源
本文是对在 Pubmed 上搜索以下关键词后确定的研究进行的文献综述:“新辅助化疗”、“晚期胃癌”、“胃癌引起的腹膜转移”、“高温化疗”。确定了 83 项研究,其中排除了无法获得全文的研究、以英语以外的其他语言撰写的研究以及病例报告。最后,确定了 35 项研究,论文发表于1995 年至 2021年之间。
新辅助HIPEC原理
预防性腹腔热灌注化疗
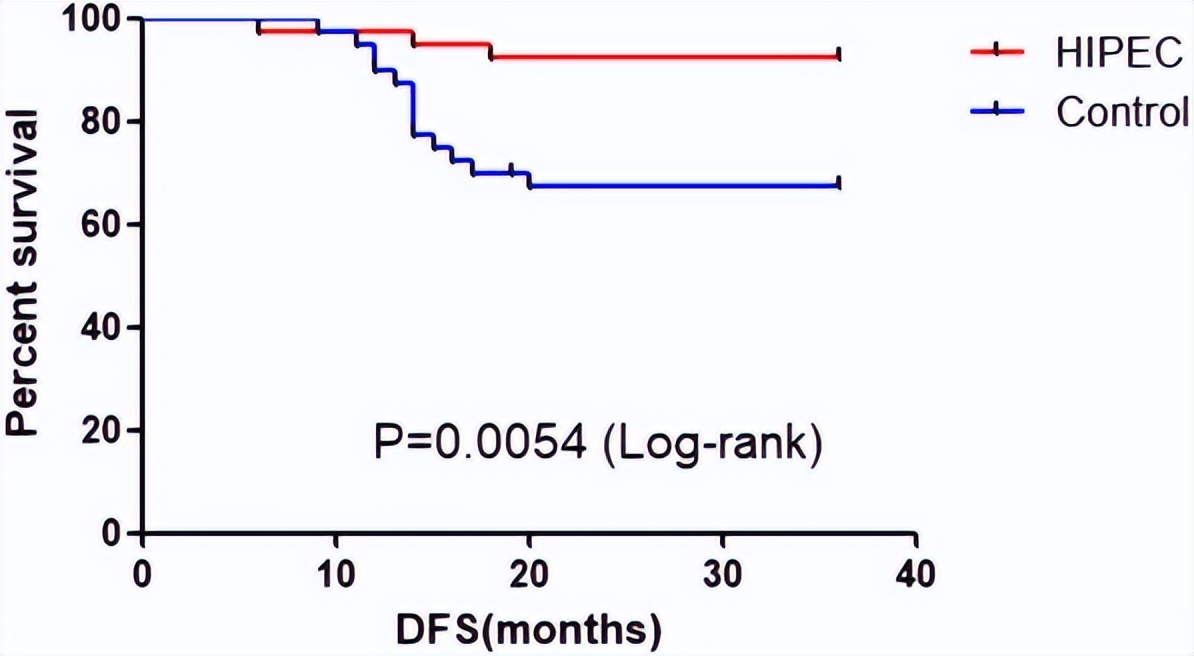
古贺等 1988 年首次报道了使用腹膜内高温化疗 (HIPEC) 作为预防因手术创伤或疾病进展引起的腹膜播散,其中 3 年生存率和腹膜复发率显着改善 。 1992-2002年128例胃癌腹膜播散患者纳入HIPEC实验,切除组5年生存率为5.5%,非切除组5年生存率为0% , HIPEC 是多变量分析的独立预后因素。在另一项试验中发现当比较接受手术+HIPEC 的 42 名受试者与仅接受手术的 54 名受试者,仅手术组复发率分别为 34.7%,在HIPEC 组腹膜复发率10.3%,支持 HIPEC。
在Cui等人的一项研究中192名AGC患者被随机分为以下四组(对照组、NAC、HIPEC和联合组),结果表明NAC联合HIPEC治疗AGC具有良好的耐受性和表现提高合规性和效率。在我们团队的另一项研究中,有 80名患者,其中40名患者接受预防性HIPEC,而对照组仅接受手术,结果显示实验组具有显著的生存获益腹膜转移率降低。

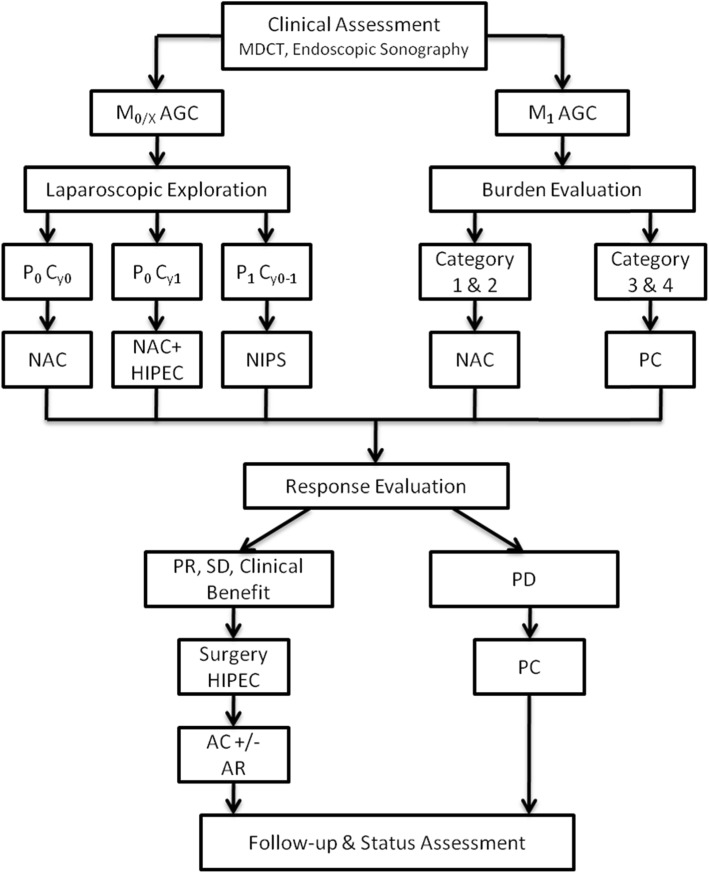
研究最广泛的治疗策略之一是使用 HIPEC 作为新辅助手术,然后进行间隔减瘤手术。这种以腹腔镜方式进行的方法似乎与高达 25% 的腹膜转移完全消失和总体存活率增加有关 。因此,微创手术联合新辅助 HIPEC(在没有减瘤手术的情况下)似乎可以最大限度地提高肿瘤学益处并将围手术期发病率的风险降至最低。
此外,其他作者也研究了在细胞学阳性患者中进行新辅助 HIPEC 作为腹膜癌转移预防的可能性;在出现浆膜浸润的病例中应进行腹膜细胞学检查,遇到恶性细胞时新辅助 HIPEC 后间隔根治性胃切除术应该是首选方案。
然而东西方国家之间有意见分歧,虽然在迄今为止发表的亚洲试验研究均证实HIPEC 对浆膜浸润患者和腹膜癌患者有效,但在西方国家,该方法似乎仅在浆膜浸润病例中被证明特别有效。这种差异可以通过以下事实来解释:两种类型的肿瘤在肿瘤生物学、遗传学和治疗类型方面存在显著差异。
另一个有趣的概念是在诊断为晚期胃癌的患者中进行预防性围手术期 HIPEC;根据 Sugarbaker 报道,当患有浆膜浸润晚期胃癌患者接受手术时,通过多种机制发生术中腹膜污染的风险增加,包括标本的手术操作,淋巴结清扫期间的淋巴横断以及术中静脉出血可能导致腹膜种植。每当淋巴管被横切且其内容物被恶性细胞污染或静脉被切开并且可能含有肿瘤栓塞的静脉血到达腹膜表面时,腹膜污染的风险就会增加。同时,在术后早期粘附综合征和纤维蛋白包埋的发展将肿瘤细胞固定在腹膜表面水平,并进一步促进腹膜癌的发展。因此 提出了一种预防所有诊断为晚期胃癌的病例的围手术期HIPEC方案。
HIPEC 在胃癌腹膜癌新辅助治疗中的有效性
新辅助腹腔内化疗的概念最初是在没有热疗的情况下考虑的,但与全身化疗有关。该方法也称为新辅助腹腔内和全身化疗 (NIPS),已被证明可以结合两种细胞毒*药性**物给药途径的优点;因此,更多的化疗药物将集中在腹膜结节水平,通过血行和直接通过腹膜通路到达这些病变。根据 Sugarbaker 的说法,这种治疗策略最合适的候选人是年龄小于 65 岁、一般状况良好(东部临床肿瘤组评分为 2 分或以下)、无血行或淋巴转移、正常血、肝、肾状态。该治疗可以应用 4 到 6 个周期,如果获得阳性反应(由阴性细胞学和腹膜病变消退定义),则进一步进行根治性手术。
迄今为止,已经彻底研究了新辅助 HIPEC 在胃癌腹膜转移中的作用。似乎该方法在从初步诊断时起就出现扩展性腹膜病变的病例中起着至关重要的作用。因此,进行 2 到 5 次新辅助 HIPEC 似乎可以显著降低腹膜病变的范围 [通过腹膜癌病指数 (PCI) 量化],从而提高完全细胞减灭率。
Yu等人最近发表了一项最有说服力的研究,证明了新辅助 HIPEC 在减少 PCI 和延长寿命方面的功效。该研究包括 38 名接受新辅助全身化疗、HIPEC 和减瘤手术的患者(18 例,转化治疗组),并将他们的结果与对照组(20 名仅接受化疗和 HIPEC 的患者)报告的结果进行比较。作者报告转化治疗组的中位总生存期显著增加到21.1 个月,对照组中位总生存期仅为 10.8 个月,P=0.002。此外, 作者强调了这样一个事实,即在第二次腹腔镜检查时 PCI 值低于 6 的病例与该值较高的病例相比结果显著改善。
迄今为止公布的数据以及此时正在进行的临床试验旨在证明新辅助 HIPEC 单独或联合新辅助全身化疗对细胞学阳性或腹膜病变有限的患者的有效性 (23 )。
根据 Beeharry等人的说法,细胞学阳性且在腹腔镜检查期间没有肉眼可见的腹膜病变的患者应进一步行新辅助HIPEC,而呈现肉眼可见但病变有限的病例应进一步行NIPS。同一个研究小组制定了一项方案比较新辅助腹腔镜 HIPEC 联合新辅助全身化疗后根治性胃切除术和 HIPEC 与根治性胃切除术后辅助化疗在晚期胃癌中的疗效。多中心 III 期随机对照试验包括 326 名患者,他们在腹腔镜探查后被随机分配。
第一组中的病例接受了一次新辅助腹腔镜 HIPEC 手术(43˚C 下 60 分钟,80 mg/m 2紫杉醇),然后是三个周期的奥沙利铂新辅助全身化疗、术中 HIPEC 根治性 D2 胃切除术和另外 5 个周期的基于奥沙利铂的辅助化疗。对照组接受标准根治性 D2 胃切除术,随后接受 8 个周期的奥沙利铂辅助全身化疗。该研究的目的是比较两组之间的长期结果包括 5 年无进展生存率、5 年总生存率和腹膜转移率,短期结果为总体发病率 。
Badgwell在 2017 年证明了新辅助 HIPEC 在腹膜细胞学阳性患者以及新辅助化疗甚至放化疗后放射学隐匿性腹膜转移病例中的有效性和安全性。
Yonemura等人的另一项有趣研究于 2017 年发表;该研究包括 105 名被诊断患有胃癌腹膜转移的患者。有 53 例患者接受了 2 个周期的新辅助 HIPEC,随后进行了间隔减瘤手术,52 例患者接受了 3 个周期的 NIPS,随后进行了减瘤手术。作者证明,在进行腹膜内化疗后,两组的 PCI 值均显着降低,而整个研究组的总细胞减灭率为 57.6%。此外,中位生存率为 19.2 个月,而两年生存率为 41%。
因为独立于细胞减灭术的完整性,PCI (腹膜癌病指数)的价值似乎显著影响长期结果。在 Glehen等人进行的一项研究中,作者证明在根治性手术和 HIPEC 后的三年随访中,即使已经实现了完全细胞减灭术,在 PCI(腹膜癌病指数)>12的患者中也没有一个存活下来。所以存在扩展腹膜病变患者应该是减积手术和HIPEC的禁忌症。
结论
作为HIPEC或与NIPS联合进行的新辅助腹腔化疗在细胞学阳性的晚期胃癌以及出现腹膜转移的高度选择性病例中提供了有希望的结果。这些方法已被证明可有效减少腹膜污染并增加在根治性手术时实现根治性切除的机会。