晚期胆管细胞癌的治疗现状与进展
胆管细胞癌近年来在我国发病率有升高趋势,对于晚期胆管细胞癌来说,目前治疗方式不再局限于姑息性手术和GC方案化疗(吉西他滨+顺铂),肝动脉灌注法等局部疗法以及针对胆管细胞癌特异性靶点或多突变位点的靶向治疗和免疫治疗的出现,使得一线药物失效后,还可以采用不良反应相对较小的个体化治疗,使患者获得更长的生存时间和更高的生活质量。
胆管细胞癌包括起源于胆管上皮的所有肿瘤,多数胆管细胞癌为腺癌,可分为肝内胆管细胞癌和肝外胆管细胞癌两大类。随着影像技术和分子诊断学的发展,从1973年至2012年的大数据中可见肝内胆管细胞癌发病率大幅上升(350%),肝外细胞癌发生率则稳步升高(20%)。
肝内胆管细胞癌位于肝实质内,肝外胆管细胞癌可发生于肝外胆道的任何位置,从左右肝管的汇合部到胰腺内的胆总管部分,可进一步分为肝门部胆管细胞癌和远端胆管细胞癌,前者为肝门处或左右肝管汇合处附近的肿瘤,后者为起源于Vater壶腹部以上肝外胆道的病灶,这一分类方式与患者治疗方式及预后密切相关。胆管细胞癌因预后不佳,一线化疗方案失败后,在靶向药物和免疫药物未出现时,患者的无进展生存时间(progression-free survival,PFS)一般不足4个月,近年治疗方法的进步使患者的生存时间有了明显延长,生活质量明显改善。
局部治疗
对于可手术切除的患者,完全性切除为唯一的治愈手段。然而多数就诊患者已为晚期,但并非失去局部治疗机会。对于肝内胆管细胞,可行高剂量3D适形放疗联合肝动脉灌注化疗或高剂量立体定向放疗或高剂量低分割质子束治疗。另外还有以肝动脉为基础的治疗方式,包括肝动脉灌注、经导管动脉化疗栓塞术、药物洗脱珠-经导管动脉化疗栓塞术和钇90放射栓塞,四者中肝动脉灌注的中位生存(overall survival,OS)最长(22.8个月),反应率最高(56.9%),但同时Ⅲ/Ⅳ级不良反应发生率也为最高,一定程度上限制了疗效。对于肝外胆管细胞癌,为促进胆道降压,可行支架引流联合光动力疗法,即内镜方法与光敏剂配伍,利用光和氧启动线粒体的凋亡程序,患者生存时间可延长1.26倍,且术后胆管炎发生率明显降低,患者的生活质量也随之提高。另有随机试验发现内镜射频消融联合支架置入术亦可将患者的平均生存时间从8.3个月延长至13.2个月,在不良事件发生概率不增加的原则下,患者保持支架通畅的时间也明显延长。综上,化疗联合放疗可作为局部晚期无法行手术切除的患者优先治疗方式,在不良反应可控的前提下,可考虑肝动脉灌注或联合局部放疗。因梗阻而胆汁引流不畅的患者,可予支架植入并联合光动力或消融治疗。由于符合米兰标准的患者较少且可观疗效多见于早期的患者,因此肝移植不作为首选。
全身治疗
化疗
Ⅲ期临床试验ABC-02确定了晚期患者的一线治疗方案:吉西他滨联合顺铂。研究结果提示联合用药组的中位OS为11.7个月,吉西他滨组为8.1个月,中位 PFS分别为8.0、5.0个月。另外,日本JCOG1113试验数据提示对于不能耐受顺铂的患者,可选择吉西他滨联合替吉奥,二者的OS差异并无统计学意义,也有研究将顺铂换做白蛋白紫杉醇,疗效相当。Roth等将白蛋白紫杉醇加入经典一线方案(吉西他滨800 mg/m2,白蛋白紫杉醇100 mg/m2,顺铂25 mg/m2 ):中位PFS达11.8个月,中位OS达19.2个月,Ⅲ~Ⅳ级不良反应的发生率也从82%降至58%。但一线治疗失败后,目前尚未建立标准的二线化疗方案。近期的回顾性研究用二线化疗(以吉西他滨或氟尿嘧啶为基础的化疗方案)起始到失败的时间(time to treatment failure from second- line therapy,TTF2)代替二线化疗开始后的无进展生存期 (progressionfree survival from the initiation of secondline chemotherapy,PFS2),发现二线化疗仅能维持2.2个月,短于既往数据。由于后续临床试验和后线化疗的存在,以及化疗期间出现不可逆转的不良反应和因肝外胆道 梗阻不得不暂停化疗等突发事件,TTF2更能反映出真实世界的情况。因此迫切需要继续探索其他有效的治疗方式。
靶向治疗
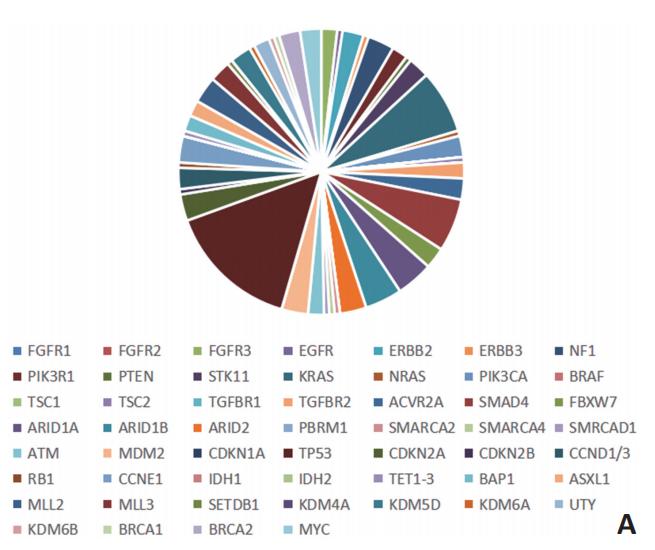
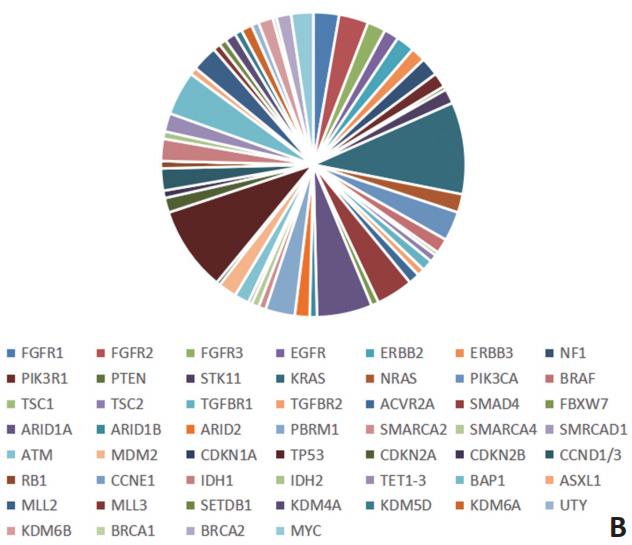
随着生物检测技术的成熟,现已逐步揭示胆管细胞癌的可能病因。在对260例胆道癌患者行分子变异分析后发现,近40%的患者有潜在治疗靶点,且基因改变具有部位特异性。如成纤维细胞生长因子受体(fibroblast growth factor receptor,FGFR)改变主要发生在肝内胆管细胞癌中,而蛋白激酶A(protein kinase A,PKA)的改变在肝内外均有发现(图1)。
FGFR 髓样细胞白血病-1(myeloid cell leukemia-1,MCL-1)是BCL-2家族的成员之一,后者是决定细胞生存的三大要素之一。FGFR *制剂抑**正是通过诱导 MCL-1 的丢失引起线粒体氧化代谢的失调,从而使细胞坏死。研究显示,在61例一线治疗失败或不能耐受化疗不良反应而接受 FGFR *制剂抑**BGJ398的患者中,48例患者为FGFR2基因融合,8例为FGFR2基因突变,3例为FGFR2基因扩增,总体反应率(overall response rate,ORR)为 14.8%,疾病控制 率(disease control rate,DCR)达 75%,中位 PFS 达 5.8 个月,且对BGJ398有应答的患者均包含FGFR2基因融合。进一步分析提示基因融合患者获益更多,由此推测FGFR2基因融合的患者可能对该*制剂抑**更加敏感。类似试验包括ARQ 087,试验中受试者均为FGFR融合患者,试验药物derazantinib为多激酶*制剂抑**,FGFR 为其靶点之一,ORR 为 20.7%,DCR、中位PFS分别为82.8%、5.7个月,因此,FGFR2融合基因可能是潜在的重要靶点。
异柠檬酸脱氢酶 异柠檬酸脱氢酶(isocitrate dehydrogenase,IDH)是三羧酸循环中的关键酶之一,其将异柠檬酸转化为 α-酮戊二酸(alpha-ketoglutarate,AKG),后者为DNA 和组蛋白修饰的辅助因子。当IDH发生功能性突变后,可使α-酮戊二酸转为二羟基戊二酸,从而干扰AKG相关的酶发挥作用,导致基因表达的紊乱。Ivosidenib(AG-120)为第一代口服的IDH*制剂抑**,在Ⅰ期临床试验中,40%患者获得6个月无病生存。此外,IDH突变细胞的存活主要依 赖于激酶—SRC酶的活性,多激酶*制剂抑**dasatinib的 靶点之一包括SRC,在体内外,IDH突变的肝内胆管癌细胞已显示出对dasatinib的高度敏感。
EGFR ErbB/HER家族是一类在细胞增殖、分化和迁移等行为中重要的酪氨酸激酶受体,在胆管细胞癌中常高表达,从而促进肿瘤进展。研究显示,将表达表皮生长因子受体(epidermal growth factor receptor,EGFR)-特异性嵌合抗原受体的自体T细胞回输至患者体内,在此之前患者需接受白蛋白紫杉醇联合环磷酰胺的化疗,17 例患者中 1 例获得完全缓
解,10例疾病稳定,中位PFS提升至4个月。尽管在免疫治疗后1周,患者常会出现可能由细胞因子风暴引起的一系列全身性改变,但均可逐渐恢复。嵌合抗原受体T细胞治疗有望在晚期胆管细胞癌治疗中发挥重要作用。
C-Met/RON C-Met 和RON 均为跨膜磷酸酪氨酸受体,二者常常在多种实体肿瘤*共中**同过表达,提示预后不佳。动物研究显示,输注双靶药物BMS- 777607的小鼠与接受吉西他滨和奥沙利铂化疗的小鼠相比,在动物 PET/CT 中,病灶的 SUV 值在治疗后有明显下降。但其最终疗效仍需临床试验进一步验证。
BRAF/MEK Raf/MEK/ERK转导级联反应是细胞生长、增殖等生理活动的重要介质。BRAF 为Raf 的异构体,由RAS 激活后,协同参与细胞对生长因子的应答。但患者口服选择性BRAF V600激酶*制剂抑**vemurafenib后,ORR仅12%。而在ROAR篮 子试验中,同为具有 BRAF 600E 突变的患者,将BRAF*制剂抑**与MEK*制剂抑**联合应用后,ORR提升至41%,中位PFS延长至7.2个月。因此,BRAF*制剂抑**联合MEK*制剂抑**可能较单药更有效,其依赖的信号转导机制还需进一步明确。
免疫治疗
目前免疫药物已经被纳入多个瘤种的一线或二线治疗队列,其主要针对程序性死亡蛋白-1(programmed death-1,PD-1)和相应配体程序性死亡蛋白配体-1(programmed death ligand-1,PD-L1)。KEYNOTE028 篮子试验中,20 例患者接受 PD-1 *制剂抑**pembrolizumab
治疗后,3 例部分缓解,4 例疾病稳定。Le等研究中,4例胆管细胞癌的患者同样接 受 pembrolizumab 治疗后,1 例获得完全缓解,剩余 3 例未见肿瘤进展,DCR达100%。虽然各试验的入组 例数较少,但免疫治疗依然为日后的研究方向提供了重要线索。
联合治疗
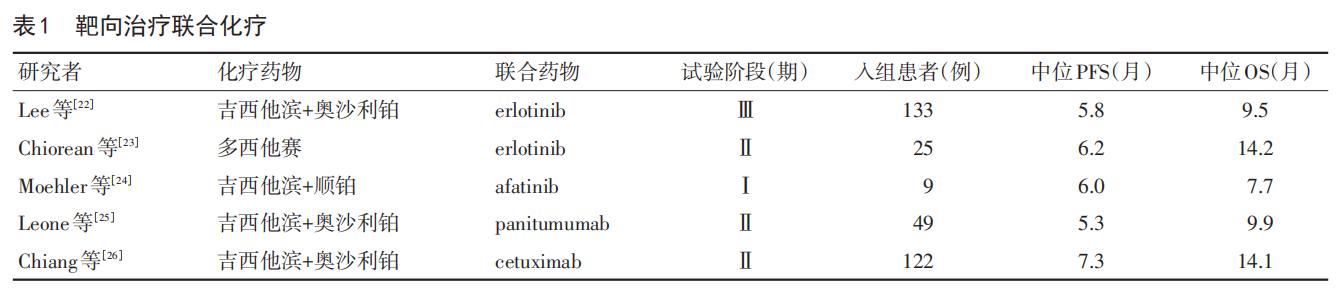
靶向治疗+化疗 靶向治疗联合化疗的疗效优于单纯化疗,尤其是EGFR*制剂抑**与化疗的联合(表1)。但同类靶向药物联合不同的化疗药物或同一化疗药物联合不同的靶向药物之间的疗效尚有差异。
靶向治疗+靶向治疗 除上述ROAR篮子试验外,血管内皮生长因子(vascular endothelial growth factor,VEGF)*制剂抑** pazopanib 联合 MEK *制剂抑** trametinib 二线治疗晚期胆管细胞癌的单臂试验显示, 患者的 PFS 和 OS 并未延长,分别为 3.6、6.4 个月。 但 VEGF *制剂抑** bevacizumab 联合 EGFR *制剂抑** erlotinib时,患者的OS却可达9.9个月。此结果可能受入组患者例数的限制或VEGF 受体表达数量的不同或靶向药物组合不同的影响。
免疫治疗+化疗/靶向治疗 近期一项开放的多中心Ⅰ期试验显示,PD-1*制剂抑**nivolumab联合吉西他滨和顺铂后,患者的中位PFS为4.2个月,虽未见显著延长,但中位OS达15.4个月。在2019年ASCO会议上,秦叔逵教授公布了抗PD-1抗体卡瑞利珠单抗联合FOLFOX4或GEMOX治疗晚期肝细胞癌或胆道癌的Ⅱ期试验的中期结果(NCT03092895),报道提示在胆道癌队列中,ORR为9.4%,DCR达90.6%。 此外,还有研究探讨了多激酶*制剂抑**lenvatinib 联合PD-1*制剂抑**在14例已接受二线或多线治疗的肝内胆管细胞癌患者中发现,3例获得部分缓解,ORR为21.4%,DCR达92.9%,中位PFS达5.9个月,进一步分析提示高肿瘤突变负荷的患者获益更多,为进一步选择获益人群提供了一定依据。
总结
晚期胆管细胞癌的治疗手段局限于化疗和手术治疗,但靶向药物和免疫药物的出现使这一难点得到突破。对于一线治疗失败的患者,目前已有对IDH、FGFR、EGFR、C-Met、BRAF等特异位点的靶向治疗以及针对肿瘤细胞的免疫疗法,患者的生存期得以明显延长,但仍需随机对照试验进一步筛选出最可能获益的人群。另外,不同药物组合的疗效尚存在差异,其机制仍值得思考和继续研究。